Microzide 25mg Hydrochlorothiazide Bruk, bivirkninger og dosering. Pris i nettapotek. Generisk medisin uten resept.
Hva er Microzide 25mg og hvordan brukes det?
Microzide er et reseptbelagt legemiddel som brukes til å behandle symptomene på høyt blodtrykk (hypertensjon) og hevelse (ødem). Microzide kan brukes alene eller sammen med andre medisiner.
Microzide tilhører en klasse legemidler som heter diuretika, tiazid.
Det er ikke kjent om Microzide er trygt og effektivt hos barn yngre enn 6 måneder.
Hva er de mulige bivirkningene av Microzide?
Microzide kan forårsake alvorlige bivirkninger, inkludert:
- . svimmelhet, . øyesmerter, . synsproblemer, . gulfarging av hud eller øyne (gulsott), . blek hud, . lett blåmerker, . uvanlig blødning (nese, munn, vagina eller endetarm), . kortpustethet, . hvesing, . hoste med skummende slim, . brystsmerter, . tørr i munnen, . tørst, . døsighet, . lite energi, . rastløshet, . muskelsmerter eller svakhet, . rask puls, . kvalme, . oppkast, . lite eller ingen urin, . feber, . sår hals, . hevelse i ansiktet eller tungen, . brenner i øynene, og . hudsmerter etterfulgt av rødt eller lilla hudutslett som sprer seg (spesielt i ansiktet eller overkroppen) og forårsaker blemmer og avskalling
Få medisinsk hjelp med en gang hvis du har noen av symptomene nevnt ovenfor.
De vanligste bivirkningene av Microzide inkluderer:
- . kvalme, . oppkast, . tap av Appetit, . diaré, . forstoppelse, . muskelspasme, . svimmelhet, og . hodepine
Fortell legen dersom du har noen bivirkninger som plager deg eller som ikke går over.
Dette er ikke alle mulige bivirkninger av Microzide. Spør legen din eller apoteket for mer informasjon.
Ring legen din for medisinsk råd om bivirkninger. Du kan rapportere bivirkninger til FDA på 1-800-FDA-1088.
BESKRIVELSE
MICROZIDE® (hydroklortiazid, USP 12,5 mg) er 3,4-dihydroderivatet av klortiazid. Det kjemiske navnet er 6-klor-3,4-dihydro-2H-1,2,4-benzotiadiazin-7-sulfonamid 1,1-dioksid. Dens empiriske formel er C7H8CIN304S2; dens molekylvekt er 297,74; og dens strukturformel er:
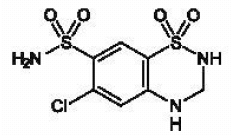
Det er et hvitt, eller praktisk talt hvitt, krystallinsk pulver som er lett løselig i vann, men fritt løselig i natriumhydroksidløsning.
MICROZIDE (hydroklortiazid kapsel) leveres som 12,5 mg kapsler for oral bruk.
Inaktive ingredienser : kolloidalt silisiumdioksid, maisstivelse, laktosemonohydrat, magnesiumstearat. Gelatinkapsler inneholder D&C Red No. 28, D&C Yellow No. 10, FD&C Blue No. 1, gelatin, titandioksid. Kapslene er trykt med spiselig blekk som inneholder svart jernoksid, D&C Yellow No. 10, FD&C Blue No. 1, FD&C Blue No. 2, FD&C Red No. 40.
INDIKASJONER
MICROZIDE (hydroklortiazidkapsel) er indisert for behandling av hypertensjon enten som eneste terapeutiske middel eller i kombinasjon med andre antihypertensiva. I motsetning til kaliumsparende kombinasjonsdiuretika, kan MICROZIDE (hydroklortiazidkapsel) brukes hos pasienter der utviklingen av hyperkalemi ikke kan risikeres, inkludert pasienter som tar ACE-hemmere.
Bruk under graviditet
Rutinemessig bruk av diuretika hos en ellers frisk kvinne er upassende og utsetter mor og foster for unødvendig fare. Diuretika forhindrer ikke utvikling av toksemi i svangerskapet, og det er ingen tilfredsstillende bevis for at de er nyttige i behandlingen av utviklet toksemi.
Ødem under graviditet kan oppstå av patologiske årsaker eller fra de fysiologiske og mekaniske konsekvensene av graviditet. Diuretika er indisert under graviditet når ødem skyldes patologiske årsaker, akkurat som de er i fravær av graviditet. Avhengig ødem i svangerskapet som følge av begrensning av venøs retur av den utvidede livmoren behandles riktig gjennom heving av underekstremitetene og bruk av støtteslange; bruk av diuretika for å senke intravaskulært volum i dette tilfellet er ulogisk og unødvendig. Det er hypervolemi under normal graviditet som verken er skadelig for fosteret eller moren (i fravær av kardiovaskulær sykdom), men som er assosiert med ødem, inkludert generalisert ødem hos de fleste gravide kvinner. Hvis dette ødemet gir ubehag, vil økt tilbakelenthet ofte gi lindring. I sjeldne tilfeller kan dette ødemet forårsake ekstremt ubehag som ikke lindres ved hvile. I disse tilfellene kan en kort kur med diuretika gi lindring og kan være aktuelt.
DOSERING OG ADMINISTRASJON
For kontroll av hypertensjon : Voksenstartdosen av MICROZIDE (hydroklortiazidkapsel) er én kapsel gitt én gang daglig enten gitt alene eller i kombinasjon med andre antihypertensiva. Totale daglige doser større enn 50 mg anbefales ikke.
HVORDAN LEVERES
MICROZIDE (hydroklortiazid kapsel) Kapsler er #4 Teal Opaque/Teal Opaque todelte harde gelatinkapsler merket med MICROZIDE (hydroklortiazidkapsel) og 12,5 mg i svart blekk. De leveres i flasker på 100 stk med barnesikre lukkinger ( NDC 52544-622-01).
Dispenser i en tett, lysbestandig beholder som definert i USP.
Oppbevares utilgjengelig for barn.
Oppbevares ved 20°-25°C (68°-77°F). [Se USP kontrollert romtemperatur.] Beskyttes mot lys, fuktighet, frysing, -20°C (-4°F). Hold beholderen tett lukket.
Rett medisinske henvendelser til: WATSON., Medical Communications PO Box 1953, Morristown, NJ 07962-1953. 800-272-5525. Produsert av: Watson Pharma Private Limited. Verna, Salcette, Goa 403 722 INDIA. Distribuert av: Watson Pharma, Inc. Morristown, NJ 07962 USA. Revidert: februar 2011
BIVIRKNINGER
Bivirkningene forbundet med hydroklortiazid har vist seg å være doserelaterte. I kontrollerte kliniske studier var bivirkningene rapportert med doser på 12,5 mg hydroklortiazid én gang daglig sammenlignbare med placebo. Følgende bivirkninger er rapportert for doser av hydroklortiazid 25 mg og mer, og innenfor hver kategori er de oppført i rekkefølgen etter avtagende alvorlighetsgrad.
Kroppen som helhet : Svakhet.
Kardiovaskulær : Hypotensjon inkludert ortostatisk hypotensjon (kan forverres av alkohol, barbiturater, narkotika eller antihypertensiva).
Fordøyelseskanal Pankreatitt, gulsott (intrahepatisk kolestatisk gulsott), diaré, oppkast, sialadenitt, kramper, forstoppelse, mageirritasjon, kvalme, anoreksi.
Hematologisk : Aplastisk anemi, agranulocytose, leukopeni, hemolytisk anemi, trombocytopeni.
Overfølsomhet : Anafylaktiske reaksjoner, nekrotiserende angiitt (vaskulitt og kutan vaskulitt), pustebesvær inkludert pneumonitt og lungeødem, lysfølsomhet, feber, urticaria, utslett, purpura.
Metabolsk : Elektrolyttubalanse (se FORHOLDSREGLER ), hyperglykemi, glykosuri, hyperurikemi.
Muskuloskeletal : Muskelspasme.
Nervesystem/psykiatrisk : Vertigo, parestesi, svimmelhet, hodepine, rastløshet.
Nyre : Nyresvikt, nedsatt nyrefunksjon, interstitiell nefritt (se ADVARSLER ).
Hud : Erythema multiforme inkludert Stevens-Johnsons syndrom, eksfoliativ dermatitt inkludert toksisk epidermal nekrolyse, alopecia.
Spesielle sanser Forbigående tåkesyn, xantopsi.
Urogenital : Impotens.
Når bivirkningene er moderate eller alvorlige, bør tiaziddosen reduseres eller behandlingen seponeres.
NARKOTIKAHANDEL
Når de gis samtidig, kan følgende legemidler interagere med tiaziddiuretika:
Alkohol, barbiturater eller narkotika - potensering av ortostatisk hypotensjon kan forekomme.
Antidiabetiske legemidler - (orale midler og insulin) dosejustering av det antidiabetiske legemidlet kan være nødvendig.
Andre antihypertensiva - additiv effekt eller potensering.
Kolestyramin og kolestipolharpikser – Kolestyramin- og kolestipolharpikser binder hydroklortiazidet og reduserer absorpsjonen fra mage-tarmkanalen med henholdsvis opptil 85 og 43 prosent.
Kortikosteroid, ACTH - intensivert elektrolyttmangel, spesielt hypokalemi.
Pressoraminer (f.eks. noradrenalin) - mulig redusert respons på pressoraminer, men ikke tilstrekkelig til å utelukke bruken av dem.
Skjelettmuskelavslappende midler, ikke-depolariserende (f.eks. tubokurarin) mulig økt respons på muskelavslappende midler.
Litium - bør generelt ikke gis sammen med diuretika. Vanndrivende midler reduserer renal clearance av litium og øker risikoen for litiumtoksisitet betydelig. Se pakningsvedlegget for litiumpreparater før bruk av slike preparater med MICROZIDE (hydroklortiazidkapsel).
Ikke-steroide antiinflammatoriske legemidler - Hos noen pasienter kan administrering av et ikke-steroid antiinflammatorisk middel redusere de vanndrivende, natriuretiske og antihypertensive effektene av loop-, kaliumsparende og tiaziddiuretika. Når MICROZIDE (hydroklortiazidkapsel) og ikke-steroide antiinflammatoriske midler brukes samtidig, bør pasientene observeres nøye for å avgjøre om den ønskede effekten av diuretikaet oppnås.
Interaksjoner med legemiddel/laboratorietest
Tiazider bør seponeres før det utføres tester for biskjoldbruskfunksjon (se FORHOLDSREGLER, Generelt ).
ADVARSLER
Diabetes og hypoglykemi: Latent diabetes mellitus kan bli manifest og diabetikere som får tiazider kan trenge justering av insulindosen.
Nyresykdom: Kumulative effekter av tiazidene kan utvikles hos pasienter med nedsatt nyrefunksjon. Hos slike pasienter kan tiazider utløse azotemi.
FORHOLDSREGLER
Elektrolytt- og væskebalansestatus
I publiserte studier har klinisk signifikant hypokalemi vært konsekvent mindre vanlig hos pasienter som fikk 12,5 mg hydroklortiazid enn hos pasienter som fikk høyere doser. Ikke desto mindre bør periodisk bestemmelse av serumelektrolytter utføres hos pasienter som kan ha risiko for utvikling av hypokalemi. Pasienter bør observeres for tegn på væske- eller elektrolyttforstyrrelser, dvs. hyponatremi, hypokloremisk alkalose og hypokalemi og hypomagnesemi.
Advarselstegn eller symptomer på væske- og elektrolyttubalanse inkluderer munntørrhet, tørste, svakhet, slapphet, døsighet, rastløshet, muskelsmerter eller -kramper, muskeltretthet, hypotensjon, oliguri, takykardi og gastrointestinale forstyrrelser som kvalme og oppkast.
Hypokalemi kan utvikles, spesielt med rask diurese når alvorlig cirrhose er tilstede, ved samtidig bruk av kortikosteroid eller adrenokortikotropt hormon (ACTH) eller etter langvarig behandling. Interferens med tilstrekkelig oralt elektrolyttinntak vil også bidra til hypokalemi. Hypokalemi og hypomagnesemi kan provosere ventrikulære arytmier eller sensibilisere eller overdrive hjertets respons på de toksiske effektene av digitalis. Hypokalemi kan unngås eller behandles med kaliumtilskudd eller økt inntak av kaliumrik mat.
Fortynningshyponatremi er livstruende og kan forekomme hos ødematøse pasienter i varmt vær; passende terapi er vannrestriksjon i stedet for saltadministrasjon, bortsett fra i sjeldne tilfeller når hyponatremien er livstruende. Ved faktisk saltmangel er passende erstatning den foretrukne terapien.
Hyperurikemi
Hyperurikemi eller akutt gikt kan utløses hos enkelte pasienter som får tiaziddiuretika.
Nedsatt leverfunksjon
Tiazider bør brukes med forsiktighet hos pasienter med nedsatt leverfunksjon. De kan utløse leverkoma hos pasienter med alvorlig leversykdom.
Parathyroid sykdom
Kalsiumutskillelse reduseres av tiazider, og patologiske endringer i biskjoldbruskkjertlene, med hyperkalsemi og hypofosfatemi, har blitt observert hos noen få pasienter på langvarig tiazidbehandling.
Karsinogenese, mutagenese, svekkelse av fruktbarhet
To-årige fôringsstudier på mus og rotter utført i regi av National Toxicology Program (NTP) avdekket ingen bevis på et kreftfremkallende potensiale for hydroklortiazid hos hunnmus (ved doser på opptil ca. 600 mg/kg/dag) eller hos hanner. og hunnrotter (ved doser på ca. 100 mg/kg/dag). NTP fant imidlertid tvetydige bevis for hepatokarsinogenitet hos hannmus. Hydroklortiazid var ikke genotoksisk in vitro i Ames-mutagenisitetsanalysen av Salmonella typhimurium-stammer TA 98, TA 100, TA 1535, TA 1537 og TA 1538 og i Chinese Hamster Ovary (CHO)-testen for kromosomavvik ved bruk av vibrasjoner, eller musekimcellekromosomer, benmargskromosomer fra kinesisk hamster og det kjønnsbundne recessive dødelige trekkgenet Drosophila. Positive testresultater ble kun oppnådd i in vitro CHO Sister Chromatid Exchange (klastogenesitet) og i muselymfomcelle (mutagenisitet) assayene, ved bruk av konsentrasjoner av hydroklortiazid fra 43 til 1300 mcg/ml, og i Aspergillus nidulans non-disjunction assay kl. en uspesifisert konsentrasjon.
Hydroklortiazid hadde ingen negative effekter på fertiliteten til mus og rotter av begge kjønn i studier der disse artene ble eksponert, via kosten, for doser på henholdsvis opptil 100 og 4 mg/kg før unnfangelse og gjennom hele svangerskapet.
Svangerskap
Teratogene effekter
Graviditetskategori B: Studier der hydroklortiazid ble administrert oralt til gravide mus og rotter i deres respektive perioder med større organogenese i doser opp til henholdsvis 3000 og 1000 mg hydroklortiazid/kg, ga ingen tegn på skade på fosteret.
Det finnes imidlertid ingen tilstrekkelige og godt kontrollerte studier på gravide kvinner. Fordi reproduksjonsstudier på dyr ikke alltid er prediktive for menneskelig respons, bør dette legemidlet kun brukes under graviditet hvis det er klart nødvendig.
Ikke-ratatogene effekter
Tiazider krysser placentabarrieren og vises i navlestrengsblod. Det er en risiko for føtal eller neonatal gulsott, trombocytopeni og muligens andre bivirkninger som har oppstått hos voksne.
Ammende mødre
Tiazider skilles ut i morsmelk. På grunn av potensialet for alvorlige bivirkninger hos ammende spedbarn, bør det tas en beslutning om å avbryte ammingen eller seponere hydroklortiazid, tatt i betraktning stoffets betydning for moren.
Pediatrisk bruk
Sikkerhet og effektivitet hos pediatriske pasienter er ikke fastslått.
Eldre bruk
En større blodtrykksreduksjon og en økning i bivirkninger kan observeres hos eldre (dvs. > 65 år) med hydroklortiazid. Det anbefales derfor å starte behandlingen med den laveste tilgjengelige dosen av hydroklortiazid (12,5 mg). Hvis ytterligere titrering er nødvendig, bør trinn på 12,5 mg brukes.
OVERDOSE
De vanligste tegnene og symptomene som er observert er de forårsaket av elektrolyttmangel (hypokalemi, hypokloremi, hyponatremi) og dehydrering som følge av overdreven diurese. Hvis digitalis også har blitt administrert, kan hypokalemi fremheve hjertearytmier.
Ved overdosering bør symptomatiske og støttende tiltak brukes. Emesis bør induseres eller mageskylling utføres. Korriger dehydrering, elektrolyttubalanse, leverkoma og hypotensjon ved etablerte prosedyrer. Gi om nødvendig oksygen eller kunstig åndedrett ved åndedrettssvikt. I hvilken grad hydroklortiazid fjernes ved hemodialyse er ikke fastslått.
Den orale LD50 av hydroklortiazid er større enn 10 g/kg hos mus og rotte.
KONTRAINDIKASJONER
Hydroklortiazid er kontraindisert hos pasienter med anuri. Overfølsomhet overfor dette produktet eller andre sulfonamidavledede legemidler er også kontraindisert.
KLINISK FARMAKOLOGI
Hydroklortiazid blokkerer reabsorpsjonen av natrium- og kloridioner, og øker dermed mengden natrium som passerer den distale tubuli og volumet av vann som skilles ut. En del av det ekstra natriumet som presenteres til det distale røret, byttes der ut med kalium- og hydrogenioner. Ved fortsatt bruk av hydroklortiazid og nedbrytning av natrium, har kompenserende mekanismer en tendens til å øke denne utvekslingen og kan gi for stort tap av kalium-, hydrogen- og kloridioner. Hydroklortiazid reduserer også utskillelsen av kalsium og urinsyre, kan øke utskillelsen av jodid og kan redusere glomerulær filtrasjonshastighet. Metabolske toksisiteter assosiert med for store elektrolyttforandringer forårsaket av hydroklortiazid har vist seg å være doserelatert.
Farmakokinetikk og metabolisme
Hydroklortiazid absorberes godt (65 % til 75 %) etter oral administrering. Absorpsjon av hydroklortiazid er redusert hos pasienter med kongestiv hjertesvikt.
Maksimal plasmakonsentrasjon observeres innen 1 til 5 timer etter dosering, og varierer fra 70 til 490 ng/ml etter orale doser på 12,5 til 100 mg. Plasmakonsentrasjoner er lineært relatert til administrert dose. Konsentrasjonene av hydroklortiazid er 1,6 til 1,8 ganger høyere i fullblod enn i plasma. Binding til serumproteiner er rapportert å være omtrent 40 % til 68 %. Plasmaeliminasjonshalveringstiden er rapportert å være 6 til 15 timer. Hydroklortiazid elimineres primært via nyrene. Etter orale doser på 12,5 til 100 mg vises 55 % til 77 % av den administrerte dosen i urinen og mer enn 95 % av den absorberte dosen utskilles i urinen som uendret legemiddel. Hos pasienter med nyresykdom øker plasmakonsentrasjonen av hydroklortiazid og eliminasjonshalveringstiden forlenges.
Når MICROZIDE (hydroklortiazidkapsel) administreres sammen med mat, reduseres biotilgjengeligheten med 10 %, maksimal plasmakonsentrasjon reduseres med 20 %, og tiden til maksimal konsentrasjon øker fra 1,6 til 2,9 timer.
Farmakodynamikk
Akutte antihypertensive effekter av tiazider antas å skyldes reduksjon i blodvolum og hjertevolum, sekundært til en natriuretisk effekt, selv om en direkte vasodilatorisk mekanisme også er foreslått. Ved kronisk administrering går plasmavolumet tilbake til det normale, men perifer vaskulær motstand reduseres. Den nøyaktige mekanismen for den antihypertensive effekten av hydroklortiazid er ikke kjent.
Tiazider påvirker ikke normalt blodtrykk. Virkningen begynner innen 2 timer etter dosering, maksimal effekt observeres etter ca. 4 timer, og aktiviteten vedvarer i opptil 24 timer.
Kliniske studier
en 87 pasienter 4 ukers dobbeltblind, placebokontrollert, parallell gruppestudie, hadde pasienter som fikk MICROZIDE (hydroklortiazidkapsel) reduksjoner i sittende systoliske og diastoliske blodtrykk som var signifikant høyere enn de som ble sett hos pasienter som fikk placebo. I publiserte placebokontrollerte studier som sammenlignet 12,5 mg hydroklortiazid med 25 mg, bevarte 12,5 mg-dosen mesteparten av den placebokorrigerte blodtrykksreduksjonen sett med 25 mg.
PASIENTINFORMASJON
Ingen informasjon gitt. Vennligst referer til ADVARSLER og FORHOLDSREGLER seksjoner.
