Asacol 400mg Mesalamine Bruk, bivirkninger og dosering. Pris i nettapotek. Generisk medisin uten resept.
Hva er Asacol 400mg og hvordan brukes det?
Asacol er et reseptbelagt legemiddel som brukes til å behandle symptomene på ulcerøs kolitt. Asacol 400mg kan brukes alene eller sammen med andre medisiner.
Asacol tilhører en klasse legemidler som kalles 5-aminosalisylsyrederivater.
Det er ikke kjent om Asacol 400mg er trygt og effektivt hos barn under 5 år.
Hva er de mulige bivirkningene av Asacol 400mg?
Asacol kan forårsake alvorlige bivirkninger, inkludert:
- . sterke magesmerter, . magekramper, . blodig diaré, . feber, . hodepine, . hudutslett, . blodig eller tjæreaktig avføring, . hoster opp blod, . oppkast som ser ut som kaffegrut, . lite eller ingen vannlating, . smertefull eller vanskelig vannlating, . hevelse i føttene eller anklene, . føler meg sliten, . kortpustethet, . tap av Appetit, . smerter i øvre mage, . lett blåmerker eller blødninger, . mørk urin, . leirefarget avføring, og . gulfarging av hud eller øyne (gulsott)
Få medisinsk hjelp med en gang hvis du har noen av symptomene nevnt ovenfor.
De vanligste bivirkningene av Asacol inkluderer:
- . kvalme, . oppkast, . magesmerter, . diaré, . fordøyelsesbesvær, . gass, . hodepine, . utslett, og . unormale leverfunksjonstester
Fortell legen dersom du har noen bivirkninger som plager deg eller som ikke går over.
Dette er ikke alle mulige bivirkninger av Asacol. Spør legen din eller apoteket for mer informasjon.
Ring legen din for medisinsk råd om bivirkninger. Du kan rapportere bivirkninger til FDA på 1-800-FDA-1088.
BESKRIVELSE
Hver Asacol (mesalamin) tablett med forsinket frigjøring for oral administrering inneholder 400 mg mesalamin, et aminosalisylat. Asacol (mesalamin) tabletter med forsinket frigjøring inneholder akrylbasert harpiks, Eudragit S (metakrylsyrekopolymer type B, NF), som løses opp ved pH 7 eller høyere og frigjør mesalamin i terminal ileum og utover for topisk anti-inflammatorisk virkning i tykktarmen . Mesalamin (også referert til som 5-aminosalisylsyre eller 5-ASA) har det kjemiske navnet 5-amino-2-hydroksybenzosyre. Dens strukturformel er:
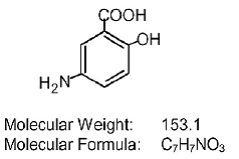
Inaktive ingredienser: Hver tablett inneholder kolloidalt silisiumdioksid, dibutylftalat, spiselig svart blekk, rødt jernoksid, gult jernoksid, laktosemonohydrat, magnesiumstearat, metakrylsyrekopolymer B (Eudragit S), polyetylenglykol, povidon, natriumstivelsesglykolat og talkum.
INDIKASJONER
Behandling av mild til moderat aktiv ulcerøs kolitt
Asacol® (mesalamin) tabletter med forsinket frigjøring er indisert for behandling av mild til moderat aktiv ulcerøs kolitt hos pasienter 5 år og eldre.
Vedlikehold av remisjon av ulcerøs kolitt hos voksne
Asacol (mesalamin) tabletter med forsinket frigjøring er indisert for å opprettholde remisjon av ulcerøs kolitt hos voksne. Sikkerheten og effektiviteten til Asacol for opprettholdelse av remisjon av ulcerøs kolitt hos pediatriske pasienter er ikke fastslått.
DOSERING OG ADMINISTRASJON
Dosering for behandling av mild til moderat aktiv ulcerøs kolitt
Voksne
For voksne er den anbefalte dosen av Asacol 400 mg to 400 mg tabletter som skal tas tre ganger daglig med eller uten mat (total daglig dose på 2,4 gram), i en varighet på 6 uker [se Kliniske studier ].
Pediatri
For pediatriske pasienter er den anbefalte totale daglige dosen av Asacol vektbasert (opptil maksimalt 2,4 gram/dag) (se tabell 1). Asacol 400 mg tabletter skal tas to ganger daglig med eller uten mat i en varighet på 6 uker [se Kliniske studier ].
Dosering for vedlikehold av remisjon av ulcerøs kolitt hos voksne
For voksne er den anbefalte dosen av Asacol 1,6 gram daglig, i delte doser, med eller uten mat [se Kliniske studier ].
Viktige administrasjonsinstruksjoner
Svelg Asacol tabletter hele. Ikke kutt, knekk eller tygg tablettene.
To Asacol 400 mg tabletter har ikke vist seg å være bioekvivalente med én Asacol® HD (mesalamin) 800 mg tablett med forsinket frigjøring og bør ikke brukes om hverandre.
Testing før administrasjon av Asacol 400mg
Evaluer nyrefunksjonen før oppstart av Asacol [se ADVARSLER OG FORHOLDSREGLER ].
HVORDAN LEVERES
Doseringsformer og styrker
Asacol (mesalamin) Tabletter med forsinket frigjøring: 400 mg (rød-brune, kapselformet og merket med "0752 DR" i svart).
Oppbevaring og håndtering
Asacol (mesalamin) tabletter med forsinket frigjøring er tilgjengelig som rødbrune, kapselformede tabletter som inneholder 400 mg mesalamin og merket med "0752 DR" i svart.
NDC 0430-0752-27 Flaske med 180 tabletter
Oppbevares ved 20 ° til 25 ° C (68 ° til 77 ° F); utflukter tillatt 15° til 30° C (59° til 86° F) [Se USP kontrollert romtemperatur ].
Produsert av: Warner Chilcott Deutschland GmbH D-64331 Weiterstadt Tyskland. Markedsført av: Warner Chilcott (US), LLC Rockaway, NJ 07866. Revidert: okt 2013
BIVIRKNINGER
De alvorligste bivirkningene sett i kliniske studier med Asacol eller med andre produkter som inneholder mesalamin eller metaboliseres til mesalamin er:
- . Nedsatt nyrefunksjon, inkludert nyresvikt [se ADVARSLER OG FORHOLDSREGLER ] . Akutt intoleransesyndrom [se ADVARSLER OG FORHOLDSREGLER ] . Overfølsomhetsreaksjoner [se ADVARSLER OG FORHOLDSREGLER ] . Leversvikt [se ADVARSLER OG FORHOLDSREGLER ]
Erfaring fra kliniske forsøk
Fordi kliniske studier utføres under vidt forskjellige forhold, kan bivirkningsrater observert i kliniske studier av et medikament ikke sammenlignes direkte med rater i kliniske studier av et annet medikament og gjenspeiler kanskje ikke hyppighetene observert i praksis.
Totalt har Asacol 400 mg tabletter blitt evaluert hos 2690 pasienter med ulcerøs kolitt i kontrollerte og åpne studier. Bivirkninger presentert i de følgende avsnittene kan forekomme uavhengig av behandlingens lengde, og lignende reaksjoner er rapportert i kort- og langtidsstudier og etter markedsføring.
Kliniske studier som støtter bruk av Asacol 400 mg for behandling av mild til moderat aktiv ulcerøs kolitt inkluderte to 6-ukers, placebokontrollerte, randomiserte, dobbeltblinde studier hos voksne med mild til moderat aktiv ulcerøs kolitt (studier 1 og 2), og en 6-ukers, randomisert, dobbeltblind studie av 2 dosenivåer hos barn med mild til moderat aktiv ulcerøs kolitt. Kliniske studier som støtter bruken av Asacol 400 mg tabletter for å opprettholde remisjon av ulcerøs kolitt inkluderte en 6-måneders, randomisert, dobbeltblind, placebokontrollert, multisenterstudie og fire aktivt kontrollerte vedlikeholdsforsøk som sammenlignet Asacol 400 mg tabletter med sulfasalazin . Asacol 400mg har blitt evaluert hos 427 voksne og 82 barn med ulcerøs kolitt i disse kontrollerte studiene.
Behandling av mild til moderat aktiv ulcerøs kolitt hos voksne
to 6-ukers placebokontrollerte kliniske studier (studier 1 og 2) som involverte 245 pasienter, hvorav 155 ble randomisert til Asacol [se Kliniske studier ], 3,2 prosent av de Asacol-behandlede pasientene avbrøt behandlingen på grunn av bivirkninger sammenlignet med 2,2 prosent av de placebo-behandlede pasientene. Gjennomsnittsalderen for pasientene i studie 1 var 42 år og 48 prosent av pasientene var menn. Gjennomsnittsalderen for pasientene i studie 2 var 42 år og 59 prosent av pasientene var menn. Bivirkninger som førte til seponering fra Asacol inkludert (hver hos én pasient): diaré og kolittoppblussing; svimmelhet, kvalme, leddsmerter og hodepine; utslett, sløvhet og forstoppelse; tørr munn, ubehag, ubehag i korsryggen, mild desorientering, mild fordøyelsesbesvær og kramper; hodepine, kvalme, verking, oppkast, muskelkramper, tett hode, tette ører og feber.
Bivirkninger hos pasienter behandlet med Asacol som forekommer med en frekvens på minst 2 prosent og med en frekvens som er høyere enn placebo i 6 ukers, dobbeltblinde, placebokontrollerte studier (studier 1 og 2) er oppført i tabell 2 nedenfor.
Behandling av mild til moderat aktiv ulcerøs kolitt hos pediatriske pasienter 5 til 17 år gamle
En randomisert, dobbeltblind, 6-ukers studie av 2 dosenivåer av Asacol (studie 3) ble utført hos 82 pediatriske pasienter i alderen 5 til 17 år med mild til moderat aktiv ulcerøs kolitt. Alle pasientene ble delt inn etter kroppsvektkategori (17 til mindre enn 33 kg, 33 til mindre enn 54 kg og 54 til 90 kg) og tilfeldig tildelt en lav dose (1,2, 2,0 og 2,4 g/dag for de respektive kroppsvektkategori) eller en høy dose (2,0, 3,6 og 4,8 g/dag).
Den høye dosen er ikke en godkjent dose fordi den ikke ble funnet å være mer effektiv enn den godkjente dosen [se DOSERING OG ADMINISTRASJON og Kliniske studier ].
Varigheten av eksponering for mesalamin blant de 82 pasientene i studien varierte fra 12 til 50 dager (gjennomsnittlig 40 dager i hver dosegruppe). Flertallet (88 prosent) av pasientene i hver gruppe ble behandlet i mer enn 5 uker. Tabell 3 gir et sammendrag av de spesifikke rapporterte bivirkningene (AR).
Tolv prosent av pasientene i lavdosegruppen og 5 prosent av pasientene i høydosegruppen hadde alvorlige bivirkninger (AR). Ulcerøs kolitt ble rapportert som en alvorlig AR hos ett individ i hver gruppe. Andre alvorlige AR besto av bihulebetennelse, magesmerter, redusert kroppsmasseindeks, adenovirusinfeksjon, blodig diaré, skleroserende kolangitt og pankreatitt hos ett individ hver i lavdosegruppen og anemi og synkope hos ett individ hver i høydosegruppen.
Syv pasienter ble trukket fra studien på grunn av ARs: 5 (12 prosent) i lavdosegruppen (ulcerøs kolitt, adenovirusinfeksjon, skleroserende kolangitt, pankreatitt) og 2 (5 prosent) i høydosegruppen (økt amylase og økt lipase). smerter i øvre del av magen).
Generelt var arten og alvorlighetsgraden av reaksjoner i den pediatriske populasjonen lik de som ble rapportert i voksne populasjoner av pasienter med ulcerøs kolitt.
Vedlikehold av remisjon av ulcerøs kolitt hos voksne
I en 6-måneders placebokontrollert vedlikeholdsstudie som involverte 264 pasienter (studie 4), hvorav 177 ble randomisert til Asacol, avbrøt seks (3,4 prosent) av pasientene som brukte Asacol behandlingen på grunn av bivirkninger, sammenlignet med fire (4,6 prosent) av pasienter som bruker placebo [se Kliniske studier ]. Gjennomsnittsalderen til pasientene i studie 4 var 42 år og 55 prosent av pasientene var menn. Bivirkninger som førte til studieabstinens hos pasienter som bruker Asacol inkluderte (hver hos én pasient): angst; hodepine; kløe; redusert libido; leddgikt; og stomatitt og asteni.
I tillegg til reaksjonene som er oppført i tabell 2, oppsto følgende bivirkninger hos pasienter som brukte Asacol med en frekvens på 2 prosent eller mer i studie 4: abdominal utvidelse, gastroenteritt, gastrointestinal blødning, infeksjon, leddlidelse, migrene, nervøsitet, parestesi, rektal lidelse, rektal blødning, avføringsavvik, tenesmus, urinfrekvens, vasodilatasjon og synsforstyrrelser.
Hos 3342 pasienter i ukontrollerte kliniske studier forekom følgende bivirkninger med en frekvens på 5 prosent eller mer og så ut til å øke i frekvens med økende dose: asteni, feber, influensasyndrom, smerte, magesmerter, ryggsmerter, flatulens, gastrointestinal blødning , artralgi og rhinitt.
Postmarketing-erfaring
I tillegg til bivirkningene rapportert ovenfor i kliniske studier som involverer Asacol, har bivirkningene som er oppført nedenfor blitt identifisert under bruk av Asacol 400mg og andre mesalaminholdige produkter etter godkjenning. Fordi disse reaksjonene rapporteres frivillig fra en populasjon av usikker størrelse, er det ikke alltid mulig å pålitelig estimere frekvensen deres eller etablere en årsakssammenheng med legemiddeleksponering.
Kroppen som helhet: Nakkesmerter, ansiktsødem, ødem, lupuslignende syndrom, medikamentfeber.
Kardiovaskulær: Perikarditt, myokarditt [se ADVARSLER OG FORHOLDSREGLER ].
Gastrointestinale: Anoreksi, pankreatitt, gastritt, økt appetitt, kolecystitt, munntørrhet, munnsår, perforert magesår blodig diaré.
Hematologisk: Agranulocytose aplastisk anemi, trombocytopeni, eosinofili, leukopeni, anemi, lymfadenopati.
Muskuloskeletal: Gikt.
Nervøs: Depresjon, somnolens, emosjonell labilitet, hyperestesi, svimmelhet, forvirring, skjelving, perifer nevropati, tverrgående myelitt, Guillain-Barré syndrom.
Nyre: Nyresvikt, interstitiell nefritis, minimal change nefropati [se ADVARSLER OG FORHOLDSREGLER ].
Luftveier/lunge: Eosinofil pneumoni, interstitiell pneumonitt, astmaforverring, pleuritt.
Hud: Alopecia, psoriasis, pyoderma gangrenosus, tørr hud, erythema nodosum, urticaria.
Spesielle sanser: Øyesmerter, smaksperversjon, tåkesyn, tinnitus.
Urogenital: Dysuri, urintrang, hematuri, epididymitt, menoragi, reversibel oligospermi.
Laboratorieavvik: Forhøyet AST (SGOT) eller ALT (SGPT), forhøyet alkalisk fosfatase, forhøyet GGT, forhøyet LDH, forhøyet bilirubin, forhøyet serumkreatinin og BUN.

NARKOTIKAHANDEL
Ingen formelle legemiddelinteraksjonsstudier er utført med Asacol 400mg med andre legemidler. Imidlertid er følgende interaksjoner mellom produkter som inneholder mesalamin og andre legemidler rapportert.
Nefrotoksiske midler, inkludert ikke-steroide antiinflammatoriske legemidler
Samtidig bruk av mesalamin med kjente nefrotoksiske midler, inkludert ikke-steroide antiinflammatoriske legemidler (NSAIDs) kan øke risikoen for nyrereaksjoner [se ADVARSLER OG FORHOLDSREGLER ].
Azatioprin eller 6-merkaptopurin
Samtidig bruk av mesalamin og azatioprin eller 6-merkaptopurin kan øke risikoen for blodsykdommer.
ADVARSLER
Inkludert som en del av FORHOLDSREGLER seksjon.
FORHOLDSREGLER
Nedsatt nyrefunksjon
Nedsatt nyrefunksjon, inkludert nefropati med minimal forandring, akutt og kronisk interstitiell nefritis og nyresvikt, er rapportert hos pasienter som tar produkter som Asacol 400 mg som inneholder mesalamin eller som er omdannet til mesalamin.
Det anbefales at pasienter har en evaluering av nyrefunksjonen før oppstart av Asacol 400 mg og med jevne mellomrom under behandling.
Forskrivere bør nøye vurdere risikoen og fordelene ved bruk av Asacol hos pasienter med kjent nedsatt nyrefunksjon eller historie med nyresykdom [se NARKOTIKAHANDEL og Ikke-klinisk toksikologi ].
Mesalamin-indusert akutt intoleransesyndrom
Mesalamin har vært assosiert med et akutt intoleransesyndrom som kan være vanskelig å skille fra en forverring av ulcerøs kolitt. Selv om den nøyaktige frekvensen av forekomsten ikke er bestemt, har den forekommet i 3 prosent av kontrollerte kliniske studier av mesalamin eller sulfasalazin. Symptomer inkluderer kramper, magesmerter, blodig diaré, og noen ganger feber, hodepine og utslett. Observer pasienter nøye for forverring av disse symptomene mens de er på behandling. Ved mistanke om akutt intoleransesyndrom, avbryt behandlingen med Asacol umiddelbart.
Overfølsomhetsreaksjoner
Noen pasienter som har opplevd en overfølsomhetsreaksjon overfor sulfasalazin kan ha en lignende reaksjon som Asacol 400 mg eller andre forbindelser som inneholder eller omdannes til mesalamin.
Mesalamin-induserte hjerteoverfølsomhetsreaksjoner (myokarditt og perikarditt) er rapportert med Asacol og andre mesalaminmedisiner. Forsiktighet bør utvises ved forskrivning av dette legemidlet til pasienter med tilstander som disponerer dem for utvikling av myokarditt eller perikarditt.
Leversvikt
Det har vært rapporter om leversvikt hos pasienter med eksisterende leversykdom som har fått mesalamin. Forsiktighet bør utvises ved administrering av Asacol til pasienter med leversykdom.
Langvarig gastrisk retensjon hos pasienter med øvre gastrointestinal obstruksjon
Organisk eller funksjonell obstruksjon i den øvre mage-tarmkanalen kan forårsake forlenget mageretensjon av Asacol 400 mg som vil forsinke frigjøring av mesalamin i tykktarmen.
Ikke-klinisk toksikologi
Karsinogenese, mutagenese, svekkelse av fruktbarhet
Karsinogenese
Mesalamin var ikke kreftfremkallende ved diettdoser på opptil 480 mg/kg/dag hos rotter og 2000 mg/kg/dag hos mus, som er omtrent 2,9 og 6,1 ganger den maksimale anbefalte vedlikeholdsdosen av Asacol 400 mg på 1,6 g/dag eller 26,7 mg/kg/dag, basert på henholdsvis 60 kg kroppsvekt, basert på kroppsoverflate.
Mutagenese
Mesalamin var negativ i Ames-analysen for mutagenese, negativ for induksjon av søsterkromatidutvekslinger (SCE) og kromosomavvik i eggstokkceller fra kinesisk hamster in vitro, og negativ for induksjon av mikrokjerner (MN) i polykromatiske erytrocytter av benmarg hos mus.
Nedsatt fertilitet
Mesalamin, ved orale doser opptil 480 mg/kg/dag (ca. 1,9 ganger anbefalt human behandlingsdose på basis av kroppsoverflate), ble funnet å ikke ha noen effekt på fertilitet eller reproduksjonsevne hos hann- og hunnrotter.
Bruk i spesifikke populasjoner
Svangerskap
Graviditetskategori C
Risikosammendrag
Det er ingen tilstrekkelige og godt kontrollerte studier av bruk av Asacol 400mg hos gravide kvinner. Begrensede publiserte humane data om mesalamin viser ingen økning i den totale frekvensen av medfødte misdannelser. Noen data viser en økt frekvens av prematur fødsel, dødfødsel og lav fødselsvekt; Imidlertid er disse ugunstige graviditetsutfallene også assosiert med aktiv inflammatorisk tarmsykdom. Videre har alle svangerskap, uavhengig av medikamenteksponering, en bakgrunnsrate på 2 til 4 prosent for store misdannelser, og 15 til 20 prosent for svangerskapstap. Ingen bevis for fosterskade ble observert i reproduksjonsstudier på dyr av mesalamin hos rotter og kaniner ved orale doser omtrent 1,9 ganger (rotte) og 3,9 ganger (kanin) den anbefalte dosen til mennesker. Dibutylftalat (DBP) er imidlertid en inaktiv ingrediens i Asacols enteriske belegg, og i dyrestudier på rotter ved doser som er større enn 190 ganger dosen hos mennesker basert på kroppsoverflate, var mors DBP assosiert med eksterne misdannelser og skjelettmisdannelser og uønskede effekter på det mannlige reproduktive systemet. Asacol 400mg skal kun brukes under graviditet hvis den potensielle fordelen rettferdiggjør den potensielle risikoen for fosteret.
Menneskelige data
Mesalamin krysser morkaken. I prospektive og retrospektive studier av over 600 kvinner eksponert for mesalamin under graviditet, var den observerte frekvensen av medfødte misdannelser ikke økt over bakgrunnsfrekvensen i den generelle befolkningen. Noen data viser økt forekomst av prematur fødsel, dødfødsel og lav fødselsvekt, men det er uklart om dette skyldtes underliggende morssykdom, medikamenteksponering eller begge deler, da aktiv inflammatorisk tarmsykdom også er assosiert med ugunstige graviditetsutfall.
Dyredata
Reproduksjonsstudier med mesalamin ble utført under organogenese hos rotter og kaniner ved orale doser opptil 480 mg/kg/dag. Det var ingen tegn på nedsatt fertilitet eller skade på fosteret. Disse mesalamindosene var omtrent 1,9 ganger (rotte) og 3,9 ganger (kanin) den anbefalte dosen til mennesker, basert på kroppsoverflate.
Dibutylftalat (DBP) er en inaktiv ingrediens i Asacols enteriske belegg. Menneskets daglige inntak av DBP fra den maksimale anbefalte dosen av Asacol-tabletter er ca. 21 mg. Publiserte rapporter om rotter viser at avkom av hannrotter som er eksponert in utero for DBP (større enn eller lik 100 mg/kg/dag, omtrent 39 ganger den menneskelige dosen basert på kroppsoverflate), viser reproduksjonssystemavvik som er forenlige med forstyrrelse av androgene avhengige. utvikling. Den kliniske betydningen av dette funnet hos rotter er ukjent. Ved høyere doser (større enn eller lik 500 mg/kg/dag, omtrent 194 ganger human dose basert på kroppsoverflate), reduseres tilleggseffekter, inkludert kryptorkisme, hypospadier, atrofi eller agenesis av kjønnsorganer, testikkelskade, daglig. sædproduksjon, permanent retensjon av brystvortene og redusert anogenital avstand er notert. Kvinnelige avkom er upåvirket. Høye doser av DBP, administrert til gravide rotter var assosiert med økt forekomst av utviklingsavvik, slik som ganespalte (større enn eller lik 630 mg/kg/dag, omtrent 244 ganger human dose, basert på kroppsoverflate) og skjelett abnormiteter (større enn eller lik 750 mg/kg/dag, ca. 290 ganger human dose basert på kroppsoverflate) hos avkommet.
Ammende mødre
Mesalamin og dets N-acetylmetabolitt finnes i morsmelk. I publiserte laktasjonsstudier varierte maternelle mesalamindoser fra ulike orale og rektale formuleringer og produkter fra 500 mg til 3 g daglig. Konsentrasjonen av mesalamin i melk varierte fra ikke-påviselig til 0,11 mg/L. Konsentrasjonen av N-acetyl-5-aminosalisylsyremetabolitten varierte fra 5 til 18,1 mg/L. Basert på disse konsentrasjonene er estimerte daglige doser for spedbarn for et spedbarn som kun ammes 0 til 0,017 mg/kg/dag mesalamin og 0,75 til 2,72 mg/kg/dag N-acetyl-5-aminosalisylsyre.
Dibutylftalat (DBP), en inaktiv ingrediens i det enteriske belegget til Asacol 400 mg tabletter, og dets primære metabolitt monobutylftalat (MBP) skilles ut i morsmelk. Den kliniske betydningen av dette er ikke fastslått.
De utviklingsmessige og helsemessige fordelene ved amming bør vurderes sammen med morens kliniske behov for Asacol 400mg og eventuelle potensielle bivirkninger på det ammede barnet fra stoffet eller fra den underliggende morens tilstand. Vær forsiktig når Asacol 400 mg gis til en ammende kvinne.
Pediatrisk bruk
Sikkerheten og effektiviteten til Asacol 400 mg hos pediatriske pasienter i alderen 5 til 17 år for behandling av mild til moderat aktiv ulcerøs kolitt er fastslått over en 6-ukers periode. Bruk av Asacol i disse aldersgruppene støttes av bevis fra tilstrekkelige og godt kontrollerte studier av Asacol 400 mg hos voksne og en enkelt studie hos pediatriske pasienter [se BIVIRKNINGER , KLINISK FARMAKOLOGI og Kliniske studier ].
Asacol 400 mg ble studert i en randomisert, dobbeltblind, parallellgruppe, 6-ukers behandlingsstudie av to dosenivåer av Asacol 400 mg hos 82 pediatriske pasienter i alderen 5 til 17 år med mild til moderat aktiv ulcerøs kolitt. Alle pasienter ble delt inn etter vektkategori (17 til mindre enn 33 kg, 33 til mindre enn 54 kg og 54 til 90 kg) og tilfeldig tildelt en lav dose (1,2, 2,0 og 2,4 g/dag for den respektive vekten) kategori) eller en høy dose (2,0, 3,6 og 4,8 g/dag). Baseline- og screeningbesøk ble fulgt av en behandlingsperiode på 6 uker [se DOSERING OG ADMINISTRASJON ]. Den høye dosen var ikke mer effektiv enn den lave dosen og er ikke en godkjent dosering [se Kliniske studier ].
Sikkerheten og effekten av Asacol hos pediatriske pasienter under 5 år er ikke fastslått. Sikkerheten og effektiviteten til Asacol i vedlikehold av remisjon av ulcerøs kolitt hos pediatriske pasienter er ikke fastslått.
Geriatrisk bruk
Kliniske studier av Asacol inkluderte ikke tilstrekkelig antall forsøkspersoner i alderen 65 år og over til å avgjøre om de responderer annerledes enn yngre forsøkspersoner. Annen rapportert klinisk erfaring har ikke identifisert forskjeller i respons mellom eldre og yngre pasienter. Generelt bør den høyere frekvensen av nedsatt lever-, nyre- eller hjertefunksjon og samtidig sykdom eller annen medikamentell behandling hos eldre pasienter vurderes ved forskrivning av Asacol. Rapporter fra ukontrollerte kliniske studier og rapporteringssystemer etter markedsføring tyder på en høyere forekomst av bloddyskrasier, det vil si agranulocytose, nøytropeni, pancytopeni, hos personer som får Asacol og som er 65 år eller eldre. Forsiktighet bør utvises for å overvåke antall blodceller nøye under behandling med Asacol.
Nedsatt nyrefunksjon
Mesalamin er kjent for å bli vesentlig utskilt av nyrene, og risikoen for toksiske reaksjoner på dette legemidlet kan være større hos pasienter med nedsatt nyrefunksjon. Fordi det er mer sannsynlig at eldre pasienter har nedsatt nyrefunksjon, bør det utvises forsiktighet ved forskrivning av denne medikamentelle behandlingen. Det anbefales at alle pasienter har en evaluering av nyrefunksjonen før oppstart av Asacol-behandling og med jevne mellomrom mens de er på Asacol-behandling [se DOSERING OG ADMINISTRASJON , ADVARSLER OG FORHOLDSREGLER ].
OVERDOSE
Det finnes ingen spesifikk motgift for overdosering av mesalamin, og behandling for mistanke om akutt alvorlig toksisitet med Asacol bør være symptomatisk og støttende. Dette kan omfatte forebygging av ytterligere absorpsjon i mage-tarmkanalen, korrigering av væskeelektrolytt-ubalanse og vedlikehold av tilstrekkelig nyrefunksjon. Asacol 400mg er et pH-avhengig produkt med forsinket frigjøring, og denne faktoren bør vurderes ved behandling av en mistenkt overdose.
KONTRAINDIKASJONER
Asacol er kontraindisert hos pasienter med kjent overfølsomhet overfor salisylater eller aminosalisylater eller overfor noen av ingrediensene i Asacol [se ADVARSLER OG FORHOLDSREGLER , BIVIRKNINGER , og BESKRIVELSE ].
ASACOL (mesalamin) tabletter med forsinket frigjøring, til oral bruk
KLINISK FARMAKOLOGI
Virkningsmekanismen
Virkningsmekanismen til mesalamin er ukjent, men ser ut til å være aktuell snarere enn systemisk. Slimhinneproduksjonen av arakidonsyremetabolitter, både gjennom cyklooksygenasebanene, det vil si prostanoider, og gjennom lipoksygenasebanene, det vil si leukotriener og hydroxyeicosatetraensyrer, økes hos pasienter med kronisk ulcerøs kolitt, og det er mulig at mesalamin reduserer betennelse. blokkerer cyklooksygenase og hemmer prostaglandinproduksjonen i tykktarmen.
Farmakokinetikk
Absorpsjon
Omtrent 28 prosent av mesalamin i Asacol 400mg tabletter absorberes etter oralt inntak. Absorpsjon av mesalamin er lik hos fastende og matede personer. T max for mesalamin og dets metabolitt er vanligvis forsinket, noe som gjenspeiler forsinket frigjøring, og varierer fra 4 til 16 timer.
Metabolisme
Det absorberte mesalaminet acetyleres raskt i tarmslimhinneveggen og av leveren til N-acetyl-5aminosalisylsyre.
Utskillelse
Absorbert mesalamin skilles hovedsakelig ut av nyrene som N-acetyl-5-aminosalisylsyre. Uabsorbert mesalamin skilles ut i avføring.
Etter intravenøs administrering er eliminasjonshalveringstiden for mesalamin rapportert å være ca. 40 minutter. Etter oral dosering er de terminale t½-verdiene for mesalamin og N-acetyl-5-aminosalisylsyre vanligvis ca. 12 timer, men varierer fra 2 til 15 timer. Det er en stor variasjon mellom individer og intra-individer i plasmakonsentrasjonene av mesalamin og N-acetyl-5aminosalisylsyre og i deres eliminasjonshalveringstider etter administrering av Asacol.
Spesifikke populasjoner
Pediatriske pasienter
I en PK-studie som evaluerer 30, 60 og 90 mg/kg/dag doser av Asacol 400 mg administrert to ganger daglig i fire uker, varierte de gjennomsnittlige Cavg-verdiene for mesalamin hos pediatriske ulcerøs kolittpasienter fra omtrent 400 ng/ml til 2100 ng /ml basert på data fra alle dosenivåer.
en studie på pediatriske ulcerøs kolittpasienter (studie 3) var gjennomsnittlig plasmakonsentrasjon av mesalamin (basert på sparsom prøvetaking) 820 til 988 ng/ml ved det lave dosenivået (det vil si 1,2, 2,0 eller 2,4 g/dag basert på kroppsvektlag på henholdsvis 17 til mer enn 33 kg, 33 til mindre enn 54 kg og 54 til mindre enn 90 kg).
Dyretoksikologi og/eller farmakologi
I dyrestudier (rotter, mus, hunder) var nyrene det viktigste organet for toksisitet. (I det følgende er sammenligninger av dyredosering med anbefalt dosering basert på kroppsoverflate og en dose på 2,4 g/dag for en person på 60 kg.)
Mesalamin forårsaker nyrepapillær nekrose hos rotter ved enkeltdoser på ca. 750 mg/kg til 1000 mg/kg (omtrent 3 til 4 ganger anbefalt human dose basert på kroppsoverflate). Doser på 170 og 360 mg/kg/dag (omtrent 0,7 og 1,5 ganger anbefalt human dose basert på kroppsoverflate) gitt til rotter i seks måneder ga papillær nekrose, papillært ødem, tubulær degenerasjon, tubulær mineralisering og urotelial hyperplasi.
Hos mus ga orale doser på 4000 mg/kg/dag mesalamin (ca. 8 ganger anbefalt human dose basert på kroppsoverflate) i tre måneder tubulær nefrose, multifokal/diffus tubulo-interstitiell betennelse og multifokal/diffus papillær nekrose.
Hos hunder resulterte enkeltdoser på 6000 mg (omtrent 8 ganger den anbefalte dosen til mennesker basert på kroppsoverflate) av mesalamintabletter med forsinket frigivelse i nyrepapillær nekrose, men var ikke dødelig. Nyreforandringer har forekommet hos hunder som har fått kronisk administrering av mesalamin i doser på 80 mg/kg/dag (1,1 ganger anbefalt dose til mennesker basert på kroppsoverflate).
Kliniske studier
Behandling av mild til moderat aktiv ulcerøs kolitt
Voksne
To placebokontrollerte studier (studier 1 og 2) har vist effekten av Asacol-tabletter hos pasienter med mild til moderat aktiv ulcerøs kolitt.
en randomisert, dobbeltblind, multisenterstudie med 158 pasienter (studie 1), ble Asacol-doser på 1,6 g/dag og 2,4 g/dag i 6 uker sammenlignet med placebo. Poengsystemet for bestemmelse av behandlingseffektivitet inkluderte vurdering av avføringsfrekvens, rektal blødning, sigmoidoskopiske funn, pasientens funksjonsvurdering og en global vurdering av legen. Ved dosen 2,4 g/dag viste 21 av 43 (49 prosent) pasienter som brukte Asacol-tabletter en forbedring i sigmoidoskopisk utseende av tarmen sammenlignet med 12 av 44 (27 prosent) pasienter som brukte placebo (p = 0,048). I tillegg viste signifikant flere pasienter i gruppen Asacol tabletter 2,4 g/dag bedring i rektal blødning og avføringsfrekvens. Dosen på 1,6 g/dag ga ikke konsistente bevis på effektivitet.
en andre randomisert, dobbeltblind, placebokontrollert klinisk studie med 6 ukers varighet hos 87 pasienter (studie 2), resulterte Asacol-tabletter i en dose på 4,8 g/dag i 6 uker i sigmoidoskopisk forbedring hos 28 av 38 (74 prosent) pasienter sammenlignet med 10 av 38 (26 prosent) placebopasienter (p mindre enn 0,001). Også flere pasienter i gruppen Asacol 400 mg tabletter 4,8 g/dag enn placebogruppen viste forbedring i generelle symptomer.
Dosen på 4,8 g/dag er ikke en godkjent dosering for behandling av mild til moderat aktiv ulcerøs kolitt.
Pediatri
Sikkerheten og effektiviteten til Asacol 400 mg hos pediatriske pasienter i alderen 5 til 17 år for behandling av mild til moderat aktiv ulcerøs kolitt støttes av bevis fra tilstrekkelige og godt kontrollerte studier av Asacol 400 mg hos voksne og en enkelt studie hos pediatriske pasienter.
En randomisert, dobbeltblind, 6-ukers studie av 2 dosenivåer av Asacol (studie 3) ble utført hos 82 pediatriske pasienter i alderen 5 til 17 år med mild eller moderat aktiv ulcerøs kolitt. Alle pasienter ble delt inn etter vektkategori (17 til mindre enn 33 kg, 33 til mindre enn 54 kg og 54 til 90 kg) og tilfeldig tildelt en lav dose (1,2, 2,0 og 2,4 g/dag for den respektive vekten) kategori) eller en høy dose (2,0, 3,6 og 4,8 g/dag). Doser ble administrert hver 12. time.
Andelen pasienter som oppnådde suksess basert på Truncated Mayo Score (TM-Mayo) (basert på avføringsfrekvensen og rektal blødningssubscore av Mayo Score) og basert på Pediatric Ulcerative Colitis Activity Index (PUCAI) (som inkluderte vurdering av magesmerter, rektal blødning, konsistens og frekvens av avføring, tilstedeværelse av nattlig avføring og aktivitetsnivå) ble målt etter 6 ukers behandling. Suksess basert på TM-Mayo ble definert som enten delvis respons (forbedring fra baseline i avføringsfrekvens eller rektal blødningssubscore uten forverring i den andre) eller fullstendig respons (både avføringsfrekvens og rektal blødningssubscore lik 0). Suksess basert på PUCAI ble definert som enten delvis respons (PUCAI-reduksjon på større enn eller lik 20 poeng fra baseline til uke 6 med uke 6-score større enn eller lik 10) eller fullstendig respons (PUCAI mindre enn 10 ved uke 6).
Det var 41 pasienter i lavdosegruppen og 41 pasienter i høydosegruppen som fikk minst én dose Asacol; 36 pasienter i hver dosegruppe fullførte studien. Pasienter ble ansett som mislykkede behandlinger hvis de ikke oppnådde suksess eller droppet ut på grunn av bivirkning eller manglende effekt.
Ved uke 6 oppnådde 73,2 prosent av pasientene i lavdosegruppen og 70,0 prosent av pasientene i høydosegruppen suksess basert på TM-Mayo; 34,1 prosent av pasientene i lavdosegruppen og 42,5 prosent av pasientene i høydosegruppen oppnådde fullstendig respons. Ved uke 6 oppnådde 56,1 prosent av pasientene i lavdosegruppen og 55,0 prosent av pasientene i høydosegruppen suksess basert på PUCAI; 46,3 prosent av pasientene i lavdosegruppen og 42,5 prosent av pasientene i høydosegruppen oppnådde fullstendig respons.
Den høye dosen var ikke mer effektiv enn den lave dosen og er ikke en godkjent dosering [se DOSERING OG ADMINISTRASJON ].
Vedlikehold av remisjon av ulcerøs kolitt hos voksne
En 6-måneders, randomisert, dobbeltblind, placebokontrollert, multisenterstudie (studie 4) involverte 264 pasienter behandlet med Asacol 400 mg tabletter 0,8 g/dag (n = 90), 1,6 g/dag (n = 87) , eller placebo (n = 87). I 0,8 g/dag-armen ble pasientene dosert to ganger daglig; i 1,6 g/dag-armen ble pasientene dosert fire ganger daglig. Andelen pasienter behandlet med 0,8 g/dag som opprettholdt endoskopisk remisjon var ikke statistisk signifikant sammenlignet med placebo. Andelen pasienter som brukte Asacol tabletter 1,6 g/dag som opprettholdt endoskopisk remisjon av ulcerøs kolitt var hos 61 av 87 (70,1 prosent) sammenlignet med 42 av 87 (48,3 prosent) av placebopasientene (p = 0,005).
En samlet effektanalyse av 4 vedlikeholdsstudier sammenlignet Asacol 400 mg tabletter, i doser på 0,8 g/dag til 2,8 g/dag, i delte doser fra to ganger daglig til fire ganger daglig, med sulfasalazin, i doser på 2 g/dag til 4 g/dag. Behandlingssuksess ble sett hos 59 av 98 (59 prosent) pasienter som brukte Asacol-tabletter og 70 av 102 (69 prosent) av pasientene som brukte sulfasalazin, en ikke-signifikant forskjell.
PASIENTINFORMASJON
- . Instruer pasientene til å svelge Asacol-tabletter hele, og pass på at de ikke brytes, kuttes eller tygges, fordi belegget er en viktig del av formuleringen med forsinket frigjøring. . Informer pasienter om at hvis de bytter fra en tidligere oral mesalaminbehandling til Asacol, bør de avbryte sin tidligere orale mesalaminbehandling og følge doseringsinstruksjonene for Asacol. Informer pasientene om at de ikke skal erstatte to Asacol 400 mg tabletter med en Asacol 400mg HD 800 mg tablett [se DOSERING OG ADMINISTRASJON ]. . Informer pasienter om at intakte, delvis intakte og/eller tablettskall er rapportert i avføringen. Instruer pasienter om å kontakte legen sin hvis dette skjer gjentatte ganger. . Instruer pasienter om å beskytte Asacol 400 mg tabletter mot fuktighet. Instruer pasientene om å lukke beholderen tett og la eventuelle tørkemiddelposer være i flasken sammen med tablettene. . Informer kvinner som er gravide, ammer eller er i fertil alder at Asacol 400 mg inneholder dibutylftalat, som var assosiert med misdannelser og negative effekter på det mannlige reproduksjonssystemet i dyrestudier. Dibutylftalat skilles ut i morsmelk.
