Naprosyn 250mg, 500mg Naproxen Bruk, bivirkninger og dosering. Pris i nettapotek. Generisk medisin uten resept.
Hva er Naprosyn 500mg og hvordan brukes det?
Naprosyn 250mg er et reseptbelagt legemiddel som brukes til å behandle symptomer på smerte eller betennelse forårsaket av leddgikt, ankyloserende spondylitt, senebetennelse, bursitt, gikt eller menstruasjonssmerter. Naprosyn kan brukes alene eller sammen med andre medisiner.
Naprosyn 250mg er en ikke-steroid antiinflammatorisk medisin (NSAID).
Det er ikke kjent om Naprosyn er trygt og effektivt hos barn under 2 år.
Hva er de mulige bivirkningene av Naprosyn?
Naprosyn kan forårsake alvorlige bivirkninger, inkludert:
- . kortpustethet, . hevelse eller rask vektøkning, . hudutslett eller blemmer, . blodig eller tjæreaktig avføring, . hoste opp blod eller oppkast som ser ut som kaffegrut, . kvalme, . smerter i øvre mage, . tap av Appetit, . mørk urin, . leirefarget avføring, . gulfarging av hud eller øyne (gulsott), . lite eller ingen vannlating, . smertefull vannlating, . hevelse i føttene eller anklene, . anemi (lavt antall røde blodlegemer), . blek hud, . tretthet, . føler seg svimmel, og . kalde hender eller føtter
Få medisinsk hjelp med en gang hvis du har noen av symptomene nevnt ovenfor.
De vanligste bivirkningene av Naprosyn inkluderer:
- . hodepine, . fordøyelsesbesvær, . halsbrann, og . influensasymptomer
Fortell legen dersom du har noen bivirkninger som plager deg eller som ikke går over.
Dette er ikke alle mulige bivirkninger av Naprosyn. Spør legen din eller apoteket for mer informasjon.
Ring legen din for medisinsk råd om bivirkninger. Du kan rapportere bivirkninger til FDA på 1-800-FDA-1088.
ADVARSEL
RISIKO FOR ALVORLIG HJERTE- OG GASTROINTESTINALE HENDELSER
Kardiovaskulære trombotiske hendelser
- . Ikke-steroide antiinflammatoriske legemidler (NSAIDs) forårsaker økt risiko for alvorlige kardiovaskulære trombotiske hendelser, inkludert hjerteinfarkt og hjerneslag, som kan være dødelige. Denne risikoen kan oppstå tidlig i behandlingen og kan øke med varigheten av bruken [se ADVARSLER OG FORHOLDSREGLER]. . NAPROSYN tabletter, EC-NAPROSYN og ANAPROX DS er kontraindisert i forbindelse med koronar bypassoperasjon (CABG) [se KONTRAINDIKASJONER, ADVARSLER OG FORHOLDSREGLER].
Gastrointestinal blødning, sårdannelse og perforering
- . NSAIDs forårsaker økt risiko for alvorlige gastrointestinale (GI) bivirkninger, inkludert blødning, sårdannelse og perforering av mage eller tarm, som kan være dødelig. Disse hendelsene kan oppstå når som helst under bruk og uten varselsymptomer. Eldre pasienter og pasienter med tidligere magesårsykdom og/eller GI-blødninger har større risiko for alvorlige GI-hendelser [se ADVARSLER OG FORHOLDSREGLER].
BESKRIVELSE
NAPROSYN (naproxen) tabletter, EC-NAPROSYN (naproxen) tabletter med forsinket frigivelse og ANAPROX DS (naproxen natrium) tabletter er ikke-steroide antiinflammatoriske legemidler tilgjengelig som følger: NAPROSYN 250 mg tabletter er tilgjengelige som gule tabletter som inneholder 500 mg naproxen for oral administrering .
EC-NAPROSYN tabletter med forsinket frigivelse er tilgjengelig som enterisk belagte hvite tabletter som inneholder 375 mg naproksen eller 500 mg naproksen for oral administrering.
ANAPROX DS tabletter er tilgjengelige som mørkeblå tabletter som inneholder 550 mg naproxennatrium for oral administrering.
Naproxen er et propionsyrederivat relatert til aryleddiksyregruppen av ikke-steroide antiinflammatoriske legemidler. De kjemiske navnene for naproksen og naproksennatrium er henholdsvis (S)-6-metoksy-a-metyl-2-naftaleneddiksyre og (S)-6metoksy-a-metyl-2-naftaleneddiksyre, natriumsalt. Naproxen har en molekylvekt på 230,26 og en molekylformel på C14H14O3. Naproxennatrium har en molekylvekt på 252,23 og en molekylformel på C14H13NaO3. Naproxen og naproxennatrium har henholdsvis følgende strukturer:
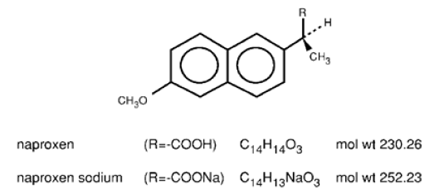
Naproxen er et luktfritt, hvitt til off-white krystallinsk stoff. Det er lipidløselig, praktisk talt uløselig i vann ved lav pH og fritt løselig i vann ved høy pH. Oktanol/vann-fordelingskoeffisienten til naproxen ved pH 7,4 er 1,6 til 1,8. Naproxennatrium er et hvitt til kremhvitt, krystallinsk fast stoff, fritt løselig i vann ved nøytral pH.
De inaktive ingrediensene i NAPROSYN 250 mg tabletter inkluderer: kroskarmellosenatrium, jernoksider, povidon og magnesiumstearat.
De inaktive ingrediensene i EC-NAPROSYN tabletter med forsinket frigivelse inkluderer: kroskarmellosenatrium, povidon og magnesiumstearat. Den enteriske beleggdispersjonen inneholder metakrylsyrekopolymer, talkum, trietylsitrat, natriumhydroksid og renset vann. Påtrykket på nettbrettene er svart blekk. Oppløsningen av denne enterisk belagte naproksen-tabletten er pH-avhengig med rask oppløsning over pH 6. Det er ingen oppløsning under pH 4.
De inaktive ingrediensene i ANAPROX DS tabletter inkluderer: magnesiumstearat, mikrokrystallinsk cellulose, povidon og talkum. Beleggssuspensjonen kan inneholde hydroksypropylmetylcellulose 2910, Opaspray K-1-4227, polyetylenglykol 8000 eller Opadry YS-1-4216.
INDIKASJONER
NAPROSYN 500mg tabletter, EC-NAPROSYN 250mg og ANAPROX DS er indisert for:
lindring av tegn og symptomer på:
- . leddgikt . slitasjegikt . ankyloserende spondylitt . Polyartikulær juvenil idiopatisk artritt
NAPROSYN tabletter og ANAPROX DS er også indisert for:
lindring av tegn og symptomer på:
- . senebetennelse . bursitt . akutt gikt
ledelsen av:
- . smerte . primær dysmenoré
DOSERING OG ADMINISTRASJON
Generelle doseringsinstruksjoner
Vurder nøye de potensielle fordelene og risikoene ved NAPROSYN tabletter, EC-NAPROSYN og ANAPROX DS og andre behandlingsalternativer før du bestemmer deg for å bruke NAPROSYN 250mg tabletter, EC-NAPROSYN 500mg og ANAPROX DS. Bruk den laveste effektive dosen for den korteste varigheten i samsvar med individuelle pasientbehandlingsmål [se ADVARSLER OG FORHOLDSREGLER ].
Etter å ha observert responsen på innledende behandling med NAPROSYN 250mg tabletter, EC-NAPROSYN 500mg eller ANAPROX DS, bør dosen og frekvensen justeres for å passe den individuelle pasientens behov.
For å opprettholde integriteten til det enteriske belegget, bør EC-NAPROSYN tabletten ikke knuses, knuses eller tygges under inntak.
Naproksenholdige produkter som NAPROSYN 500mg, EC-NAPROSYN 250mg og ANAPROX DS og andre naproksenprodukter bør ikke brukes samtidig siden de alle sirkulerer i plasma som naproksenanion.
Revmatoid artritt, slitasjegikt og ankyloserende spondylitt
De anbefalte dosene av NAPROSYN 500 mg tabletter, ANAPROX DS og EC-NAPROSYN 250 mg er vist i tabell 1.
Ved langtidsadministrasjon kan dosen av naproksen justeres opp eller ned avhengig av den kliniske responsen til pasienten. En lavere daglig dose kan være tilstrekkelig for langtidsadministrasjon.
Morgen- og kveldsdosene trenger ikke å være like store, og administrering av stoffet oftere enn to ganger daglig gir vanligvis ingen forskjell i respons.
Hos pasienter som tåler lavere doser godt, kan dosen økes til naproxen 1500 mg/dag i begrensede perioder på opptil 6 måneder når et høyere nivå av antiinflammatorisk/analgetisk aktivitet er nødvendig. Ved behandling av slike pasienter med naproksen 1500 mg/dag, bør legen observere tilstrekkelig økte kliniske fordeler for å oppveie den potensielle økte risikoen.
Polyartikulær juvenil idiopatisk artritt
Naproxen solid-orale doseringsformer tillater kanskje ikke den fleksible dosetitreringen som er nødvendig hos pediatriske pasienter med polyartikulær juvenil idiopatisk artritt. En flytende formulering kan være mer passende for vektbasert dosering og på grunn av behovet for dosefleksibilitet hos barn.
Hos pediatriske pasienter ga doser på 5 mg/kg/dag plasmanivåer av naproksen som ligner på de som ble sett hos voksne som tok 500 mg naproksen [se KLINISK FARMAKOLOGI ]. Den anbefalte totale daglige dosen av naproxen er ca. 10 mg/kg gitt i 2 oppdelte doser. Dosering med NAPROSYN tabletter er ikke egnet for barn som veier mindre enn 50 kg.
Håndtering av smerte, primær dysmenoré og akutt senebetennelse og bursitt
Den anbefalte startdosen av ANAPROX DS (naproxennatrium) tabletter er 550 mg etterfulgt av 550 mg hver 12. time eller 275 mg (halvparten av en 550 mg tablett) hver 6. til 8. time etter behov. Den totale daglige initialdosen bør ikke overstige 1375 mg (to og en halv tablett) naproksennatrium. Deretter bør den totale daglige dosen ikke overstige 1100 mg naproksennatrium. Fordi natriumsaltet av naproxen absorberes raskere, anbefales ANAPROX DS for behandling av akutte smertefulle tilstander når det er ønskelig med rask innsettende smertelindring. NAPROSYN tabletter kan også brukes. Den anbefalte startdosen av NAPROSYN tabletter er 500 mg etterfulgt av 250 mg (halvparten av en 500 mg NAPROSYN tablett) hver 6.-8. time etter behov. Den totale daglige dosen bør ikke overstige 1250 mg naproksen.
EC-NAPROSYN 250mg anbefales ikke for initial behandling av akutte smerter fordi absorpsjon av naproksen er forsinket sammenlignet med andre naproksenholdige produkter [se KLINISK FARMAKOLOGI ].
Akutt gikt
Anbefalt startdose er 750 mg (en og en halv tablett) NAPROSYN 250 mg tabletter etterfulgt av 250 mg (en halv tablett) hver 8. time til angrepet har avtatt. ANAPROX DS kan også brukes med en startdose på 825 mg (en og en halv tablett) etterfulgt av 275 mg (en halv tablett) hver 8. time. EC-NAPROSYN anbefales ikke på grunn av forsinket absorpsjon.
Ikke-utskiftbarhet med andre formuleringer av naproxen
Ulike dosestyrker og formuleringer (f.eks. tabletter, suspensjon) av naproxen er ikke utskiftbare. Denne forskjellen bør tas i betraktning når du endrer styrker eller formuleringer.
HVORDAN LEVERES
Doseringsformer og styrker
NAPROSYN® (naproxen) tabletter: 500 mg: gule, kapselformede, gravert med NPR LE 500 på den ene siden og delestrek på den andre.
EC-NAPROSYN® (naproxen) tabletter med forsinket frigjøring: 375 mg: hvite, ovale, bikonvekse tabletter merket med NPR EC 375 på den ene siden.
EC-NAPROSYN® (naproxen) tabletter med forsinket frigivelse: 500 mg: hvite, avlange drasjerte tabletter merket med NPR EC 500 på den ene siden.
ANAPROX® DS (naproxennatrium) tabletter: 550 mg: mørkeblå, avlange, gravert med NPS 550 på den ene siden og delestrek på begge sider.
Oppbevaring og håndtering
NAPROSYN (naproxen) tabletter 500 mg : gule, kapselformede tabletter, merket med NPR LE 500 på den ene siden og delestrek på den andre. Pakket i lysbestandige flasker á 100 stk. Leveres som:
NDC 69437-316-01 100-tallet (flaske)
Oppbevares ved 15°C til 30°C (59°F til 86°F) i godt lukkede beholdere; dispensere i lysbestandige beholdere.
EC-NAPROSYN (naproxen) tabletter med forsinket frigivelse 375 mg : hvite, ovale bikonvekse tabletter merket med NPR EC 375 på den ene siden. Pakket i lysbestandige flasker á 100 stk. Leveres som:
NDC 69437-415-01 100-tallet (flaske)
500 mg hvite, avlange belagte tabletter merket med NPR EC 500 på den ene siden. Pakket i lysbestandige flasker á 100 stk. Leveres som:
NDC 69437-416-01 100-tallet (flaske)
Oppbevares ved 15°C til 30°C (59°F til 86°F) i godt lukkede beholdere; dispensere i lysbestandige beholdere.
ANAPROX DS (naproxen natrium) Tabletter 550 mg : mørkeblå, avlange tabletter, merket med NPS 550 på den ene siden og delestrek på begge sider. Pakket i flasker á 100. Leveres som:
NDC 69437-203-01 100-tallet (flaske)
Oppbevares ved 15° til 30°C (59° til 86°F) i godt lukkede beholdere.
Produsert for: Atnahs Pharma, Miles Gray Road, Basildon, Essex, SS14 3FR, Storbritannia. Distribuert av: Canton Laboratories, LLC., Alpharetta, GA 30004-5945, USA. Revidert: april 2021
BIVIRKNINGER
Følgende bivirkninger er omtalt mer detaljert i andre deler av merkingen:
- . Kardiovaskulære trombotiske hendelser [se ADVARSLER OG FORHOLDSREGLER ] . GI-blødning, sårdannelse og perforering [se ADVARSLER OG FORHOLDSREGLER ] . Levertoksisitet [se ADVARSLER OG FORHOLDSREGLER ] . Hypertensjon [se ADVARSLER OG FORHOLDSREGLER ] . Hjertesvikt og ødem [se ADVARSLER OG FORHOLDSREGLER ] . Nyretoksisitet og hyperkalemi [se ADVARSLER OG FORHOLDSREGLER ] . Anafylaktiske reaksjoner [se ADVARSLER OG FORHOLDSREGLER ] . Alvorlige hudreaksjoner [se ADVARSLER OG FORHOLDSREGLER ] . Hematologisk toksisitet [se ADVARSLER OG FORHOLDSREGLER ]
Erfaring fra kliniske forsøk
Fordi kliniske studier utføres under vidt forskjellige forhold, kan bivirkningsrater observert i kliniske studier av et medikament ikke sammenlignes direkte med rater i kliniske studier av et annet medikament og gjenspeiler kanskje ikke hyppighetene observert i praksis.
Bivirkninger rapportert i kontrollerte kliniske studier hos 960 pasienter behandlet for revmatoid artritt eller slitasjegikt er oppført nedenfor. Generelt ble reaksjoner hos pasienter behandlet kronisk rapportert 2 til 10 ganger hyppigere enn de var i korttidsstudier hos de 962 pasientene behandlet for mild til moderat smerte eller dysmenoré. De hyppigste rapporterte plagene var knyttet til mage-tarmkanalen.
En klinisk studie fant at gastrointestinale reaksjoner var hyppigere og mer alvorlig hos pasienter med revmatoid artritt som tok daglige doser på 1500 mg naproksen sammenlignet med de som tok 750 mg naproksen.
kontrollerte kliniske studier med ca. 80 pediatriske pasienter og i godt overvåkede, åpne studier med ca. 400 pediatriske pasienter med polyartikulær juvenil idiopatisk artritt behandlet med naproxen, var forekomsten av utslett og forlengede blødningstider høyere, forekomsten av gastrointestinale og sentrale nervesystemets reaksjoner var omtrent det samme, og forekomsten av andre reaksjoner var lavere hos pediatriske pasienter enn hos voksne.
Hos pasienter som tok naproxen i kliniske studier, var de hyppigst rapporterte bivirkningene hos omtrent 1 % til 10 % av pasientene:
Gastrointestinale (GI) erfaringer, inkludert: halsbrann*, magesmerter*, kvalme*, forstoppelse*, diaré, dyspepsi, stomatitt
Sentralnervesystemet: hodepine*, svimmelhet*, døsighet*, svimmelhet, svimmelhet
Dermatologisk: kløe (kløe)*, hudutbrudd*, ekkymoser*, svette, purpura
Spesielle sanser: tinnitus*, synsforstyrrelser, hørselsforstyrrelser
Kardiovaskulær: ødem*, hjertebank
Generell: dyspné*, tørste
*Forekomst av rapportert reaksjon mellom 3 % og 9 %. De reaksjonene som forekommer hos mindre enn 3 % av pasientene er umerkede.
Hos pasienter som tar NSAIDs, har følgende bivirkninger også blitt rapportert hos omtrent 1 % til 10 % av pasientene.
Gastrointestinale (GI) erfaringer, inkludert: flatulens, grov blødning/perforering, GI-sår (mage/duodenal), oppkast
Generell: unormal nyrefunksjon, anemi, forhøyede leverenzymer, økt blødningstid, utslett
Følgende er ytterligere bivirkninger rapportert hos
Gastrointestinale: pankreatitt, oppkast
Lever og galleveier: gulsott
Hemisk og lymfatisk: melena, trombocytopeni, agranulocytose
Nervesystemet: manglende evne til å konsentrere seg
Dermatologisk: hudutslett
Postmarketing-erfaring
Følgende bivirkninger er identifisert under bruk av naproxen etter godkjenning. Fordi disse reaksjonene rapporteres frivillig fra en populasjon av usikker størrelse, er det ikke alltid mulig å pålitelig estimere frekvensen deres eller etablere en årsakssammenheng med legemiddeleksponering.
Følgende er ytterligere bivirkninger rapportert hos
Kroppen som helhet: anafylaktoide reaksjoner, angioneurotisk ødem, menstruasjonsforstyrrelser, pyreksi (frysninger og feber)
Kardiovaskulær: kongestiv hjertesvikt, vaskulitt, hypertensjon, lungeødem
Gastrointestinale: betennelse, blødning (noen ganger dødelig, spesielt hos eldre), sårdannelse, perforering og obstruksjon av øvre eller nedre mage-tarmkanal. Esofagitt, stomatitt, hematemese, kolitt, forverring av inflammatorisk tarmsykdom (ulcerøs kolitt, Crohns sykdom).
Lever og galleveier: unormale leverfunksjonstester, hepatitt (noen tilfeller har vært dødelige)
Hemisk og lymfatisk: eosinofili, leukopeni, granulocytopeni, hemolytisk anemi, aplastisk anemi
Metabolsk og ernæringsmessig: hyperglykemi, hypoglykemi
Nervesystemet: depresjon, drømmeabnormiteter, søvnløshet, ubehag, myalgi, muskelsvakhet, aseptisk meningitt, kognitiv dysfunksjon, kramper
Luftveiene: eosinofil pneumonitt, astma
Dermatologisk: alopecia, urticaria, toksisk epidermal nekrolyse, erythema multiforme, erythema nodosum, fast legemiddelutbrudd, lichen planus, pustulær reaksjon, systemisk lupus erythematoser, bulløse reaksjoner, inkludert Stevens-Johnsons syndrom, fotosensitiv dermatitt, fotosensitivitetsreaksjoner som ligner porfysreaksjoner, inkludert (pseudoporfyri) eller epidermolysis bullosa. Hvis hudskjørhet, blemmer eller andre symptomer som tyder på pseudoporfyri oppstår, bør behandlingen avbrytes og pasienten overvåkes.
Spesielle sanser: nedsatt hørsel, hornhinneopasitet, papillitt, retrobulbar optikusnevritt, papilleødem
Urogenital: glomerulær nefritt, hematuri, hyperkalemi, interstitiell nefritt, nefrotisk syndrom, nyresykdom, nyresvikt, nyrepapillær nekrose, forhøyet serumkreatinin
Reproduksjon (kvinnelig): infertilitet
Hos pasienter som tar NSAIDs, har følgende bivirkninger også blitt rapportert hos
Kroppen som helhet: feber, infeksjon, sepsis, anafylaktiske reaksjoner, appetittforandringer, død
Kardiovaskulær: hypertensjon, takykardi, synkope, arytmi, hypotensjon, hjerteinfarkt
Gastrointestinale: tørr munn, øsofagitt, magesår, gastritt, glossitt, eruktasjon
Lever og galleveier: hepatitt, leversvikt
Hemisk og lymfatisk: rektal blødning, lymfadenopati, pancytopeni
Metabolsk og ernæringsmessig: vektendringer
Nervesystemet: angst, asteni, forvirring, nervøsitet, parestesi, somnolens, skjelvinger, kramper, koma, hallusinasjoner
Luftveiene: astma, respirasjonsdepresjon, lungebetennelse
Dermatologisk: eksfoliativ dermatitt
Spesielle sanser: tåkesyn, konjunktivitt
Urogenital: cystitt, dysuri, oliguri/polyuri, proteinuri
NARKOTIKAHANDEL
Se tabell 1 for klinisk signifikante legemiddelinteraksjoner med naproxen.
Interaksjoner med legemiddel/laboratorietest
ADVARSLER
Inkludert som en del av FORHOLDSREGLER seksjon.
FORHOLDSREGLER
Kardiovaskulære trombotiske hendelser
Kliniske studier av flere COX-2 selektive og ikke-selektive NSAIDs av opptil tre års varighet har vist økt risiko for alvorlige kardiovaskulære (CV) trombotiske hendelser, inkludert hjerteinfarkt (MI) og hjerneslag, som kan være dødelige. Basert på tilgjengelige data er det uklart at risikoen for CV-trombotiske hendelser er lik for alle NSAIDs. Den relative økningen i alvorlige CV-trombotiske hendelser over baseline forårsaket av NSAID-bruk ser ut til å være lik hos de med og uten kjent CV-sykdom eller risikofaktorer for CV-sykdom. Pasienter med kjent CV-sykdom eller risikofaktorer hadde imidlertid en høyere absolutt forekomst av overskytende alvorlige CV-trombotiske hendelser, på grunn av økt baselinerate. Noen observasjonsstudier fant at denne økte risikoen for alvorlige CV-trombotiske hendelser begynte så tidlig som de første ukene av behandlingen. Økningen i CV-trombotisk risiko har blitt observert mest konsekvent ved høyere doser.
For å minimere den potensielle risikoen for en uønsket CV-hendelse hos NSAID-behandlede pasienter, bruk den laveste effektive dosen for kortest mulig varighet. Leger og pasienter bør være på vakt for utviklingen av slike hendelser, gjennom hele behandlingsforløpet, selv i fravær av tidligere CV-symptomer. Pasienter bør informeres om symptomene på alvorlige CV-hendelser og trinnene de skal ta hvis de oppstår.
Det er ingen konsistente bevis for at samtidig bruk av aspirin reduserer den økte risikoen for alvorlige CV-trombotiske hendelser forbundet med NSAID-bruk. Samtidig bruk av aspirin og et NSAID, slik som naproxen, øker risikoen for alvorlige gastrointestinale (GI) hendelser.
Status etter koronar bypass graft (CABG) kirurgi
To store, kontrollerte kliniske studier av et COX-2 selektivt NSAID for behandling av smerte i de første 10–14 dagene etter CABG-operasjon fant en økt forekomst av hjerteinfarkt og hjerneslag. NSAIDs er kontraindisert ved CABG [se KONTRAINDIKASJONER ].
Pasienter etter MI
Observasjonsstudier utført i det danske folkeregisteret har vist at pasienter behandlet med NSAIDs i post-MI-perioden hadde økt risiko for reinfarkt, CV-relatert død og dødelighet av alle årsaker fra den første uken av behandlingen. I denne samme kohorten var forekomsten av død det første året etter MI 20 per 100 personår hos NSAID-behandlede pasienter sammenlignet med 12 per 100 personår hos ikke-NSAID-eksponerte pasienter. Selv om den absolutte dødsraten falt noe etter det første året etter MI, vedvarte den økte relative risikoen for død hos NSAID-brukere over minst de neste fire årene med oppfølging.
Unngå bruk av NAPROSYN tabletter, EC-NAPROSYN og ANAPROX DS hos pasienter med nylig hjerteinfarkt med mindre fordelene forventes å oppveie risikoen for tilbakevendende CV-trombotiske hendelser. Hvis NAPROSYN 250 mg tabletter, EC-NAPROSYN og ANAPROX DS brukes hos pasienter med nylig hjerteinfarkt, overvåk pasientene for tegn på hjerteiskemi.
Gastrointestinal blødning, sårdannelse og perforering
NSAIDs, inkludert naproxen, forårsaker alvorlige gastrointestinale (GI) bivirkninger, inkludert betennelse, blødning, sårdannelse og perforering av spiserøret, magen, tynntarmen eller tykktarmen, som kan være dødelig. Disse alvorlige bivirkningene kan oppstå når som helst, med eller uten varselsymptomer, hos pasienter behandlet med NSAIDs.
Bare én av fem pasienter som utvikler en alvorlig øvre GI-bivirkning under NSAID-behandling er symptomatisk. Øvre GI-sår, grov blødning eller perforasjon forårsaket av NSAIDs forekom hos ca. 1 % av pasientene behandlet i 3-6 måneder, og hos ca. 2 %-4 % av pasientene behandlet i ett år. Men selv kortvarig NSAID-behandling er ikke uten risiko.
Risikofaktorer for GI-blødning, sårdannelse og perforering
Pasienter med tidligere magesårsykdom og/eller GI-blødninger som brukte NSAIDs hadde en mer enn 10 ganger økt risiko for å utvikle GI-blødning sammenlignet med pasienter uten disse risikofaktorene. Andre faktorer som øker risikoen for GI-blødning hos pasienter behandlet med NSAIDs inkluderer lengre varighet av NSAID-behandling; samtidig bruk av orale kortikosteroider, aspirin, antikoagulantia eller selektive serotoninreopptakshemmere (SSRI); røyking; bruk av alkohol; eldre alder; og dårlig generell helsetilstand. De fleste postmarketingrapporter om fatale GI-hendelser skjedde hos eldre eller svekkede pasienter. I tillegg har pasienter med avansert leversykdom og/eller koagulopati økt risiko for GI-blødning.
Strategier for å minimere GI-risikoen hos NSAID-behandlede pasienter
- . Bruk den laveste effektive dosen for kortest mulig varighet. . Unngå administrering av mer enn ett NSAID om gangen. . Unngå bruk hos pasienter med høyere risiko med mindre fordelene forventes å oppveie den økte risikoen for blødning. For slike pasienter, så vel som de med aktiv GI-blødning, bør du vurdere alternative behandlinger andre enn NSAIDs. . Vær på vakt for tegn og symptomer på magesår og blødninger under NSAID-behandling. . Hvis det er mistanke om en alvorlig GI-bivirkning, initier umiddelbart evaluering og behandling, og seponer NAPROSYN-tabletter, EC-NAPROSYN eller ANAPROX DS inntil en alvorlig GI-bivirkning er utelukket. . Ved samtidig bruk av lavdose acetylsalisylsyre for hjerteprofylakse, overvåk pasienter tettere for tegn på GI-blødning [se NARKOTIKAHANDEL ].
Hepatotoksisitet
Forhøyelser av ALAT eller ASAT (tre eller flere ganger øvre normalgrense [ULN]) er rapportert hos omtrent 1 % av NSAID-behandlede pasienter i kliniske studier. I tillegg er det rapportert sjeldne, noen ganger dødelige, tilfeller av alvorlig leverskade, inkludert fulminant hepatitt, levernekrose og leversvikt.
Forhøyelser av ALAT eller ASAT (mindre enn tre ganger ULN) kan forekomme hos opptil 15 % av pasientene som behandles med NSAIDs inkludert naproxen.
Informer pasientene om varseltegn og symptomer på levertoksisitet (f.eks. kvalme, tretthet, sløvhet, diaré, kløe, gulsott, ømhet i øvre øvre kvadrant og "influensalignende" symptomer). Hvis kliniske tegn og symptomer forenlig med leversykdom utvikles, eller hvis systemiske manifestasjoner oppstår (f.eks. eosinofili, utslett, etc.), seponer behandlingen med NAPROSYN 500 mg tabletter, EC-NAPROSYN 250 mg eller ANAPROX DS umiddelbart, og utfør en klinisk evaluering av pasienten .
Hypertensjon
NSAIDs, inkludert NAPROSYN 250 mg tabletter, EC-NAPROSYN og ANAPROX DS, kan føre til ny oppstart av hypertensjon eller forverring av allerede eksisterende hypertensjon, som begge kan bidra til økt forekomst av CV-hendelser. Pasienter som tar angiotensin-konverterende enzym (ACE)-hemmere, tiaziddiuretika eller loop-diuretika kan ha nedsatt respons på disse behandlingene når de tar NSAIDs [se NARKOTIKAHANDEL ].
Overvåk blodtrykket (BP) under oppstart av NSAID-behandling og gjennom hele behandlingen.
Hjertesvikt og ødem
Coxib and traditional NSAID Trialists' Collaboration meta-analyse av randomiserte kontrollerte studier viste en omtrent to ganger økning i sykehusinnleggelser for hjertesvikt hos COX-2 selektivt behandlede pasienter og ikke-selektive NSAID-behandlede pasienter sammenlignet med placebo-behandlede pasienter. I en dansk nasjonal registerstudie av pasienter med hjertesvikt økte NSAID-bruk risikoen for MI, sykehusinnleggelse for hjertesvikt og død.
I tillegg har væskeretensjon og ødem blitt observert hos noen pasienter behandlet med NSAIDs. Bruk av naproxen kan sløve CV-effektene til flere terapeutiske midler som brukes til å behandle disse medisinske tilstandene (f.eks. diuretika, ACE-hemmere eller angiotensinreseptorblokkere [ARB]) [se NARKOTIKAHANDEL ].
Unngå bruk av NAPROSYN 250 mg tabletter, EC-NAPROSYN eller ANAPROX DS hos pasienter med alvorlig hjertesvikt med mindre fordelene forventes å oppveie risikoen for forverret hjertesvikt. Hvis NAPROSYN 250 mg tabletter, EC-NAPROSYN 250 mg eller ANAPROX DS brukes til pasienter med alvorlig hjertesvikt, overvåk pasientene for tegn på forverret hjertesvikt.
Siden hver ANAPROX DS-tablett inneholder 50 mg natrium (ca. 2 mEq per hver 500 mg naproksen), bør dette vurderes hos pasienter hvis totale inntak av natrium må begrenses sterkt.
Nyretoksisitet og hyperkalemi
Nyretoksisitet
Langvarig administrering av NSAIDs har resultert i nyrepapillær nekrose og annen nyreskade.
Nyretoksisitet er også sett hos pasienter hvor nyreprostaglandiner har en kompenserende rolle i vedlikehold av nyreperfusjon. Hos disse pasientene kan administrering av et NSAID forårsake en doseavhengig reduksjon i prostaglandindannelse og, sekundært, i nyreblodstrømmen, noe som kan utløse åpenbar nyredekompensasjon. Pasienter med størst risiko for denne reaksjonen er de med nedsatt nyrefunksjon, dehydrering, hypovolemi, hjertesvikt, leverdysfunksjon, de som tar diuretika og ACE-hemmere eller ARB, og eldre. Seponering av NSAID-behandling etterfølges vanligvis av gjenoppretting til forbehandlingstilstand.
Ingen informasjon er tilgjengelig fra kontrollerte kliniske studier angående bruk av NAPROSYN 500 mg tabletter, EC-NAPROSYN eller ANAPROX DS hos pasienter med avansert nyresykdom. Nyreeffekten av NAPROSYN 500 mg tabletter, EC-NAPROSYN eller ANAPROX DS kan fremskynde utviklingen av nyresvikt hos pasienter med eksisterende nyresykdom.
Korrekt volumstatus hos dehydrerte eller hypovolemiske pasienter før oppstart av NAPROSYN tabletter, EC-NAPROSYN 250 mg eller ANAPROX DS. Overvåk nyrefunksjonen hos pasienter med nedsatt nyre- eller leverfunksjon, hjertesvikt, dehydrering eller hypovolemi under bruk av NAPROSYN 500 mg tabletter, EC-NAPROSYN og ANAPROX DS [se NARKOTIKAHANDEL ]. Unngå bruk av NAPROSYN 250 mg tabletter, EC-NAPROSYN 500 mg og ANAPROX DS hos pasienter med avansert nyresykdom med mindre fordelene forventes å oppveie risikoen for forverret nyrefunksjon. Hvis NAPROSYN 500mg tabletter, EC-NAPROSYN 500mg eller ANAPROX DS brukes til pasienter med avansert nyresykdom, overvåk pasienter for tegn på forverret nyrefunksjon.
Hyperkalemi
Økning i serumkaliumkonsentrasjon, inkludert hyperkalemi, er rapportert ved bruk av NSAIDs, selv hos noen pasienter uten nedsatt nyrefunksjon. Hos pasienter med normal nyrefunksjon har disse effektene blitt tilskrevet en tilstand av hyporeninemhypoaldosteronisme.
Anafylaktiske reaksjoner
Naproxen har vært assosiert med anafylaktiske reaksjoner hos pasienter med og uten kjent overfølsomhet overfor naproxen og hos pasienter med aspirinsensitiv astma [se KONTRAINDIKASJONER og ADVARSLER OG FORHOLDSREGLER ].
Søk nødhjelp hvis en anafylaktisk reaksjon oppstår.
Forverring av astma relatert til aspirinfølsomhet
En underpopulasjon av pasienter med astma kan ha aspirinsensitiv astma som kan omfatte kronisk rhinosinusitt komplisert av nesepolypper; alvorlig, potensielt dødelig bronkospasme; og/eller intoleranse mot aspirin og andre NSAIDs.
Fordi kryssreaktivitet mellom aspirin og andre NSAIDs er rapportert hos slike aspirinsensitive pasienter, er NAPROSYN 250 mg tabletter, EC-NAPROSYN 500 mg og ANAPROX DS kontraindisert hos pasienter med denne formen for aspirinfølsomhet [se KONTRAINDIKASJONER ]. Når NAPROSYN 250mg tabletter, EC-NAPROSYN 250mg eller ANAPROX DS brukes til pasienter med eksisterende astma (uten kjent aspirinfølsomhet), overvåk pasientene for endringer i tegn og symptomer på astma.
Alvorlige hudreaksjoner
NSAIDs, inkludert naproxen, kan forårsake alvorlige hudbivirkninger som eksfoliativ dermatitt, Stevens-Johnsons syndrom (SJS) og toksisk epidermal nekrolyse (TEN), som kan være dødelig. Disse alvorlige hendelsene kan oppstå uten forvarsel. Informer pasienter om tegn og symptomer på alvorlige hudreaksjoner, og om å avbryte bruken av NAPROSYN 250 mg tabletter, EC-NAPROSYN 500 mg eller ANAPROX DS ved første opptreden av hudutslett eller andre tegn på overfølsomhet. NAPROSYN tabletter, EC-NAPROSYN og ANAPROX DS er kontraindisert hos pasienter med tidligere alvorlige hudreaksjoner på NSAIDs [se KONTRAINDIKASJONER ].
Legemiddelreaksjon med eosinofili og systemiske symptomer (DRESS)
Legemiddelreaksjon med eosinofili og systemiske symptomer (DRESS) er rapportert hos pasienter som tar NSAIDs som NAPROSYN tabletter, EC-NAPROSYN 500mg og ANAPROX DS. Noen av disse hendelsene har vært dødelige eller livstruende. DRESS gir vanligvis, men ikke utelukkende, feber, utslett, lymfadenopati og/eller hevelse i ansiktet. Andre kliniske manifestasjoner kan inkludere hepatitt, nefritt, hematologiske abnormiteter, myokarditt eller myositt. Noen ganger kan symptomer på DRESS ligne på en akutt virusinfeksjon. Eosinofili er ofte tilstede. Fordi denne lidelsen er variabel i presentasjonen, kan andre organsystemer som ikke er nevnt her være involvert. Det er viktig å merke seg at tidlige manifestasjoner av overfølsomhet, som feber eller lymfadenopati, kan være tilstede selv om utslett ikke er tydelig. Hvis slike tegn eller symptomer er tilstede, seponer behandlingen med NAPROSYN 500 mg tabletter, EC-NAPROSYN og ANAPROX DS og evaluer pasienten umiddelbart.
Fostertoksisitet
For tidlig stenging av føtal ductus arteriosus
Unngå bruk av NSAIDs, inkludert NAPROSYN 500 mg tabletter, EC-NAPROSYN og ANAPROX DS, hos gravide kvinner ved ca. 30 ukers svangerskap og senere. NSAIDs, inkludert NAPROSYN 500 mg tabletter, EC-NAPROSYN og ANAPROX DS, øker risikoen for for tidlig stenging av fosterets ductus arteriosus ved omtrent denne svangerskapsalderen.
Oligohydramnios/neonatal nyresvikt
Bruk av NSAIDs, inkludert NAPROSYN tabletter, EC-NAPROSYN 250mg og ANAPROX DS, ved ca. 20 svangerskapsuker eller senere i svangerskapet kan forårsake føtal nyresvikt som fører til oligohydramnios og, i noen tilfeller, nyresvikt hos nyfødte. Disse uønskede utfallene sees i gjennomsnitt etter dager til uker med behandling, selv om oligohydramnios sjelden har blitt rapportert så snart som 48 timer etter NSAID-start. Oligohydramnios er ofte, men ikke alltid, reversibelt ved seponering av behandlingen. Komplikasjoner av langvarig oligohydramnios kan for eksempel inkludere lemmerkontrakturer og forsinket lungemodning. I noen tilfeller etter markedsføring av nedsatt nyrefunksjon hos nyfødte, var invasive prosedyrer som utvekslingstransfusjon eller dialyse nødvendig.
Hvis NSAID-behandling er nødvendig mellom ca. 20 uker og 30 ukers svangerskap, begrense bruken av NAPROSYN 250 mg tabletter, EC-NAPROSYN 250 mg eller ANAPROX DS til lavest mulig effektive dose og kortest mulig varighet. Vurder ultralydovervåking av fostervann hvis behandling med NAPROSYN tabletter, EC-NAPROSYN eller ANAPROX DS varer utover 48 timer. Seponer NAPROSYN 500 mg tabletter, EC-NAPROSYN og ANAPROX DS hvis det oppstår oligohydramnios og følg opp i henhold til klinisk praksis [se Bruk i spesifikke populasjoner ].
Hematologisk toksisitet
Anemi har forekommet hos NSAID-behandlede pasienter. Dette kan skyldes okkult eller grovt blodtap, væskeretensjon eller en ufullstendig beskrevet effekt på erytropoesen. Hvis en pasient behandlet med NAPROSYN tabletter, EC-NAPROSYN 500mg eller ANAPROX DS har noen tegn eller symptomer på anemi, overvåk hemoglobin eller hematokrit.
NSAIDs, inkludert NAPROSYN tabletter, EC-NAPROSYN og ANAPROX DS, kan øke risikoen for blødningshendelser. Komorbide tilstander som koagulasjonsforstyrrelser eller samtidig bruk av warfarin og andre antikoagulantia, blodplatehemmere (f.eks. aspirin), serotoninreopptakshemmere (SSRI) og serotonin noradrenalin reopptakshemmere (SNRI) kan øke denne risikoen. Overvåk disse pasientene for tegn på blødning [se NARKOTIKAHANDEL ].
Maskering av betennelse og feber
Den farmakologiske aktiviteten til NAPROSYN tabletter, EC-NAPROSYN 500mg og ANAPROX DS for å redusere betennelse, og muligens feber, kan redusere nytten av diagnostiske tegn for å oppdage infeksjoner.
Langtidsbruk og laboratorieovervåking
Fordi alvorlig GI-blødning, hepatotoksisitet og nyreskade kan oppstå uten advarselssymptomer eller tegn, bør du vurdere å overvåke pasienter på langvarig NSAID-behandling med en CBC og en kjemiprofil med jevne mellomrom [se ADVARSLER OG FORHOLDSREGLER ].
Pasienter med initiale hemoglobinverdier på 10 g eller mindre som skal få langtidsbehandling, bør få hemoglobinverdier bestemt med jevne mellomrom.
På grunn av uønskede øyefunn i dyrestudier med legemidler av denne klassen, anbefales det at oftalmiske studier utføres hvis det oppstår endringer eller synsforstyrrelser.
Informasjon om pasientveiledning
Råd pasienten til å lese den FDA-godkjente pasientmerkingen (Medikamentveiledning) som følger med hver resept som utleveres. Informer pasienter, familier eller deres omsorgspersoner om følgende informasjon før du starter behandling med NAPROSYN tabletter, EC-NAPROSYN eller ANAPROX DS og med jevne mellomrom i løpet av pågående behandling.
Kardiovaskulære trombotiske hendelser
Råd pasientene til å være på vakt for symptomene på kardiovaskulære trombotiske hendelser, inkludert brystsmerter, kortpustethet, svakhet eller sløret tale, og rapportere alle disse symptomene til helsepersonell umiddelbart [se ADVARSLER OG FORHOLDSREGLER ].
Gastrointestinal blødning, sårdannelse og perforering
Råd pasientene til å rapportere symptomer på sårdannelser og blødninger, inkludert epigastriske smerter, dyspepsi, melena og hematemese til helsepersonell. Ved samtidig bruk av lavdose aspirin for hjerteprofylakse, informer pasientene om økt risiko for og tegn og symptomer på GI-blødning [se ADVARSLER OG FORHOLDSREGLER ].
Hepatotoksisitet
Informer pasientene om varseltegn og symptomer på levertoksisitet (f.eks. kvalme, tretthet, sløvhet, kløe, diaré, gulsott, ømhet i øvre øvre kvadrant og "influensalignende" symptomer). Hvis disse oppstår, instruer pasientene om å slutte med NAPROSYN 500mg tabletter, EC-NAPROSYN 250mg eller ANAPROX DS og oppsøke øyeblikkelig medisinsk behandling [se ADVARSLER OG FORHOLDSREGLER ].
Hjertesvikt og ødem
Råd pasientene til å være på vakt for symptomene på kongestiv hjertesvikt inkludert kortpustethet, uforklarlig vektøkning eller ødem og kontakte helsepersonell dersom slike symptomer oppstår [se ADVARSLER OG FORHOLDSREGLER ].
Anafylaktiske reaksjoner
Informer pasientene om tegn på en anafylaktisk reaksjon (f.eks. pustevansker, hevelse i ansikt eller hals). Instruer pasienter om å søke øyeblikkelig nødhjelp hvis disse oppstår [se KONTRAINDIKASJONER og ADVARSLER OG FORHOLDSREGLER ].
Alvorlige hudreaksjoner, inkludert DRESS
Råd pasienter om å slutte å ta NAPROSYN 250 mg tabletter, EC-NAPROSYN 500 mg eller ANAPROX DS umiddelbart hvis de utvikler noen form for utslett eller feber og kontakte helsepersonell så snart som mulig [se ADVARSLER OG FORHOLDSREGLER ].
Kvinnelig fruktbarhet
Informer kvinner med reproduksjonspotensiale som ønsker å bli gravide at NSAIDs, inkludert NAPROSYN tabletter, ECNAPROSYN 250 mg og ANAPROX DS, kan være assosiert med en reversibel forsinkelse i eggløsning (se Bruk i spesifikke populasjoner .]
Fostertoksisitet
Informer gravide kvinner om å unngå bruk av NAPROSYN 250 mg tabletter, EC-NAPROSYN eller ANAPROX DS og andre NSAIDs som starter ved 30 ukers svangerskap på grunn av risikoen for for tidlig lukking av fosterets ductus arteriosus. Hvis behandling med NAPROSYN tabletter, EC-NAPROSYN 500mg eller ANAPROX DS er nødvendig for en gravid kvinne mellom 20 og 30 ukers svangerskap, informer henne om at hun kanskje må overvåkes for oligohydramnios, hvis behandlingen fortsetter i mer enn 48 timer [se ADVARSLER OG FORHOLDSREGLER og Bruk i spesifikke populasjoner ].
Unngå samtidig bruk av NSAIDs
Informer pasientene om at samtidig bruk av NAPROSYN tabletter, EC-NAPROSYN 500 mg og ANAPROX DS med andre NSAIDs eller salisylater (f.eks. diflunisal, salsalat) ikke anbefales på grunn av økt risiko for gastrointestinal toksisitet og liten eller ingen økning i effekt [se ADVARSLER OG FORHOLDSREGLER og NARKOTIKAHANDEL ]. Varsle pasienter om at NSAIDs kan være til stede i "reseptfri" medisiner for behandling av forkjølelse, feber eller søvnløshet.
Bruk av NSAID og lavdose aspirin
Informer pasienter om ikke å bruke lavdose aspirin samtidig med NAPROSYN 500 mg tabletter, EC-NAPROSYN og ANAPROX DS før de har snakket med helsepersonell [se NARKOTIKAHANDEL ].
Ikke-klinisk toksikologi
Karsinogenese, mutagenese, svekkelse av fruktbarhet
Karsinogenese
En 2-årig studie ble utført på rotter for å evaluere det kreftfremkallende potensialet til naproxen ved rottedoser på 8, 16 og 24 mg/kg/dag (0,05, 0,1 og 0,16 ganger den maksimale anbefalte daglige dosen for mennesker [MRHD] på 1500 mg/dag basert på en sammenligning av kroppsoverflate). Det ble ikke funnet tegn på tumorgenisitet.
Mutagenese
Naproxen testet positivt i in vivo søsterkromatidutvekslingsanalysen for, men var ikke mutagent i in vitro bakteriell reversmutasjonsanalyse (Ames-testen).
Nedsatt fruktbarhet
Hannrotter ble behandlet med 2, 5, 10 og 20 mg/kg naproksen ved oral sonde i 60 dager før paring, og hunnrotter ble behandlet med samme doser i 14 dager før paring og i de første 7 dagene av svangerskapet. Det ble ikke observert noen negative effekter på fertilitet (opptil 0,13 ganger MRDH basert på kroppsoverflate).
Bruk i spesifikke populasjoner
Svangerskap
Risikosammendrag
Bruk av NSAIDs, inkludert NAPROSYN 250 mg tabletter, EC-NAPROSYN og ANAPROX DS, kan forårsake for tidlig lukking av fosterets ductus arteriosus og fosterets nyresvikt som fører til oligohydramnios og, i noen tilfeller, nyresvikt hos nyfødte. På grunn av disse risikoene, begrense dosen og varigheten av NAPROSYN tabletter, EC-NAPROSYN 500mg eller ANAPROX DS bruk mellom ca. 20 og 30 uker av svangerskapet, og unngå bruk av NAPROSYN 500mg tabletter, EC-NAPROSYN og ANAPROX DS ved ca. 30 uker. svangerskap og senere i svangerskapet (se Kliniske betraktninger , Data ).
For tidlig stenging av føtal ductus arteriosus
Bruk av NSAIDs, inkludert NAPROSYN-tabletter, EC-NAPROSYN og ANAPROX DS, ved ca. 30 svangerskapsuker eller senere i svangerskapet øker risikoen for for tidlig stenging av fosterets ductus arteriosus.
Oligohydramnios/neonatal nyresvikt
Bruk av NSAIDs ved ca. 20 ukers svangerskap eller senere i svangerskapet har vært assosiert med tilfeller av føtal nyresvikt som fører til oligohydramnios, og i noen tilfeller nyresvikt hos nyfødte.
Data fra observasjonsstudier angående andre potensielle embryoføtale risikoer ved bruk av NSAID hos kvinner i første eller andre trimester av svangerskapet er ikke konklusive. I reproduksjonsstudier på dyr på rotter, kaniner og mus ingen tegn på teratogenisitet eller fosterskade når naproksen ble administrert i løpet av organogeneseperioden i doser på henholdsvis 0,13, 0,26 og 0,6 ganger den maksimale anbefalte daglige dosen for mennesker på 1500 mg/dag [ se Data ]. Basert på dyredata har prostaglandiner vist seg å ha en viktig rolle i endometrial vaskulær permeabilitet, blastocystimplantasjon og decidualisering. I dyrestudier resulterte administrering av prostaglandinsyntesehemmere som naproxen i økt tap før og etter implantasjon. Prostaglandiner har også vist seg å ha en viktig rolle i fosterets nyreutvikling. I publiserte dyrestudier har prostaglandinsyntesehemmere blitt rapportert å svekke nyreutviklingen når de administreres i klinisk relevante doser.
Estimert bakgrunnsrisiko for alvorlige fødselsskader og spontanabort for den eller de angitte populasjonene er ukjent. Alle graviditeter har en bakgrunnsrisiko for fødselsskader, tap eller andre uheldige utfall. I den generelle befolkningen i USA er den estimerte bakgrunnsrisikoen for alvorlige fødselsskader og spontanabort i klinisk anerkjente svangerskap henholdsvis 2 % til 4 % og 15 % til 20 %.
Kliniske betraktninger
Fetale/neonatale bivirkninger
For tidlig stenging av føtal ductus arteriosus
Unngå bruk av NSAIDs hos kvinner ved ca. 30 ukers svangerskap og senere i svangerskapet, fordi NSAIDs, inkludert NAPROSYN 500mg tabletter, EC-NAPROSYN 250mg og ANAPROX DS, kan forårsake for tidlig stenging av fosterets ductus arteriosus (se Data ).
Oligohydramnios/neonatal nyresvikt
Hvis et NSAID er nødvendig ved ca. 20 ukers svangerskap eller senere i svangerskapet, begrense bruken til den laveste effektive dosen og kortest mulig varighet. Hvis behandlingen med NAPROSYN tabletter, EC-NAPROSYN eller ANAPROX DS varer utover 48 timer, bør du vurdere å overvåke med ultralyd for oligohydramnios. Hvis oligohydramnios oppstår, seponer behandlingen med NAPROSYN 250 mg tabletter, ECNAPROSYN 250 mg og ANAPROX DS, og følg opp i henhold til klinisk praksis (se Data ).
Arbeid eller levering
Det er ingen studier på effekten av NAPROSYN tabletter, EC-NAPROSYN eller ANAPROX DS under fødsel eller fødsel. I dyrestudier hemmer NSAIDs, inkludert naproxen, prostaglandinsyntesen, forårsaker forsinket fødsel og øker forekomsten av dødfødsler.
Data
Menneskelige data
Det er noen bevis som tyder på at når hemmere av prostaglandinsyntese brukes til å utsette prematur fødsel, er det økt risiko for neonatale komplikasjoner som nekrotiserende enterokolitt, patent ductus arteriosus og intrakraniell blødning. Naproksenbehandling gitt sent i svangerskapet for å utsette fødsel har vært assosiert med vedvarende pulmonal hypertensjon, nyresvikt og unormale prostaglandin E-nivåer hos premature spedbarn. På grunn av den kjente effekten av ikke-steroide antiinflammatoriske legemidler på fosterets kardiovaskulære system (lukking av ductus arteriosus), bør bruk under graviditet (spesielt ved 30-veker av svangerskapet eller tredje trimester) unngås.
For tidlig stenging av føtal ductus arteriosus
Publisert litteratur rapporterer at bruk av NSAIDs ved ca. 30 uker av svangerskapet og senere i svangerskapet kan forårsake for tidlig lukking av fosterets ductus arteriosus.
Oligohydramnios/neonatal nyresvikt
Publiserte studier og rapporter etter markedsføring beskriver mors NSAID-bruk ved ca. 20 ukers svangerskap eller senere i svangerskapet assosiert med føtal nyresvikt som fører til oligohydramnios, og i noen tilfeller, nyresvikt hos nyfødte. Disse uønskede utfallene sees i gjennomsnitt etter dager til uker med behandling, selv om oligohydramnios sjelden har blitt rapportert så snart som 48 timer etter NSAID-start. I mange tilfeller, men ikke alle, var nedgangen i fostervann forbigående og reversibel ved seponering av medikamentet. Det har vært et begrenset antall kasusrapporter om bruk av NSAID hos mor og nyresvikt hos nyfødte uten oligohydramnios, hvorav noen var irreversible. Noen tilfeller av nyresvikt hos nyfødte krevde behandling med invasive prosedyrer, som utvekslingstransfusjon eller dialyse.
Metodiske begrensninger ved disse postmarketing-studiene og rapportene inkluderer mangel på en kontrollgruppe; begrenset informasjon om dose, varighet og tidspunkt for medikamenteksponering; og samtidig bruk av andre medisiner. Disse begrensningene utelukker etablering av et pålitelig estimat av risikoen for uønskede føtale og neonatale utfall ved bruk av NSAID hos mor. Fordi de publiserte sikkerhetsdataene om nyfødte utfall hovedsakelig involverte premature spedbarn, er det usikkert om visse rapporterte risikoer for fullbårne spedbarn eksponert for NSAIDs ved bruk av mor kan generaliseres.
Dyredata
Reproduksjonsstudier er utført på rotter med 20 mg/kg/dag (0,13 ganger maksimal anbefalt daglig dose på 1500 mg/dag basert på sammenligning av kroppsoverflate), kaniner med 20 mg/kg/dag (0,26 ganger maksimal anbefalt menneskers daglige dose, basert på sammenligning av kroppsoverflate), og mus på 170 mg/kg/dag (0,6 ganger den maksimale anbefalte daglige dosen for mennesker basert på sammenligning av kroppsoverflate) uten tegn på nedsatt fertilitet eller skade på fosteret pga. dopet.
Amming
Risikosammendrag
Naproksenanion er funnet i melken til ammende kvinner i en konsentrasjon tilsvarende ca. 1 % av maksimal naproksenkonsentrasjon i plasma. De utviklingsmessige og helsemessige fordelene ved amming bør vurderes sammen med mors kliniske behov for NAPROSYN-tabletter, EC-NAPROSYN 500mg eller ANAPROX DS og eventuelle bivirkninger på det ammede spedbarnet fra NAPROSYN-tabletter, EC-NAPROSYN, eller ANAPROX DS eller fra den underliggende morens tilstand.
Kvinner og menn med reproduktivt potensial
Infertilitet
Kvinner
Basert på virkningsmekanismen, kan bruk av prostaglandin-mediert NSAID, inkludert NAPROSYN tabletter, ECNAPROSYN og ANAPROX DS, forsinke eller forhindre ruptur av eggstokkfollikler, som har vært assosiert med reversibel infertilitet hos noen kvinner. Publiserte dyrestudier har vist at administrering av prostaglandinsyntesehemmere har potensial til å forstyrre prostaglandinmediert follikulær ruptur som kreves for eggløsning. Små studier på kvinner behandlet med NSAIDs har også vist en reversibel forsinkelse i eggløsning. Vurder seponering av NSAIDs, inkludert NAPROSYN tabletter, EC-NAPROSYN og ANAPROX DS, hos kvinner som har vanskeligheter med å bli gravide eller som er under utredning av infertilitet.
Pediatrisk bruk
Sikkerhet og effektivitet hos pediatriske pasienter under 2 år er ikke fastslått. Pediatriske doseringsanbefalinger for polyartikulær juvenil idiopatisk artritt er basert på godt kontrollerte studier [se DOSERING OG ADMINISTRASJON ]. Det er ingen tilstrekkelige effekt- eller dose-responsdata for andre pediatriske tilstander, men erfaring med polyartikulær juvenil idiopatisk artritt og annen brukserfaring har vist at enkeltdoser på 2,5 til 5 mg/kg som naproksensuspensjon, med total daglig dose som ikke overstiger 15 mg/kg/dag, tolereres godt hos pediatriske pasienter over 2 år.
Geriatrisk bruk
Lever- og nyretoleransen ved langtidsadministrasjon av naproksen ble studert i to dobbeltblindede kliniske studier med 586 pasienter. Av de studerte pasientene var 98 pasienter 65 år og eldre og 10 av de 98 pasientene var 75 år og eldre. NAPROXEN ble administrert i doser på 375 mg to ganger daglig eller 750 mg to ganger daglig i opptil 6 måneder. Forbigående abnormiteter i laboratorietester for å vurdere lever- og nyrefunksjon ble observert hos noen pasienter, selv om det ikke ble observert noen forskjeller i forekomsten av unormale verdier mellom ulike aldersgrupper.
Eldre pasienter, sammenlignet med yngre pasienter, har større risiko for NSAID-assosierte alvorlige kardiovaskulære, gastrointestinale og/eller renale bivirkninger. Hvis den forventede fordelen for den eldre pasienten oppveier disse potensielle risikoene, start doseringen i den lave enden av doseringsområdet og overvåk pasientene for bivirkninger [se ADVARSLER OG FORHOLDSREGLER ].
Studier indikerer at selv om total plasmakonsentrasjon av naproksen er uendret, øker den ubundne plasmafraksjonen av naproksen hos eldre. Den kliniske betydningen av dette funnet er uklar, selv om det er mulig at økningen i konsentrasjonen av fritt naproksen kan være assosiert med en økning i frekvensen av bivirkninger per gitt dose hos noen eldre pasienter. Forsiktighet tilrådes når høye doser er nødvendig, og noen justeringer av dosen kan være nødvendig hos eldre pasienter. Som med andre legemidler som brukes til eldre, er det fornuftig å bruke den laveste effektive dosen.
Erfaring tilsier at geriatriske pasienter kan være spesielt følsomme for visse bivirkninger av ikke-steroide antiinflammatoriske legemidler. Eldre eller svekkede pasienter synes å tolerere magesår eller blødning dårligere når disse hendelsene oppstår. De fleste spontane rapporter om fatale GI-hendelser er i den geriatriske befolkningen [se ADVARSLER OG FORHOLDSREGLER ].
Naproxen er kjent for å utskilles vesentlig av nyrene, og risikoen for toksiske reaksjoner på dette legemidlet kan være større hos pasienter med nedsatt nyrefunksjon. Fordi eldre pasienter er mer sannsynlig å ha nedsatt nyrefunksjon, bør det utvises forsiktighet ved dosevalg, og det kan være nyttig å overvåke nyrefunksjonen [se KLINISK FARMAKOLOGI ]. Geriatriske pasienter kan ha en større risiko for utvikling av en form for nyretoksisitet utløst av redusert prostaglandindannelse under administrering av ikke-steroide antiinflammatoriske legemidler [se ADVARSLER OG FORHOLDSREGLER ].
Nedsatt leverfunksjon
Forsiktighet tilrådes når høye doser er nødvendig, og noen justeringer av dosen kan være nødvendig hos disse pasientene. Det er klokt å bruke den laveste effektive dosen [se KLINISK FARMAKOLOGI ].
Nedsatt nyrefunksjon
Naproksenholdige produkter anbefales ikke til pasienter med moderat til alvorlig og alvorlig nedsatt nyrefunksjon (kreatininclearance ADVARSLER OG FORHOLDSREGLER , KLINISK FARMAKOLOGI ].
OVERDOSE
Symptomer etter akutte NSAID-overdoser har vanligvis vært begrenset til sløvhet, døsighet, kvalme, oppkast og epigastriske smerter, som generelt har vært reversible med støttebehandling. Gastrointestinal blødning har oppstått. Hypertensjon, akutt nyresvikt, respirasjonsdepresjon og koma har forekommet, men var sjeldne [se ADVARSLER OG FORHOLDSREGLER ].Fordi naproxennatrium kan absorberes raskt, bør høye og tidlige blodnivåer forventes.
Noen få pasienter har opplevd kramper, men det er ikke klart om disse var legemiddelrelaterte eller ikke. Det er ikke kjent hvilken dose av stoffet som vil være livstruende. [se ADVARSLER OG FORHOLDSREGLER ].
Behandle pasienter med symptomatisk og støttende behandling etter en NSAID-overdosering. Det er ingen spesifikke motgift.
Vurder brekninger og/eller aktivt kull (60 til 100 gram hos voksne, 1 til 2 gram per kg kroppsvekt hos pediatriske pasienter) og/eller osmotisk katarsis hos symptomatiske pasienter sett innen fire timer etter inntak eller hos pasienter med stor overdosering ( 5 til 10 ganger anbefalt dose). Tvunget diurese, alkalisering av urin, hemodialyse eller hemoperfusjon er kanskje ikke nyttig på grunn av høy proteinbinding.
For ytterligere informasjon om overdoseringsbehandling, kontakt et giftkontrollsenter (1-800-222-1222).
KONTRAINDIKASJONER
NAPROSYN 500 mg tabletter, EC-NAPROSYN og ANAPROX DS er kontraindisert hos følgende pasienter:
- . Kjent overfølsomhet (f.eks. anafylaktiske reaksjoner og alvorlige hudreaksjoner) overfor naproksen eller andre komponenter i legemiddelet [se ADVARSLER OG FORHOLDSREGLER ] . Anamnese med astma, urticaria eller andre allergiske reaksjoner etter inntak av aspirin eller andre NSAIDs. Alvorlige, noen ganger fatale, anafylaktiske reaksjoner på NSAIDs er rapportert hos slike pasienter [se ADVARSLER OG FORHOLDSREGLER ] . I forbindelse med koronar bypass-operasjon (CABG) [se ADVARSLER OG FORHOLDSREGLER ]
KLINISK FARMAKOLOGI
Virkningsmekanismen
Naproxen har smertestillende, anti-inflammatoriske og febernedsettende egenskaper. ANAPROX DS (naproxen natrium) er utviklet som en raskere absorbert formulering av naproxen for bruk som smertestillende middel.
Virkningsmekanismen til naproxen, i likhet med andre NSAIDs, er ikke fullstendig forstått, men involverer hemming av cyklooksygenase (COX-1 og COX-2).
Naproxen er en potent hemmer av prostaglandinsyntese in vitro. Naproksenkonsentrasjoner oppnådd under behandlingen har gitt in vivo-effekter. Prostaglandiner sensibiliserer afferente nerver og potenserer virkningen av bradykinin for å indusere smerte i dyremodeller. Prostaglandiner er mediatorer av betennelse. Fordi naproksen er en hemmer av prostaglandinsyntese, kan dets virkemåte skyldes en reduksjon av prostaglandiner i perifert vev.
Farmakodynamikk
en studie med friske frivillige, viste 10 dager med samtidig administrering av naproxen 220 mg én gang daglig med lavdose aspirin med umiddelbar frigjøring (81 mg) en interaksjon med antiblodplateaktiviteten til aspirin målt ved % serum tromboksan B2-hemming etter 24 timer etter dag 10-dose [98,7 % (aspirin alene) vs. 93,1 % (naproxen og aspirin)]. Interaksjonen ble observert selv etter seponering av naproxen på dag 11 (mens aspirindosen ble fortsatt), men normalisert ved dag 13. I samme studie var interaksjonen større når naproxen ble administrert 30 minutter før aspirin [98,7 % vs 87,7 %] og minimal når aspirin ble administrert 30 minutter før naproxen [98,7 % vs 95,4 %].
Etter administrering av naproksen 220 mg to ganger daglig med lavdose aspirin med umiddelbar frigjøring (første naproksendose gitt 30 minutter før aspirin), var interaksjonen minimal 24 timer etter dag 10-dose [98,7 % vs 95,7 %]. Imidlertid var interaksjonen mer fremtredende etter seponering av naproxen (utvasking) på dag 11 [98,7 % vs 84,3 %] og normaliserte seg ikke fullstendig på dag 13 [98,5 % vs 90,7 %]. [se NARKOTIKAHANDEL ].
Farmakokinetikk
Naproxen og naproxen natrium absorberes raskt og fullstendig fra mage-tarmkanalen med en in vivo biotilgjengelighet på 95 %. De forskjellige doseringsformene av NAPROSYN 250 mg er bioekvivalente når det gjelder grad av absorpsjon (AUC) og toppkonsentrasjon (Cmax); imidlertid er produktene forskjellige i absorpsjonsmønsteret. Disse forskjellene mellom naproxen-produkter er relatert til både den kjemiske formen av naproxen som brukes og dens formulering. Selv med de observerte forskjellene i absorpsjonsmønster, er eliminasjonshalveringstiden for naproksen uendret på tvers av produkter som varierer fra 12 til 17 timer. Steady-state-nivåer av naproksen nås i løpet av 4 til 5 dager, og graden av naproksenakkumulering er i samsvar med denne halveringstiden. Dette antyder at forskjellene i frigjøringsmønsteret bare spiller en ubetydelig rolle i oppnåelsen av steady-state plasmanivåer.
Absorpsjon
NAPROSYN Tabletter/ANAPROX DS
Etter administrering av NAPROSYN 500 mg tabletter, oppnås maksimale plasmanivåer etter 2 til 4 timer. Etter oral administrering av ANAPROX DS oppnås maksimale plasmanivåer etter 1 til 2 timer. Forskjellen i hastigheter mellom de to produktene skyldes den økte vannløseligheten til natriumsaltet av naproxen brukt i ANAPROX DS.
EC-NAPROSYN
EC-NAPROSYN er designet med et pH-følsomt belegg for å gi en barriere mot oppløsning i det sure miljøet i magen og for å miste integritet i det mer nøytrale miljøet i tynntarmen. Det enteriske polymerbelegget valgt for EC-NAPROSYN 250 mg løses opp over pH 6. Når EC-NAPROSYN ble gitt til fastende personer, ble maksimale plasmanivåer oppnådd ca. 4 til 6 timer etter den første dosen (område: 2 til 12 timer). En in vivo-studie på mennesker med radiomerkede EC-NAPROSYN 250 mg tabletter viste at EC-NAPROSYN oppløses primært i tynntarmen i stedet for i magesekken, slik at absorpsjonen av legemidlet forsinkes til magen er tømt.
Når EC-NAPROSYN og NAPROSYN 500 mg tabletter ble gitt til fastende personer (n=24) i en crossover-studie etter 1 ukes dosering, ble det observert forskjeller i tid til maksimale plasmanivåer (Tmax), men det var ingen forskjeller i total absorpsjon som målt ved Cmax og AUC:
Syrenøytraliserende effekter
Når EC-NAPROSYN 250mg ble gitt som en enkeltdose med syrenøytraliserende (54 mEq bufferkapasitet), var de maksimale plasmanivåene av naproxen uendret, men tiden til toppen ble redusert (gjennomsnittlig Tmax fastet 5,6 timer, gjennomsnittlig Tmax med syrenøytraliserende 5 timer) , men ikke vesentlig [se NARKOTIKAHANDEL ].
Mateffekter
Når EC-NAPROSYN 500 mg ble gitt som en enkeltdose sammen med mat, ble maksimale plasmanivåer hos de fleste forsøkspersoner oppnådd i løpet av ca. 12 timer (intervall: 4 til 24 timer). Oppholdstid i tynntarmen frem til desintegrasjon var uavhengig av matinntak. Tilstedeværelsen av mat forlenget tiden tablettene forble i magen, tid til første påvisbare serumnaproksennivåer og tid til maksimale naproksennivåer (Tmax), men påvirket ikke toppnivåer av naproksen (Cmax).
Fordeling
Naproxen har et distribusjonsvolum på 0,16 l/kg. Ved terapeutiske nivåer er naproksen mer enn 99 % albuminbundet. Ved doser av naproksen større enn 500 mg/dag er det mindre enn proporsjonal økning i plasmanivåer på grunn av en økning i clearance forårsaket av metning av plasmaproteinbinding ved høyere doser (gjennomsnittlig bunn Css 36,5, 49,2 og 56,4 mg/L med 500, 1000 og 1500 mg daglige doser av henholdsvis naproxen). Naproksenanion er funnet i melken til ammende kvinner i en konsentrasjon som tilsvarer omtrent 1 % av maksimal naproksenkonsentrasjon i plasma [se Bruk i spesifikke populasjoner ].
Eliminering
Metabolisme
Naproksen metaboliseres i stor grad i leveren til 6-0-desmetylnaproksen, og både foreldre og metabolitter induserer ikke metaboliserende enzymer. Både naproksen og 6-0-desmetylnaproksen metaboliseres videre til deres respektive acylglukuronid-konjugerte metabolitter.
Utskillelse
Clearance av naproxen er 0,13 ml/min/kg. Omtrent 95 % av naproksenet fra enhver dose skilles ut i urinen, primært som naproksen ( ADVARSLER OG FORHOLDSREGLER ].
Spesifikke populasjoner
Pediatrisk
Hos pediatriske pasienter i alderen 5 til 16 år med leddgikt, plasmanaproksennivåer etter en 5 mg/kg enkeltdose av naproksensuspensjon [se DOSERING OG ADMINISTRASJON ble funnet å være lik de som ble funnet hos normale voksne etter en dose på 500 mg. Den terminale halveringstiden ser ut til å være lik hos pediatriske og voksne pasienter. Farmakokinetiske studier av naproksen ble ikke utført hos pediatriske pasienter yngre enn 5 år. Farmakokinetiske parametere ser ut til å være like etter administrering av naproksen suspensjon eller tabletter hos pediatriske pasienter.
Geriatrisk
Studier indikerer at selv om den totale plasmakonsentrasjonen av naproksen er uendret, er den ubundne plasmafraksjonen av naproksen økt hos eldre, selv om den ubundne fraksjonen er
Nedsatt leverfunksjon
Naproksens farmakokinetikk er ikke bestemt hos personer med leverinsuffisiens.
Kronisk alkoholisk leversykdom og sannsynligvis andre sykdommer med reduserte eller unormale plasmaproteiner (albumin) reduserer den totale plasmakonsentrasjonen av naproksen, men plasmakonsentrasjonen av ubundet naproksen økes.
Nedsatt nyrefunksjon
Naproksens farmakokinetikk er ikke bestemt hos personer med nyreinsuffisiens. Gitt at naproksen, dets metabolitter og konjugater primært skilles ut av nyrene, er det potensial for at naproksenmetabolitter kan akkumuleres ved nyresvikt. Eliminasjon av naproksen er redusert hos pasienter med alvorlig nedsatt nyrefunksjon.
Legemiddelinteraksjonsstudier
Aspirin
Når NSAIDs ble administrert sammen med aspirin, ble proteinbindingen til NSAIDs redusert, selv om clearance av fri NSAID ikke ble endret. Den kliniske betydningen av denne interaksjonen er ikke kjent. Se tabell 1 for klinisk signifikante legemiddelinteraksjoner av NSAIDs med aspirin [se NARKOTIKAHANDEL ].
Kliniske studier
Naproxen har blitt studert hos pasienter med revmatoid artritt, slitasjegikt, polyartikulær juvenil idiopatisk artritt, ankyloserende spondylitt, senebetennelse og bursitt og akutt gikt. Forbedring hos pasienter behandlet for revmatoid artritt ble demonstrert ved en reduksjon i leddhevelse, en reduksjon i varighet av morgenstivhet, en reduksjon i sykdomsaktivitet som vurdert av både utforsker og pasient, og ved økt mobilitet som demonstrert ved reduksjon i gangtid . Generelt har ikke respons på naproxen vist seg å være avhengig av alder, kjønn, alvorlighetsgrad eller varighet av revmatoid artritt.
Hos pasienter med slitasjegikt har den terapeutiske virkningen av naproxen vist seg ved reduksjon i leddsmerter eller ømhet, økt bevegelsesområde i kneledd, økt mobilitet som demonstrert ved reduksjon i gangtid og forbedring i kapasitet til å utføre aktiviteter dagliglivet svekket av sykdommen.
en klinisk studie som sammenlignet standardformuleringer av naproxen 375 mg to ganger daglig (750 mg daglig) mot 750 mg to ganger daglig (1500 mg/dag), avsluttet 9 pasienter i 750 mg-gruppen for tidlig på grunn av bivirkninger. Nitten pasienter i 1500 mg-gruppen avsluttet for tidlig på grunn av uønskede hendelser. De fleste av disse bivirkningene var gastrointestinale hendelser.
I kliniske studier hos pasienter med revmatoid artritt, slitasjegikt og polyartikulær juvenil idiopatisk artritt, har naproxen vist seg å være sammenlignbar med aspirin og indometacin når det gjelder å kontrollere de nevnte målene for sykdomsaktivitet, men frekvensen og alvorlighetsgraden av de mildere gastrointestinale bivirkningene (nause uønskede effekter). , dyspepsi, halsbrann) og bivirkninger på nervesystemet (tinnitus, svimmelhet, svimmelhet) var mindre hos naproksenbehandlede pasienter enn hos de behandlet med aspirin eller indometacin.
Hos pasienter med ankyloserende spondylitt har naproxen vist seg å redusere nattsmerter, morgenstivhet og hvilesmerter. I dobbeltblinde studier ble stoffet vist å være like effektivt som aspirin, men med færre bivirkninger.
Hos pasienter med akutt gikt ble det vist en gunstig respons på naproksen ved signifikant klaring av inflammatoriske endringer (f.eks. reduksjon i hevelse, varme) innen 24 til 48 timer, samt lindring av smerte og ømhet.
Naproxen har blitt studert hos pasienter med milde til moderate smerter sekundært til postoperativ, ortopedisk, postpartum episiotomi og smerter i livmor sammentrekning og dysmenoré. Smertelindring kan begynne innen 1 time hos pasienter som tar naproxen og innen 30 minutter hos pasienter som tar naproxennatrium. Analgetisk effekt ble vist ved slike tiltak som reduksjon av smerteintensitetsskår, økning i smertelindringsskår, reduksjon i antall pasienter som trenger ytterligere smertestillende medisiner, og forsinkelse i tid til remedisinering. Den smertestillende effekten har vist seg å vare i opptil 12 timer.
Naproxen kan trygt brukes i kombinasjon med gullsalter og/eller kortikosteroider; Men i kontrollerte kliniske studier, når det ble lagt til regimet til pasienter som fikk kortikosteroider, så det ikke ut til å gi større forbedring enn det som ble sett med kortikosteroider alene. Hvorvidt naproxen har en "steroidbesparende" effekt er ikke tilstrekkelig studert. Når det ble lagt til kuren til pasienter som fikk gullsalter, resulterte naproksen i større forbedring. Bruken i kombinasjon med salisylater anbefales ikke fordi det er bevis for at aspirin øker utskillelseshastigheten av naproksen og data er utilstrekkelige for å vise at naproksen og aspirin gir større forbedring enn det som oppnås med aspirin alene. I tillegg, som med andre NSAIDs, kan kombinasjonen resultere i høyere frekvens av bivirkninger enn det som er påvist for begge produktene alene.
51Cr blodtap- og gastroskopistudier med normale frivillige, har daglig administrering av 1000 mg naproxen som 1000 mg NAPROSYN (naproxen) eller 1100 mg ANAPROX DS (naproxennatrium) vist seg å forårsake statistisk signifikant mindre gastrisk blødning enn 3250. mg aspirin.
Tre 6-ukers, dobbeltblinde, multisenterstudier med EC-NAPROSYN (naproxen) (375 eller 500 mg to ganger daglig, n=385) og NAPROSYN (375 eller 500 mg to ganger daglig, n=279) ble utført for å sammenligne EC -NAPROSYN med NAPROSYN, inkludert 355 pasienter med revmatoid artritt og slitasjegikt som nylig har hatt NSAID-relaterte GI-symptomer. Disse studiene indikerte at EC-NAPROSYN og NAPROSYN 500 mg ikke viste noen signifikante forskjeller i effekt eller sikkerhet og hadde lignende prevalens av mindre GI-plager. Individuelle pasienter kan imidlertid finne en formulering å foretrekke fremfor den andre.
Fem hundre og femtitre pasienter fikk EC-NAPROSYN under langsiktige åpne studier (gjennomsnittlig behandlingslengde var 159 dager). Hyppighetene for klinisk diagnostiserte magesår og GI-blødninger var lik det som historisk er rapportert for langvarig bruk av NSAIDs.
PASIENTINFORMASJON
Medisineringsveiledning for ikke-steroide antiinflammatoriske legemidler (NSAIDs)
Hva er den viktigste informasjonen jeg bør vite om medisiner som kalles ikke-steroide antiinflammatoriske legemidler (NSAIDs)?
NSAIDs kan forårsake alvorlige bivirkninger, inkludert:
- . Økt risiko for hjerteinfarkt eller hjerneslag som kan føre til døden. Denne risikoen kan oppstå tidlig i behandlingen og kan øke:
- . med økende doser av NSAIDs . ved lengre bruk av NSAIDs
Ikke ta NSAIDs rett før eller etter en hjerteoperasjon kalt "koronararterie bypass graft (CABG)."
Unngå å ta NSAIDs etter et nylig hjerteinfarkt, med mindre helsepersonell ber deg om det. Du kan ha økt risiko for et nytt hjerteinfarkt hvis du tar NSAIDs etter et nylig hjerteinfarkt.
- . Økt risiko for blødning, sår og rifter (perforering) av spiserøret (rør som fører fra munnen til magesekken), mage og tarm:
- . når som helst under bruk . uten varselsymptomer . som kan forårsake død
Risikoen for å få sår eller blødning øker med:
- . tidligere historie med magesår, eller mage- eller tarmblødninger ved bruk av NSAIDs . tar medisiner kalt "kortikosteroider", "antikoagulantia", "SSRI" eller "SNRI" . økende doser av NSAIDs . lengre bruk av NSAIDs . røyking . drikker alkohol . eldre alder . dårlig helse . avansert leversykdom . blødningsproblemer
NSAIDs skal kun brukes:
- . akkurat som foreskrevet . ved lavest mulig dose for din behandling . for kortest mulig tid
Hva er NSAIDs?
NSAIDs brukes til å behandle smerte og rødhet, hevelse og varme (betennelse) fra medisinske tilstander som forskjellige typer leddgikt, menstruasjonssmerter og andre typer kortvarige smerter.
Hvem bør ikke ta NSAIDs?
Ikke ta NSAIDs:
- . hvis du har hatt et astmaanfall, elveblest eller annen allergisk reaksjon med aspirin eller andre NSAIDs. . rett før eller etter bypassoperasjon.
Før du tar NSAID, fortell helsepersonell om alle dine medisinske tilstander, inkludert hvis du:
- . har lever- eller nyreproblemer . har høyt blodtrykk . har astma . er gravid eller planlegger å bli gravid. Å ta NSAIDs ved ca. 20 uker av svangerskapet eller senere kan skade det ufødte barnet. Hvis du trenger å ta NSAIDs i mer enn 2 dager når du er mellom 20 og 30 uker av svangerskapet, kan det hende at helsepersonell må overvåke mengden væske i livmoren rundt babyen din. Du bør ikke ta NSAIDs etter ca. 30 uker med graviditet. . ammer eller planlegger å amme.
Fortell helsepersonell om alle medisinene du tar, inkludert reseptbelagte eller reseptfrie medisiner, vitaminer eller urtetilskudd. NSAIDs og noen andre medisiner kan samhandle med hverandre og forårsake alvorlige bivirkninger. Ikke begynn å ta noen ny medisin uten å snakke med helsepersonell først.
Hva er de mulige bivirkningene av NSAIDs?
NSAIDs kan forårsake alvorlige bivirkninger, inkludert:
Se "Hva er den viktigste informasjonen jeg bør vite om medisiner kalt ikke-steroide antiinflammatoriske legemidler (NSAIDs)?"
- . nytt eller verre høyt blodtrykk . hjertefeil . leverproblemer inkludert leversvikt . nyreproblemer inkludert nyresvikt . lavt antall røde blodlegemer (anemi) . livstruende hudreaksjoner . livstruende allergiske reaksjoner
Andre bivirkninger av NSAIDs inkluderer: magesmerter, forstoppelse, diaré, gass, halsbrann, kvalme, oppkast og svimmelhet. Få nødhjelp umiddelbart hvis du får noen av følgende symptomer:
- . kortpustethet eller problemer med å puste . brystsmerter . svakhet i en del eller side av kroppen din . utydelig tale . hevelse i ansiktet eller halsen
Slutt å ta NSAID og ring legen din med en gang hvis du får noen av følgende symptomer:
- . kvalme . mer sliten eller svakere enn vanlig . diaré . kløe . huden eller øynene dine ser gule ut . fordøyelsesbesvær eller magesmerter . influensalignende symptomer . spy blod . det er blod i avføringen eller den er svart og klissete som tjære . uvanlig vektøkning . hudutslett eller blemmer med feber . hevelse i armer, ben, hender og føtter
Hvis du tar for mye av NSAID-en, ring legen din eller få medisinsk hjelp med en gang.
Dette er ikke alle mulige bivirkninger av NSAIDs. For mer informasjon, spør helsepersonell eller apotek om NSAIDs.
Ring legen din for medisinsk råd om bivirkninger. Du kan rapportere bivirkninger til FDA på 1-800-FDA-1088.
Annen informasjon om NSAIDs
- . Aspirin er et NSAID, men det øker ikke sjansen for hjerteinfarkt. Aspirin kan forårsake blødninger i hjernen, magen og tarmen. Aspirin kan også forårsake sår i mage og tarm. . Noen NSAIDs selges i lavere doser uten resept (reseptfri). Snakk med helsepersonell før du bruker reseptfrie NSAIDs i mer enn 10 dager.
Generell informasjon om sikker og effektiv bruk av NSAIDs
Medisiner er noen ganger foreskrevet for andre formål enn de som er oppført i en medisinveiledning. Ikke bruk NSAIDs for en tilstand det ikke er foreskrevet for. Ikke gi NSAIDs til andre mennesker, selv om de har de samme symptomene som du har. Det kan skade dem.
Hvis du vil ha mer informasjon om NSAIDs, snakk med helsepersonell. Du kan spørre apoteket eller helsepersonell om informasjon om NSAIDs som er skrevet for helsepersonell.
Denne medisinveiledningen er godkjent av US Food and Drug Administration.
