Neoral 25mg, 100mg Cyclosporine Bruk, bivirkninger og dosering. Pris i nettapotek. Generisk medisin uten resept.
Hva er Neoral 25mg og hvordan brukes det?
Neoral 25mg er et reseptbelagt legemiddel som brukes som profylakse for å forhindre organavstøtning etter transplantasjon, og for å behandle symptomene på revmatoid artritt og psoriasis. Neoral kan brukes alene eller sammen med andre medisiner.
Neoral tilhører en klasse legemidler som kalles DMARDs, immunmodulatorer; Immundempende midler; Calcineurin-hemmere.
Det er ikke kjent om Neoral 25mg er trygt og effektivt hos barn.
Hva er de mulige bivirkningene av Neoral?
Neoral kan forårsake alvorlige bivirkninger, inkludert:
- . utslett, . pustevansker, . hevelse i ansiktet, leppene, tungen eller halsen, . problemer med tale, tanke, syn eller muskelbevegelse, . anfall, . alvorlig hodepine, . tåkesyn, . dunker i nakken eller ørene, . blek hud, . lett blåmerker, . uvanlig blødning, . kvalme, . svakhet, . prikkende følelse, . brystsmerter, . uregelmessige hjerteslag, . tap av bevegelse, . lite eller ingen vannlating, . hevelse i føttene eller anklene, . føler meg sliten, . kortpustethet, . tap av Appetit, . magesmerter (øvre høyre side), . gulfarging av hud eller øyne, . feber, . frysninger, . influensasymptomer, . munnsår, . hudsår, . sår hals, og . hoste
Få medisinsk hjelp med en gang hvis du har noen av symptomene nevnt ovenfor.
De vanligste bivirkningene av Neoral inkluderer:
- . skjelvinger eller skjelvinger, . kviser, . økt vekst av ansikts- eller kroppshår, . økt blodtrykk, . kvalme, . diaré, og . hovent eller smertefullt tannkjøtt
Fortell legen dersom du har noen bivirkninger som plager deg eller som ikke går over.
Dette er ikke alle mulige bivirkninger av Neoral. Spør legen din eller apoteket for mer informasjon.
Ring legen din for medisinsk råd om bivirkninger. Du kan rapportere bivirkninger til FDA på 1-800-FDA-1088.
ADVARSEL
Kun leger med erfaring i behandling av systemisk immunsuppressiv terapi for den angitte sykdommen bør forskrive Neoral®. Ved doser som brukes ved solid organtransplantasjon, bør kun leger med erfaring i immunsuppressiv terapi og behandling av organtransplanterte forskrive Neoral®. Pasienter som får legemidlet bør behandles i fasiliteter utstyrt og bemannet med tilstrekkelige laboratorie- og støttemedisinske ressurser. Legen som er ansvarlig for vedlikeholdsbehandling bør ha fullstendig informasjon som kreves for oppfølging av pasienten. Neoral®, et systemisk immunsuppressivt middel, kan øke mottakelighet for infeksjon og utvikling av neoplasi. Hos nyre-, lever- og hjertetransplanterte pasienter kan Neoral® administreres sammen med andre immunsuppressive midler. Økt mottakelighet for infeksjon og mulig utvikling av lymfom og andre neoplasmer kan skyldes økningen i graden av immunsuppresjon hos transplanterte pasienter.
Neoral® Soft Gelatin Capsules (cyclosporine capsules, USP) MODIFIED og Neoral® Oral Solution (cyclosporine oral solution, USP) MODIFIED har økt biotilgjengelighet sammenlignet med Sandimmune® Soft Gelatin Capsules (cyclosporine capsules, USP) og Sandimmune® oral oppløsning (cyclosporine oral Solution) løsning, USP). Neoral® og Sandimmune® er ikke bioekvivalente og kan ikke brukes om hverandre uten tilsyn av lege. For en gitt bunnkonsentrasjon vil ciklosporineksponeringen være større med Neoral® enn med Sandimmune®. Hvis en pasient som får eksepsjonelt høye doser Sandimmune® konverteres til Neoral®, bør det utvises spesiell forsiktighet. Blodkonsentrasjoner av cyklosporin bør overvåkes hos transplanterte og revmatoid artrittpasienter som tar Neoral® for å unngå toksisitet på grunn av høye konsentrasjoner. Dosejusteringer bør gjøres hos transplanterte pasienter for å minimere mulig organavstøtning på grunn av lave konsentrasjoner. Sammenligning av blodkonsentrasjoner i den publiserte litteraturen med blodkonsentrasjoner oppnådd ved bruk av gjeldende analyser må gjøres med detaljert kunnskap om analysemetodene som brukes.
For psoriasispasienter (se også ADVARSLER i boks ovenfor)
Psoriasispasienter som tidligere er behandlet med PUVA og i mindre grad metotreksat eller andre immunsuppressive midler, UVB, kulltjære eller strålebehandling, har økt risiko for å utvikle hudkreft når de tar Neoral®.
Cyklosporin, den aktive ingrediensen i Neoral®, i anbefalte doser, kan forårsake systemisk hypertensjon og nefrotoksisitet. Risikoen øker med økende dose og varighet av ciklosporinbehandling. Nyredysfunksjon, inkludert strukturell nyreskade, er en potensiell konsekvens av ciklosporin, og derfor må nyrefunksjonen overvåkes under behandlingen.
BESKRIVELSE
Neoral® er en oral formulering av ciklosporin som umiddelbart danner en mikroemulsjon i et vandig miljø.
Cyklosporin, det aktive prinsippet i Neoral®, er et syklisk polypeptid immunsuppressivt middel som består av 11 aminosyrer. Den produseres som en metabolitt av sopparten Beauveria nivea.
Kjemisk er cyklosporin betegnet som [R-[R*,R*-(E)]]-syklisk-(L-alanyl-D-alanyl-N-metyl-L-leucylN-metyl-L-leucyl-N-metyl -L-valyl-3-hydroksy-N,4-dimetyl-L-2-amino-6-oktenoyl-L-a-aminobutyryl-N-metylglysyl-N-metyl-L-leucyl-L-valyl-N-metyl -L-leucyl).
Neoral® Soft Gelatin Capsules (cyclosporine capsules, USP) MODIFIED er tilgjengelig i styrker på 25 mg og 100 mg.
Hver 25 mg kapsel inneholder:
cyklosporin………………………………25 mg alkohol, USP dehydrert................................11,9 % v/v (9,5 % vekt/vol.)
Hver 100 mg kapsel inneholder:
ciklosporin…………………………………...100 mg alkohol, USP dehydrert.........................11.9 % v/v (9,5 % vekt/vol.)
Inaktive ingredienser: Maisolje-mono-di-triglyserider, polyoksyl 40 hydrogenert ricinusolje NF, DL-atokoferol USP, gelatin NF, glyserol, svart jernoksid, propylenglykol USP, titandioksid USP, karmin og andre ingredienser.
Neoral® mikstur (ciklosporin mikstur, USP) MODIFIED er tilgjengelig i 50 ml flasker.
Hver ml inneholder:
ciklosporin………………………………………..100 mg/ml alkohol, USP dehydrert................ ...........11,9 % v/v (9,5 % vekt/vol.)
Inaktive ingredienser: Maisolje-mono-di-triglyserider, polyoksyl 40 hydrogenert ricinusolje NF, DL-α tokoferol USP, propylenglykol USP.
Den kjemiske strukturen til cyklosporin (også kjent som cyklosporin A) er:
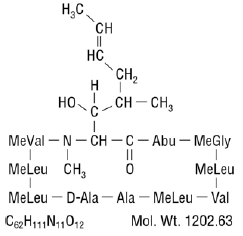
INDIKASJONER
Nyre-, lever- og hjertetransplantasjon
Neoral 25 mg er indisert for profylakse av organavstøtning ved allogene nyre-, lever- og hjertetransplantasjoner. Neoral 100 mg har blitt brukt i kombinasjon med azatioprin og kortikosteroider.
Leddgikt
Neoral er indisert for behandling av pasienter med alvorlig aktiv, revmatoid artritt der sykdommen ikke har respondert tilstrekkelig på metotreksat. Neoral kan brukes i kombinasjon med metotreksat hos pasienter med revmatoid artritt som ikke responderer tilstrekkelig på metotreksat alene.
Psoriasis
Neoral er indisert for behandling av voksne, ikke-immunkompromitterte pasienter med alvorlig (dvs. omfattende og/eller invalidiserende), gjenstridig plakkpsoriasis som ikke har respondert på minst én systemisk terapi (f.eks. PUVA, retinoider eller metotreksat) eller i pasienter som andre systemiske terapier er kontraindisert for, eller ikke kan tolereres.
Mens tilbakefall sjelden forekommer, vil de fleste pasienter oppleve tilbakefall med Neoral 100 mg som med andre terapier ved avsluttet behandling.
DOSERING OG ADMINISTRASJON
Neoral 25 mg myke gelatinkapsler (cyklosporinkapsler, USP) MODIFISERT og Neoral oral oppløsning (ciklosporin oral oppløsning, USP) MODIFIS D
Neoral har økt biotilgjengelighet sammenlignet med Sandimmune. Neoral 25mg og Sandimmune er ikke bioekvivalente og kan ikke brukes om hverandre uten tilsyn av lege.
Den daglige dosen av Neoral 100 mg skal alltid gis i to delte doser (BID). Det anbefales at Neoral administreres etter en konsistent tidsplan med hensyn til tidspunkt på dagen og forhold til måltider. Grapefrukt og grapefruktjuice påvirker metabolismen, øker blodkonsentrasjonen av ciklosporin, og bør derfor unngås.
Spesifikke populasjoner
Nedsatt nyrefunksjon ved nyre-, lever- og hjertetransplantasjon
Syklosporin gjennomgår minimal renal eliminering og farmakokinetikken ser ikke ut til å være signifikant endret hos pasienter med nyresykdom i sluttstadiet som får rutinemessige hemodialysebehandlinger (se KLINISK FARMAKOLOGI ). Men på grunn av dets nefrotoksiske potensiale (se ADVARSLER ), anbefales nøye overvåking av nyrefunksjonen; Doseringen av ciklosporin bør reduseres hvis indisert (se ADVARSLER og FORHOLDSREGLER ).
Nedsatt nyrefunksjon ved revmatoid artritt og psoriasis
Pasienter med nedsatt nyrefunksjon bør ikke få ciklosporin (se KONTRAINDIKASJONER , ADVARSLER og FORHOLDSREGLER ).
Nedsatt leverfunksjon
Clearance av ciklosporin kan være betydelig redusert hos pasienter med alvorlig leversykdom (se KLINISK FARMAKOLOGI ). Dosereduksjon kan være nødvendig hos pasienter med alvorlig nedsatt leverfunksjon for å opprettholde blodkonsentrasjonen innenfor det anbefalte målområdet (se ADVARSLER og FORHOLDSREGLER ).
Nytransplanterte pasienter
Den initiale orale dosen av Neoral 25 mg kan gis 4 til 12 timer før transplantasjon eller gis postoperativt. Startdosen av Neoral 25 mg varierer avhengig av det transplanterte organet og de andre immunsuppressive midlene inkludert i den immunsuppressive protokollen. Hos nylig transplanterte pasienter er den orale initialdosen av Neoral den samme som den orale initialdosen av Sandimmune. Foreslåtte startdoser er tilgjengelig fra resultatene av en undersøkelse fra 1994 av bruken av Sandimmune i amerikanske transplantasjonssentre. Gjennomsnittlige ± SD startdoser var 9 ± 3 mg/kg/dag for nyretransplanterte pasienter (75 sentre), 8 ± 4 mg/kg/dag for levertransplanterte pasienter (30 sentre) og 7 ± 3 mg/kg/dag for hjertetransplanterte pasienter (24 sentre). Totale daglige doser ble delt inn i to like daglige doser. Neoral-dosen justeres deretter for å oppnå en forhåndsdefinert konsentrasjon av ciklosporin i blodet (se Blodkonsentrasjonsovervåking hos transplanterte pasienter nedenfor). Hvis bunnkonsentrasjoner i blodet av ciklosporin brukes, er målområdet det samme for Neoral 100 mg som for Sandimmune. Bruk av samme bunnkonsentrasjonsmålområde for Neoral 100 mg som for Sandimmune resulterer i større ciklosporineksponering når Neoral administreres (se Farmakokinetikk, Absorpsjon ). Doseringen bør titreres basert på kliniske vurderinger av avstøtning og toleranse. Lavere Neoral 100 mg doser kan være tilstrekkelig som vedlikeholdsbehandling.
Tilleggsbehandling med binyrekortikosteroider anbefales initialt. Ulike nedtrappende doseringsplaner av prednison ser ut til å oppnå lignende resultater. Et representativt doseringsskjema basert på pasientens vekt startet med 2,0 mg/kg/dag de første 4 dagene trappet ned til 1,0 mg/kg/dag etter 1 uke, 0,6 mg/kg/dag etter 2 uker, 0,3 mg/kg/dag innen 1 måned, og 0,15 mg/kg/dag etter 2 måneder og deretter som vedlikeholdsdose. Steroiddoser kan nedtrappes ytterligere på en individualisert basis, avhengig av pasientens status og transplantatets funksjon. Dosering av prednison må justeres i henhold til den kliniske situasjonen.
Konvertering fra Sandimmune til Neoral 25 mg hos transplanterte pasienter
Hos transplanterte pasienter som vurderes for konvertering til Neoral fra Sandimmune, bør Neoral startes med samme daglige dose som tidligere ble brukt med Sandimmune (1:1 dosekonvertering). Neoral-dosen bør deretter justeres for å oppnå bunnkonsentrasjonen av ciklosporin før konvertering. Bruk av samme bunnkonsentrasjonsmålområde for Neoral 100 mg som for Sandimmune resulterer i større ciklosporineksponering når Neoral administreres (se Farmakokinetikk, Absorpsjon ). Pasienter med mistanke om dårlig absorpsjon av Sandimmune krever ulike doseringsstrategier (se Transplantasjonspasienter med dårlig absorpsjon av sandimmune, under). Hos noen pasienter er økningen i bunnkonsentrasjonen i blodet mer uttalt og kan være av klinisk betydning.
Inntil bunnkonsentrasjonen i blodet når verdien før konvertering, anbefales det på det sterkeste at bunnkonsentrasjonen av ciklosporin i blodet overvåkes hver 4. til 7. dag etter konvertering til Neoral I tillegg bør kliniske sikkerhetsparametere, som serumkreatinin og blodtrykk, overvåkes annenhver uke i løpet av de to første månedene etter konvertering. Hvis bunnkonsentrasjonene i blodet er utenfor ønsket område og/eller hvis de kliniske sikkerhetsparametrene forverres, må dosen av Neoral 100 mg justeres tilsvarende.
Transplantasjonspasienter med dårlig absorpsjon av Sandimmune
Pasienter med lavere enn forventet blodkonsentrasjon av ciklosporin i forhold til den orale dosen av Sandimmune kan ha dårlig eller inkonsekvent absorpsjon av ciklosporin fra Sandimmune. Etter konvertering til Neoral har pasienter en tendens til å ha høyere ciklosporinkonsentrasjoner. På grunn av økningen i biotilgjengeligheten av ciklosporin etter konvertering til Neoral, kan bunnkonsentrasjonen av ciklosporin i blodet overskride målområdet. Spesiell forsiktighet bør utvises når pasienter konverterer til Neoral 100 mg ved doser større enn 10 mg/kg/dag. Dosen av Neoral bør titreres individuelt basert på bunnkonsentrasjoner av ciklosporin, tolerabilitet og klinisk respons. I denne populasjonen bør bunnkonsentrasjonen av ciklosporin i blodet måles oftere, minst to ganger i uken (daglig, hvis startdosen overstiger 10 mg/kg/dag) inntil konsentrasjonen stabiliserer seg innenfor ønsket område.
Leddgikt
Startdosen av Neoral er 2,5 mg/kg/dag, tatt to ganger daglig som en delt (BID) oral dose. Salisylater, NSAIDs og orale kortikosteroider kan fortsettes (se ADVARSLER og FORHOLDSREGLER , NARKOTIKAHANDEL ). Virkningen begynner vanligvis mellom 4 og 8 uker. Hvis utilstrekkelig klinisk fordel er sett og toleransen er god (inkludert serumkreatinin mindre enn 30 % over baseline), kan dosen økes med 0,5 til 0,75 mg/kg/dag etter 8 uker og igjen etter 12 uker til maksimalt 4 mg /kg/dag. Hvis ingen fordel er sett etter 16 ukers behandling, bør Neoral 25 mg-behandling avbrytes.
Dosereduksjoner med 25 % til 50 % bør gjøres når som helst for å kontrollere bivirkninger, f.eks. hypertensjonsøkninger i serumkreatinin (30 % over pasientens nivå før behandling) eller klinisk signifikante laboratorieavvik (se ADVARSLER og FORHOLDSREGLER ).
Hvis dosereduksjon ikke er effektiv for å kontrollere abnormiteter eller hvis bivirkningen eller unormaliteten er alvorlig, bør Neoral 25 mg seponeres. Den samme startdosen og doseringsområdet bør brukes hvis Neoral 25 mg kombineres med anbefalt dose metotreksat. De fleste pasienter kan behandles med Neoral 25 mg doser på 3 mg/kg/dag eller lavere når de kombineres med metotreksatdoser på opptil 15 mg/uke (se KLINISK FARMAKOLOGI , Kliniske studier ).
Det er begrenset langtidsbehandlingsdata. Tilbakefall av revmatoid artritt sykdomsaktivitet er generelt synlig innen 4 uker etter seponering av ciklosporin.
Psoriasis
Startdosen av Neoral 100 mg bør være 2,5 mg/kg/dag. Neoral bør tas to ganger daglig, som en delt (1,25 mg/kg BID) oral dose. Pasienter bør holdes ved denne dosen i minst 4 uker, unntatt bivirkninger. Hvis signifikant klinisk bedring ikke har oppstått hos pasienter innen den tid, bør pasientens dosering økes med 2 ukers intervaller. Basert på pasientrespons bør doseøkninger på ca. 0,5 mg/kg/dag gjøres til maksimalt 4,0 mg/kg/dag.
Dosereduksjoner med 25 % til 50 % bør gjøres når som helst for å kontrollere uønskede hendelser, f.eks. hypertensjon, økning i serumkreatinin (≥ 25 % over pasientens nivå før behandling), eller klinisk signifikante laboratorieavvik. Hvis dosereduksjon ikke er effektiv for å kontrollere abnormiteter, eller hvis bivirkningen eller unormaliteten er alvorlig, bør Neoral 25 mg seponeres (se Spesiell overvåking av psoriasispasienter ).
Pasienter viser generelt en viss forbedring i de kliniske manifestasjonene av psoriasis i løpet av 2 uker. Tilfredsstillende kontroll og stabilisering av sykdommen kan ta 12 til 16 uker å oppnå. Resultater fra en klinisk studie med dosetitrering med Neoral 25 mg indikerer at en forbedring av psoriasis med 75 % eller mer (basert på PASI) ble oppnådd hos 51 % av pasientene etter 8 uker og hos 79 % av pasientene etter 16 uker. Behandlingen bør seponeres dersom tilfredsstillende respons ikke kan oppnås etter 6 uker ved 4 mg/kg/dag eller pasientens maksimalt tolererte dose. Når en pasient er tilstrekkelig kontrollert og ser stabil ut, bør dosen av Neoral 25 mg reduseres, og pasienten behandles med den laveste dosen som opprettholder en adekvat respons (dette bør ikke nødvendigvis være total clearing av pasienten). I kliniske studier var ciklosporindoser i den nedre enden av det anbefalte doseringsområdet effektive for å opprettholde en tilfredsstillende respons hos 60 % av pasientene. Doser under 2,5 mg/kg/dag kan også være like effektive.
Ved avsluttet behandling med ciklosporin vil tilbakefall oppstå i løpet av ca. 6 uker (50 % av pasientene) til 16 uker (75 % av pasientene). Hos de fleste pasienter oppstår ikke rebound etter avsluttet behandling med ciklosporin. Tretten tilfeller av transformasjon av kronisk plakkpsoriasis til mer alvorlige former for psoriasis er rapportert. Det var 9 tilfeller av pustulær og 4 tilfeller av erytrodermisk psoriasis. Langtidserfaring med Neoral hos psoriasispasienter er begrenset, og kontinuerlig behandling i lengre perioder på mer enn ett år anbefales ikke. Veksling med andre former for behandling bør vurderes i langsiktig behandling av pasienter med denne livslange sykdommen.
Neoral 25 mg mikstur (ciklosporin mikstur, USP) MODIFISERT - Anbefalinger for administrasjon
For å gjøre Neoral 25mg mikstur (ciklosporin mikstur, USP) MODIFIED mer velsmakende, bør den fortynnes med appelsin- eller eplejuice som har romtemperatur. Pasienter bør unngå å bytte fortynningsvæsker ofte. Grapefruktjuice påvirker metabolismen av ciklosporin og bør unngås. Kombinasjonen av Neoral-løsning med melk kan være usmakelig. Effekten av melk på biotilgjengeligheten av ciklosporin når det administreres som Neoral 100 mg oral oppløsning er ikke evaluert.
Ta den foreskrevne mengden Neoral 25 mg oral oppløsning (ciklosporin mikstur, USP) MODIFISERT fra beholderen ved å bruke den medfølgende doseringssprøyten, etter at beskyttelsesdekselet er fjernet, og overfør oppløsningen til et glass appelsin- eller eplejuice. Rør godt og drikk med en gang. Ikke la fortynnet mikstur stå før du drikker. Bruk en glassbeholder (ikke plast). Skyll glasset med mer fortynningsmiddel for å sikre at den totale dosen er konsumert. Etter bruk, tørk utsiden av doseringssprøyten med et rent håndkle og sett på beskyttelsesdekselet. Ikke skyll doseringssprøyten med vann eller andre rengjøringsmidler. Hvis sprøyten trenger rengjøring, må den være helt tørr før bruk igjen.
Blodkonsentrasjonsovervåking hos transplanterte pasienter
Transplantasjonssentre har funnet at blodkonsentrasjonsovervåking av ciklosporin er en viktig del av pasientbehandlingen. Av betydning for blodkonsentrasjonsanalyse er typen analyse som brukes, det transplanterte organet og andre immunsuppressive midler som administreres. Selv om ingen fast sammenheng er etablert, kan blodkonsentrasjonsovervåking hjelpe til med den kliniske evalueringen av avvisning og toksisitet, dosejusteringer og vurdering av samsvar.
Ulike analyser har blitt brukt for å måle blodkonsentrasjoner av ciklosporin. Eldre studier som brukte en uspesifikk analyse, siterte ofte konsentrasjoner som var omtrent det dobbelte av de spesifikke analysene. Derfor må sammenligning mellom konsentrasjoner i den publiserte litteraturen og en individuell pasientkonsentrasjon ved bruk av gjeldende analyser gjøres med detaljert kunnskap om analysemetodene som brukes. Gjeldende analyseresultater er heller ikke utskiftbare, og bruken av dem bør veiledes av deres godkjente merking. En diskusjon av de forskjellige analysemetodene finnes i Annals of Clinical Biochemistry 1994; 31: 420-446. Selv om flere analyser og analysematriser er tilgjengelige, er det enighet om at foreldre-sammensetningsspesifikke analyser korrelerer best med kliniske hendelser. Av disse er HPLC standardreferansen, men det monoklonale antistoffet RIA og det monoklonale antistoffet FPIA tilbyr sensitivitet, reproduserbarhet og bekvemmelighet. De fleste klinikere baserer sin overvåking på laveste ciklosporinkonsentrasjoner. Applied Pharmacokinetics, Principles of Therapeutic Drug Monitoring (1992) inneholder en bred diskusjon av ciklosporin-farmakokinetikk og medikamentovervåkingsteknikker. Blodkonsentrasjonsovervåking er ikke en erstatning for nyrefunksjonsovervåking eller vevsbiopsier.
HVORDAN LEVERES
Neoral® Soft Gelatin Capsules (Cyclosporine Capsules, USP) MODIFISERT
25 mg
Oval, blågrå påtrykt i rødt, "Neoral" over "25 mg."
Pakninger med 30 enhetsdoseblister ( NDC 0078-0246-15).
100 mg
Avlang, blågrå påtrykt i rødt, "NEORAL" over "100 mg."
Pakninger med 30 enhetsdoseblister ( NDC 0078-0248-15).
Lagre og dispensere
I den originale enhetsdosebeholderen ved kontrollert romtemperatur 68°F til 77°F (20°C til 25°C).
Neoral® oral oppløsning (ciklosporin oral oppløsning, USP) MODIFISERT
En klar, gul væske levert i 50 ml flasker som inneholder 100 mg/ml ( NDC 0078-0274-22).
Lagre og dispensere
originalbeholderen ved kontrollert romtemperatur 68°F til 77°F (20° til 25°C). Må ikke oppbevares i kjøleskapet. Etter åpning må innholdet brukes innen to måneder. Ved temperaturer under 68°F (20°C) kan løsningen gelere; lett flokkulering eller dannelse av et lett sediment kan også forekomme. Det er ingen innvirkning på produktets ytelse eller dosering ved bruk av sprøyten som følger med. La det varmes opp til romtemperatur 25 °C (77 °F) for å reversere disse endringene.
Neoral® Soft Gelatin Capsules (cyklosporinkapsler, USP) MODIFISERT
Neoral® mikstur (ciklosporin mikstur, USP) MODIFISERT
Distribuert av: Novartis Pharmaceuticals Corporation, East Hanover, New Jersey 07936. Revidert juni 2021.
BIVIRKNINGER
Nyre-, lever- og hjertetransplantasjon
De viktigste bivirkningene ved cyklosporinbehandling er nyredysfunksjon, tremor, hirsutisme, hypertensjon og tannkjøtthyperplasi.
Hypertensjon
Hypertensjon, som vanligvis er mild til moderat, kan forekomme hos omtrent 50 % av pasientene etter nyretransplantasjon og hos de fleste hjertetransplanterte pasienter.
Glomerulær kapillær trombose
Glomerulær kapillær trombose er funnet hos pasienter behandlet med ciklosporin og kan utvikle seg til graftsvikt. De patologiske endringene lignet på de som ble sett ved hemolytisk-uremisk syndrom og inkluderte trombose av nyremikrovaskulaturen, med blodplate-fibrintrombi som okkluderer glomerulære kapillærer og afferente arterioler, mikroangiopatisk hemolytisk anemi, trombocytopeni og nedsatt nyrefunksjon. Lignende funn er observert når andre immundempende midler har blitt brukt etter transplantasjon.
Hypomagnesemi
Hypomagnesemi er rapportert hos noen, men ikke alle, pasienter som viser kramper mens de er på cyklosporinbehandling. Selv om studier av magnesiumdeplesjon hos normale forsøkspersoner tyder på at hypomagnesemi er assosiert med nevrologiske lidelser, ser det ut til at flere faktorer, inkludert hypertensjon, høydose metylprednisolon, hypokolesterolemi og nefrotoksisitet assosiert med høye plasmakonsentrasjoner av ciklosporin, er relatert til de nevrologiske manifestasjonene av ciklosporintoksisitet.
NARKOTIKAHANDEL
Effekt av legemidler og andre midler på syklosporins farmakokinetikk og/eller sikkerhet
Alle de individuelle legemidlene som er sitert nedenfor er godt underbygget for å interagere med ciklosporin. I tillegg kan samtidig bruk av NSAIDs og ciklosporin, spesielt ved dehydrering, potensere nyredysfunksjon. Forsiktighet bør utvises ved bruk av andre legemidler som er kjent for å svekke nyrefunksjonen (se ADVARSLER , Nefrotoksisitet ).
Legemidler som kan forsterke nyresvikt
Ved samtidig bruk av et legemiddel som kan vise additiv eller synergistisk nyresvikt med ciklosporin, bør det utføres nøye overvåking av nyrefunksjonen (spesielt serumkreatinin). Hvis det oppstår en betydelig nedsatt nyrefunksjon, bør dosen av det samtidig administrerte legemidlet reduseres eller en alternativ behandling vurderes.
Cyklosporin metaboliseres i stor grad av CYP 3A isoenzymer, spesielt CYP3A4, og er et substrat for multimedikamentutstrømningstransportøren P-glykoprotein. Ulike midler er kjent for å enten øke eller redusere plasma- eller fullblodkonsentrasjoner av ciklosporin, vanligvis ved inhibering eller induksjon av CYP3A4 eller P-glykoproteintransporter eller begge deler. Forbindelser som reduserer cyklosporinabsorpsjonen, som orlistat, bør unngås. Passende Neoral 100 mg dosejustering for å oppnå de ønskede ciklosporinkonsentrasjonene er avgjørende når legemidler som signifikant endrer ciklosporinkonsentrasjoner brukes samtidig (se B overvåking av blodkonsentrasjon ).
1. Legemidler som øker konsentrasjonen av cyklosporin
HIV-proteasehemmere
HIV-proteasehemmere (f.eks. indinavir, nelfinavir, ritonavir og sakinavir) er kjent for å hemme cytokrom P-450 3A og kan derfor potensielt øke konsentrasjonen av ciklosporin, men ingen formelle studier av interaksjonen er tilgjengelige. Forsiktighet bør utvises når disse legemidlene administreres samtidig.
Grapefrukt juice
Grapefrukt og grapefruktjuice påvirker metabolismen, øker blodkonsentrasjonen av ciklosporin, og bør derfor unngås.
2. Legemidler/kosttilskudd som reduserer konsentrasjonen av syklosporin
Bosentan
Samtidig administrering av bosentan (250 til 1000 mg hver 12. time basert på toleranse) og ciklosporin (300 mg hver 12. time i 2 dager, deretter dosering for å oppnå en Cmax på 200 til 250 ng/ml) i 7 dager hos friske personer resulterte i reduksjoner i ciklosporin gjennomsnittlig dosenormalisert AUC, Cmax og bunnkonsentrasjon på henholdsvis ca. 50 %, 30 % og 60 %, sammenlignet med når ciklosporin ble gitt alene (se Effekt av cyklosporin på farmakokinetikken og/eller sikkerheten til andre legemidler eller midler ). Samtidig administrering av ciklosporin og bosentan bør unngås.
Boceprevir
Samtidig administrering av boceprevir (800 mg tre ganger daglig i 7 dager) og ciklosporin (100 mg enkeltdose) hos friske forsøkspersoner resulterte i økning i gjennomsnittlig AUC og Cmax for ciklosporin henholdsvis ca. 2,7 ganger og 2 ganger, sammenlignet med når ciklosporin ble gitt alene.
Telaprevir
Samtidig administrering av telaprevir (750 mg hver 8. time i 11 dager) med ciklosporin (10 mg på dag 8) hos friske forsøkspersoner resulterte i økninger i gjennomsnittlig dosenormalisert AUC og Cmax for ciklosporin henholdsvis ca. 4,5 ganger og 1,3 ganger. sammenlignet med når ciklosporin (100 mg enkeltdose) ble gitt alene.
Johannesurt
Det har vært rapporter om en alvorlig legemiddelinteraksjon mellom ciklosporin og urtekosttilskuddet johannesurt. Denne interaksjonen er rapportert å gi en markant reduksjon i blodkonsentrasjonen av ciklosporin, noe som resulterer i subterapeutiske nivåer, avstøtning av transplanterte organer og tap av transplantat.
Rifabutin
Rifabutin er kjent for å øke metabolismen av andre legemidler som metaboliseres av cytokrom P-450-systemet. Interaksjonen mellom rifabutin og ciklosporin er ikke studert. Forsiktighet bør utvises når disse to legemidlene administreres samtidig.
Effekt av cyklosporin på farmakokinetikken og/eller sikkerheten til andre legemidler eller midler
Cyklosporin er en hemmer av CYP3A4 og av flere medikamentutstrømningstransportører (f.eks. P-glykoprotein) og kan øke plasmakonsentrasjonen av medikamenter som er substrater for CYP3A4, P-glykoprotein eller organiske aniontransporterproteiner.
Syklosporin kan redusere clearance av digoksin, kolkisin, prednisolon, HMG-CoA-reduktasehemmere (statiner), og aliskiren, bosentan, dabigatran, repaglinid, NSAIDs, sirolimus, etoposid og andre legemidler.
Se den fullstendige forskrivningsinformasjonen til det andre stoffet for ytterligere informasjon og spesifikke anbefalinger. Beslutningen om samtidig administrering av ciklosporin med andre legemidler eller midler bør tas av helsepersonell etter en nøye vurdering av fordeler og risikoer.
Digoksin
Alvorlig digitalis-toksisitet har blitt sett i løpet av dager etter oppstart av ciklosporin hos flere pasienter som tar digoksin. Hvis digoksin brukes samtidig med ciklosporin, bør serumkonsentrasjonen av digoksin overvåkes.
Kolkisin
Det er rapporter om potensialet til ciklosporin for å forsterke de toksiske effektene av kolkisin som myopati og nevropati, spesielt hos pasienter med nedsatt nyrefunksjon. Samtidig administrering av ciklosporin og kolkisin resulterer i signifikant økning i plasmakonsentrasjonen av kolkisin. Hvis kolkisin brukes samtidig med ciklosporin, anbefales en reduksjon i dosen av kolkisin.
HMG-CoA reduktasehemmere (statiner)
Litteratur- og ettermarkedstilfeller av myotoksisitet, inkludert muskelsmerter og -svakhet, myositt og rabdomyolyse, er rapportert ved samtidig administrering av ciklosporin med lovastatin, simvastatin, atorvastatin, pravastatin og i sjeldne tilfeller fluvastatin. Når det administreres samtidig med ciklosporin, bør dosen av disse statinene reduseres i henhold til anbefalingene på etiketten. Statinbehandling må midlertidig avbrytes eller seponeres hos pasienter med tegn og symptomer på myopati eller de med risikofaktorer som disponerer for alvorlig nyreskade, inkludert nyresvikt, sekundært til rabdomyolyse.
Repaglinid
Syklosporin kan øke plasmakonsentrasjonen av repaglinid og dermed øke risikoen for hypoglykemi. Hos 12 friske mannlige forsøkspersoner som fikk to doser på 100 mg ciklosporin kapsel oralt med 12 timers mellomrom med en enkeltdose på 0,25 mg repaglinidtablett (halvparten av en 0,5 mg tablett) oralt 13 timer etter startdosen med ciklosporin, var repaglinid gjennomsnittlig Cmax. og AUC ble økt henholdsvis 1,8 ganger (område: 0,6 til 3,7 ganger) og 2,4 ganger (område 1,2 til 5,3 ganger). Nøye overvåking av blodsukkernivået er tilrådelig for en pasient som tar ciklosporin og repaglinid samtidig.
Ambrisentan
Samtidig administrering av ambrisentan (5 mg daglig) og ciklosporin (100 til 150 mg to ganger daglig initialt, deretter dosering for å oppnå Cmax 150 til 200 ng/ml) i 8 dager hos friske personer resulterte i gjennomsnittlig økning i ambrisentan AUC og Cmax på ca. henholdsvis fold og 1,5 ganger sammenlignet med ambrisentan alene. Ved samtidig administrering av ambrisentan og ciklosporin, bør ambrisentandosen ikke titreres til anbefalt maksimal daglig dose
Antracyklin antibiotika
Høye doser ciklosporin (f.eks. ved en start intravenøs dose på 16 mg/kg/dag) kan øke eksponeringen for antracyklinantibiotika (f.eks. doksorubicin, mitoksantron, daunorubicin) hos kreftpasienter.
Aliskiren
Syklosporin endrer farmakokinetikken til aliskiren, et substrat av P-glykoprotein og CYP3A4. Hos 14 friske forsøkspersoner som samtidig fikk enkeltdoser av ciklosporin (200 mg) og redusert dose aliskiren (75 mg), ble gjennomsnittlig Cmax for aliskiren økt med omtrent 2,5 ganger (90 % KI: 1,96 til 3,17) og gjennomsnittlig AUC med ca. 4,3 ganger (90 % KI: 3,52 til 5,21), sammenlignet med når disse personene fikk aliskiren alene. Samtidig administrering av aliskiren og ciklosporin forlenget median eliminasjonshalveringstid for aliskiren (26 timer versus 43 til 45 timer) og T (0,5 timer versus 1,5 til 2,0 timer). Gjennomsnittlig AUC og Cmax for ciklosporin var sammenlignbare med rapporterte litteraturverdier. Samtidig administrering av ciklosporin og aliskiren hos disse pasientene resulterte også i en økning i antall og/eller intensitet av bivirkninger, hovedsakelig hodepine, hetetokter, kvalme, oppkast og somnolens. Samtidig administrering av ciklosporin og aliskiren anbefales ikke.
Bosentan
Hos friske personer resulterte samtidig administrering av bosentan og ciklosporin i tidsavhengig gjennomsnittlig økning i dosenormalisert
bunnkonsentrasjoner av bosentan (dvs. ca. 21 ganger på dag 1 og 2 ganger på dag 8 (steady state)) sammenlignet med når bosentan ble gitt alene som en enkeltdose på dag 1 (se Effekt av legemidler og andre midler på syklosporins farmakokinetikk og/eller sikkerhet ). Samtidig administrering av ciklosporin og bosentan bør unngås.
Dabigatran
Effekten av ciklosporin på dabigatrankonsentrasjoner var ikke formelt studert. Samtidig administrering av dabigatran og ciklosporin kan resultere i økte plasmakonsentrasjoner av dabigatran på grunn av den P-gp-hemmende aktiviteten til ciklosporin. Samtidig administrering av ciklosporin og dabigatran bør unngås.
Kaliumsparende diuretika
Cyklosporin bør ikke brukes sammen med kaliumsparende diuretika fordi hyperkalemi kan oppstå. Forsiktighet er også nødvendig når ciklosporin gis samtidig med kaliumsparende legemidler (f.eks. angiotensinkonverterende enzymhemmere, angiotensin II-reseptorantagonister), kaliumholdige legemidler samt hos pasienter på en kaliumrik diett. Kontroll av kaliumnivået i disse situasjonene er tilrådelig.
Ikke-steroide antiinflammatoriske legemidler (NSAID) interaksjoner
Klinisk status og serumkreatinin bør overvåkes nøye når ciklosporin brukes sammen med NSAIDs hos pasienter med revmatoid artritt (se ADVARSLER ).
Farmakodynamiske interaksjoner er rapportert å forekomme mellom cyklosporin og både naproksen og sulindak, ved at samtidig bruk er assosiert med additiv reduksjon i nyrefunksjonen, bestemt av 99mTc-dietylentriaminpentaeddiksyre (DTPA) og (p-aminohippursyre) PAH-clearance. Selv om samtidig administrering av diklofenak ikke påvirker blodkonsentrasjonen av ciklosporin, har det vært assosiert med omtrentlig dobling av diklofenak-blodkonsentrasjoner og sporadiske rapporter om reversibel reduksjon i nyrefunksjonen. Følgelig bør dosen av diklofenak være i den nedre enden av det terapeutiske området.
Metotreksat interaksjon
Foreløpige data indikerer at når metotreksat og cyklosporin ble administrert samtidig til pasienter med revmatoid artritt (N = 20), ble metotreksatkonsentrasjonene (AUC) økt med ca. 30 % og konsentrasjonene (AUC) av metabolitten, 7-hydroksymetotreksat, ble redusert med ca. 80 %. Den kliniske betydningen av denne interaksjonen er ikke kjent. Syklosporinkonsentrasjoner ser ikke ut til å ha blitt endret (N = 6).
Sirolimus
Forhøyelser i serumkreatinin ble observert i studier med sirolimus i kombinasjon med full dose ciklosporin. Denne effekten er ofte reversibel med ciklosporin-dosereduksjon. Samtidig administrering av ciklosporin øker signifikant blodnivået av sirolimus. For å minimere økninger i sirolimuskonsentrasjoner, anbefales det at sirolimus gis 4 timer etter administrering av ciklosporin.
Nifedipin
Hyppig gingival hyperplasi når nifedipin gis samtidig med ciklosporin er rapportert. Samtidig bruk av nifedipin bør unngås hos pasienter hvor gingival hyperplasi utvikles som en bivirkning av ciklosporin.
Metylprednisolon
Kramper når høye doser metylprednisolon gis samtidig med ciklosporin er rapportert.
Andre immunsuppressive legemidler og midler
Psoriasispasienter som får andre immunsuppressive midler eller strålebehandling (inkludert PUVA og UVB) bør ikke samtidig få ciklosporin på grunn av muligheten for overdreven immunsuppresjon.
Effekt av cyklosporin på effekten av levende vaksiner
Under behandling med ciklosporin kan vaksinasjon være mindre effektiv. Bruk av levende vaksiner bør unngås.
For ytterligere informasjon om Cyclosporine Drug Interactions, vennligst kontakt Novartis Medical Affairs Department på 1-888- NOW-NOVA [1-888-669-6682].
ADVARSLER
(Se også ADVARSEL i boks )
Alle pasienter
Cyklosporin, den aktive ingrediensen i Neoral 25mg, kan forårsake nefrotoksisitet og levertoksisitet. Risikoen øker med økende doser av ciklosporin. Nyredysfunksjon inkludert strukturell nyreskade er en potensiell konsekvens av Neoral 100 mg, og derfor må nyrefunksjonen overvåkes under behandlingen. Forsiktighet bør utvises ved bruk av ciklosporin med nefrotoksiske legemidler (se FORHOLDSREGLER ).
Pasienter som får Neoral krever hyppig overvåking av serumkreatinin (se Spesiell overvåking under DOSERING OG ADMINISTRASJON ). Eldre pasienter bør overvåkes med spesiell forsiktighet, siden nedsatt nyrefunksjon også oppstår med alderen. Hvis pasientene ikke overvåkes ordentlig og dosene ikke er riktig justert, kan ciklosporinbehandling være assosiert med forekomsten av strukturell nyreskade og vedvarende nyresvikt.
En økning i serumkreatinin og BUN kan forekomme under Neoral-behandling og reflekterer en reduksjon i den glomerulære filtrasjonshastigheten. Nedsatt nyrefunksjon krever til enhver tid nøye overvåking, og hyppige dosejusteringer kan være indisert. Frekvensen og alvorlighetsgraden av forhøyede serumkreatinin øker med dose og varighet av ciklosporinbehandling. Disse økningene vil sannsynligvis bli mer uttalt uten dosereduksjon eller seponering.
Fordi Neoral 100 mg ikke er bioekvivalent med Sandimmune, kan konvertering fra Neoral til Sandimmune ved bruk av et 1:1-forhold (mg/kg/dag) føre til lavere blodkonsentrasjoner av ciklosporin. Konvertering fra Neoral til Sandimmune bør gjøres med økt overvåking for å unngå potensialet for underdosering.
Nyre-, lever- og hjertetransplantasjon
Nefrotoksisitet
Cyklosporin, den aktive ingrediensen i Neoral, kan forårsake nefrotoksisitet og levertoksisitet når det brukes i høye doser. Det er ikke uvanlig at serumkreatinin og BUN-nivåer blir forhøyet under ciklosporinbehandling. Disse økningene hos nyretransplanterte pasienter indikerer ikke nødvendigvis avstøtning, og hver pasient må evalueres fullstendig før dosejustering settes i gang.
Basert på Sandimmunes historiske erfaring med mikstur, var nefrotoksisitet assosiert med ciklosporin blitt observert i 25 % av tilfellene med nyretransplantasjon, 38 % av tilfellene med hjertetransplantasjon og 37 % av tilfellene av levertransplantasjoner. Mild nefrotoksisitet ble generelt sett 2 til 3 måneder etter nyretransplantasjon og besto av en stans i fallet av preoperative økninger av BUN og kreatinin i et område på henholdsvis 35 til 45 mg/dL og 2,0 til 2,5 mg/dL. Disse økningene var ofte respons på reduksjon av ciklosporindosering.
Mer åpenbar nefrotoksisitet ble sett tidlig etter transplantasjon og var preget av en raskt stigende BUN og kreatinin. Siden disse hendelsene ligner på nyreavstøtingsepisoder, må man være forsiktig med å skille mellom dem. Denne formen for nefrotoksisitet reagerer vanligvis på reduksjon av ciklosporindosering.
Selv om spesifikke diagnostiske kriterier som pålitelig skiller nyretransplantatavstøtning fra legemiddeltoksisitet ikke er funnet, har en rekke parametere vært signifikant assosiert med det ene eller det andre. Det skal imidlertid bemerkes at opptil 20 % av pasientene kan ha samtidig nefrotoksisitet og avstøtning.
En form for en cyklosporin-assosiert nefropati er preget av seriell forverring av nyrefunksjonen og morfologiske endringer i nyrene. Fra 5 % til 15 % av transplanterte som har fått ciklosporin vil ikke vise en reduksjon i økende serumkreatinin til tross for en reduksjon eller seponering av ciklosporinbehandling. Nyrebiopsier fra disse pasientene vil vise en eller flere av følgende endringer: tubulær vakuolisering, tubulære mikrokalsifikasjoner, peritubulær kapillær kongestion, arteriolopati og en stripete form for interstitiell fibrose med tubulær atrofi. Selv om ingen av disse morfologiske endringene er helt spesifikke, krever en diagnose av ciklosporin-assosiert strukturell nefrotoksisitet bevis på disse funnene.
Når man vurderer utviklingen av cyklosporinassosiert nefropati, er det bemerkelsesverdig at flere forfattere har rapportert en sammenheng mellom forekomsten av interstitiell fibrose og høyere kumulative doser eller vedvarende høye sirkulerende bunnkonsentrasjoner av ciklosporin. Dette gjelder spesielt i løpet av de første 6 månedene etter transplantasjon når dosen har en tendens til å være høyest og når, hos nyremottakere, organet ser ut til å være mest sårbart for de toksiske effektene av ciklosporin. Blant andre medvirkende faktorer til utvikling av interstitiell fibrose hos disse pasientene er forlenget perfusjonstid, varm iskemitid, samt episoder med akutt toksisitet og akutt og kronisk avstøtning. Reversibiliteten av interstitiell fibrose og dens korrelasjon til nyrefunksjonen er ennå ikke bestemt. Reversibilitet av arteriolopati er rapportert etter seponering av ciklosporin eller senking av dosen.
Nedsatt nyrefunksjon krever til enhver tid nøye overvåking, og hyppige dosejusteringer kan være indisert.
Ved alvorlig og uavbrutt avstøtning, når redningsbehandling med pulssteroider og monoklonale antistoffer ikke klarer å reversere avstøtningsepisoden, kan det være å foretrekke å bytte til alternativ immunsuppressiv behandling i stedet for å øke Neoral-dosen til for høye blodkonsentrasjoner.
På grunn av potensialet for additiv eller synergistisk svekkelse av nyrefunksjonen, bør det utvises forsiktighet ved samtidig administrering av Neoral med andre legemidler som kan svekke nyrefunksjonen (se FORHOLDSREGLER , NARKOTIKAHANDEL ).
Trombotisk mikroangiopati
Noen ganger har pasienter utviklet et syndrom med trombocytopeni og mikroangiopatisk hemolytisk anemi som kan resultere i graftsvikt. Vaskulopatien kan oppstå i fravær av avstøtning og er ledsaget av ivrig blodplateforbruk i transplantatet som demonstrert av Indium 111-merkede blodplatestudier. Verken patogenesen eller håndteringen av dette syndromet er klart. Selv om oppløsning har skjedd etter reduksjon eller seponering av ciklosporin og 1) administrering av streptokinase og heparin eller 2) plasmaferese, ser dette ut til å avhenge av tidlig påvisning med Indium 111-merket blodplateskanning (se BIVIRKNINGER ).
Hyperkalemi
Betydelig hyperkalemi (noen ganger assosiert med hyperkloremisk metabolsk acidose) og hyperurikemi er av og til sett hos individuelle pasienter.
Hepatotoksisitet
Tilfeller av levertoksisitet og leverskade, inkludert kolestase, gulsott, hepatitt og leversvikt, er rapportert hos pasienter behandlet med ciklosporin. De fleste rapportene inkluderte pasienter med betydelige komorbiditeter, underliggende tilstander og andre forvirrende faktorer, inkludert smittsomme komplikasjoner og komikasjoner med hepatotoksisk potensial. I noen tilfeller, hovedsakelig hos transplanterte pasienter, har dødelige utfall blitt rapportert (se BIVIRKNINGER , Erfaring etter markedsføring, nyre-, lever- og hjertetransplantasjon ).
Levertoksisitet, vanligvis manifestert ved forhøyede leverenzymer og bilirubin, ble rapportert hos pasienter behandlet med ciklosporin i kliniske studier: 4 % ved nyretransplantasjon, 7 % ved hjertetransplantasjon og 4 % ved levertransplantasjon. Dette ble vanligvis observert i løpet av den første måneden av behandlingen når høye doser ciklosporin ble brukt. Kjemiøkningene avtok vanligvis med en reduksjon i dosen.
Maligniteter
Som hos pasienter som får andre immundempende midler, har de pasientene som får ciklosporin økt risiko for utvikling av lymfomer og andre maligniteter, spesielt de i huden. Pasienter som tar ciklosporin bør advares om å unngå for høy eksponering for ultrafiolett lys. Den økte risikoen ser ut til å være relatert til intensiteten og varigheten av immunsuppresjon snarere enn til bruken av spesifikke midler. På grunn av faren for oversuppresjon av immunsystemet som resulterer i økt risiko for infeksjon eller malignitet, bør et behandlingsregime som inneholder flere immundempende midler brukes med forsiktighet. Noen maligniteter kan være dødelige. Transplantasjonspasienter som får ciklosporin har økt risiko for alvorlig infeksjon med dødelig utgang.
Alvorlige infeksjoner
Pasienter som får immunsuppressiva, inkludert Neoral 100 mg, har økt risiko for å utvikle bakterielle, virus-, sopp- og protozoinfeksjoner, inkludert opportunistiske infeksjoner. Disse infeksjonene kan føre til alvorlige, inkludert dødelige utfall (se ADVARSEL i boks , og BIVIRKNINGER ).
Polyoma virusinfeksjoner
Pasienter som får immunsuppressiva, inkludert Neoral 100 mg, har økt risiko for opportunistiske infeksjoner, inkludert polyomavirusinfeksjoner. Polyomavirusinfeksjoner hos transplanterte pasienter kan ha alvorlige, og noen ganger dødelige utfall. Disse inkluderer tilfeller av JC-virusassosiert progressiv multifokal leukoencefalopati (PML) og polyomavirusassosiert nefropati (PVAN), spesielt på grunn av BK-virusinfeksjon, som er observert hos pasienter som får ciklosporin. PVAN er assosiert med alvorlige utfall, inkludert forverret nyrefunksjon og tap av nyretransplantat (se BIVIRKNINGER , Erfaring etter markedsføring, nyre-, lever- og hjertetransplantasjon ). Pasientovervåking kan bidra til å oppdage pasienter med risiko for PVAN.
Tilfeller av PML er rapportert hos pasienter behandlet med Neoral. PML, som noen ganger er dødelig, viser seg ofte med hemiparese, apati, forvirring, kognitive mangler og ataksi. Risikofaktorer for PML inkluderer behandling med immunsuppressive terapier og svekkelse av immunfunksjonen. Hos immunsupprimerte pasienter bør leger vurdere PML i differensialdiagnosen hos pasienter som rapporterer nevrologiske symptomer, og konsultasjon med en nevrolog bør vurderes som klinisk indisert.
Det bør vurderes å redusere total immunsuppresjon hos transplanterte pasienter som utvikler PML eller PVAN. Imidlertid kan redusert immunsuppresjon sette transplantatet i fare.
Nevrotoksisitet
Det har vært rapporter om kramper hos voksne og pediatriske pasienter som får ciklosporin, spesielt i kombinasjon med høydose metylprednisolon.
Encefalopati, inkludert posterior reversibelt encefalopatisyndrom (PRES), er beskrevet både i rapporter etter markedsføring og i litteraturen. Manifestasjoner inkluderer nedsatt bevissthet, kramper, synsforstyrrelser (inkludert blindhet), tap av motorisk funksjon, bevegelsesforstyrrelser og psykiatriske forstyrrelser. I mange tilfeller har endringer i den hvite substansen blitt oppdaget ved bruk av bildeteknikker og patologiske prøver. Predisponerende faktorer, som hypertensjon, hypomagnesemi, hypokolesterolemi, høydose kortikosteroider, høye blodkonsentrasjoner av ciklosporin og graft-versus-host-sykdom, har blitt observert i mange, men ikke alle, rapporterte tilfellene. Endringene har i de fleste tilfeller vært reversible ved seponering av ciklosporin, og i noen tilfeller ble bedring observert etter reduksjon av dosen. Det ser ut til at pasienter som får levertransplantasjon er mer utsatt for encefalopati enn de som får nyretransplantasjon. En annen sjelden manifestasjon av cyklosporin-indusert nevrotoksisitet, som forekommer hyppigere hos transplanterte pasienter enn ved andre indikasjoner, er optisk skiveødem inkludert papilødem, med mulig synshemming, sekundært til benign intrakraniell hypertensjon.
Det bør utvises forsiktighet ved bruk av ciklosporin med nefrotoksiske legemidler (se FORHOLDSREGLER ).
Leddgikt
Syklosporin nefropati ble påvist i nyrebiopsier hos 6 av 60 (10 %) pasienter med revmatoid artritt etter gjennomsnittlig behandlingsvarighet på 19 måneder. Bare én pasient, av disse 6 pasientene, ble behandlet med en dose ≤ 4 mg/kg/dag. Serumkreatinin ble forbedret hos alle unntatt én pasient etter seponering av ciklosporin. Den "maksimale kreatininøkningen" ser ut til å være en faktor i å forutsi ciklosporin nefropati.

Det er et potensial, som med andre immunsuppressive midler, for en økning i forekomsten av maligne lymfomer med ciklosporin. Det er ikke klart om risikoen med ciklosporin er større enn hos revmatoid artrittpasienter eller hos revmatoid artrittpasienter på cellegift for denne indikasjonen. Fem tilfeller av lymfom ble oppdaget: fire i en undersøkelse av ca. 2300 pasienter behandlet med ciklosporin for revmatoid artritt, og et annet tilfelle av lymfom ble rapportert i en klinisk studie. Selv om andre svulster (12 hudkreftformer, 24 solide svulster av forskjellige typer og 1 myelomatose) også ble rapportert i denne undersøkelsen, støttet ikke epidemiologiske analyser et forhold til ciklosporin annet enn for maligne lymfomer.
Pasienter bør evalueres grundig før og under Neoral 25 mg behandling for utvikling av maligniteter. Dessuten kan bruk av Neoral 25 mg-behandling sammen med andre immunsuppressive midler indusere en overdreven immunsuppresjon som er kjent for å øke risikoen for malignitet.
Psoriasis
(Se også ADVARSEL i boks for psoriasis )
Siden ciklosporin er et potent immunsuppressivt middel med en rekke potensielt alvorlige bivirkninger, bør risikoene og fordelene ved bruk av Neoral 100 mg vurderes før behandling av pasienter med psoriasis. Syklosporin, den aktive ingrediensen i Neoral, kan forårsake nefrotoksisitet og hypertensjon (se FORHOLDSREGLER ) og risikoen øker med økende dose og varighet av behandlingen. Pasienter som kan ha økt risiko, som de med unormal nyrefunksjon, ukontrollert hypertensjon eller maligniteter, bør ikke få Neoral.
Nyredysfunksjon er en potensiell konsekvens av Neoral, derfor må nyrefunksjonen overvåkes under behandlingen.
Pasienter som får Neoral 100 mg krever hyppig overvåking av serumkreatinin (se Spesiell overvåking under DOSERING OG ADMINISTRASJON ). Eldre pasienter bør overvåkes med spesiell forsiktighet, siden nedsatt nyrefunksjon også oppstår med alderen. Hvis pasientene ikke overvåkes ordentlig og dosene ikke er riktig justert, kan ciklosporinbehandling forårsake strukturell nyreskade og vedvarende nyresvikt.
En økning i serumkreatinin og BUN kan forekomme under Neoral 25 mg-behandling og reflekterer en reduksjon i den glomerulære filtrasjonshastigheten.
Nyrebiopsier fra 86 psoriasispasienter behandlet i en gjennomsnittlig varighet på 23 måneder med 1,2 til 7,6 mg/kg/dag ciklosporin viste tegn på cyklosporin nefropati hos 18/86 (21 %) av pasientene. Patologien besto av renal tubulær atrofi og interstitiell fibrose. Ved gjentatt biopsi av 13 av disse pasientene som ble holdt på forskjellige doser ciklosporin i gjennomsnittlig 2 år til, steg antallet med cyklosporinindusert nefropati til 26/86 (30 %). Flertallet av pasientene (19/26) fikk en dose på ≥ 5,0 mg/kg/dag (høyeste anbefalte dose er 4 mg/kg/dag). Pasientene var også på ciklosporin i mer enn 15 måneder (18/26) og/eller hadde en klinisk signifikant økning i serumkreatinin i mer enn 1 måned (21/26). Kreatininnivået gikk tilbake til normalområdet hos 7 av 11 pasienter der ciklosporinbehandlingen ble seponert.
Det er en økt risiko for utvikling av hud og lymfoproliferative maligniteter hos ciklosporinbehandlede psoriasispasienter. Den relative risikoen for maligniteter er sammenlignbar med den som er observert hos psoriasispasienter behandlet med andre immunsuppressive midler.
Tumorer ble rapportert hos 32 (2,2 %) av 1439 psoriasispasienter behandlet med ciklosporin over hele verden fra kliniske studier. Ytterligere svulster er rapportert hos 7 pasienter etter markedsføring av ciklosporin. Maligniteter i huden ble rapportert hos 16 (1,1 %) av disse pasientene; alle unntatt 2 av dem hadde tidligere mottatt PUVA-behandling. Metotreksat ble mottatt av 7 pasienter.
UVB og kulltjære hadde blitt brukt av henholdsvis 2 og 3 pasienter. Syv pasienter hadde enten en historie med tidligere hudkreft eller en potensielt disponerende lesjon var tilstede før eksponering for ciklosporin. Av de 16 pasientene med hudkreft hadde 11 pasienter 18 plateepitelkarsinomer og 7 pasienter hadde 10 basalcellekarsinomer.
Det var to lymfoproliferative maligniteter; ett tilfelle av non-Hodgkins lymfom som krevde kjemoterapi, og ett tilfelle av mycosis fungoides som regresserte spontant ved seponering av ciklosporin. Det var fire tilfeller av godartet lymfatisk infiltrasjon: 3 regresserte spontant ved seponering av ciklosporin, mens det fjerde gikk tilbake til tross for fortsettelse av stoffet. Resten av malignitetene, 13 tilfeller (0,9 %), involverte ulike organer.
Pasienter bør ikke behandles samtidig med ciklosporin og PUVA eller UVB, annen strålebehandling eller andre immunsuppressive midler, på grunn av muligheten for overdreven immunsuppresjon og den påfølgende risikoen for maligniteter (se KONTRAINDIKASJONER ). Pasienter bør også advares om å beskytte seg selv på riktig måte når de er i solen, og unngå overdreven soleksponering. Pasienter bør evalueres grundig før og under behandling for tilstedeværelse av maligniteter, og husk at ondartede lesjoner kan være skjult av psoriatiske plakk. Hudlesjoner som ikke er typiske for psoriasis bør biopsieres før behandlingsstart. Pasienter bør kun behandles med Neoral etter fullstendig opphør av mistenkelige lesjoner, og kun hvis det ikke finnes andre behandlingsalternativer (se Spesiell overvåking for psoriasispasienter ).
Spesielle hjelpestoffer
Alkohol (etanol)
Alkoholinnholdet (se BESKRIVELSE av Neoral 100 mg bør tas i betraktning når det gis til pasienter hvor alkoholinntak bør unngås eller minimeres, f.eks. gravide eller ammende kvinner, hos pasienter med leversykdom eller epilepsi, hos alkoholiserte pasienter eller pediatriske pasienter. For en voksen som veier 70 kg, vil den maksimale daglige orale dosen gi omtrent 1 gram alkohol, som er omtrent 6 % av mengden alkohol i en standarddrikk.
FORHOLDSREGLER
Generell
Hypertensjon
Cyclosporine er den aktive ingrediensen i Neoral. Hypertensjon er en vanlig bivirkning av ciklosporinbehandling som kan vedvare (se BIVIRKNINGER og DOSERING OG ADMINISTRASJON for overvåkingsanbefalinger). Mild eller moderat hypertensjon forekommer hyppigere enn alvorlig hypertensjon, og forekomsten avtar over tid. Hos mottakere av nyre-, lever- og hjerte-allograft behandlet med ciklosporin, kan antihypertensiv behandling være nødvendig (se Spesiell overvåking av revmatoid artritt og Psoriasispasienter ). Men siden ciklosporin kan forårsake hyperkalemi, bør kaliumsparende diuretika ikke brukes. Mens kalsiumantagonister kan være effektive midler ved behandling av ciklosporinassosiert hypertensjon, kan de forstyrre cyklosporinmetabolismen (se NARKOTIKAHANDEL ).
Vaksinasjon
Under behandling med ciklosporin kan vaksinasjon være mindre effektiv; og bruk av levende svekkede vaksiner bør unngås.
Spesiell overvåking av pasienter med revmatoid artritt
Før behandlingen startes, bør det utføres en nøye fysisk undersøkelse, inkludert blodtrykksmålinger (ved minst to anledninger) og to kreatininnivåer for å estimere baseline. Blodtrykk og serumkreatinin bør evalueres annenhver uke i løpet av de første 3 månedene og deretter månedlig hvis pasienten er stabil. Det er tilrådelig å overvåke serumkreatinin og blodtrykk alltid etter en økning av dosen av ikke-steroide antiinflammatoriske legemidler (NSAIDs) og etter oppstart av ny NSAID-behandling under Neoral 25 mg-behandling. Hvis det gis samtidig med metotreksat, anbefales det å overvåke CBC- og leverfunksjonstester månedlig (se FORHOLDSREGLER , Generelt, hypertensjon ).
Hos pasienter som får ciklosporin, bør dosen av Neoral reduseres med 25 % til 50 % hvis hypertensjon oppstår. Hvis hypertensjon vedvarer, bør dosen av Neoral 100 mg reduseres ytterligere eller blodtrykket kontrolleres med antihypertensiva. I de fleste tilfeller har blodtrykket gått tilbake til baseline når ciklosporin ble seponert.
I placebokontrollerte studier av pasienter med revmatoid artritt, forekom systolisk hypertensjon (definert som en forekomst av to systoliske blodtrykksmålinger > 140 mmHg) og diastolisk hypertensjon (definert som to diastoliske blodtrykksavlesninger > 90 mmHg) hos 33 % og 19 % av pasienter behandlet med henholdsvis ciklosporin. De tilsvarende placeboratene var 22 % og 8 %.
Spesiell overvåking for psoriasispasienter
Før behandling igangsettes, bør det utføres en nøye dermatologisk og fysisk undersøkelse, inkludert blodtrykksmålinger (ved minst to anledninger). Siden Neoral er et immunsuppressivt middel, bør pasienter undersøkes for tilstedeværelse av okkult infeksjon ved deres første fysiske undersøkelse og for tilstedeværelse av svulster initialt, og gjennom behandlingen med Neoral. Hudlesjoner som ikke er typiske for psoriasis, bør biopsieres før du starter Neoral. Pasienter med ondartede eller premaligne hudforandringer bør kun behandles med Neoral 100 mg etter passende behandling av slike lesjoner og hvis det ikke finnes andre behandlingsalternativer.
Baseline-laboratorier bør inkludere serumkreatinin (ved to anledninger), BUN, CBC, serummagnesium, kalium, urinsyre og lipider.
Risikoen for ciklosporin nefropati reduseres når startdosen er lav (2,5 mg/kg/dag), maksimal dose ikke overstiger 4,0 mg/kg/dag, serumkreatinin overvåkes regelmessig mens ciklosporin administreres, og dosen av Neoral 25 mg reduseres når økningen i kreatinin er større enn eller lik 25 % over pasientens nivå før behandling. Økningen i kreatinin er vanligvis reversibel ved rettidig reduksjon av dosen av Neoral eller seponering av den.
Serumkreatinin og BUN bør evalueres annenhver uke i løpet av de første 3 månedene av behandlingen og deretter månedlig hvis pasienten er stabil. Hvis serumkreatinin er større enn eller lik 25 % over pasientens forbehandlingsnivå, bør serumkreatinin gjentas innen to uker. Hvis endringen i serumkreatinin forblir større enn eller lik 25 % over baseline, bør Neoral 25 mg reduseres med 25 % til 50 %. Hvis kl når som helst serumkreatinin øker med mer enn eller lik 50 % over nivået før behandling, Neoral 25 mg bør reduseres med 25 % til 50 %. Neoral bør seponeres hvis reversibilitet (innen 25 % av baseline) av serumkreatinin ikke er oppnåelig etter to doseendringer. Det er tilrådelig å overvåke serumkreatinin etter en økning av dosen av ikke-steroide antiinflammatoriske legemidler og etter oppstart av ny ikke-steroid antiinflammatorisk behandling under Neoral 25 mg-behandling.
Blodtrykket bør evalueres annenhver uke i løpet av de første 3 månedene av behandlingen og deretter månedlig hvis pasienten er stabil, eller oftere når dosejusteringer gjøres. Pasienter uten tidligere hypertensjon i anamnesen før oppstart av behandling med Neoral, bør få stoffet redusert med 25 % til 50 % dersom de viser seg å ha vedvarende hypertensjon. Hvis pasienten fortsetter å være hypertensiv til tross for gjentatte reduksjoner av Neoral 25 mg, bør Neoral seponeres. For pasienter med behandlet hypertensjon, før oppstart av Neoral 100 mg-behandling, bør medisinen deres justeres for å kontrollere hypertensjon mens de bruker Neoral. Neoral 100 mg bør seponeres hvis en endring i hypertensjonsbehandling ikke er effektiv eller tolererbar.
CBC, urinsyre, kalium, lipider og magnesium bør også overvåkes hver 2. uke de første 3 månedene av behandlingen, og deretter månedlig hvis pasienten er stabil eller oftere når dosejusteringer gjøres. Neoral 25 mg-dose bør reduseres med 25 % til 50 % for eventuelle unormale kliniske problemer.
I kontrollerte studier av ciklosporin hos psoriasispasienter, korrelerte ikke konsentrasjonen av ciklosporin i blodet godt med verken bedring eller med bivirkninger som nyresvikt.
Laboratorietester
Hos alle pasienter som behandles med ciklosporin, bør nyre- og leverfunksjoner vurderes gjentatte ganger ved måling av serumkreatinin, BUN, serumbilirubin og leverenzymer. Serumlipider, magnesium og kalium bør også overvåkes.
Blodkonsentrasjoner av cyklosporin bør overvåkes rutinemessig hos transplanterte pasienter (se DOSERING OG ADMINISTRASJON , Blodkonsentrasjonsovervåking hos transplanterte pasienter ), og regelmessig overvåket hos pasienter med revmatoid artritt.
Karsinogenese, mutagenese og svekkelse av fruktbarhet
Karsinogenitetsstudier ble utført på hann- og hunnrotter og mus. I den 78-ukers musestudien ble det funnet bevis på en statistisk signifikant trend for lymfocytiske lymfomer hos kvinner, og forekomsten av hepatocellulære karsinomer hos menn med middels dose oversteg kontrollverdien betydelig. I den 24-måneders rottestudien overskred pankreasøycelleadenomer kontrollfrekvensen i det lave dosenivået betydelig. Doser brukt i mus- og rottestudiene var 0,01 til 0,16 ganger den kliniske vedlikeholdsdosen (6 mg/kg). De hepatocellulære karsinomene og pankreasøycelleadenomene var ikke doserelaterte. Publiserte rapporter indikerer at samtidig behandling av hårløse mus med UV-bestråling og ciklosporin eller andre immunsuppressive midler forkorter tiden til hudsvulstdannelse sammenlignet med UV-bestråling alene.
Syklosporin var ikke mutagent i passende testsystemer. Cyklosporin er ikke funnet å være mutagent/gentoksisk i Ames-testen, V79-HGPRT-testen, mikronukleustesten i mus og kinesiske hamstere, kromosomavvikstestene i benmarg fra kinesisk hamster, musedominant letal-analysen og DNA-reparasjonstest i sædceller fra behandlede mus. En fersk studie som analyserte induksjon av søsterkromatidutveksling (SCE) med cyklosporin ved bruk av humane lymfocytter in vitro ga indikasjoner på en positiv effekt (dvs. induksjon av SCE), ved høye konsentrasjoner i dette systemet. I to publiserte forskningsstudier viste kaniner eksponert for ciklosporin in utero (10 mg/kg/dag subkutant) redusert antall nefroner, nyrehypertrofi, systemisk hypertensjon og progressiv nyresvikt opp til 35 ukers alder. Gravide rotter som fikk 12 mg/kg/dag ciklosporin intravenøst (to ganger anbefalt human intravenøs dose) hadde fostre med økt forekomst av ventrikkelseptumdefekt. Disse funnene er ikke påvist hos andre arter, og deres relevans for mennesker er ukjent.
Ingen svekkelse av fertilitet ble vist i studier på hann- og hunnrotter.
Utbredt papillomatose i huden ble observert etter kronisk behandling av hunder med ciklosporin ved 9 ganger den humane initiale psoriasisbehandlingsdosen på 2,5 mg/kg, hvor doser er uttrykt på basis av kroppsoverflate. Denne papillomatosen viste en spontan regresjon ved seponering av ciklosporin.
Økt forekomst av malignitet er en anerkjent komplikasjon av immunsuppresjon hos mottakere av organtransplantasjoner og pasienter med revmatoid artritt og psoriasis. De vanligste formene for neoplasmer er non-Hodgkins lymfom og karsinomer i huden. Risikoen for malignitet hos ciklosporin-mottakere er høyere enn i den normale, friske befolkningen, men lik den hos pasienter som får andre immunsuppressive terapier. Reduksjon eller seponering av immunsuppresjon kan føre til at lesjonene går tilbake.
Hos psoriasispasienter på ciklosporin er det rapportert utvikling av maligniteter, spesielt de i huden (se ADVARSLER ). Hudlesjoner som ikke er typiske for psoriasis bør biopsieres før behandling med ciklosporin startes. Pasienter med ondartede eller premaligne hudforandringer bør kun behandles med ciklosporin etter hensiktsmessig behandling av slike lesjoner og hvis det ikke finnes andre behandlingsalternativer.
Svangerskap
Dyrestudier har vist reproduksjonstoksisitet hos rotter og kaniner. Syklosporin ga ingen tegn på mutagene eller teratogene effekter i standard testsystemene med oral applikasjon (rotter opp til 17 mg/kg og kaniner opp til 30 mg/kg per dag oralt.) Bare ved dosenivåer som var giftige for dam, ble det sett bivirkninger i reproduksjonsstudier hos rotter. Syklosporin har vist seg å være embryo- og føtotoksisk hos rotter og kaniner etter oral administrering ved maternalt toksiske doser. Fostertoksisitet ble observert hos rotter ved 0,8 og kaniner ved 5,4 ganger transplantasjonsdosene hos mennesker på 6,0 mg/kg, der dosekorreksjoner er basert på kroppsoverflate. Syklosporin var embryo- og føtotoksisk som indikert av økt pre- og postnatal mortalitet og redusert fostervekt sammen med relatert skjelettretardasjon.
Det er ingen adekvate og velkontrollerte studier på gravide kvinner, og Neoral bør derfor ikke brukes under graviditet med mindre den potensielle fordelen for moren rettferdiggjør den potensielle risikoen for fosteret.
Hos gravide transplanterte som behandles med immunsuppressiva er risikoen for for tidlig fødsel økt. Følgende data representerer de rapporterte resultatene av 116 graviditeter hos kvinner som fikk ciklosporin under svangerskapet, 90 % av disse var transplanterte pasienter, og de fleste fikk ciklosporin gjennom hele svangerskapet. De eneste konsistente mønstrene for abnormitet var for tidlig fødsel (svangerskapsperiode på 28 til 36 uker) og lav fødselsvekt for svangerskapsalder. Seksten fostertap skjedde. De fleste av svangerskapene (85 av 100) var komplisert av lidelser; inkludert svangerskapsforgiftning, eclampsia, prematur fødsel, abruptio placentae, oligohydramnios, Rh-inkompatibilitet og føtoplacental dysfunksjon. For tidlig fødsel skjedde hos 47 %. Syv misdannelser ble rapportert hos 5 levedyktige spedbarn og i 2 tilfeller av fostertap. Tjueåtte prosent av spedbarnene var små for svangerskapsalderen. Neonatale komplikasjoner forekom hos 27 %. Derfor bør risikoen og fordelene ved å bruke Neoral under graviditet veies nøye.
Et begrenset antall observasjoner hos barn eksponert for ciklosporin in utero er tilgjengelig, opp til en alder på ca. 7 år. Nyrefunksjonen og blodtrykket hos disse barna var normalt.
På grunn av mulig forstyrrelse av mor-føtal interaksjon, bør risiko/nytte-forholdet ved bruk av Neoral hos psoriasispasienter under graviditet veies nøye med alvorlig vurdering for seponering av Neoral.
Alkoholinnholdet i Neoral 100 mg formuleringer bør også tas i betraktning hos gravide kvinner (se ADVARSLER , Spesielle hjelpestoffer ).
Ammende mødre
Syklosporin finnes i morsmelk. På grunn av potensialet for alvorlige bivirkninger hos ammende spedbarn fra Neoral 100 mg, bør det tas en beslutning om å avbryte ammingen eller å avbryte medikamentet, tatt i betraktning stoffets betydning for moren. Neoral inneholder etanol. Etanol vil være tilstede i morsmelk i nivåer som ligner på det som finnes i mors serum, og hvis det finnes i morsmelk vil det absorberes oralt av et ammende spedbarn (se ADVARSLER ).
Pediatrisk bruk
Selv om det ikke er fullført tilstrekkelige og godt kontrollerte studier på barn, har transplanterte så unge som ett år fått Neoral uten uvanlige bivirkninger. Sikkerhet og effekt av Neoral-behandling hos barn med juvenil revmatoid artritt eller psoriasis under 18 år er ikke fastslått.
Geriatrisk bruk
kliniske studier med revmatoid artritt med ciklosporin var 17,5 % av pasientene 65 år eller eldre. Disse pasientene hadde større sannsynlighet for å utvikle systolisk hypertensjon under behandling, og mer sannsynlig at de viste serumkreatininstigninger ≥ 50 % over baseline etter 3 til 4 måneders behandling.
Kliniske studier av Neoral 100 mg hos transplanterte og psoriasispasienter inkluderte ikke et tilstrekkelig antall forsøkspersoner i alderen 65 år og over til å avgjøre om de responderer annerledes enn yngre forsøkspersoner. Andre rapporterte kliniske erfaringer har ikke identifisert forskjeller i respons mellom eldre og yngre pasienter. Generelt bør dosevalg for en eldre pasient være forsiktig, vanligvis fra den lave enden av doseringsområdet, noe som gjenspeiler den høyere frekvensen av nedsatt lever-, nyre- eller hjertefunksjon, og samtidig sykdom eller annen medikamentell behandling.
OVERDOSE
Det er minimal erfaring med overdosering av ciklosporin. Tvungen brekninger og mageskylling kan være av verdi opptil 2 timer etter administrering av Neoral. Forbigående levertoksisitet og nefrotoksisitet kan forekomme, som bør forsvinne etter seponering av legemidlet. Orale doser av ciklosporin opp til 10 g (ca. 150 mg/kg) har blitt tolerert med relativt små kliniske konsekvenser, som oppkast, døsighet, hodepine, takykardi og, hos noen få pasienter, moderat alvorlig, reversibel nedsatt nyrefunksjon. Imidlertid er alvorlige symptomer på forgiftning rapportert etter utilsiktet parenteral overdosering med ciklosporin hos premature nyfødte. Generelle støttetiltak og symptomatisk behandling bør følges i alle tilfeller av overdosering. Syklosporin er ikke dialyserbart i særlig grad, og det fjernes heller ikke godt ved kullhemoperfusjon. Den orale dosen der halvparten av forsøksdyrene anslås å dø er 31 ganger, 39 ganger og > 54 ganger human vedlikeholdsdose for transplanterte pasienter (6 mg/kg; korreksjoner basert på kroppsoverflate) hos mus, rotter og kaniner .
KONTRAINDIKASJONER
Generell
Neoral 100mg er kontraindisert hos pasienter med overfølsomhet overfor ciklosporin eller noen av ingrediensene i formuleringen.
Leddgikt
Pasienter med revmatoid artritt med unormal nyrefunksjon, ukontrollert hypertensjon eller maligniteter bør ikke få Neoral.
Psoriasis
Psoriasispasienter som behandles med Neoral 100 mg bør ikke få samtidig PUVA- eller UVB-behandling, metotreksat eller andre immunsuppressive midler, kulltjære eller strålebehandling. Psoriasispasienter med unormal nyrefunksjon, ukontrollert hypertensjon eller malignitet bør ikke få Neoral.
KLINISK FARMAKOLOGI
Cyklosporin er et kraftig immunsuppressivt middel som hos dyr forlenger overlevelsen av allogene transplantasjoner som involverer hud, nyre, lever, hjerte, bukspyttkjertel, benmarg, tynntarm og lunge. Cyklosporin har vist seg å undertrykke en viss humoral immunitet og i større grad cellemedierte immunreaksjoner som allograftavstøtning, forsinket overfølsomhet, eksperimentell allergisk encefalomyelitt, Freunds adjuvansartritt og graft versus host sykdom hos mange dyrearter for en rekke organer. .
Effektiviteten til ciklosporin er et resultat av spesifikk og reversibel hemming av immunkompetente lymfocytter i G0- og G1-fasen av cellesyklusen. T-lymfocytter hemmes fortrinnsvis. T-hjelpercellen er hovedmålet, selv om Tsuppressor-cellen også kan være undertrykt. Cyklosporin hemmer også lymfokinproduksjon og -frigjøring, inkludert interleukin-2.
Ingen effekter på fagocytisk funksjon (endringer i enzymsekresjoner, kjemotaktisk migrasjon av granulocytter, makrofagmigrering, karbonclearance in vivo) er påvist hos dyr. Syklosporin forårsaker ikke benmargsundertrykkelse i dyremodeller eller mennesker.
Farmakokinetikk
Den immunsuppressive aktiviteten til ciklosporin skyldes først og fremst modermedisinen. Etter oral administrering er absorpsjonen av ciklosporin ufullstendig. Graden av absorpsjon av ciklosporin er avhengig av den enkelte pasient, pasientpopulasjonen og formuleringen. Eliminering av ciklosporin er primært biliær med kun 6 % av dosen (modermedikament og metabolitter) utskilles i urinen. Disponeringen av ciklosporin fra blod er vanligvis bifasisk, med en terminal halveringstid på ca. 8,4 timer (fra 5 til 18 timer). Etter intravenøs administrering er blodclearance av ciklosporin (analyse: HPLC) ca. 5 til 7 ml/min/kg hos voksne mottakere av nyre- eller leverallograft. Blodsyklosporinclearance ser ut til å være litt langsommere hos hjertetransplanterte pasienter.
Neoral Soft Gelatin Capsules (cyclosporine capsules, USP) MODIFIED og Neoral Oral Solution (cyclosporine oral solution, USP) MODIFIED er bioekvivalente. Neoral 25 mg mikstur fortynnet med appelsinjuice eller eplejuice er bioekvivalent med Neoral mikstur fortynnet med vann. Effekten av melk på biotilgjengeligheten av ciklosporin når det administreres som Neoral Oral Solution har ikke blitt evaluert.
Forholdet mellom administrert dose og eksponering (areal under kurven for konsentrasjon versus tid, AUC) er lineær innenfor det terapeutiske doseområdet. Variabiliteten mellom individene (total, %CV) av ciklosporineksponering (AUC) når Neoral eller Sandimmune administreres varierer fra omtrent 20 % til 50 % hos nyretransplanterte pasienter. Denne interindividuelle variasjonen bidrar til behovet for individualisering av doseringsregimet for optimal terapi (se DOSERING OG ADMINISTRASJON ).
Variabiliteten i AUC hos nyretransplanterte (%CV) var 9 % til 21 % for Neoral og 19 % til 26 % for Sandimmune. I de samme studiene var variasjonen i bunnkonsentrasjoner (%CV) mellom individer 17 % til 30 % for Neoral og 16 % til 38 % for Sandimmune.
Absorpsjon
Neoral har økt biotilgjengelighet sammenlignet med Sandimmune. Den absolutte biotilgjengeligheten av ciklosporin administrert som Sandimmune er avhengig av pasientpopulasjonen, beregnet til å være mindre enn 10 % hos levertransplanterte pasienter og så stor som 89 % hos enkelte nyretransplanterte pasienter. Den absolutte biotilgjengeligheten av ciklosporin administrert som Neoral er ikke bestemt hos voksne. I studier av nyretransplanterte, revmatoid artritt- og psoriasispasienter var gjennomsnittlig ciklosporin-AUC ca. 20 % til 50 % høyere og maksimal ciklosporinkonsentrasjon i blodet var ca. 40 % til 106 % høyere etter administrering av Neoral 100 mg sammenlignet med etter administrering av Sandimmune . Den dosenormaliserte AUC hos de novo levertransplanterte pasienter administrert Neoral 28 dager etter transplantasjon var 50 % høyere og Cmax var 90 % høyere enn hos de pasientene som fikk Sandimmune. AUC og Cmax er også økt (neoralt i forhold til Sandimmune) hos hjertetransplanterte pasienter, men data er svært begrenset. Selv om AUC- og Cmax-verdiene er høyere på Neoral 100 mg i forhold til Sandimmune, er bunnkonsentrasjonene før dose (dosenormalisert) like for de to formuleringene.
Etter oral administrering av Neoral varierte tiden til maksimal ciklosporinkonsentrasjon i blodet (Tmax) fra 1,5 til 2,0 timer. Administrering av mat med Neoral 25 mg reduserer ciklosporin AUC og Cmax. Et fettrikt måltid (669 kcal, 45 gram fett) inntatt innen en halv time før Neoral 25 mg administrering reduserte AUC med 13 % og Cmax med 33 %. Effektene av et fettfattig måltid (667 kcal, 15 gram fett) var like.
Effekten av T-rørsavledning av galle på absorpsjonen av ciklosporin fra Neoral 25 mg ble undersøkt hos elleve de novo levertransplanterte pasienter. Når pasientene ble administrert Neoral med og uten T-rørsavledning av galle, ble det observert svært liten forskjell i absorpsjon, målt ved endringen i maksimale ciklosporin-blodkonsentrasjoner fra før-doseverdier med T-røret lukket i forhold til når det var åpen: 6,9 ± 41 % (område 55 % til 68 %).
PasientpopulasjonFordeling
Syklosporin distribueres stort sett utenfor blodvolumet. Distribusjonsvolumet ved steady state under intravenøs dosering er rapportert som 3 til 5 l/kg hos mottakere av solide organtransplantasjoner. I blod er fordelingen konsentrasjonsavhengig. Omtrent 33 % til 47 % er i plasma, 4 % til 9 % i lymfocytter, 5 % til 12 % i granulocytter og 41 % til 58 % i erytrocytter. Ved høye konsentrasjoner blir bindingskapasiteten til leukocytter og erytrocytter mettet. I plasma er omtrent 90 % bundet til proteiner, først og fremst lipoproteiner. Syklosporin skilles ut i morsmelk (se FORHOLDSREGLER , Ammende mødre ).
Metabolisme
Syklosporin metaboliseres i stor grad av cytokrom P-450 3A enzymsystemet i leveren, og i mindre grad i mage-tarmkanalen og nyrene. Metabolismen av ciklosporin kan endres ved samtidig administrering av en rekke midler (se FORHOLDSREGLER , NARKOTIKAHANDEL ). Minst 25 metabolitter er identifisert fra menneskelig galle, avføring, blod og urin. Den biologiske aktiviteten til metabolittene og deres bidrag til toksisitet er betydelig mindre enn moderforbindelsen. Hovedmetabolittene (M1, M9 og M4N) skyldes oksidasjon i henholdsvis 1-beta-, 9-gamma- og 4-N-demetylerte posisjoner. Ved steady state etter oral administrering av Sandimmune er gjennomsnittlig AUC for blodkonsentrasjoner av M1, M9 og M4N henholdsvis ca. 70 %, 21 % og 7,5 % av AUC for ciklosporinkonsentrasjoner i blodet. Basert på blodkonsentrasjonsdata fra stabile nyretransplanterte pasienter (13 pasienter administrert Neoral og Sandimmune i en crossover-studie), og gallekonsentrasjonsdata fra de novo levertransplanterte pasienter (4 administrerte Neoral 100 mg, 3 administrerte Sandimmune), prosentandelen av dosen tilstede som M1-, M9- og M4N-metabolitter er like når enten Neoral 25 mg eller Sandimmune administreres.
Utskillelse
Bare 0,1 % av en ciklosporindose skilles ut uendret i urinen. Eliminasjon er primært biliær med kun 6 % av dosen (modermedikament og metabolitter) utskilles i urinen. Verken dialyse eller nyresvikt endrer ciklosporinclearance nevneverdig.
Narkotikahandel
(Se FORHOLDSREGLER , NARKOTIKAHANDEL ) Når diklofenak eller metotreksat ble administrert samtidig med ciklosporin hos pasienter med revmatoid artritt, var AUC for diklofenak og metotreksat signifikant økt (se FORHOLDSREGLER , NARKOTIKAHANDEL ). Ingen klinisk signifikante farmakokinetiske interaksjoner forekom mellom ciklosporin og aspirin, ketoprofen, piroksikam eller indometacin.
Spesifikke populasjoner
Nedsatt nyrefunksjon
en studie utført på 4 personer med nyresykdom i sluttstadiet (kreatininclearance
Nedsatt leverfunksjon
Syklosporin metaboliseres i stor grad av leveren. Siden alvorlig nedsatt leverfunksjon kan føre til betydelig økt eksponering for ciklosporin, kan det være nødvendig å redusere doseringen av ciklosporin hos disse pasientene.
Pediatrisk populasjon
Farmakokinetiske data fra pediatriske pasienter som får Neoral eller Sandimmune er svært begrenset. Hos 15 nyretransplanterte pasienter i alderen 3-16 år var ciklosporin fullblodsclearance etter IV administrering av Sandimmune 10,6 ± 3,7 ml/min/kg (analyse: Cyclo-trac-spesifikk RIA). I en studie med 7 nyretransplanterte pasienter i alderen 2 til 16 år varierte ciklosporinclearance fra 9,8 til 15,5 ml/min/kg. Hos 9 levertransplanterte pasienter i alderen 0,6 til 5,6 år var clearance 9,3 ± 5,4 ml/min/kg (analyse: HPLC).
I den pediatriske populasjonen viser Neoral også en økt biotilgjengelighet sammenlignet med Sandimmune. Hos 7 lever de novo-transplanterte pasienter i alderen 1,4 til 10 år var den absolutte biotilgjengeligheten av Neoral 43 % (område 30 % til 68 %) og for Sandimmune hos de samme individene var absolutt biotilgjengelighet 28 % (område 17 % til 42 %).
Geriatrisk befolkning
Sammenligning av enkeltdosedata fra både normale eldre frivillige (N = 18, gjennomsnittsalder 69 år) og eldre pasienter med revmatoid artritt (N = 16, gjennomsnittsalder 68 år) med enkeltdosedata hos unge voksne frivillige (N = 16, gjennomsnittsalder) 26 år) viste ingen signifikant forskjell i farmakokinetiske parametere.
Kliniske studier
Leddgikt
Effektiviteten av Sandimmune og Neoral 100 mg i behandlingen av alvorlig revmatoid artritt ble evaluert i 5 kliniske studier med totalt 728 ciklosporinbehandlede pasienter og 273 placebobehandlede pasienter.
En oppsummering av resultatene er presentert for "responder"-ratene per behandlingsgruppe, der en responder er definert som en pasient som har fullført forsøket med en 20 % forbedring i ømme og hovne ledd og en 20 % forbedring i 2 av 4 av etterforsker globale, pasient globale, funksjonshemming og erytrocyttsedimentasjonsrater (ESR) for studiene 651 og 652 og 3 av 5 av etterforsker globalt, pasient globalt, funksjonshemming, visuell analog smerte og ESR for studiene 2008, 654 og 302.
Studie 651 inkluderte 264 pasienter med aktiv revmatoid artritt med minst 20 involverte ledd, som hadde sviktet minst ett hovedlegemiddel mot RA, ved å bruke en 3:3:2 randomisering til en av følgende tre grupper: (1) ciklosporin dosert ved 2,5 til 5 mg/kg/dag, (2) metotreksat ved 7,5 til 15 mg/uke, eller (3) placebo. Behandlingsvarigheten var 24 uker. Gjennomsnittlig ciklosporindose ved siste besøk var 3,1 mg/kg/dag. Se grafen nedenfor.
Studie 652 inkluderte 250 pasienter med aktiv RA med > 6 aktive smertefulle eller ømme ledd som hadde sviktet minst ett større RA-legemiddel. Pasientene ble randomisert ved å bruke en 3:3:2 randomisering til 1 av 3 behandlingsarmer: (1) 1,5 til 5 mg/kg/dag cyklosporin, (2) 2,5 til 5 mg/kg/dag cyklosporin, og (3) placebo. Behandlingsvarigheten var 16 uker. Gjennomsnittlig ciklosporindose for gruppe 2 ved siste besøk var 2,92 mg/kg/dag. Se grafen nedenfor.
Studie 2008 inkluderte 144 pasienter med aktiv RA og > 6 aktive ledd som hadde mislykkede behandlingsforløp med aspirin og gull eller penicillamin. Pasientene ble randomisert til 1 av 2 behandlingsgrupper (1) ciklosporin 2,5 til 5 mg/kg/dag med justeringer etter den første måneden for å oppnå et bunnnivå og (2) placebo. Behandlingsvarigheten var 24 uker. Gjennomsnittlig ciklosporindose ved siste besøk var 3,63 mg/kg/dag. Se grafen nedenfor.
Studie 654 inkluderte 148 pasienter som forble med aktive leddtall på 6 eller mer til tross for behandling med maksimalt tolererte metotreksatdoser i minst tre måneder. Pasientene fortsatte å ta sin nåværende dose metotreksat og ble randomisert til å motta i tillegg en av følgende medisiner: (1) ciklosporin 2,5 mg/kg/dag med doseøkninger på 0,5 mg/kg/dag i uke 2 og 4 hvis det var ingen tegn på toksisitet og ytterligere økninger på 0,5 mg/kg/dag i uke 8 og 16 hvis en
Studie 302 inkluderte 299 pasienter med alvorlig aktiv RA, hvorav 99 % ikke responderte eller var intolerante overfor minst ett tidligere alvorlig RA-legemiddel. Pasientene ble randomisert til 1 av 2 behandlingsgrupper (1) Neoral 25 mg og (2) ciklosporin, som begge ble startet med 2,5 mg/kg/dag og økt etter 4 uker for ineffektivitet i trinn på 0,5 mg/kg/dag til en maksimalt 5 mg/kg/dag og redusert til enhver tid for toksisitet. Behandlingsvarigheten var 24 uker. Gjennomsnittlig ciklosporindose ved siste besøk var 2,91 mg/kg/dag (område: 0,72 til 5,17) for Neoral og 3,27 mg/kg/dag (område: 0,73 til 5,68) for ciklosporin. Se grafen nedenfor.
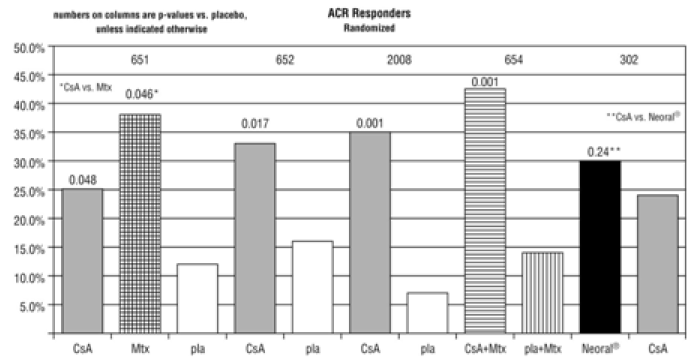
Kliniske studier
I kontrollerte studier var arten, alvorlighetsgraden og forekomsten av bivirkningene som ble observert hos 493 transplanterte pasienter behandlet med Neoral sammenlignbare med de som ble observert hos 208 transplanterte pasienter som fikk Sandimmune i disse samme studiene da dosen av de to legemidlene ble justert. for å oppnå de samme bunnkonsentrasjonene av ciklosporin i blodet.
Basert på historisk erfaring med Sandimmune, oppsto følgende reaksjoner hos 3 % eller mer av 892 pasienter involvert i kliniske studier med nyre-, hjerte- og levertransplantasjoner.
Blant 705 nyretransplanterte pasienter behandlet med ciklosporin mikstur (Sandimmune) i kliniske studier, var årsaken til seponering av behandlingen nyretoksisitet hos 5,4 %, infeksjon hos 0,9 %, manglende effekt hos 1,4 %, akutt tubulær nekrose hos 1,0 %, lymfoproliferative lidelser. hos 0,3 %, hypertensjon hos 0,3 %, og andre årsaker hos 0,7 % av pasientene.
Følgende reaksjoner oppstod hos 2 % eller mindre av ciklosporin-behandlede pasienter: allergiske reaksjoner, anemi, anoreksi, forvirring, konjunktivitt, ødem, feber, sprø negler, gastritt, hørselstap, hikke, hyperglykemi, migrene (neoral), muskelsmerter, magesår, trombocytopeni, tinnitus.
Følgende reaksjoner forekom sjelden: angst, brystsmerter, forstoppelse, depresjon, hårbrudd, hematuri, leddsmerter, sløvhet, munnsår, hjerteinfarkt, nattesvette, pankreatitt, kløe, svelgevansker, prikking, blødning i øvre GI, synsforstyrrelse, svakhet, vekttap.
Pasienter som mottar immunsuppressive terapier, inkludert kurer som inneholder ciklosporin og ciklosporin, har økt risiko for infeksjoner (virale, bakterielle, sopp-, parasittiske). Både generaliserte og lokaliserte infeksjoner kan forekomme. Eksisterende infeksjoner kan også forverres. Dødelige utfall er rapportert (se ADVARSLER ).
Erfaring etter markedsføring, nyre-, lever- og hjertetransplantasjon
Hepatotoksisitet
Tilfeller av levertoksisitet og leverskade, inkludert kolestase, gulsott, hepatitt og leversvikt; alvorlige og/eller dødelige utfall er rapportert (se ADVARSLER , Hepatotoksisitet ).
Økt risiko for infeksjoner
Tilfeller av JC-virusassosiert progressiv multifokal leukoencefalopati (PML), noen ganger dødelig; og polyomavirus-assosiert nefropati (PVAN), spesielt BK-virus som resulterer i transplantattap er rapportert (se ADVARSLER , Polyoma virusinfeksjon ).
Hodepine, inkludert migrene
Tilfeller av migrene er rapportert. I noen tilfeller har pasienter ikke vært i stand til å fortsette med ciklosporin, men den endelige avgjørelsen om behandlingsavbrudd bør tas av den behandlende legen etter en nøye vurdering av fordeler kontra risiko.
Smerter i nedre ekstremiteter
Isolerte tilfeller av smerter i nedre ekstremiteter er rapportert i forbindelse med ciklosporin. Smerter i nedre ekstremiteter har også blitt notert som en del av Calcineurin-Inhibitor Induced Pain Syndrome (CIPS) som beskrevet i litteraturen.
Leddgikt
De viktigste bivirkningene forbundet med bruk av ciklosporin ved revmatoid artritt er nedsatt nyrefunksjon (se ADVARSLER ), hypertensjon (se FORHOLDSREGLER ), hodepine, gastrointestinale forstyrrelser og hirsutisme/hypertrikose.
Hos pasienter med revmatoid artritt behandlet i kliniske studier innenfor det anbefalte doseområdet, ble ciklosporinbehandlingen seponert hos 5,3 % av pasientene på grunn av hypertensjon og hos 7 % av pasientene på grunn av økt kreatinin. Disse endringene er vanligvis reversible med rettidig dosereduksjon eller seponering av medikamentet. Frekvensen og alvorlighetsgraden av forhøyede serumkreatinin øker med dose og varighet av ciklosporinbehandling. Disse økningene vil sannsynligvis bli mer uttalt uten dosereduksjon eller seponering.
Følgende bivirkninger forekom i kontrollerte kliniske studier:
I tillegg er følgende bivirkninger rapportert hos 1 % til
Autonome nervesystem: tørr munn, økt svetting
Kroppen som helhet: allergi, asteni, hetetokter, ubehag, overdose, prosedyre NOS*, tumor NOS*, vektreduksjon, vektøkning
Kardiovaskulær: unormale hjertelyder, hjertesvikt, hjerteinfarkt, perifer iskemi
Sentral- og perifert nervesystem: hypoestesi, nevropati, vertigo
Endokrine: struma
Gastrointestinale: forstoppelse, dysfagi, enanthema, eruktasjon, øsofagitt, magesår, gastritt, gastroenteritt, gingival blødning, glossitt, magesår, spyttkjertelforstørrelse, tungelidelse, tannlidelse
Infeksjon: abscess, bakteriell infeksjon, cellulitt, follikulitt, soppinfeksjon, herpes simplex, herpes zoster, nyreabscess, moniliasis, betennelse i mandlene, virusinfeksjon
Hematologisk: anemi, neseblødning, leukopeni, lymfadenopati
Lever og gallesystem: bilirubinemi
Metabolsk og ernæringsmessig: diabetes mellitus, hyperkalemi, hyperurikemi, hypoglykemi
Muskel- og skjelettsystemet: artralgi, benbrudd, bursitt, leddluksasjon, myalgi, stivhet, synovial cyste, senelidelse
Neoplasmer: brystfibroadenose, karsinom
Psykiatrisk: angst, forvirring, redusert libido, emosjonell labilitet, nedsatt konsentrasjon, økt libido, nervøsitet, paroniria, somnolens
Reproduktiv (kvinnelig): brystsmerter, livmorblødning
Luftveiene: unormale brystlyder, bronkospasmer
Hud og vedheng: unormal pigmentering, angioødem, dermatitt, tørr hud, eksem, neglelidelse, kløe, hudlidelse, urticaria
Spesielle sanser: unormalt syn, grå stær, konjunktivitt, døvhet, øyesmerter, smaksperversjon, tinnitus, vestibulær lidelse
Urinsystemet: unormal urin, hematuri, økt BUN, vannlating haster, nokturi, polyuri, pyelonefritt, urininkontinens
*NOS = Ikke annet spesifisert
Psoriasis
De viktigste bivirkningene forbundet med bruk av ciklosporin hos pasienter med psoriasis er nyredysfunksjon, hodepine, hypertensjon, hypertriglyseridemi, hirsutisme/hypertrikose, parestesi eller hyperestesi, influensalignende symptomer, kvalme/oppkast, diaré, magebesvær, magebesvær, eller leddsmerter.
Hos psoriasispasienter behandlet i amerikanske kontrollerte kliniske studier innenfor anbefalt doseområde, ble ciklosporinbehandlingen seponert hos 1,0 % av pasientene på grunn av hypertensjon og hos 5,4 % av pasientene på grunn av økt kreatinin. I de fleste tilfellene var disse endringene reversible etter dosereduksjon eller seponering av ciklosporin.
Det har vært ett rapportert dødsfall forbundet med bruk av ciklosporin ved psoriasis. En 27 år gammel mann utviklet nyreforverring og ble fortsatt på ciklosporin. Han hadde progressiv nyresvikt som førte til døden.
Frekvens og alvorlighetsgrad av serumkreatinin øker med dose og varighet av ciklosporinbehandling. Disse økningene vil sannsynligvis bli mer uttalte og kan føre til irreversibel nyreskade uten dosereduksjon eller seponering.
Følgende hendelser oppsto hos 1 % til mindre enn 3 % av psoriasispasientene behandlet med ciklosporin:
Kroppen som helhet: feber, rødmer, hetetokter
Kardiovaskulær: brystsmerter
Sentral- og perifert nervesystem: økt appetitt, søvnløshet, svimmelhet, nervøsitet, svimmelhet
Gastrointestinale: abdominal oppblåsthet, forstoppelse, gingival blødning
Lever og gallesystem: hyperbilirubinemi
Neoplasmer: hudkreft [plateepitel- (0,9 %) og basalcelle- (0,4 %) karsinomer]
Retikuloendotelial: blodplate-, blødnings- og koagulasjonsforstyrrelser, røde blodlegemer
Luftveiene: infeksjon, viral og annen infeksjon
Hud og vedheng: akne, follikulitt, keratose, kløe, utslett, tørr hud
Urinsystemet: miksjonsfrekvens
Syn: unormalt syn
Mild hypomagnesemi og hyperkalemi kan forekomme, men er asymptomatiske. Økning i urinsyre kan forekomme, og angrep av gikt er sjelden rapportert. En mindre og doserelatert hyperbilirubinemi har blitt observert i fravær av hepatocellulær skade. Syklosporinbehandling kan være assosiert med en beskjeden økning av serumtriglyserider eller kolesterol. Forhøyelser av triglyserider (> 750 mg/dL) forekommer hos ca. 15 % av psoriasispasientene; forhøyelser av kolesterol (> 300 mg/dL) er observert hos mindre enn 3 % av psoriasispasientene. Vanligvis er disse laboratorieavvik reversible ved dosereduksjon eller seponering av ciklosporin.
Postmarketing-erfaring, psoriasis
Tilfeller av transformasjon til erytrodermisk psoriasis eller generalisert pustuløs psoriasis ved enten seponering eller reduksjon av ciklosporin hos pasienter med kronisk plakkpsoriasis er rapportert.
PASIENTINFORMASJON
Pasienter bør informeres om at enhver endring av ciklosporinformuleringen bør gjøres med forsiktighet og kun under tilsyn av lege, fordi det kan føre til behov for endring i dosen.
Pasienter bør informeres om nødvendigheten av gjentatte laboratorietester mens de får ciklosporin. Pasienter bør informeres om potensielle risikoer under graviditet og informeres om økt risiko for neoplasi. Pasienter bør også informeres om risikoen for hypertensjon og nedsatt nyrefunksjon.
Pasienter bør informeres om at vaksinasjon under behandling med ciklosporin kan være mindre effektiv og bruk av levende svekkede vaksiner bør unngås.
Pasienter bør gis nøye doseringsinstruksjoner. Neoral mikstur (ciklosporin mikstur, USP) MODIFIED bør fortynnes, helst med appelsin- eller eplejuice som har romtemperatur. Kombinasjonen av Neoral oral oppløsning (ciklosporin oral oppløsning, USP) MODIFISERT med melk kan være usmakelig.
Pasienter bør rådes til å ta Neoral 100 mg på en konsistent tidsplan med hensyn til tidspunkt på dagen og forhold til måltider. Grapefrukt og grapefruktjuice påvirker metabolismen, øker blodkonsentrasjonen av ciklosporin, og bør derfor unngås.
