Flonase Nasal Spray 50mcg Fluticasone Bruk, bivirkninger og dosering. Pris i nettapotek. Generisk medisin uten resept.
Hva er Flonase og hvordan brukes det?
Flonase er en reseptbelagt medisin som brukes til å behandle symptomene på allergisk rhinitt (nysing, rennende nese og kløende eller rennende øyne) og nesepolypper. Flonase kan brukes alene eller sammen med andre medisiner.
Flonase tilhører en klasse legemidler som kalles kortikosteroider, intranasale, immunsuppressive midler, PHD.
Det er ikke kjent om Flonase er trygt og effektivt hos barn under 4 år.
Hva er de mulige bivirkningene av Flonase?
Flonase kan forårsake alvorlige bivirkninger, inkludert:
- . alvorlige eller pågående neseblødninger, . støyende pust, . rennende nese, . skorpe rundt neseborene dine, . rødhet, sår eller hvite flekker i munnen eller halsen, . feber, . frysninger, . Smerter i kroppen, . tåkesyn, . øyesmerter, . ser glorier rundt lys, . sår som ikke vil gro, . forverret tretthet, . muskel svakhet, . svimmelhet, . kvalme, og . oppkast
Få medisinsk hjelp med en gang hvis du har noen av symptomene nevnt ovenfor.
De vanligste bivirkningene av Flonase inkluderer:
- . mindre neseblod, . brenning eller kløe i nesen, . sår eller hvite flekker inne i eller rundt nesen, . hoste, . problemer med å puste, . hodepine, . ryggsmerte, . bihulesmerter, . sår hals, . feber, . kvalme, og . oppkast
BESKRIVELSE
Den aktive komponenten i FLONASE nesespray 50mcg er flutikasonpropionat, et kortikosteroid med det kjemiske navnet S-(fluormetyl) 6α,9-difluoro-11β,17-dihydroksy-16α-metyl-3oksoandrosta-1,4-dien-17β-karbotioat , 17-propionat og følgende kjemiske struktur:
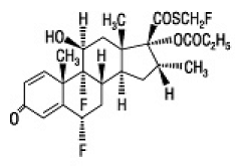
Flutikasonpropionat er et hvitt pulver med en molekylvekt på 500,6, og den empiriske formelen er C25H31F3O5S. Det er praktisk talt uløselig i vann, fritt løselig i dimetylsulfoksid og dimetylformamid, og lett løselig i metanol og 95 % etanol.
FLONASE Nesespray, 50 mcg er en vandig suspensjon av mikrofin flutikasonpropionat for topisk administrering til neseslimhinnen ved hjelp av en doseringsspraypumpe. FLONASE Nesespray 50 mcg inneholder også mikrokrystallinsk cellulose og karboksymetylcellulosenatrium, dekstrose, 0,02 % w/w benzalkoniumklorid, polysorbat 80 og 0,25 % w/w fenyletylalkohol, og har en pH mellom 5 og 7.
Etter innledende priming leverer hver aktivering 50 mcg flutikasonpropionat i 100 mg formulering gjennom neseadapteren.
INDIKASJONER
FLONASE® nesespray er indisert for behandling av nesesymptomer på flerårig ikke-allergisk rhinitt hos voksne og pediatriske pasienter i alderen 4 år og eldre.
DOSERING OG ADMINISTRASJON
Administrer kun FLONASE nesespray intranasal vei. Prime FLONASE nesespray før første gangs bruk eller etter en periode uten bruk (1 uke eller mer) ved å riste innholdet godt og slippe 6 sprayer ut i luften vekk fra ansiktet. Rist FLONASE nesespray forsiktig før hver bruk.
Pasienter bør bruke FLONASE nesespray med jevne mellomrom siden effektiviteten avhenger av regelmessig bruk. Maksimal effekt kan ta flere dager og individuelle pasienter vil oppleve varierende tid til debut og ulik grad av symptomlindring.
Voksne
Anbefalt startdose hos voksne er 2 sprayer (50 mcg flutikasonpropionat hver) i hvert nesebor én gang daglig (total daglig dose, 200 mcg). Den samme totale daglige dosen, 1 spray i hvert nesebor administrert to ganger daglig (f.eks. kl. 08.00 og kl. 20.00) er også effektiv. Etter de første dagene kan pasienter være i stand til å redusere dosen til 1 spray i hvert nesebor én gang daglig for vedlikeholdsbehandling.
Maksimal totale daglige dose bør ikke overstige 2 spray i hvert nesebor (total dose, 200 mcg/dag). Det er ingen bevis for at overskridelse av anbefalt dose er mer effektivt.
Ungdom og barn (i alderen 4 år og eldre)
Anbefalt startdose hos ungdom og barn i alderen 4 år og eldre er 1 spray i hvert nesebor én gang daglig (total daglig dose, 100 mcg). Pasienter som ikke responderer tilstrekkelig på 1 spray i hvert nesebor, kan bruke 2 spray i hvert nesebor en gang daglig (total daglig dose, 200 mcg). Når tilstrekkelig kontroll er oppnådd, bør dosen reduseres til 1 spray i hvert nesebor én gang daglig.
Den maksimale totale daglige dosen bør ikke overstige 2 sprayer i hvert nesebor (200 mcg/dag). Det er ingen bevis for at overskridelse av anbefalt dose er mer effektivt.
HVORDAN LEVERES
Doseringsformer og styrker
FLONASE Nesespray er en nesespraysuspensjon. Hver 100 mg spray gir 50 mcg flutikasonpropionat.
Oppbevaring og håndtering
FLONASE Nesespray, 50 mcg leveres i en gul glassflaske utstyrt med en hvit doseringsforstøvningspumpe, hvit neseadapter og grønt støvdeksel i en boks med 1 ( NDC 0173-0453-01) med FDA-godkjent Pasientmerking (se Pasientens bruksanvisning for riktig aktivering av enheten ). Hver flaske inneholder en netto fyllvekt på 16 g og vil gi 120 aktiveringer. Hver aktivering leverer 50 mcg flutikasonpropionat i 100 mg formulering gjennom neseadapteren. Riktig mengde medisiner i hver spray kan ikke garanteres etter 120 sprayer selv om flasken ikke er helt tom. Flasken skal kastes når det merkede antallet aktiveringer er brukt.
Oppbevares mellom 4° og 30°C (39° og 86°F).
GlaxoSmithKline Research Triangle Park, NC 27709. Revidert: Jan 2015
BIVIRKNINGER
Systemisk og lokal kortikosteroidbruk kan føre til følgende:
- . Neseblødning, nesesår, Candida albicans-infeksjon, perforering av neseseptum og nedsatt sårtilheling [se ADVARSLER OG FORHOLDSREGLER ] . Grå stær og glaukom [se ADVARSLER OG FORHOLDSREGLER ] . Immunsuppresjon [se ADVARSLER OG FORHOLDSREGLER ] . Hyperkortisisme og binyresuppresjon [se ADVARSLER OG FORHOLDSREGLER ] . Effekt på vekst [se ADVARSLER OG FORHOLDSREGLER ]
Erfaring fra kliniske forsøk
Fordi kliniske studier utføres under vidt forskjellige forhold, kan bivirkningsrater observert i kliniske studier av et medikament ikke sammenlignes direkte med rater i kliniske studier av et annet medikament og gjenspeiler kanskje ikke ratene observert i praksis.
I kontrollerte amerikanske kliniske studier fikk mer enn 3300 personer med allergisk og ikke-allergisk rhinitt behandling med intranasal flutikasonpropionat. Generelt har bivirkninger i kliniske studier primært vært assosiert med irritasjon av neseslimhinnene, og bivirkningene ble rapportert med omtrent samme frekvens av personer behandlet med placebo. Mindre enn 2 % av pasientene i kliniske studier avbrøt på grunn av bivirkninger; denne frekvensen var lik for vehikelplacebo og aktive komparatorer.
Sikkerhetsdataene beskrevet nedenfor er basert på 7 placebokontrollerte kliniske studier hos personer med allergisk rhinitt. De 7 studiene inkluderte 536 forsøkspersoner (57 jenter og 108 gutter i alderen 4 til 11 år, 137 kvinner og 234 mannlige ungdommer og voksne) behandlet med FLONASE 200 mcg én gang daglig over 2 til 4 uker og 2 placebokontrollerte kliniske studier som inkluderte 246 personer (119 kvinner og 127 mannlige ungdommer og voksne) behandlet med FLONASE 200 mcg én gang daglig over 6 måneder (tabell 1). Også inkludert i tabell 1 er bivirkninger fra 2 studier der 167 barn (45 jenter og 122 gutter i alderen 4 til 11 år) ble behandlet med FLONASE 100 mcg én gang daglig i 2 til 4 uker.
Andre bivirkninger med FLONASE nesespray 50mcg observert med en forekomst mindre enn eller lik 3 %, men større enn eller lik 1 % og mer vanlige enn med placebo inkludert: blod i neseslimet, rennende nese, magesmerter, diaré, feber, influensalignende symptomer, smerter, svimmelhet og bronkitt.
Postmarketing-erfaring
tillegg til bivirkninger rapportert fra kliniske studier, har følgende bivirkninger blitt identifisert under bruk av intranasal flutikasonpropionat etter godkjenning. Fordi disse reaksjonene rapporteres frivillig fra en populasjon av usikker størrelse, er det ikke alltid mulig å pålitelig estimere frekvensen deres eller etablere en årsakssammenheng med legemiddeleksponering. Disse hendelsene er valgt for inkludering enten på grunn av deres alvorlighet, hyppighet av rapportering eller årsakssammenheng til flutikasonpropionat eller en kombinasjon av disse faktorene.
Generelle lidelser og administrasjonsbetingelser
Overfølsomhetsreaksjoner, inkludert angioødem, hudutslett, ødem i ansikt og tunge, pruritus, urticaria, bronkospasme, hvesing, dyspné og anafylaksi/anafylaktoide reaksjoner, som i sjeldne tilfeller var alvorlige.
Øre- og labyrintlidelser
Endring eller tap av smaks- og/eller luktesans og, i sjeldne tilfeller, perforering av neseseptum, nesesår, sår hals, irritasjon og tørrhet i halsen, hoste, heshet og stemmeendringer.
Øyelidelser
Tørrhet og irritasjon, konjunktivitt, tåkesyn, glaukom, økt intraokulært trykk og grå stær.
Tilfeller av veksthemming er rapportert for intranasale kortikosteroider, inkludert FLONASE [se ADVARSLER OG FORHOLDSREGLER ].
NARKOTIKAHANDEL
Hemmere av Cytokrom P450 3A4
Flutikasonpropionat er et substrat for CYP3A4. Bruk av sterke CYP3A4-hemmere (f.eks. ritonavir, atazanavir, klaritromycin, indinavir, itrakonazol, nefazodon, nelfinavir, sakinavir, ketokonazol, telitromycin, konivaptan, lopinavir, nefazodon, voriconazole, voriconazole, fordi økt nesesteroideffekt ikke anbefales, fordi FLONASE-systemets adverse effekt ikke anbefales. kan forekomme.
Ritonavir
En legemiddelinteraksjonsstudie med vandig nesespray av flutikasonpropionat hos friske personer har vist at ritonavir (en sterk CYP3A4-hemmer) kan øke plasmaeksponeringen av flutikasonpropionat betydelig, noe som resulterer i betydelig reduserte serumkortisolkonsentrasjoner [se KLINISK FARMAKOLOGI ]. Under bruk etter markedsføring har det vært rapporter om klinisk signifikante legemiddelinteraksjoner hos pasienter som får flutikasonpropionatprodukter, inkludert FLONASE, med ritonavir, noe som har resultert i systemiske kortikosteroideffekter inkludert Cushings syndrom og binyresuppresjon.
Ketokonazol
Samtidig administrering av oralt inhalert flutikasonpropionat (1000 mcg) og ketokonazol (200 mg én gang daglig) resulterte i en 1,9 ganger økning i plasmaflutikasonpropionateksponering og en 45 % reduksjon i plasmakortisolareal under kurven (AUC), men hadde ingen effekt. på urinutskillelse av kortisol.
ADVARSLER
Inkludert som en del av FORHOLDSREGLER seksjon.
FORHOLDSREGLER
Lokale neseeffekter
Epistaxis
kliniske studier av 2 til 26 ukers varighet ble neseblødning observert hyppigere hos personer behandlet med FLONASE nesespray enn de som fikk placebo [se BIVIRKNINGER ].
Nasal sårdannelse
Etter markedsføring er det rapportert tilfeller av nesesår hos pasienter behandlet med FLONASE nesespray [se BIVIRKNINGER ].
Candida-infeksjon
I kliniske studier med flutikasonpropionat administrert intranasalt har utvikling av lokaliserte infeksjoner i nese og svelg med Candida albicans forekommet. Når en slik infeksjon utvikler seg, kan det kreve behandling med passende lokal terapi og seponering av FLONASE nesespray. Pasienter som bruker FLONASE nesespray over flere måneder eller lenger bør undersøkes med jevne mellomrom for tegn på Candida-infeksjon eller andre tegn på bivirkninger på neseslimhinnen.
Perforering av neseseptum
Etter markedsføring er det rapportert tilfeller av perforering av neseseptum hos pasienter behandlet med FLONASE nesespray [se BIVIRKNINGER ].
Nedsatt sårheling
På grunn av den hemmende effekten av kortikosteroider på sårtilheling, bør pasienter som nylig har opplevd nesesår, neseoperasjoner eller nesetraumer unngå å bruke FLONASE nesespray inntil tilheling har funnet sted.
Grønn stær og grå stær
Bruk av intranasale og inhalerte kortikosteroider kan føre til utvikling av glaukom og/eller grå stær. Derfor er nøye overvåking nødvendig hos pasienter med endret syn eller med en historie med økt intraokulært trykk, glaukom og/eller grå stær.
Overfølsomhetsreaksjoner inkludert anafylaksi
Overfølsomhetsreaksjoner (f.eks. anafylaksi, angioødem, urticaria, kontaktdermatitt og utslett) er rapportert etter administrering av FLONASE nesespray. Avslutt FLONASE
Nesespray hvis slike reaksjoner oppstår [se KONTRAINDIKASJONER ]. I sjeldne tilfeller kan det oppstå umiddelbare overfølsomhetsreaksjoner etter administrering av FLONASE nesespray.
Immunsuppresjon
Personer som bruker legemidler som undertrykker immunsystemet er mer utsatt for infeksjoner enn friske personer. Vannkopper og meslinger, for eksempel, kan ha et mer alvorlig eller til og med dødelig forløp hos mottakelige barn eller voksne som bruker kortikosteroider. Hos slike barn eller voksne som ikke har hatt disse sykdommene eller blitt skikkelig immunisert, bør det utvises spesiell forsiktighet for å unngå eksponering. Hvordan dosen, ruten og varigheten av kortikosteroidadministrasjon påvirker risikoen for å utvikle en spredt infeksjon er ikke kjent. Bidraget fra den underliggende sykdommen og/eller tidligere kortikosteroidbehandling til risikoen er heller ikke kjent. Dersom en pasient blir utsatt for vannkopper, kan profylakse med varicella zoster immunglobulin (VZIG) være indisert. Dersom en pasient er eksponert for meslinger, kan profylakse med sammenslått intramuskulært immunglobulin (IG) være indisert. (Se den fullstendige forskrivningsinformasjonen for VZIG og IG. Hvis det utvikler seg vannkopper, kan behandling med antivirale midler vurderes.
Intranasale kortikosteroider bør brukes med forsiktighet, hvis i det hele tatt, hos pasienter med aktive eller hvilende tuberkuløse infeksjoner i luftveiene; systemiske sopp-, bakterie-, virus- eller parasittiske infeksjoner; eller okulær herpes simplex.
Hyperkortisisme og binyresuppresjon
Når intranasale kortikosteroider brukes i høyere doser enn anbefalt eller hos mottakelige personer ved anbefalte doser, kan systemiske kortikosteroideffekter som hyperkortisisme og binyresuppresjon vises. Hvis slike endringer oppstår, bør doseringen av FLONASE nesespray seponeres sakte i samsvar med aksepterte prosedyrer for seponering av oral kortikosteroidbehandling.
Utskifting av et systemisk kortikosteroid med et lokalt kortikosteroid kan være ledsaget av tegn på binyrebarksvikt. I tillegg kan noen pasienter oppleve symptomer på kortikosteroidabstinens (f.eks. ledd- og/eller muskelsmerter, slapphet, depresjon). Pasienter som tidligere er behandlet i lengre perioder med systemiske kortikosteroider og overført til topikale kortikosteroider, bør overvåkes nøye for akutt binyrebarksvikt som respons på stress. Hos pasienter som har astma eller andre kliniske tilstander som krever langvarig systemisk kortikosteroidbehandling, kan raske reduksjoner i systemiske kortikosteroiddoser forårsake en alvorlig forverring av symptomene deres.
Legemiddelinteraksjoner med sterke cytokrom P450 3A4-hemmere
Bruk av sterke cytokrom P450 3A4 (CYP3A4)-hemmere (f.eks. ritonavir, atazanavir, klaritromycin, indinavir, itrakonazol, nefazodon, nelfinavir, sakinavir, ketokonazol, telitromycin, konivaptan, lopinavir, lopinavir, nefazodon, fordi det ikke anbefales med vor FL nefconazolase) økte systemiske kortikosteroidbivirkninger kan forekomme [se NARKOTIKAHANDEL , KLINISK FARMAKOLOGI ].
Effekt på vekst
Intranasale kortikosteroider kan forårsake reduksjon i veksthastighet når de administreres til pediatriske pasienter [se Bruk i spesifikke populasjoner ]. Overvåk veksten rutinemessig hos pediatriske pasienter som får FLONASE nesespray. For å minimere de systemiske effektene av intranasale kortikosteroider, inkludert FLONASE nesespray, titreres hver pasients dose til den laveste dosen som effektivt kontrollerer hans/hennes symptomer [se DOSERING OG ADMINISTRASJON , Bruk i spesifikke populasjoner ].
Informasjon om pasientveiledning
Råd pasienten til å lese den FDA-godkjente pasientmerkingen ( PASIENTINFORMASJON og bruksanvisning ).
Lokale neseeffekter
Informer pasienter om at behandling med FLONASE nesespray 50mcg kan føre til bivirkninger, som inkluderer neseblødning og nesesår. Candida-infeksjon kan også forekomme ved behandling med FLONASE nesespray. I tillegg har FLONASE nesespray 50mcg vært assosiert med perforering av neseseptum og nedsatt sårtilheling. Pasienter som nylig har opplevd nesesår, neseoperasjoner eller nesetraumer bør ikke bruke FLONASE nesespray 50mcg før tilheling har funnet sted [se ADVARSLER OG FORHOLDSREGLER ].
Grønn stær og grå stær
Informer pasienter om at glaukom og grå stær er assosiert med bruk av nasal og inhalerte kortikosteroider. Oppfordre pasienter til å varsle helsepersonell dersom en endring i synet registreres mens de bruker FLONASE nesespray [se ADVARSLER OG FORHOLDSREGLER ].
Overfølsomhetsreaksjoner, inkludert anafylaksi
Informer pasienter om at overfølsomhetsreaksjoner, inkludert anafylaksi, angioødem, urticaria, kontaktdermatitt og utslett, kan oppstå etter administrering av FLONASE nesespray. Hvis slike reaksjoner oppstår, bør pasienter slutte å bruke FLONASE nesespray [se ADVARSLER OG FORHOLDSREGLER ].
Immunsuppresjon
Advar pasienter som er på immunsuppressive doser av kortikosteroider for å unngå eksponering for vannkopper eller meslinger, og hvis de blir utsatt for å konsultere helsepersonell uten forsinkelse. Informer pasienter om potensiell forverring av eksisterende tuberkulose; sopp-, bakterie-, virus- eller parasittiske infeksjoner; eller okulær herpes simplex [se ADVARSLER OG FORHOLDSREGLER ].
Redusert veksthastighet
Informer foreldre om at FLONASE nesespray 50mcg kan forårsake en reduksjon i veksthastigheten når den administreres til pediatriske pasienter. Leger bør følge nøye med på veksten til barn og ungdom som tar kortikosteroider uansett vei [se ADVARSLER OG FORHOLDSREGLER , Pediatrisk bruk ].
Bruk daglig for best effekt
Informer pasientene om at de bør bruke FLONASE nesespray 50mcg regelmessig. FLONASE Nesespray 50mcg, som andre kortikosteroider, har ikke umiddelbar effekt på rhinittsymptomer. Maksimal fordel kan ikke nås før flere dager. Pasienter bør ikke øke den foreskrevne dosen, men bør kontakte helsepersonell dersom symptomene ikke blir bedre eller hvis tilstanden forverres.
Hold spray ute av øyne og munn
Informer pasienter om å unngå å spraye FLONASE nesespray i øynene og munnen.
Ikke-klinisk toksikologi
Karsinogenese, mutagenese, svekkelse av fruktbarhet
Flutikasonpropionat viste ingen tumorogent potensial hos mus ved orale doser opptil 1000 mcg/kg (omtrent 20 ganger MRHDID hos voksne og omtrent 10 ganger MRHDID hos barn på mcg/m² basis) i 78 uker eller hos rotter ved inhalasjonsdoser opp. til 57 mcg/kg (omtrent 2 ganger MRHDID hos voksne og omtrent tilsvarende MRHDID hos barn på mcg/m² basis) i 104 uker.
Flutikasonpropionat induserte ikke genmutasjon i prokaryote eller eukaryote celler in vitro. Ingen signifikant klastogen effekt ble sett i dyrkede humane perifere lymfocytter in vitro eller i mikronukleustesten hos mus.
Ingen tegn på nedsatt fertilitet ble observert hos hann- og hunnrotter ved subkutane doser på opptil 50 mcg/kg (ca. 2 ganger MRHDID hos voksne på mcg/m²-basis). Prostatavekten ble betydelig redusert ved en subkutan dose på 50 mcg/kg.
Kliniske studier
Flerårig ikke-allergisk rhinitt
Tre randomiserte, dobbeltblindede, parallellgruppe, placebokontrollerte vehikelforsøk ble utført på 1191 personer for å undersøke regelmessig bruk av FLONASE nesespray 50 mcg hos personer med flerårig ikke-allergisk rhinitt. Disse studiene evaluerte individ-vurderte total nasale symptomscore (TNSS) som inkluderte neseobstruksjon, postnasal drypp, rhinoré hos forsøkspersoner som ble behandlet i 28 dager med dobbeltblind terapi og i 1 av de 3 studiene for 6 måneders åpen behandling. To av disse studiene viste at forsøkspersoner behandlet med FLONASE nesespray (100 mcg to ganger daglig) viste statistisk signifikant reduksjon i TNSS sammenlignet med forsøkspersoner behandlet med vehikel.
Bruk i spesifikke populasjoner
Svangerskap
Teratogene effekter
Graviditetskategori C. Det er ingen tilstrekkelige og godt kontrollerte studier med FLONASE nesespray hos gravide kvinner. Kortikosteroider har vist seg å være teratogene hos laboratoriedyr når de administreres systemisk i relativt lave dosenivåer. Fordi reproduksjonsstudier på dyr ikke alltid er prediktive for menneskelig respons, bør FLONASE nesespray kun brukes under graviditet hvis den potensielle fordelen rettferdiggjør den potensielle risikoen for fosteret. Kvinner bør rådes til å kontakte legen hvis de blir gravide mens de tar FLONASE nesespray.
Mus og rotter ved doser av flutikasonpropionat omtrent 1 og 4 ganger, henholdsvis den maksimale anbefalte humane daglige intranasale dosen (MRHDID) for voksne (på mg/m² basis ved maternale subkutane doser på henholdsvis 45 og 100 mcg/kg/dag) viste føtal toksisitet karakteristisk for potente kortikosteroidforbindelser, inkludert embryonal vekstretardasjon, omphalocele, ganespalte og retardert kranieforbening. Ingen teratogenisitet ble sett hos rotter ved doser opp til 3 ganger MRHDID (på mg/m² basis ved inhalasjonsdoser hos mor på opptil 68,7 mcg/kg/dag).
Hos kaniner ble fostervektreduksjon og ganespalte observert ved en flutikasonpropionatdose omtrent 0,3 ganger MRHDID for voksne (på mg/m² basis ved en maternal subkutan dose på 4 mcg/kg/dag). Imidlertid ble det ikke rapportert om teratogene effekter ved doser av flutikasonpropionat opp til ca. 20 ganger MRHDID for voksne (på mg/m² basis ved en oral dose til mor opp til 300 mcg/kg/dag). Ingen flutikasonpropionat ble påvist i plasma i denne studien, i samsvar med den etablerte lave biotilgjengeligheten etter oral administrering [se KLINISK FARMAKOLOGI ].
Flutikasonpropionat krysset placenta etter subkutan administrering til mus og rotter og oral administrering til kaniner.
Erfaring med orale kortikosteroider siden de ble introdusert i farmakologiske, i motsetning til fysiologiske doser, tyder på at gnagere er mer utsatt for teratogene effekter fra kortikosteroider enn mennesker. I tillegg, fordi det er en naturlig økning i kortikosteroidproduksjonen under svangerskapet, vil de fleste kvinner kreve en lavere eksogen kortikosteroiddose og mange vil ikke trenge kortikosteroidbehandling under svangerskapet.
Ikke-ratatogene effekter
Hypoadrenalisme kan forekomme hos spedbarn født av mødre som får kortikosteroider under graviditet. Slike spedbarn bør overvåkes nøye.
Ammende mødre
Det er ikke kjent om flutikasonpropionat skilles ut i morsmelk hos mennesker. Andre kortikosteroider er imidlertid påvist i morsmelk. Subkutan administrering til diegivende rotter av tritiert flutikasonpropionat i en dose på omtrent 0,4 ganger MRHDID for voksne på mg/m²-basis resulterte i målbar radioaktivitet i melk.
Siden det ikke finnes data fra kontrollerte studier om bruk av intranasal FLONASE nesespray 50mcg av ammende mødre, bør det utvises forsiktighet når FLONASE nesespray 50mcg gis til en ammende kvinne.
Pediatrisk bruk
Sikkerheten og effektiviteten til FLONASE nesespray hos barn i alderen 4 år og eldre har blitt fastslått [se BIVIRKNINGER , KLINISK FARMAKOLOGI ].Seks hundre og femti (650) personer i alderen 4 til 11 år og 440 personer i alderen 12 til 17 år ble studert i amerikanske kliniske studier med flutikasonpropionat nesespray. Sikkerheten og effektiviteten til FLONASE nesespray 50mcg hos barn yngre enn 4 år er ikke fastslått.
Effekter på vekst
Kontrollerte kliniske studier har vist at intranasale kortikosteroider kan forårsake en reduksjon i veksthastigheten når de administreres til pediatriske pasienter. Denne effekten ble observert i fravær av laboratoriebevis på undertrykkelse av hypothalamus-hypofyse-binyrene (HPA) akse, noe som tyder på at veksthastighet er en mer sensitiv indikator på systemisk kortikosteroideksponering hos pediatriske pasienter enn noen vanlig brukte tester av HPA-aksefunksjon. De langsiktige effektene av denne reduksjonen i veksthastighet assosiert med intranasale kortikosteroider, inkludert virkningen på den endelige voksenhøyden, er ukjent. Potensialet for "catch-up" vekst etter seponering av behandling med intranasale kortikosteroider er ikke tilstrekkelig studert. Veksten hos pediatriske pasienter som får intranasale kortikosteroider, inkludert FLONASE nesespray, bør overvåkes rutinemessig (f.eks. via stadiometri). De potensielle veksteffektene av langvarig behandling bør veies opp mot de kliniske fordelene som oppnås og risikoen forbundet med alternative behandlinger. For å minimere de systemiske effektene av intranasale kortikosteroider, inkludert FLONASE nesespray, bør hver pasients dosering titreres til den laveste dosen som effektivt kontrollerer hans/hennes symptomer.
En 1-årig placebokontrollert studie ble utført med 150 pediatriske personer (i alderen 3 til 9 år) for å vurdere effekten av FLONASE nesespray (enkelt daglig dose på 200 mcg) på veksthastigheten. Fra primærpopulasjonen som fikk FLONASE nesespray (n = 56) og placebo (n = 52), var punktestimatet for veksthastighet med FLONASE nesespray 50 mcg 0,14 cm/år lavere enn placebo (95 % KI: -0,54, 0,27 cm) /år). Det ble således ikke observert noen statistisk signifikant effekt på vekst sammenlignet med placebo. Ingen bevis på klinisk relevante endringer i HPA-aksefunksjon eller bentetthet ble observert ved henholdsvis 12-timers kortisolutskillelse i urin og dobbelt-energi røntgenabsorptiometri.
Potensialet for at FLONASE nesespray 50mcg kan forårsake veksthemming hos følsomme pasienter eller når det gis i høyere doser enn anbefalt, kan ikke utelukkes.
Geriatrisk bruk
Et begrenset antall forsøkspersoner i alderen 65 år og eldre (n = 129) eller 75 år og eldre (n = 11) har blitt behandlet med FLONASE nesespray i kliniske studier. Mens antallet forsøkspersoner er for lite til å tillate separat analyse av effekt og sikkerhet, var bivirkningene rapportert i denne populasjonen lik de som ble rapportert av yngre pasienter. Generelt bør dosevalg for en eldre pasient være forsiktig, vanligvis fra den lave enden av doseringsområdet, noe som gjenspeiler den høyere frekvensen av nedsatt lever-, nyre- eller hjertefunksjon, og samtidig sykdom eller annen medikamentell behandling.
Nedsatt leverfunksjon
Formelle farmakokinetiske studier med FLONASE nesespray 50mcg har ikke blitt utført hos personer med nedsatt leverfunksjon. Siden flutikasonpropionat hovedsakelig elimineres av levermetabolisme, kan nedsatt leverfunksjon føre til akkumulering av flutikasonpropionat i plasma. Pasienter med leversykdom bør derfor overvåkes nøye.

Nedsatt nyrefunksjon
Formelle farmakokinetiske studier med FLONASE nesespray har ikke blitt utført hos personer med nedsatt nyrefunksjon.
OVERDOSE
Kronisk overdosering kan føre til tegn/symptomer på hyperkortisisme (se FORHOLDSREGLER ). Intranasal administrering av 2 mg (10 ganger anbefalt dose) flutikasonpropionat to ganger daglig i 7 dager til friske frivillige ble godt tolerert. Enkelte orale doser på opptil 16 mg er studert hos frivillige mennesker uten at det er rapportert om akutte toksiske effekter. Gjenta orale doser opptil 80 mg daglig i 10 dager hos frivillige og gjentatte orale doser opptil 10 mg daglig i 14 dager hos pasienter ble godt tolerert. Bivirkningene var av mild eller moderat alvorlighetsgrad, og forekomsten var lik i aktive og placebobehandlingsgrupper. Akutt overdosering med denne doseringsformen er usannsynlig siden 1 flaske FLONASE (flutikasonpropionat) nesespray inneholder ca. 8 mg flutikasonpropionat.
Den orale og subkutane median dødelige dosen hos mus og rotter var >1 000 mg/kg (henholdsvis >20 000 og >41 000 ganger maksimal anbefalt daglig intranasal dose hos voksne og henholdsvis >10 000 og >20 000 ganger maksimal anbefalt daglig intranasal dose dose til barn på mg/m2 basis).
KONTRAINDIKASJONER
FLONASE (flutikasonpropionat) Nesespray er kontraindisert hos pasienter med overfølsomhet overfor noen av ingrediensene.
KLINISK FARMAKOLOGI
Virkningsmekanismen
Flutikasonpropionat er et syntetisk trifluorert kortikosteroid med antiinflammatorisk aktivitet. Flutikasonpropionat har vist seg in vitro å vise en bindingsaffinitet for den humane glukokortikoidreseptoren som er 18 ganger den for deksametason, nesten dobbelt så stor som for beklometason-17-monopropionat (BMP), den aktive metabolitten til beklometasondipropionat, og over 3 ganger så stor som av budesonid. Data fra McKenzie vasokonstriktoranalysen hos mennesker stemmer overens med disse resultatene. Den kliniske betydningen av disse funnene er ukjent.
Den nøyaktige mekanismen som flutikasonpropionat påvirker rhinittsymptomer gjennom er ikke kjent. Kortikosteroider har vist seg å ha et bredt spekter av effekter på flere celletyper (f.eks. mastceller, eosinofiler, nøytrofiler, makrofager, lymfocytter) og mediatorer (f.eks. histamin, eikosanoider, leukotriener, cytokiner) involvert i betennelse. I 7 studier hos voksne har FLONASE nesespray redusert eosinofiler i neseslimhinnen hos 66 % av pasientene (35 % for placebo) og basofile hos 39 % av pasientene (28 % for placebo). Den direkte sammenhengen mellom disse funnene og langsiktig symptomlindring er ikke kjent.
Farmakodynamikk
HPA-akseeffekt
De potensielle systemiske effektene av FLONASE nesespray 50mcg på HPA-aksen ble evaluert. FLONASE nesespray 50 mcg gitt som 200 mcg en gang daglig eller 400 mcg to ganger daglig ble sammenlignet med placebo eller oral prednison 7,5 eller 15 mg gitt om morgenen. FLONASE nesespray i noen av dosene i 4 uker påvirket ikke binyreresponsen på 6-timers cosyntropinstimulering, mens begge dosene av oral prednison reduserte responsen på cosyntropin signifikant.
Hjerteelektrofysiologi
En studie spesielt utviklet for å evaluere effekten av FLONASE på QT-intervallet er ikke utført.
Farmakokinetikk
Aktiviteten til FLONASE nesespray 50mcg skyldes moderstoffet, flutikasonpropionat. På grunn av den lave biotilgjengeligheten ved intranasal vei, ble størstedelen av de farmakokinetiske dataene innhentet via andre administreringsveier.
Absorpsjon
Indirekte beregninger indikerer at flutikasonpropionat som leveres intranasalt har en absolutt biotilgjengelighet på i gjennomsnitt mindre enn 2 %. Forsøk med oral dosering av merket og umerket legemiddel har vist at den orale systemiske biotilgjengeligheten av flutikasonpropionat er ubetydelig (
Fordeling
Etter intravenøs administrering var den innledende disponeringsfasen for flutikasonpropionat rask og konsistent med dets høye lipidløselighet og vevsbinding. Distribusjonsvolumet var i gjennomsnitt 4,2 L/kg.
Prosentandelen av flutikasonpropionat bundet til humane plasmaproteiner var i gjennomsnitt 99 %. Flutikasonpropionat er svakt og reversibelt bundet til erytrocytter og er ikke signifikant bundet til humant transkortin.
Eliminering
Etter intravenøs dosering viste flutikasonpropionat polyeksponentiell kinetikk og hadde en terminal eliminasjonshalveringstid på ca. 7,8 timer. Den totale blodclearancen av flutikasonpropionat er høy (gjennomsnitt: 1 093 ml/min), med renal clearance som utgjør mindre enn 0,02 % av totalen.
Metabolisme: Den eneste sirkulerende metabolitten påvist hos mennesker er 17β-karboksylsyrederivatet av flutikasonpropionat, som dannes gjennom CYP3A4-veien. Denne metabolitten hadde mindre affinitet (omtrent 1/2000) enn moderstoffet for glukokortikoidreseptoren til human lungecytosol in vitro og ubetydelig farmakologisk aktivitet i dyrestudier. Andre metabolitter påvist in vitro ved bruk av dyrkede humane hepatomceller er ikke påvist hos mennesker.
Utskillelse: Mindre enn 5 % av en radiomerket oral dose ble skilt ut i urinen som metabolitter, mens resten ble skilt ut i feces som moderlegemiddel og metabolitter.
Spesielle populasjoner
Flutikasonpropionat nesespray ble ikke studert i noen spesielle populasjoner, og ingen kjønnsspesifikke farmakokinetiske data er innhentet.
Narkotikahandel
Hemmere av Cytokrom P450 3A4: Ritonavir: Flutikasonpropionat er et substrat for CYP3A4. Samtidig administrering av flutikasonpropionat og den sterke CYP3A4-hemmeren, ritonavir, anbefales ikke basert på en flerdose-crossover-interaksjonsstudie hos 18 friske personer. Flutikasonpropionat vandig nesespray (200 mcg én gang daglig) ble administrert samtidig i 7 dager med ritonavir (100 mg to ganger daglig). Plasmakonsentrasjoner av flutikasonpropionat etter vandig nesespray av flutikasonpropionat alene var upåviselige (
Ketokonazol: Samtidig administrering av oralt inhalert flutikasonpropionat (1000 mcg) og ketokonazol (200 mg én gang daglig) resulterte i en 1,9 ganger økning i plasmaeksponering for flutikasonpropionat og en 45 % reduksjon i plasmakortisol AUC, men hadde ingen effekt på urinutskillelse av kortisol.
Erytromycin: I en interaksjonsstudie med flere doser påvirket ikke samtidig administrering av oralt inhalert flutikasonpropionat (500 mcg to ganger daglig) og erytromycin (333 mg 3 ganger daglig) farmakokinetikken for flutikasonpropionat.
PASIENTINFORMASJON
FLONASE® [flow'naz] (flutikasonpropionat) nesespray, 50 mcg
Les pasientinformasjonen som følger med FLONASE nesespray før du begynner å bruke den og hver gang du får påfyll. Det kan komme ny informasjon. Denne pasientinformasjonen erstatter ikke å snakke med helsepersonell om din medisinske tilstand eller behandling.
Hva er FLONASE nesespray?
FLONASE Nesespray 50mcg er et reseptbelagt legemiddel som brukes til å behandle ikke-allergiske nesesymptomer som rennende nese, tett nese, nysing og nesekløe hos voksne og barn i alderen 4 år og eldre.
Det er ikke kjent om FLONASE nesespray 50mcg er trygt og effektivt hos barn yngre enn 4 år.
Hvem bør ikke bruke FLONASE nesespray 50mcg?
Ikke bruk FLONASE nesespray 50mcg hvis du er allergisk mot flutikasonpropionat eller noen av ingrediensene i FLONASE nesespray. Se "Hva er ingrediensene i FLONASE nesespray 50mcg?" nedenfor for en komplett liste over ingredienser.
Hva bør jeg fortelle helsepersonell før jeg bruker FLONASE nesespray 50mcg?
Fortell helsepersonell om alle dine helsetilstander, inkludert hvis du:
- . har eller har hatt nesesår, neseoperasjon eller neseskade. . har øyeproblemer, som grå stær eller glaukom. . har et immunsystemproblem. . er allergisk mot noen av ingrediensene i FLONASE nesespray, andre medisiner eller matprodukter. Se "Hva er ingrediensene i FLONASE nesespray?" nedenfor for en komplett liste over ingredienser. . har noen form for virus-, bakterie- eller soppinfeksjon. . er utsatt for vannkopper eller meslinger. . har andre medisinske tilstander. . er gravid eller planlegger å bli gravid. Det er ikke kjent om FLONASE nesespray kan skade det ufødte barnet. . ammer eller planlegger å amme. Det er ikke kjent om FLONASE nesespray 50mcg går over i morsmelk og om det kan skade babyen din.
Fortell helsepersonell om alle medisinene du tar, inkludert reseptbelagte og reseptfrie medisiner, vitaminer og urtetilskudd. FLONASE nesespray og visse andre legemidler kan interagere med hverandre. Dette kan forårsake alvorlige bivirkninger. Spesielt, fortell helsepersonell hvis du tar soppdrepende eller anti-HIV-medisiner.
Kjenn til medisinene du tar. Hold en liste over dem for å vise helsepersonell og apotek når du får en ny medisin.
Hvordan skal jeg bruke FLONASE nesespray?
Les trinnvise instruksjoner for bruk av FLONASE nesespray på slutten av denne pasientinformasjonen.
- . FLONASE nesespray er kun til bruk i nesen. Ikke spray det i øynene eller munnen. . Barn bør bruke FLONASE nesespray med en voksens hjelp, som instruert av barnets helsepersonell. . Bruk FLONASE nesespray 50mcg nøyaktig slik helsepersonell forteller deg. Ikke bruk FLONASE nesespray oftere enn foreskrevet. . FLONASE Nesespray kan ta flere dager med regelmessig bruk før rhinittsymptomene dine blir bedre. Hvis symptomene dine ikke blir bedre eller verre, ring legen din. . Du vil få de beste resultatene hvis du fortsetter å bruke FLONASE nesespray regelmessig hver dag uten å gå glipp av en dose. Etter at du begynner å føle deg bedre, kan helsepersonell redusere dosen din. Ikke slutte å bruke FLONASE nesespray 50mcg med mindre helsepersonell ber deg gjøre det.
Hva er de mulige bivirkningene av FLONASE nesespray 50mcg?
FLONASE nesespray 50mcg kan forårsake alvorlige bivirkninger, inkludert:
- . neseproblemer. Neseproblemer kan omfatte:
- . neseblod. . sår (sår) i nesen. . en viss soppinfeksjon i nesen, munnen og/eller halsen (trost). . hull i brusken i nesen (perforering av neseseptum). Symptomer på perforering av neseseptum kan omfatte:
- . skorpedannelse i nesen . neseblod . rennende nese . plystrelyd når du puster
- . utslett . utslett . hevelse i ansiktet, munnen og tungen . pusteproblemer
- . feber . føler seg sliten . smerte . kvalme . verker . oppkast . frysninger
- . føler seg sliten . lite energi . svakhet . kvalme og oppkast . lavt blodtrykk
De vanligste bivirkningene av FLONASE nesespray 50mcg inkluderer:
- . hodepine . kvalme og oppkast . sår hals . problemer med å puste . neseblod . hoste . nesebrenning eller kløe
Fortell helsepersonell om eventuelle bivirkninger som plager deg eller som ikke forsvinner.
Dette er ikke alle bivirkningene med FLONASE nesespray. Spør helsepersonell eller apotek for mer informasjon.
Ring legen din for medisinsk råd om bivirkninger. Du kan rapportere bivirkninger til FDA på 1-800-FDA-1088.
Hvordan oppbevarer jeg FLONASE nesespray 50mcg?
- . Oppbevar FLONASE mellom 39°F og 86°F (4°C og 30°C).
Oppbevar FLONASE nesespray 50mcg og alle medisiner utilgjengelig for barn.
Generell informasjon om sikker og effektiv bruk av FLONASE nesespray.
Medisiner blir noen ganger foreskrevet for formål som ikke er nevnt i et pasientinformasjonshefte. Ikke bruk FLONASE nesespray for en tilstand som den ikke er foreskrevet for. Ikke gi din FLONASE nesespray til andre mennesker, selv om de har samme tilstand som du har. Det kan skade dem.
Dette pasientinformasjonsheftet oppsummerer den viktigste informasjonen om FLONASE nesespray. Hvis du vil ha mer informasjon, snakk med helsepersonell. Du kan spørre apoteket eller helsepersonell om informasjon om FLONASE nesespray som er skrevet for helsepersonell.
For mer informasjon om FLONASE nesespray, ring 1-888-825-5249.
Hva er ingrediensene i FLONASE Nesespray 50mcg?
Aktiv ingrediens: flutikasonpropionat.
Inaktive ingredienser: mikrokrystallinsk cellulose, karboksymetylcellulosenatrium, dekstrose, 0,02 % w/w benzalkoniumklorid, polysorbat 80 og 0,25 % w/w fenyletylalkohol.
Instruksjoner for bruk
FLONASE® [flow'naz] (flutikasonpropionat) Nesespray, 50 mcg
FLONASE Nesespray 50mcg er kun til bruk i nesen.
Les denne informasjonen før du begynner å bruke FLONASE nesespray.
Deler av din FLONASE nesespray (Se figur A)
Figur A 
Din FLONASE Nesespray 50mcg må grunnes før du bruker den for første gang og når du ikke har brukt den på en uke eller mer.
Slik fyller du FLONASE nesespray
- . Rist flasken forsiktig og fjern deretter støvdekselet (se figur B).
Figur B 
- . Hold flasken som vist (se figur C) med neseapplikatoren pekende bort fra deg og med pekefingeren og langfingeren på hver side av neseapplikatoren og tommelen under flasken. . Trykk ned og slipp 6 ganger til en fin spray vises (se figur C). Pumpen er nå klar til bruk.
Figur C 
Bruk av FLONASE nesespray:
Trinn 1 . Puss nesen for å rense neseborene.
Steg 2 . Lukk 1 nesebor. Vipp hodet litt fremover, og hold flasken oppreist, før neseapplikatoren forsiktig inn i det andre neseboret (se figur D).
Figur D 
Trinn 3 Begynn å puste inn gjennom nesen, og mens du puster inn, trykk fast og raskt ned 1 gang på applikatoren for å frigjøre sprayen. For å få en full dose, bruk pekefingeren og langfingeren til å spraye mens du støtter bunnen av flasken med tommelen. Unngå å spraye i øynene. Pust forsiktig inn gjennom neseboret (se figur E).
Figur E 
Trinn 4 . Pust ut gjennom munnen.
Trinn 5 . Hvis en ny spray er nødvendig i det neseboret, gjenta trinn 2 til 4.
Trinn 6 . Gjenta trinn 2 til 5 i det andre neseboret.
Trinn 7 . Tørk av neseapplikatoren med en ren serviett og sett på støvdekselet (se figur F).
Figur F 
Ikke bruk denne flasken i mer enn det merket antall sprayer selv om flasken ikke er helt tom. Før du kaster flasken, bør du snakke med helsepersonell for å se om påfylling er nødvendig. Ikke ta ekstra doser eller slutt å ta FLONASE nesespray 50mcg uten å snakke med helsepersonell.
Rengjøring av FLONASE nesespray:
Nesesprayen din bør rengjøres minst 1 gang hver uke.
1. Fjern støvdekselet og trekk deretter forsiktig oppover for å frigjøre neseapplikatoren.
2. Vask applikatoren og støvdekselet under varmt vann fra springen. La tørke ved romtemperatur.
3. Sett applikatoren og støvdekselet tilbake på flasken.
4. Hvis neseapplikatoren blir blokkert, kan den fjernes og ligge i varmt vann. Skyll neseapplikatoren med kaldt vann fra springen. Tørk neseapplikatoren og sett den tilbake på flasken. Ikke prøv å fjerne blokkeringen av neseapplikatoren ved å sette inn en pinne eller en annen skarp gjenstand.
Oppbevaring av FLONASE nesespray:
- . Oppbevar FLONASE nesespray 50mcg mellom 39°F og 86°F (4°C og 30°C). . Ikke bruk FLONASE nesespray etter datoen som vises som "EXP" på etiketten eller esken.
