Precose 25mg, 50mg Acarbose Bruk, bivirkninger og dosering. Pris i nettapotek. Generisk medisin uten resept.
Hva er Precose 50mg og hvordan brukes det?
Precose (akarbosetabletter) er en oral alfa-glukosidasehemmer som brukes til å behandle type 2 diabetes. Precose 50mg brukes noen ganger i kombinasjon med insulin eller andre diabetesmedisiner du tar gjennom munnen. Precose 25mg er tilgjengelig i generisk form.
Hva er bivirkningene av Precose 25mg?
Vanlige bivirkninger av Precose inkluderer:
- . diaré, . gass, . oppblåsthet, . urolig mage, eller . magesmerter i løpet av de første ukene av behandlingen ettersom kroppen din tilpasser seg denne medisinen, men vanligvis forbedres med tiden.
Andre bivirkninger av Precose 50mg inkluderer hudutslett eller kløe. Fortell legen din dersom du har sjeldne, men svært alvorlige bivirkninger av Precose 25mg, inkludert:
- . uvanlig tretthet, . vedvarende kvalme eller oppkast, . sterke mage- eller magesmerter, . endetarmsblødning, . gulne øyne eller hud, eller . mørk urin.
BESKRIVELSE
PRECOSE® (akarbosetabletter) er en oral alfa-glukosidasehemmer for bruk ved behandling av type 2 diabetes mellitus. Akarbose er et oligosakkarid som er oppnådd fra fermenteringsprosesser av en mikroorganisme, Actinoplanes utahensis, og er kjemisk kjent som O-4,6-dideoksy4-[[(1S,4R,5S,6S)-4,5,6-trihydroksy- 3-(hydroksymetyl)-2-cykloheksen-1-yl]amino]a-D-glukopyranosyl-(1-→4)-O-a-D-glukopyranosyl-(1-→4)-D-glukose. Det er et hvitt til off-white pulver med en molekylvekt på 645,6. Akarbose er løselig i vann og har en pKa på 5,1. Dens empiriske formel er C25H43NO18 og dens kjemiske struktur er som følger:
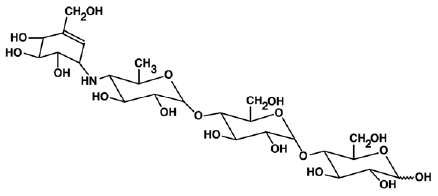
PRECOSE 50 mg er tilgjengelig som 25 mg, 50 mg og 100 mg tabletter for oral bruk. De inaktive ingrediensene er stivelse, mikrokrystallinsk cellulose, magnesiumstearat og kolloidalt silisiumdioksid.
INDIKASJONER
PRECOSE er indisert som et tillegg til kosthold og trening for å forbedre glykemisk kontroll hos voksne med type 2 diabetes mellitus.
DOSERING OG ADMINISTRASJON
Det finnes ikke noe fast doseringsregime for behandling av diabetes mellitus med PRECOSE eller andre farmakologiske midler. Dosering av PRECOSE 25 mg må individualiseres på grunnlag av både effektivitet og toleranse, mens maksimal anbefalt dose på 100 mg ikke overskrides. PRECOSE bør tas tre ganger daglig ved starten (med den første biten) av hvert hovedmåltid.
PRECOSE bør startes med en lav dose, med gradvis doseøkning som beskrevet nedenfor, både for å redusere gastrointestinale bivirkninger og for å tillate identifisering av minimumsdosen som kreves for adekvat glykemisk kontroll av pasienten. Hvis den foreskrevne dietten ikke overholdes, kan tarmbivirkningene forsterkes. Hvis det oppstår sterke plagsomme symptomer til tross for overholdelse av diabetikerdietten som er foreskrevet, må legen konsulteres og dosen reduseres midlertidig eller permanent.
Under behandlingsstart og dosetitrering (se nedenfor), kan én time postprandial plasmaglukose brukes til å bestemme den terapeutiske responsen på PRECOSE og identifisere den minste effektive dosen for pasienten. Deretter bør glykosylert hemoglobin måles med ca. tre måneders mellomrom. Det terapeutiske målet bør være å redusere nivåene av både postprandial plasmaglukose og glykosylert hemoglobin til normalt eller nær normalt ved å bruke den laveste effektive dosen av PRECOSE, enten som monoterapi eller i kombinasjon med sulfonylurea, insulin eller metformin.
Startdosering
Den anbefalte startdosen av PRECOSE 25 mg er 25 mg gitt oralt tre ganger daglig ved starten (med den første biten) av hvert hovedmåltid. Noen pasienter kan imidlertid ha nytte av mer gradvis dosetitrering for å minimere gastrointestinale bivirkninger. Dette kan oppnås ved å starte behandling med 25 mg én gang daglig og deretter øke administreringsfrekvensen for å oppnå 25 mg tid.
Vedlikeholdsdosering
Så snart et 25 mg daglig doseringsregime er nådd, bør dosen av PRECOSE 50 mg justeres med 4–8 ukers intervaller basert på en time postprandial glukose eller glykosylert hemoglobinnivå, og på toleranse. Dosen kan økes fra 25 mg tid til 50 mg tid. Noen pasienter kan ha nytte av å øke dosen ytterligere til 100 mg tid. Vedlikeholdsdosen varierer fra 50 mg tid til 100 mg tid. Siden pasienter med lav kroppsvekt kan ha økt. risiko for forhøyede serumtransaminaser, bør kun pasienter med kroppsvekt > 60 kg vurderes for dosetitrering over 50 mg tid (se FORHOLDSREGLER ). Dersom det ikke observeres ytterligere reduksjon i postprandial glukose eller glykosylert hemoglobinnivå ved titrering til 100 mg tid, bør det vurderes å redusere dosen. Når en effektiv og tolerert dosering er etablert, bør den opprettholdes.
Maksimal dosering
Maksimal anbefalt dose for pasienter ≤ 60 kg er 50 mg tid. Maksimal anbefalt dose for pasienter > 60 kg er 100 mg tid.
Pasienter som får sulfonylurea eller insulin
Sulfonylureamidler eller insulin kan forårsake hypoglykemi. PRECOSE gitt i kombinasjon med et sulfonylurea eller insulin vil føre til en ytterligere reduksjon av blodsukkeret og kan øke potensialet for hypoglykemi. Hvis hypoglykemi oppstår, bør passende justeringer i dosen av disse midlene gjøres.
HVORDAN LEVERES
PRECOSE er tilgjengelig som 25 mg, 50 mg eller 100 mg runde tabletter uten skår. Hver tablettstyrke er hvit til gulfarget. 25 mg tabletten er kodet med ordet "PRECOSE" på den ene siden og "25" på den andre siden. 50 mg tabletten er kodet med ordet "PRECOSE" og "50" på samme side. 100 mg tabletten er kodet med ordet "PRECOSE" og "100" på samme side. PRECOSE er tilgjengelig i flasker på 100 og 50 mg i enhetsdosepakninger på 100.
Oppbevares ikke over 25°C (77°F). Beskytt mot fuktighet. For flasker, hold beholderen tett lukket.
Bayer HealthCare Pharmaceuticals Inc. Wayne, NJ 07470. Laget i Tyskland. 11/11
BIVIRKNINGER
Fordøyelseskanalen
Gastrointestinale symptomer er de vanligste reaksjonene på PRECOSE. I amerikanske placebokontrollerte studier var forekomsten av magesmerter, diaré og flatulens henholdsvis 19 %, 31 % og 74 % hos 1255 pasienter behandlet med PRECOSE 50–300 mg tid, mens den tilsvarende forekomsten var 9 %, 12 % , og 29 % av 999 placebobehandlede pasienter.
en ettårig sikkerhetsstudie, der pasienter førte dagbok over gastrointestinale symptomer, hadde magesmerter og diaré en tendens til å gå tilbake til nivåer før behandling over tid, og hyppigheten og intensiteten av flatulens hadde en tendens til å avta med tiden. De økte gastrointestinale symptomene hos pasienter behandlet med PRECOSE 50 mg er en manifestasjon av virkningsmekanismen til PRECOSE og er relatert til tilstedeværelsen av ufordøyd karbohydrat i den nedre GI-kanalen.
Hvis den foreskrevne dietten ikke overholdes, kan tarmbivirkningene forsterkes. Hvis det oppstår sterke plagsomme symptomer til tross for overholdelse av diabetikerdietten som er foreskrevet, må legen konsulteres og dosen reduseres midlertidig eller permanent.
Forhøyede serumtransaminasenivåer
Se FORHOLDSREGLER .
Andre unormale laboratoriefunn
Små reduksjoner i hematokrit forekom oftere hos PRECOSE-behandlede pasienter enn hos placebo-behandlede pasienter, men var ikke assosiert med reduksjoner i hemoglobin. Lavt serumkalsium og lave plasmanivåer av vitamin B6 var assosiert med PRECOSE 50 mg-behandling, men antas å være enten falsk eller uten klinisk betydning.
Rapporter om uønskede hendelser etter markedsføring
Ytterligere bivirkninger rapportert fra verdensomspennende erfaring etter markedsføring inkluderer fulminant hepatitt med dødelig utgang, overfølsomme hudreaksjoner (for eksempel utslett, erytem, eksantem og utikaria), ødem, ileus/subileus, gulsott og/eller hepatitt og tilhørende leverskade, trombocytopeni og pneumatose cystoides intestinalis (se FORHOLDSREGLER ).
Pneumatosis Cystoides Intestinalis
Det har vært sjeldne rapporter etter markedsføring om pneumatosis cystoides intestinalis assosiert med bruk av alfa-glukosidasehemmere, inkludert Precose. Pneumatosis cystoides intestinalis kan presentere med symptomer på diaré, slimutslipp, rektal blødning og forstoppelse. Komplikasjoner kan omfatte pneumoperitoneum, volvulus, intestinal obstruksjon, intussusception, intestinal blødning og intestinal perforasjon. Ved mistanke om pneumatosis cystoides intestinalis, seponer Precose 25mg og utfør passende bildediagnostikk.
NARKOTIKAHANDEL
Enkelte legemidler har en tendens til å produsere hyperglykemi og kan føre til tap av blodsukkerkontroll. Disse legemidlene inkluderer tiazider og andre diuretika, kortikosteroider, fenotiaziner, skjoldbruskprodukter, østrogener, orale prevensjonsmidler, fenytoin, nikotinsyre, sympatomimetika, kalsiumkanalblokkerende legemidler og isoniazid. Når slike legemidler administreres til en pasient som får PRECOSE 25 mg, bør pasienten observeres nøye for tap av blodsukkerkontroll. Når slike legemidler seponeres fra pasienter som får PRECOSE 50 mg i kombinasjon med sulfonylurea eller insulin, bør pasientene observeres nøye for tegn på hypoglykemi.
Pasienter som får sulfonylurea eller insulin: Sulfonylureamidler eller insulin kan forårsake hypoglykemi. PRECOSE 25 mg gitt i kombinasjon med et sulfonylurea eller insulin kan føre til en ytterligere reduksjon av blodsukkeret og kan øke potensialet for hypoglykemi. Hvis hypoglykemi oppstår, bør passende justeringer i dosen av disse midlene gjøres. Svært sjeldne har individuelle tilfeller av hypoglykemisk sjokk blitt rapportert hos pasienter som får PRECOSE-behandling i kombinasjon med sulfonylurea og/eller insulin.
Intestinale adsorbenter (for eksempel kull) og fordøyelsesenzympreparater som inneholder karbohydratspaltende enzymer (for eksempel amylase, pankreatin) kan redusere effekten av PRECOSE og bør ikke tas samtidig.
PRECOSE 25 mg har vist seg å endre biotilgjengeligheten av digoksin når de administreres samtidig, noe som kan kreve justering av digoksindose. (Se KLINISK FARMAKOLOGI , Legemiddel-legemiddelinteraksjoner .)
ADVARSLER
Ingen informasjon gitt
FORHOLDSREGLER
Generell
Makrovaskulære utfall
Det har ikke vært noen kliniske studier som har etablert konklusive bevis på makrovaskulær risikoreduksjon med PRECOSE 25 mg eller noe annet antidiabetisk legemiddel.
Hypoglykemi
På grunn av virkningsmekanismen bør PRECOSE ikke gi hypoglykemi i fastende eller postprandial tilstand når det administreres alene. Sulfonylureamidler eller insulin kan forårsake hypoglykemi. Fordi PRECOSE 50 mg gitt i kombinasjon med et sulfonylurea eller insulin vil føre til en ytterligere reduksjon av blodsukkeret, kan det øke potensialet for hypoglykemi. Hypoglykemi forekommer ikke hos pasienter som får metformin alene under vanlige bruksforhold, og det ble ikke observert økt forekomst av hypoglykemi hos pasienter når PRECOSE 50 mg ble lagt til metforminbehandling.
Oral glukose (dekstrose), hvis absorpsjon ikke hemmes av PRECOSE, bør brukes i stedet for sukrose (rørsukker) ved behandling av mild til moderat hypoglykemi. Sukrose, hvis hydrolyse til glukose og fruktose hemmes av PRECOSE, er uegnet for rask korreksjon av hypoglykemi. Alvorlig hypoglykemi kan kreve bruk av enten intravenøs glukoseinfusjon eller glukagoninjeksjon.
Forhøyede serumtransaminasenivåer
langtidsstudier (opptil 12 måneder, og inkludert PRECOSE 25 mg doser opptil 300 mg tid) utført i USA, behandlingsfremkomne økninger av serumtransaminaser (AST og/eller ALAT) over den øvre normalgrensen (ULN) ), større enn 1,8 ganger ULN og mer enn 3 ganger ULN forekom hos henholdsvis 14 %, 6 % og 3 % av PRECOSE-behandlede pasienter sammenlignet med henholdsvis 7 %, 2 % og 1 %, av placebo-behandlede pasienter. Selv om disse forskjellene mellom behandlingene var statistisk signifikante, var disse økningene asymptomatiske, reversible, mer vanlige hos kvinner og generelt sett ikke assosiert med andre tegn på leverdysfunksjon. I tillegg så disse serumtransaminaseøkningene ut til å være doserelatert. I amerikanske studier inkludert PRECOSE 50 mg doser opp til den maksimalt godkjente dosen på 100 mg tid, var behandlingsfremkomne økninger av ASAT og/eller ALAT på et hvilket som helst nivå av alvorlighetsgrad lik mellom PRECOSE-behandlede pasienter og placebobehandlede pasienter (p ≥ 0,496) .
løpet av ca. 3 millioner pasientår med internasjonal postmarkedsføringserfaring med PRECOSE 50 mg, er det rapportert 62 tilfeller av serumtransaminaseøkninger > 500 IE/L (hvorav 29 var assosiert med gulsott). 41 av disse 62 pasientene fikk behandling med 100 mg tid eller mer, og 33 av 45 pasienter som ble rapportert vekt veide
Tap av kontroll over blodsukker
Når diabetespasienter utsettes for stress som feber, traumer, infeksjoner eller kirurgi, kan det oppstå et midlertidig tap av kontroll over blodsukkeret. I slike tilfeller kan midlertidig insulinbehandling være nødvendig.
Laboratorietester
Terapeutisk respons på PRECOSE bør overvåkes med periodiske blodsukkertester. Måling av glykosylerte hemoglobinnivåer anbefales for overvåking av langsiktig glykemisk kontroll.
PRECOSE 25 mg, spesielt ved doser over 50 mg tid, kan gi forhøyede serumtransaminaser og, i sjeldne tilfeller, hyperbilirubinemi. Det anbefales at serumtransaminasenivåer kontrolleres hver 3. måned i løpet av det første behandlingsåret med PRECOSE og periodisk deretter. Hvis forhøyede transaminaser observeres, kan en reduksjon i dose eller seponering av behandlingen være indisert, spesielt hvis forhøyelsene vedvarer.
Nedsatt nyrefunksjon
Plasmakonsentrasjoner av PRECOSE hos frivillige med nedsatt nyrefunksjon var proporsjonalt økt i forhold til graden av nedsatt nyrefunksjon. Langsiktige kliniske studier med diabetespasienter med signifikant nedsatt nyrefunksjon (serumkreatinin > 2,0 mg/dL) har ikke blitt utført. Derfor anbefales ikke behandling av disse pasientene med PRECOSE 50 mg.
Karsinogenese, mutagenese og svekkelse av fruktbarhet
Åtte karsinogenitetsstudier ble utført med akarbose. Seks studier ble utført på rotter (to stammer, Sprague-Dawley og Wistar) og to studier ble utført på hamstere.
den første rottestudien fikk Sprague-Dawley-rotter akarbose i fôr i høye doser (opptil ca. 500 mg/kg kroppsvekt) i 104 uker. Akarbosebehandling resulterte i en signifikant økning i forekomsten av nyresvulster (adenomer og adenokarsinomer) og godartede Leydig-celletumorer. Denne studien ble gjentatt med et lignende resultat. Ytterligere studier ble utført for å skille direkte kreftfremkallende effekter av akarbose fra indirekte effekter som følge av karbohydratunderernæring indusert av de store dosene akarbose som ble brukt i studiene. I en studie med Sprague-Dawley-rotter ble akarbose blandet med fôr, men karbohydratmangel ble forhindret ved tilsetning av glukose til dietten.

en 26-måneders studie av Sprague-Dawley-rotter ble akarbose administrert ved daglig postprandial sonde for å unngå de farmakologiske effektene av stoffet. I begge disse studiene forekom ikke økt forekomst av nyresvulster funnet i de opprinnelige studiene. Akarbose ble også gitt i mat og ved postprandial sonde i to separate studier på Wistar-rotter. Ingen økt forekomst av nyresvulster ble funnet i noen av disse Wistar-rottestudiene. I to fôringsstudier av hamstere, med og uten glukosetilskudd, var det heller ingen tegn på kreftfremkallende egenskaper.
Akarbose induserte ingen DNA-skade in vitro i CHO-kromosomavviksanalysen, bakteriell mutagenese (Ames)-analyse eller en DNA-bindingsanalyse. In vivo ble det ikke påvist DNA-skade i den dominante dødelige testen hos hannmus, eller musemikronukleustesten.
Fertilitetsstudier utført på rotter etter oral administrering ga ingen uheldig effekt på fertilitet eller på den generelle evnen til å reprodusere.
Svangerskap
Teratogene effekter: Graviditetskategori B.
Sikkerheten til PRECOSE hos gravide kvinner er ikke fastslått. Reproduksjonsstudier er utført på rotter i doser på opptil 480 mg/kg (tilsvarer 9 ganger eksponeringen hos mennesker, basert på medikamentets blodnivåer) og har ikke avdekket bevis på nedsatt fertilitet eller skade på fosteret på grunn av akarbose. Hos kaniner kan redusert kroppsvektøkning hos mor, sannsynligvis et resultat av den farmakodynamiske aktiviteten til høye doser akarbose i tarmen, ha vært ansvarlig for en svak økning i antall embryonale tap. Imidlertid viste kaniner som ble gitt 160 mg/kg akarbose (tilsvarende 10 ganger dosen hos mennesker, basert på kroppsoverflate) ingen tegn på embryotoksisitet, og det var ingen tegn på teratogenisitet ved en dose 32 ganger dosen hos mennesker (basert på kropp). flateareal). Det er imidlertid ingen tilstrekkelige og godt kontrollerte studier av PRECOSE 25 mg hos gravide kvinner. Fordi reproduksjonsstudier på dyr ikke alltid er prediktive for den menneskelige responsen, bør dette legemidlet kun brukes under graviditet hvis det er klart nødvendig. Fordi gjeldende informasjon sterkt tyder på at unormale blodsukkernivåer under graviditet er assosiert med en høyere forekomst av medfødte anomalier samt økt neonatal sykelighet og dødelighet, anbefaler de fleste eksperter at insulin brukes under graviditet for å opprettholde blodsukkernivået så nært normalt som mulig. .
Ammende mødre
En liten mengde radioaktivitet er funnet i melken til diegivende rotter etter administrering av radiomerket akarbose. Det er ikke kjent om dette legemidlet skilles ut i morsmelk. Fordi mange legemidler skilles ut i morsmelk, bør ikke PRECOSE 25 mg gis til en ammende kvinne.
Pediatrisk bruk
Sikkerhet og effektivitet av PRECOSE 25 mg hos pediatriske pasienter er ikke fastslått.
Geriatrisk bruk
Av det totale antallet forsøkspersoner i kliniske studier med PRECOSE 25 mg i USA, var 27 % 65 år eller eldre, mens 4 % var 75 år eller eldre. Ingen generelle forskjeller i sikkerhet og effektivitet ble observert mellom disse forsøkspersonene og yngre forsøkspersoner. Gjennomsnittlig steady-state area under the curve (AUC) og maksimale konsentrasjoner av akarbose var omtrent 1,5 ganger høyere hos eldre sammenlignet med unge frivillige; disse forskjellene var imidlertid ikke statistisk signifikante.
OVERDOSE
motsetning til sulfonylurea eller insulin, vil en overdose av PRECOSE ikke føre til hypoglykemi. En overdose kan føre til forbigående økning i flatulens, diaré og ubehag i magen som snart avtar. Ved overdosering skal pasienten ikke gis drikke eller måltider som inneholder karbohydrater (polysakkarider, oligosakkarider og disakkarider) de neste 4–6 timene.
KONTRAINDIKASJONER
PRECOSE 25mg er kontraindisert hos pasienter med kjent overfølsomhet for legemidlet. Precose 25mg er kontraindisert hos pasienter med diabetisk ketoacidose eller cirrhose. PRECOSE 25 mg er også kontraindisert hos pasienter med inflammatorisk tarmsykdom, kolonsår, delvis tarmobstruksjon eller hos pasienter som er disponert for tarmobstruksjon. I tillegg er PRECOSE kontraindisert hos pasienter som har kroniske tarmsykdommer assosiert med markerte forstyrrelser i fordøyelsen eller absorpsjonen og hos pasienter som har tilstander som kan forverres som følge av økt gassdannelse i tarmen.
KLINISK FARMAKOLOGI
Akarbose er et komplekst oligosakkarid som forsinker fordøyelsen av inntatte karbohydrater, og dermed resulterer i en mindre økning i blodsukkerkonsentrasjonen etter måltider. Som en konsekvens av plasmaglukosereduksjon, reduserer PRECOSE nivåene av glykosylert hemoglobin hos pasienter med type 2 diabetes mellitus. Systemisk ikke-enzymatisk proteinglykosylering, som reflektert av nivåer av glykosylert hemoglobin, er en funksjon av gjennomsnittlig blodsukkerkonsentrasjon over tid.
Virkningsmekanismen
motsetning til sulfonylurea, øker ikke PRECOSE 50 mg insulinsekresjon. Den antihyperglykemiske virkningen av akarbose skyldes en konkurrerende, reversibel hemming av alfa-amylase i bukspyttkjertelen og membranbundne tarm-alfa-glukosidhydrolase-enzymer. Pankreatisk alfa-amylase hydrolyserer kompleks stivelse til oligosakkarider i lumen av tynntarmen, mens de membranbundne tarm-alfa-glukosidasene hydrolyserer oligosakkarider, trisakkarider og disakkarider til glukose og andre monosakkarider i tynntarmskanten. Hos diabetespasienter resulterer denne enzymhemmingen i en forsinket glukoseabsorpsjon og en reduksjon av postprandial hyperglykemi.
Fordi virkningsmekanismen er forskjellig, er effekten av PRECOSE for å forbedre glykemisk kontroll additiv til effekten til sulfonylurea, insulin eller metformin når det brukes i kombinasjon. I tillegg reduserer PRECOSE 50mg de insulinotropiske og vektøkende effektene av sulfonylurea.
Akarbose har ingen hemmende aktivitet mot laktase og vil følgelig ikke forventes å indusere laktoseintoleranse.
Farmakokinetikk
Absorpsjon
en studie med 6 friske menn ble mindre enn 2 % av en oral dose av akarbose absorbert som aktivt medikament, mens omtrent 35 % av total radioaktivitet fra en 14C-merket oral dose ble absorbert. Gjennomsnittlig 51 % av en oral dose ble skilt ut i feces som uabsorbert medikamentrelatert radioaktivitet innen 96 timer etter inntak. Fordi akarbose virker lokalt i mage-tarmkanalen, er denne lave systemiske biotilgjengeligheten av moderforbindelsen terapeutisk ønsket. Etter oral dosering av friske frivillige med 14C-merket akarbose, ble maksimale plasmakonsentrasjoner av radioaktivitet oppnådd 14–24 timer etter dosering, mens maksimale plasmakonsentrasjoner av aktivt legemiddel ble oppnådd etter ca. 1 time. Den forsinkede absorpsjonen av akarboserelatert radioaktivitet reflekterer absorpsjonen av metabolitter som kan dannes av enten tarmbakterier eller intestinal enzymatisk hydrolyse.
Metabolisme
Akarbose metaboliseres utelukkende i mage-tarmkanalen, hovedsakelig av tarmbakterier, men også av fordøyelsesenzymer. En brøkdel av disse metabolittene (ca. 34 % av dosen) ble absorbert og deretter utskilt i urinen. Minst 13 metabolitter har blitt separert kromatografisk fra urinprøver. De viktigste metabolittene er identifisert som 4-metylpyrogallolderivater (det vil si sulfat-, metyl- og glukuronidkonjugater). Én metabolitt (dannet ved spaltning av et glukosemolekyl fra akarbose) har også alfa-glukosidasehemmende aktivitet. Denne metabolitten, sammen med moderforbindelsen, gjenvunnet fra urinen, utgjør mindre enn 2 % av den totale administrerte dosen.
Utskillelse
Fraksjonen av akarbose som absorberes som intakt medikament blir nesten fullstendig utskilt av nyrene. Når akarbose ble gitt intravenøst, ble 89 % av dosen gjenvunnet i urinen som aktivt medikament innen 48 timer. I motsetning til dette ble mindre enn 2 % av en oral dose gjenfunnet i urinen som aktivt (det vil si utgangsstoff og aktiv metabolitt) legemiddel. Dette stemmer overens med den lave biotilgjengeligheten til det opprinnelige legemidlet. Halveringstiden for plasmaeliminering av akarboseaktivitet er ca. 2 timer hos friske frivillige. Følgelig oppstår ikke legemiddelakkumulering med tre ganger daglig (tid) oral dosering.
Spesielle populasjoner
Gjennomsnittlig steady-state area under the curve (AUC) og maksimale konsentrasjoner av akarbose var omtrent 1,5 ganger høyere hos eldre sammenlignet med unge frivillige; disse forskjellene var imidlertid ikke statistisk signifikante. Pasienter med alvorlig nedsatt nyrefunksjon (Clcr
Legemiddel-legemiddelinteraksjoner
Studier på friske frivillige har vist at PRECOSE ikke har noen effekt på verken farmakokinetikken eller farmakodynamikken til nifedipin, propranolol eller ranitidin. PRECOSE interfererte ikke med absorpsjon eller disponering av sulfonylureaglyburid hos diabetikere. PRECOSE kan påvirke digoksins biotilgjengelighet og kan kreve dosejustering av digoksin med 16 % (90 % konfidensintervall: 8-23 %), redusere gjennomsnittlig Cmax for digoksin med 26 % (90 % konfidensintervall: 16–34 %) og redusere gjennomsnittlig bunnnivå. konsentrasjoner av digoksin med 9 % (90 % konfidensgrense: 19 % reduksjon til 2 % økning). (Se FORHOLDSREGLER: NARKOTIKAHANDEL .)
Mengden metformin som ble absorbert mens du tok PRECOSE var bioekvivalent med mengden som ble absorbert når du tok placebo, som indikert av plasma-AUC-verdiene. Maksimal plasmanivå av metformin ble imidlertid redusert med ca. 20 % når du tok PRECOSE på grunn av en liten forsinkelse i absorpsjonen av metformin. Det er liten eller noen klinisk signifikant interaksjon mellom PRECOSE og metformin.
Kliniske studier
Klinisk erfaring fra dosefinnende studier hos pasienter med type 2-diabetes mellitus som kun får kostholdsbehandling
Resultater fra seks kontrollerte, fastdose, monoterapistudier av PRECOSE i behandling av type 2 diabetes mellitus, som involverte 769 PRECOSE-behandlede pasienter, ble kombinert og et vektet gjennomsnitt av forskjellen fra placebo i gjennomsnittlig endring fra baseline i glykosylert hemoglobin ( HbA1c) ble beregnet for hvert dosenivå som presentert nedenfor:
Selv om studier brukte en maksimal dose på 200 eller 300 mg tid, er maksimal anbefalt dose for pasienter 60 kg er 100 mg tid
Resultater fra disse seks monoterapistudiene med faste doser ble også kombinert for å utlede et vektet gjennomsnitt av forskjellen fra placebo i gjennomsnittlig endring fra baseline for én time postprandiale plasmaglukosenivåer som vist i følgende figur:
Figur 1 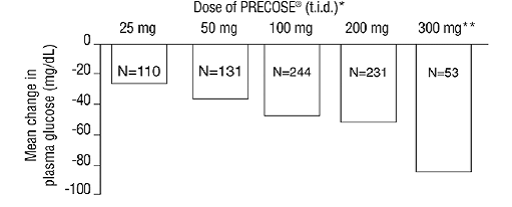
* PRECOSE 50 mg var statistisk signifikant forskjellig fra placebo ved alle doser med hensyn til effekt på én time postprandial plasmaglukose. ** 300 mg tid PRECOSE 50 mg kur var bedre enn lavere doser, men det var ingen statistisk signifikante forskjeller fra 50 til 200 mg tid
Klinisk erfaring hos pasienter med type 2 diabetes mellitus på monoterapi, eller i kombinasjon med sulfonylurea, metformin eller insulin
PRECOSE ble studert som monoterapi og som kombinasjonsbehandling med sulfonylurea-, metformin- eller insulinbehandling. Behandlingseffektene på HbA1c-nivåer og en-times postprandiale glukosenivåer er oppsummert for fire placebokontrollerte, dobbeltblinde, randomiserte studier utført i USA i henholdsvis tabell 2 og 3. De placebo-subtraherte behandlingsforskjellene, som er oppsummert nedenfor, var statistisk signifikante for begge variablene i alle disse studiene.
Studie 1 (n=109) involverte pasienter på bakgrunnsbehandling med kun diett. Gjennomsnittlig effekt av tillegg av PRECOSE til diettbehandling var en endring i HbA1c på -0,78 %, og en forbedring av én time postprandial glukose på -74,4 mg/dL.
I studie 2 (n=137) var den gjennomsnittlige effekten av tillegg av PRECOSE 25 mg til maksimal sulfonylureabehandling en endring i HbA1c på -0,54 %, og en forbedring av én time postprandial glukose på -33,5 mg/dL.
studie 3 (n=147), var den gjennomsnittlige effekten av tillegg av PRECOSE 50 mg til maksimal metforminbehandling en endring i HbA1c på -0,65 %, og en forbedring av én time postprandial glukose på -34,3 mg/dL.
Studie 4 (n=145) viste at PRECOSE lagt til pasienter på bakgrunnsbehandling med insulin resulterte i en gjennomsnittlig endring i HbA1c på -0,69 %, og en forbedring av én time postprandial glukose på -36,0 mg/dL.
En ettårig studie av PRECOSE som monoterapi eller i kombinasjon med sulfonylurea-, metformin- eller insulinbehandling ble utført i Canada der 316 pasienter ble inkludert i den primære effektanalysen (figur 2). I diett-, sulfonylurea- og metformingruppene var den gjennomsnittlige reduksjonen i HbA1c produsert ved tilsetning av PRECOSE 50 mg statistisk signifikant etter seks måneder, og denne effekten var vedvarende etter ett år. Hos PRECOSE-behandlede pasienter på insulin var det en statistisk signifikant reduksjon i HbA1c etter seks måneder, og en trend for reduksjon etter ett år.
Figur 2 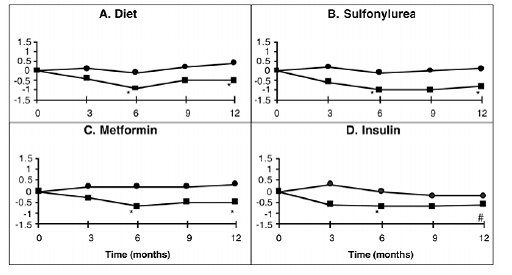
Figur 2: Effekter av PRECOSE (III) og Placebo (III) på gjennomsnittlig endring i HbA1c-nivåer fra baseline gjennom en ettårig studie hos pasienter med type 2 diabetes mellitus når de brukes i kombinasjon med: (A) diett alene; (B) sulfonylurea; (C) metformin; eller (D) insulin. Behandlingsforskjeller etter 6 og 12 måneder ble testet: * p
PASIENTINFORMASJON
Pasienter bør få beskjed om å ta PRECOSE 50 mg oralt tre ganger daglig ved starten (med den første biten) av hvert hovedmåltid. Det er viktig at pasienter fortsetter å følge kostholdsinstruksjoner, et regelmessig treningsprogram og regelmessig testing av urin og/eller blodsukker.
PRECOSE i seg selv forårsaker ikke hypoglykemi selv når det administreres til pasienter i fastende tilstand. Sulfonylurea-medisiner og insulin kan imidlertid senke blodsukkernivået nok til å forårsake symptomer eller noen ganger livstruende hypoglykemi. Fordi PRECOSE gitt i kombinasjon med et sulfonylurea eller insulin vil føre til en ytterligere reduksjon av blodsukkeret, kan det øke det hypoglykemiske potensialet til disse midlene. Hypoglykemi forekommer ikke hos pasienter som får metformin alene under vanlige bruksforhold, og det ble ikke observert økt forekomst av hypoglykemi hos pasienter når PRECOSE ble lagt til metforminbehandling. Risikoen for hypoglykemi, dens symptomer og behandling, og tilstander som disponerer for utviklingen bør være godt forstått av pasienter og ansvarlige familiemedlemmer. Fordi PRECOSE 50mg forhindrer nedbrytning av spisesukker, bør pasienter ha en lett tilgjengelig kilde til glukose (dekstrose, D-glukose) for å behandle symptomer på lavt blodsukker når de tar PRECOSE i kombinasjon med et sulfonylurea eller insulin.
Hvis bivirkninger oppstår med PRECOSE, utvikles de vanligvis i løpet av de første ukene av behandlingen. De er oftest milde til moderate gastrointestinale effekter, som flatulens, diaré eller ubehag i magen, og avtar generelt i frekvens og intensitet med tiden.
