Cartia XT 180mg Bruk, bivirkninger og dosering. Pris i nettapotek. Generisk medisin uten resept.
Hva er Cartia og hvordan brukes det?
Cartia er en reseptbelagt medisin som brukes til å behandle symptomene på brystsmerter (angina), høyt blodtrykk (hypertensjon), paroksysmal supraventrikulær takykardi og atrieflimmer (fladder). Cartia kan brukes alene eller sammen med andre medisiner.
Cartia tilhører en klasse legemidler som kalles Antidysrhythmics, IV; Kalsiumkanalblokkere; Kalsiumkanalblokkere, ikke-dihydropyridin.
Hva er de mulige bivirkningene av Cartia?
Cartia kan forårsake alvorlige bivirkninger, inkludert:
- . brystsmerter, . sakte hjerteslag, . bankende hjerteslag, . flagrende i brystet, . svimmelhet, . opphovning, . rask vektøkning, . kortpustethet, . feber, . sår hals, . brennende øyne, . hudsmerter, og . rødt eller lilla hudutslett med blemmer og avskalling
Få medisinsk hjelp med en gang hvis du har noen av symptomene nevnt ovenfor.
De vanligste bivirkningene av Cartia inkluderer:
- . mild hodepine, . lett svimmelhet, og . forkjølelsessymptomer (tett nese, nysing, sår hals)
Fortell legen dersom du har noen bivirkninger som plager deg eller som ikke går over.
Dette er ikke alle mulige bivirkninger av Cartia. Spør legen din eller apoteket for mer informasjon.
Ring legen din for medisinsk råd om bivirkninger. Du kan rapportere bivirkninger til FDA på 1-800-FDA-1088.
BESKRIVELSE
Diltiazemhydroklorid er en kalsiumioncellulær influxhemmer (langsom kanalblokker eller kalsiumantagonist). Kjemisk er diltiazemhydroklorid 1,5-benzotiazepin-4(5H)on,3-(acetyloksy)-5-[2-(dimetylamino)etyl]-2,3-dihydro-2-(4-metoksyfenyl)-, monohydroklorid ,(+)-cis-. Den kjemiske strukturen er:
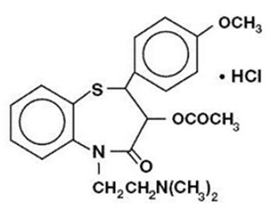
Diltiazemhydroklorid er et hvitt til off-white krystallinsk pulver med en bitter smak. Det er løselig i vann, metanol og kloroform. Den har en molekylvekt på 450,98. Diltiazemhydroklorid kapsel med forlenget frigivelse (en gang daglig dosering) er formulert som en kapsel med forlenget frigivelse én gang daglig som inneholder 120 mg, 180 mg, 240 mg eller 300 mg diltiazemhydroklorid.
tillegg inneholder hver kapsel følgende inaktive ingredienser: acetyltributylcitrat, ammoniometakrylat-kopolymer-NF, D & C Red #28, D & C Yellow #10, D & C Yellow #10 Aluminium Lake, etylcellulose, FD & C Blue #1 Aluminium Lake, FD & C Blue #2 Aluminium Lake, FD & C Red #40, FD & C Red #40 Aluminium Lake, gelatin-NF, magnesiumstearat, metakrylsyrekopolymer-NF, propylenglykol, polysorbat 80-NF, stivelse sukrose, talkum USP og titandioksyd. 180 mg og 240 mg kapslene inneholder gult jernoksid. I tillegg inneholder 240 mg kapselen også svart jernoksid og rødt jernoksid.
For oral administrering.
Dette stoffet oppfyller USP Drug Release 9.
INDIKASJONER
Diltiazemhydroklorid depotkapsler USP (en gang daglig dosering) er indisert for behandling av hypertensjon. Det kan brukes alene eller i kombinasjon med andre antihypertensive medisiner.
Diltiazemhydroklorid depotkapsler USP (en gang daglig dosering) er indisert for behandling av kronisk stabil angina og angina på grunn av koronararteriespasmer.
DOSERING OG ADMINISTRASJON
Pasienter kontrollert på diltiazem alene eller i kombinasjon med andre medisiner kan byttes til diltiazemhydroklorid depotkapsler USP (en gang daglig dosering) ved nærmeste ekvivalente totale daglige dose. Høyere doser av diltiazemhydroklorid depotkapsler USP (en gang daglig dosering) kan være nødvendig hos noen pasienter. Pasienter bør overvåkes nøye. Etterfølgende titrering til høyere eller lavere doser kan være nødvendig og bør initieres som klinisk berettiget. Det er begrenset generell klinisk erfaring med doser over 360 mg, men doser til 540 mg er studert i kliniske studier. Forekomsten av bivirkninger øker når dosen øker med førstegrads AV-blokkering, svimmelhet og sinusbradykardi som har det sterkeste forholdet til dosen.
Hypertensjon
Doseringen må justeres ved titrering til individuelle pasientbehov. Når det brukes som monoterapi, er rimelige startdoser 180 til 240 mg én gang daglig, selv om noen pasienter kan reagere på lavere doser. Maksimal antihypertensiv effekt observeres vanligvis etter 14 dager med kronisk terapi; derfor bør dosejusteringer planlegges deretter. Det vanlige doseringsområdet studert i kliniske studier var 240 til 360 mg én gang daglig. Individuelle pasienter kan respondere på høyere doser på opptil 480 mg én gang daglig.
Angina
Doser for behandling av angina bør justeres til hver pasients behov, og starter med en dose på 120 eller 180 mg én gang daglig. Individuelle pasienter kan respondere på høyere doser på opptil 480 mg én gang daglig. Ved behov kan titrering utføres over en periode på 7 til 14 dager.
Diltiazem Hydrochloride Extended-release Capsules USP (en gang daglig dosering)
Samtidig bruk med andre kardiovaskulære midler
. Sublingual NTG. Kan tas etter behov for å avbryte akutte anginaanfall under behandling med diltiazemhydroklorid depotkapsler (en gang om dagen). . Profylaktisk nitratterapi. Diltiazem hydroklorid kapsler med forlenget frigivelse (en gang daglig dosering) kan trygt administreres sammen med kort- og langtidsvirkende nitrater. . Betablokkere ( se ADVARSLER og FORHOLDSREGLER ). . Antihypertensiva. Diltiazemhydroklorid kapsler med forlenget frigivelse (en gang daglig dosering) har en additiv antihypertensiv effekt når de brukes sammen med andre antihypertensiva. Derfor kan dosen av diltiazemhydroklorid depotkapsler USP (en gang daglig dosering) eller de samtidige antihypertensiva må justeres når den ene til den andre.HVORDAN LEVERES
MERK: PRODUKTET KAN HA EN LUKT.
Lagringsforhold
Oppbevares ved 20° til 25°C (68° til 77°F) [Se USP kontrollert romtemperatur ].
Unngå overdreven fuktighet.
Dispenser i tett, lysbestandig beholder som definert i USP.
Produsert av: Actavis Laboratories FL, Inc., Fort Lauderdale, FL 33314 USA. Distribuert av: Actavis Pharma, Inc., Parsippany, NJ 07054 USA. Revidert: desember 2014
BIVIRKNINGER
Alvorlige bivirkninger har vært sjeldne i studier utført til dags dato, men det bør erkjennes at pasienter med nedsatt ventrikkelfunksjon og hjerteledningsforstyrrelser vanligvis har blitt ekskludert fra disse studiene.
Følgende tabell viser de vanligste bivirkningene rapportert i placebokontrollerte angina- og hypertensjonsstudier hos pasienter som får diltiazemhydroklorid depotkapsel (en gang daglig dosering) opp til 360 mg med rater hos placebopasienter vist for sammenligning.
Diltiazem hydroklorid kapsel med forlenget frigivelse (en gang om dagen) Placebokontrollerte angina- og hypertensjonsforsøk kombinert
kliniske studier med diltiazemhydroklorid depotkapsler (en gang daglig dosering), diltiazemhydrokloridtabletter og diltiazemhydroklorid depotkapsler som involverte over 3200 pasienter, var de vanligste hendelsene (dvs. mer enn 1 %) ødem (4,6 %) , hodepine (4,6 %), svimmelhet (3,5 %), asteni (2,6 %), førstegrads AV-blokkering (2,4 %), bradykardi (1,7 %), rødme (1,4 %), kvalme (1,4 %) og utslett ( 1,2 %).
I tillegg ble følgende hendelser rapportert sjelden (mindre enn 1 %) i angina- eller hypertensjonsforsøk:
Kardiovaskulær: Angina, arytmi, AV-blokk (andre eller tredje grad), grenblokk, kongestiv hjertesvikt, EKG-avvik, hypotensjon, hjertebank, synkope, takykardi, ventrikulære ekstrasystoler.
Nervesystemet: Unormale drømmer, hukommelsestap, depresjon, unormal gange, hallusinasjoner, søvnløshet, nervøsitet, parestesi, personlighetsforandring, somnolens, tinnitus, skjelving.
Gastrointestinale: Anoreksi, forstoppelse, diaré, munntørrhet, dysgeusi, dyspepsi, milde forhøyelser av SGOT, SGPT, LDH og alkalisk fosfatase (se ADVARSLER , Akutt leverskade ), tørste, oppkast, vektøkning.
Dermatologisk: Petekkier, lysfølsomhet, pruritus, urticaria.
Annen: Amblyopi, CPK-økning, dyspné, neseblødning, øyeirritasjon, hyperglykemi, hyperurikemi, impotens, muskelkramper, nesetetthet, nocturi, osteoartikulær smerte, polyuri, seksuelle vansker.
Følgende hendelser etter markedsføring er rapportert sjelden hos pasienter som får diltiazem: akutt generalisert eksantematøs pustulose, allergiske reaksjoner, alopecia, angioødem (inkludert ansikts- eller periorbitalt ødem), asystoli, erythema multiforme (inkludert Stevens-Johnkrotoksisk dermalitis syndrom), , ekstrapyramidale symptomer, gingival hyperplasi, hemolytisk anemi, økt blødningstid, leukopeni, fotosensitivitet (inkludert lichenoid keratose og hyperpigmentering ved soleksponerte hudområder), purpura, retinopati, myopati og trombocytopeni. I tillegg er det observert hendelser som hjerteinfarkt som ikke er lett å skille fra sykdommens naturlige historie hos disse pasientene. En rekke veldokumenterte tilfeller av generalisert utslett, noen karakterisert som leukocytoklastisk vaskulitt, er rapportert. Imidlertid er en definitiv årsak og virkning sammenheng mellom disse hendelsene og diltiazemterapi ennå ikke etablert.
For å rapportere MISTENTE BIVIRKNINGER, kontakt Actavis på 1-800-272-5525 eller FDA på 1-800-FDA-1088 eller www.fda.gov/medwatch.
NARKOTIKAHANDEL
På grunn av potensialet for additive effekter, er forsiktighet og forsiktig titrering nødvendig hos pasienter som får diltiazem samtidig med andre midler som er kjent for å påvirke hjertets kontraktilitet og/eller ledning (se ADVARSLER ). Farmakologiske studier indikerer at det kan være additive effekter for å forlenge AV-ledning ved bruk av betablokkere eller digitalis samtidig med diltiazem (se ADVARSLER ).
Som med alle legemidler, bør det utvises forsiktighet ved behandling av pasienter med flere medisiner. Diltiazem er både et substrat og en hemmer av cytokrom P-450 3A4 enzymsystemet. Andre legemidler som er spesifikke substrater, hemmere eller indusere av dette enzymsystemet kan ha en betydelig innvirkning på effektiviteten og bivirkningsprofilen til diltiazem. Pasienter som tar andre legemidler som er substrater for CYP450 3A4, spesielt pasienter med nedsatt nyre- og/eller leverfunksjon, kan trenge dosejustering ved start eller avslutning av samtidig administrering av diltiazem for å opprettholde optimale terapeutiske blodnivåer.
Bedøvelsesmidler
Depresjonen av hjertekontraktilitet, konduktivitet og automatikk samt vaskulær utvidelse forbundet med anestetika kan potenseres av kalsiumkanalblokkere. Ved samtidig bruk bør anestetika og kalsiumblokkere titreres nøye.
Benzodiazepiner
Studier viste at diltiazem økte AUC for midazolam og triazolam med 3 til 4 ganger og Cmax med 2 ganger sammenlignet med placebo. Eliminasjonshalveringstiden for midazolam og triazolam økte også (1,5 til 2,5 ganger) ved samtidig administrering med diltiazem. Disse farmakokinetiske effektene sett under samtidig administrering av diltiazem kan resultere i økte kliniske effekter (f.eks. forlenget sedasjon) av både midazolam og triazolam.
Betablokkere
Kontrollerte og ukontrollerte innenlandske studier tyder på at samtidig bruk av diltiazem og betablokkere vanligvis tolereres godt, men tilgjengelige data er ikke tilstrekkelige til å forutsi effekten av samtidig behandling hos pasienter med venstre ventrikkel dysfunksjon eller hjerteledningsforstyrrelser.
Administrering av diltiazemhydroklorid samtidig med propranolol hos fem normale frivillige resulterte i økte propranololnivåer hos alle forsøkspersoner, og biotilgjengeligheten av propranolol økte med ca. 50 %. In vitro ser det ut til at propranolol er fortrengt fra bindingsstedene av diltiazem. Hvis kombinasjonsbehandling settes i gang eller seponeres i forbindelse med propranolol, kan en justering av propranololdosen være nødvendig (se ADVARSLER ).
Buspiron
Hos ni friske forsøkspersoner økte diltiazem den gjennomsnittlige buspiron-AUC 5,5 ganger og Cmax 4,1 ganger signifikant sammenlignet med placebo. T½ og Tmax for buspiron ble ikke signifikant påvirket av diltiazem. Forsterkede effekter og økt toksisitet av buspiron kan være mulig ved samtidig administrering med diltiazem. Påfølgende dosejusteringer kan være nødvendig under samtidig administrering, og bør være basert på klinisk vurdering.
Karbamazepin
Samtidig administrering av diltiazem og karbamazepin har blitt rapportert å resultere i forhøyede serumnivåer av karbamazepin (40 % til 72 % økning), noe som resulterer i toksisitet i noen tilfeller. Pasienter som får disse legemidlene samtidig bør overvåkes for en potensiell legemiddelinteraksjon.
Cimetidin
En studie med seks friske frivillige har vist en signifikant økning i maksimale diltiazemplasmanivåer (58 %) og area-under-kurven (53 %) etter en 1-ukes kur med cimetidin med 1200 mg per dag og en enkelt dose av diltiazem 60 mg. Ranitidin ga mindre, ikke-signifikante økninger. Effekten kan være mediert av cimetidins kjente hemming av hepatisk cytokrom P-450, enzymsystemet som er ansvarlig for first-pass metabolismen av diltiazem. Pasienter som for tiden får diltiazem-behandling bør overvåkes nøye for endring i farmakologisk effekt når behandling med cimetidin startes og avsluttes. En justering av diltiazemdosen kan være nødvendig.
Klonidin
Sinusbradykardi som resulterer i sykehusinnleggelse og pacemakerinnsetting er rapportert i forbindelse med bruk av klonidin samtidig med diltiazem. Overvåk hjertefrekvensen hos pasienter som samtidig får diltiazem og klonidin.
Syklosporin
En farmakokinetisk interaksjon mellom diltiazem og ciklosporin er observert under studier med nyre- og hjertetransplanterte pasienter. Hos nyre- og hjertetransplanterte var en reduksjon av ciklosporindosen fra 15 % til 48 % nødvendig for å opprettholde bunnkonsentrasjoner av ciklosporin tilsvarende de som ble sett før tilsetning av diltiazem. Hvis disse midlene skal administreres samtidig, bør ciklosporinkonsentrasjoner overvåkes, spesielt når diltiazembehandling initieres, justeres eller seponeres.
Effekten av ciklosporin på plasmakonsentrasjoner av diltiazem er ikke evaluert.
Digitalis
Administrering av diltiazem med digoksin hos 24 friske mannlige forsøkspersoner økte plasmadigoksinkonsentrasjonene med ca. 20 %. En annen etterforsker fant ingen økning i digoksinnivåer hos 12 pasienter med koronarsykdom. Siden det har vært motstridende resultater angående effekten av digoksinnivåer, anbefales det at digoksinnivåer overvåkes når du starter, justerer og avslutter diltiazembehandling for å unngå mulig over- eller underdigitalisering (se ADVARSLER ).
Kinidin
Diltiazem øker AUC(0-→) av kinidin signifikant med 51 %, T½ med 36 %, og reduserer CL oralt med 33 %. Overvåking av kinidinbivirkninger kan være berettiget og dosen justeres deretter.
Rifampin
Samtidig administrering av rifampin og diltiazem reduserte plasmakonsentrasjonen av diltiazem til upåviselige nivåer. Samtidig administrering av diltiazem med rifampin eller en hvilken som helst kjent CYP3A4-induktor bør unngås når det er mulig, og alternativ behandling bør vurderes.
Statiner
Diltiazem er en hemmer av CYP3A4 og har vist seg å øke AUC signifikant for enkelte statiner. Risikoen for myopati og rabdomyolyse med statiner metabolisert av CYP3A4 kan øke ved samtidig bruk av diltiazem. Når det er mulig, bruk et ikke-CYP3A4-metabolisert statin sammen med diltiazem; ellers bør dosejusteringer for både diltiazem og statin vurderes sammen med nøye overvåking for tegn og symptomer på statinrelaterte bivirkninger.
en cross-over-studie med friske frivillige (N=10), resulterte samtidig administrering av en enkeltdose på 20 mg simvastatin på slutten av et 14-dagers regime med 120 mg to ganger daglig diltiazem SR i en 5 ganger økning i gjennomsnittlig simvastatin AUC versus simvastatin alene. Personer med økt gjennomsnittlig steady-state eksponering for diltiazem viste en større fold økning i simvastatineksponering. Databaserte simuleringer viste at ved en daglig dose på 480 mg diltiazem kan det forventes en 8- til 9 ganger gjennomsnittlig økning i simvastatin AUC. Hvis samtidig administrering av simvastatin og diltiazem er nødvendig, begrense daglige doser av simvastatin til 10 mg og diltiazem til 240 mg.
en randomisert, åpen, 4-veis cross-over-studie med ti forsøkspersoner, resulterte samtidig administrering av diltiazem (120 mg to ganger daglig diltiazem SR i 2 uker) med en enkeltdose på 20 mg lovastatin i 3- til 4 ganger økning i gjennomsnittet. lovastatin AUC og versus lovastatin alene. I samme studie var det ingen signifikant endring i 20 mg enkeltdose pravastatin AUC og ved samtidig administrering av diltiazem. Diltiazem plasmanivåer ble ikke signifikant påvirket av lovastatin eller pravastatin.
ADVARSLER
Hjerteledning
Diltiazem forlenger AV-knute-refraktære perioder uten vesentlig forlengelse av sinusknutegjenopprettingstiden, bortsett fra hos pasienter med sick sinus syndrome. Denne effekten kan i sjeldne tilfeller føre til unormalt langsom hjertefrekvens (spesielt hos pasienter med sick sinus syndrome) eller andre- eller tredjegrads AV-blokk (13 av 3290 pasienter eller 0,40%). Samtidig bruk av diltiazem med betablokkere eller digitalis kan resultere i additive effekter på hjerteledning. En pasient med Prinzmetals angina utviklet perioder med asystoli (2 til 5 sekunder) etter en enkeltdose på 60 mg diltiazem (se BIVIRKNINGER ).
Kongestiv hjertesvikt
Selv om diltiazem har en negativ inotrop effekt i isolerte dyrevevspreparater, har ikke hemodynamiske studier på mennesker med normal ventrikkelfunksjon vist en reduksjon i hjerteindeks eller konsistente negative effekter på kontraktilitet (dp/dt). En akutt studie av oral diltiazem hos pasienter med nedsatt ventrikkelfunksjon (ejeksjonsfraksjon 24 % ± 6 %) viste bedring i indekser for ventrikkelfunksjon uten signifikant reduksjon i kontraktil funksjon (dp/dt). Forverring av kongestiv hjertesvikt er rapportert hos pasienter med allerede eksisterende svekkelse av ventrikkelfunksjon. Erfaring med bruk av diltiazemhydroklorid i kombinasjon med betablokkere hos pasienter med nedsatt ventrikkelfunksjon er begrenset. Det bør utvises forsiktighet ved bruk av denne kombinasjonen.
Hypotensjon
Blodtrykksreduksjon assosiert med diltiazembehandling kan av og til føre til symptomatisk hypotensjon.
Akutt leverskade
Milde økninger av transaminaser med og uten samtidig økning i alkalisk fosfatase og bilirubin er observert i kliniske studier. Slike økninger var vanligvis forbigående og forsvant ofte selv ved fortsatt diltiazembehandling. I sjeldne tilfeller har betydelige økninger i enzymer som alkalisk fosfatase, LDH, SGOT, SGPT og andre fenomener forenlig med akutt leverskade blitt observert. Disse reaksjonene hadde en tendens til å oppstå tidlig etter behandlingsstart (1 til 8 uker) og har vært reversible ved seponering av medikamentell behandling. Forholdet til diltiazem er usikkert i noen tilfeller, men sannsynlig i noen (se FORHOLDSREGLER ).
FORHOLDSREGLER
Generell
Diltiazemhydroklorid metaboliseres i stor grad av leveren og skilles ut av nyrene og i galle. Som med alle legemidler gitt over lengre perioder, bør laboratorieparametre for nyre- og leverfunksjon overvåkes med jevne mellomrom. Legemidlet bør brukes med forsiktighet hos pasienter med nedsatt nyre- eller leverfunksjon. I subakutte og kroniske hunde- og rottestudier designet for å produsere toksisitet, ble høye doser diltiazem assosiert med leverskade. I spesielle subakutte leverstudier var orale doser på 125 mg/kg og høyere hos rotter assosiert med histologiske endringer i leveren, som var reversible når legemidlet ble seponert. Hos hunder var doser på 20 mg/kg også assosiert med leverforandringer; disse endringene var imidlertid reversible ved fortsatt dosering.
Dermatologiske hendelser (se BIVIRKNINGER kan være forbigående og kan forsvinne til tross for fortsatt bruk av diltiazem. Imidlertid har hudutbrudd som utvikler seg til erythema multiforme og/eller eksfoliativ dermatitt også blitt rapportert sjelden. Hvis en dermatologisk reaksjon vedvarer, bør stoffet seponeres.
Karsinogenese, mutagenese, svekkelse av fruktbarhet
En 24-måneders studie på rotter ved orale dosenivåer på opptil 100 mg/kg/dag og en 21-måneders studie på mus med orale dosenivåer på opptil 30 mg/kg/dag viste ingen tegn på karsinogenitet. Det var heller ingen mutagen respons in vitro eller in vivo i pattedyrcelleanalyser eller in vitro i bakterier. Ingen tegn på nedsatt fertilitet ble observert i en studie utført på hann- og hunnrotter ved orale doser på opptil 100 mg/kg/dag.
Svangerskap
Kategori C. Reproduksjonsstudier er utført på mus, rotter og kaniner. Administrering av doser fra fem til ti ganger større (på mg/kg-basis) enn den daglige anbefalte terapeutiske dosen har resultert i embryo- og fosterdødelighet. Disse dosene har i noen studier blitt rapportert å forårsake skjelettavvik. I de perinatale/postnatale studiene var det en økt forekomst av dødfødsler ved doser på 20 ganger human dose eller mer.
Det er ingen godt kontrollerte studier på gravide kvinner; bruk derfor diltiazem hos gravide kvinner kun hvis den potensielle fordelen rettferdiggjør den potensielle risikoen for fosteret.
Ammende mødre
Diltiazem skilles ut i morsmelk. En rapport antyder at konsentrasjoner i morsmelk kan tilnærme serumnivåene. Hvis bruk av diltiazem anses som nødvendig, bør en alternativ metode for spedbarnsmating settes i gang.
Pediatrisk bruk
Sikkerhet og effektivitet hos pediatriske pasienter er ikke fastslått.
Geriatrisk bruk
Kliniske studier av diltiazem inkluderte ikke tilstrekkelig antall forsøkspersoner i alderen 65 år og over til å avgjøre om de responderer annerledes enn yngre forsøkspersoner. Annen rapportert klinisk erfaring har ikke identifisert forskjeller i respons mellom eldre og yngre pasienter. Generelt bør dosevalg for en eldre pasient være forsiktig, vanligvis fra den lave enden av doseringsområdet, noe som gjenspeiler den høyere frekvensen av nedsatt lever-, nyre- eller hjertefunksjon, og samtidig sykdom eller annen medikamentell behandling.
OVERDOSE
De orale LD50-verdiene hos mus og rotter varierer fra henholdsvis 415 til 740 mg/kg og fra 560 til 810 mg/kg. De intravenøse LD50-verdiene hos disse artene var henholdsvis 60 og 38 mg/kg. Den orale LD50 hos hunder anses å være over 50 mg/kg, mens dødelighet ble sett hos aper ved 360 mg/kg.
Den toksiske dosen hos mennesker er ikke kjent. På grunn av omfattende metabolisme kan blodnivået etter en standarddose diltiazem variere over tidoblet, noe som begrenser nytten av blodnivåer i tilfeller av overdose.
Det har vært rapporter om overdosering av diltiazem i mengder fra
Hendelser observert etter overdosering av diltiazem inkluderte bradykardi, hypotensjon, hjerteblokk og hjertesvikt. De fleste rapporter om overdose beskrev støttende medisinske tiltak og/eller medikamentell behandling. Bradykardi reagerte ofte gunstig på atropin, det samme gjorde hjerteblokk, selv om hjertestimulering også ofte ble brukt til å behandle hjerteblokk. Væsker og vasopressorer ble brukt for å opprettholde blodtrykket, og i tilfeller av hjertesvikt ble inotrope midler administrert. I tillegg fikk noen pasienter behandling med ventilasjonsstøtte, mageskylling, aktivt kull og/eller intravenøst kalsium.
Effektiviteten av intravenøs kalsiumadministrasjon for å reversere de farmakologiske effektene av overdosering av diltiazem har vært inkonsekvent. I noen få rapporterte tilfeller ble overdosering med kalsiumkanalblokkere assosiert med hypotensjon og bradykardi som opprinnelig var refraktær overfor atropin, mer responsive overfor atropin etter at pasientene fikk intravenøs kalsium. I noen tilfeller har intravenøst kalsium blitt administrert (1 g kalsiumklorid eller 3 g kalsiumglukonat) over 5 minutter og gjentatt hvert 10. til 20. minutt etter behov. Kalsiumglukonat har også blitt administrert som en kontinuerlig infusjon med en hastighet på 2 g per time i 10 timer. Infusjoner av kalsium i 24 timer eller mer kan være nødvendig. Pasienter bør overvåkes for tegn på hyperkalsemi.
Ved overdosering eller overdreven respons bør egnede støttetiltak brukes i tillegg til gastrointestinal dekontaminering. Diltiazem ser ikke ut til å bli fjernet ved peritoneal eller hemodialyse. Begrensede data tyder på at plasmaferese eller kullhemoperfusjon kan fremskynde eliminering av diltiazem etter overdose. Basert på de kjente farmakologiske effektene av diltiazem og/eller rapporterte kliniske erfaringer, kan følgende tiltak vurderes:
Bradykardi: Administrer atropin (0,6 til 1 mg). Hvis det ikke er respons på vagal blokade, administrer isoproterenol forsiktig.
AV-blokk i høy grad: Behandle som for bradykardi ovenfor. Fast høygrads AV-blokk bør behandles med hjertestimulering.
Hjertesvikt: Administrer inotrope midler (isoproterenol, dopamin eller dobutamin) og diuretika.
Hypotensjon: Vasopressorer (f.eks. dopamin eller noradrenalin).
Faktisk behandling og dosering bør avhenge av alvorlighetsgraden av den kliniske situasjonen og den behandlende legens vurdering og erfaring.
KONTRAINDIKASJONER
Diltiazem er kontraindisert hos (1) pasienter med sick sinus syndrome bortsett fra i nærvær av en fungerende ventrikulær pacemaker, (2) pasienter med andre- eller tredjegrads AV-blokk unntatt i nærvær av en fungerende ventrikulær pacemaker, (3) pasienter med hypotensjon (mindre enn 90 mm Hg systolisk), (4) pasienter som har vist overfølsomhet for legemidlet, og (5) pasienter med akutt hjerteinfarkt og lungetetthet dokumentert ved røntgen ved innleggelse.
KLINISK FARMAKOLOGI
De terapeutiske effektene av diltiazemhydroklorid depotkapsler USP (en gang daglig dosering) antas å være relatert til dens evne til å hemme den cellulære tilstrømningen av kalsiumioner under membrandepolarisering av hjerte- og vaskulær glatt muskulatur.
Virkningsmekanismer
Hypertensjon
Diltiazemhydroklorid USP-kapsler med forlenget frigivelse (en gang daglig dosering) produserer sin antihypertensive effekt primært ved avslapning av vaskulær glatt muskulatur og den resulterende reduksjonen i perifer vaskulær motstand. Størrelsen på blodtrykksreduksjonen er relatert til graden av hypertensjon; dermed hypertensive individer opplever en antihypertensiv effekt, mens det kun er et beskjedent fall i blodtrykket hos normotensive.
Angina
Diltiazemhydroklorid kapsler USP (en gang daglig dosering) har vist seg å gi økt treningstoleranse, sannsynligvis på grunn av dens evne til å redusere myokardbehovet for oksygen. Dette oppnås via reduksjoner i hjertefrekvens og systemisk blodtrykk ved submaksimal og maksimal arbeidsbelastning. Diltiazem har vist seg å være en potent dilatator av koronararterier, både epikardielle og subendokardielle. Spontan og ergonovin-indusert koronararteriespasme hemmes av diltiazem.
dyremodeller forstyrrer diltiazem den langsomme innover (depolariserende) strømmen i eksiterbart vev. Det forårsaker eksitasjons-kontraksjon frakopling i ulike myokardvev uten endringer i konfigurasjonen av aksjonspotensialet. Diltiazem gir avslapning av koronar vaskulær glatt muskulatur og utvidelse av både store og små koronararterier ved medikamentnivåer som forårsaker liten eller ingen negativ inotrop effekt. Den resulterende økningen i koronar blodstrøm (epikardiell og subendokardiell) forekommer i iskemiske og ikke-iskemiske modeller og er ledsaget av doseavhengige reduksjoner i systemisk blodtrykk og reduksjoner i perifer motstand.
Hemodynamiske og elektrofysiologiske effekter
Som andre kalsiumkanalantagonister, reduserer diltiazem sinoatrial og atrioventrikulær ledning i isolert vev og har en negativ inotrop effekt i isolerte preparater. Hos det intakte dyret kan forlengelse av AH-intervallet sees ved høyere doser.
Hos mennesker forhindrer diltiazem spontane og ergonovin-provoserte kranspulsårer. Det forårsaker en reduksjon i perifer vaskulær motstand og et beskjedent blodtrykksfall hos normotensive individer, og i treningstoleransestudier hos pasienter med iskemisk hjertesykdom reduserer det hjertefrekvens-blodtrykkproduktet for en gitt arbeidsbelastning. Studier til dags dato, primært hos pasienter med god ventrikkelfunksjon, har ikke avdekket bevis på en negativ inotrop effekt; hjerteutgang, ejeksjonsfraksjon og venstre ventrikkels endediastoliske trykk har ikke blitt påvirket. Slike data har ingen prediktiv verdi med hensyn til effekter hos pasienter med dårlig ventrikkelfunksjon, og økt hjertesvikt er rapportert hos pasienter med allerede eksisterende svekkelse av ventrikkelfunksjon. Det er foreløpig få data om interaksjonen mellom diltiazem og betablokkere hos pasienter med dårlig ventrikkelfunksjon. Hvilepuls reduseres vanligvis litt av diltiazem.
Hos hypertensive pasienter gir diltiazemhydroklorid depotkapsler USP (en gang daglig dosering) antihypertensive effekter både i liggende og stående stilling. I en dobbeltblind, parallell, dose-respons studie med doser fra 90 til 540 mg én gang daglig, senket diltiazemhydroklorid kapsel med forlenget frigjøring (dosering én gang daglig) liggende diastolisk blodtrykk på en tilsynelatende lineær måte over hele doseområde studert. Endringene i diastolisk blodtrykk, målt ved bunnen, for placebo, 90 mg, 180 mg, 360 mg og 540 mg var henholdsvis -2,9, -4,5, -6,1, -9,5 og -10,5 mm Hg. Postural hypotensjon observeres sjelden når man plutselig inntar en oppreist stilling. Ingen reflekstakykardi er assosiert med de kroniske antihypertensive effektene. Diltiazem hydroklorid kapsler med forlenget frigivelse USP (en gang daglig dosering) reduserer vaskulær motstand, øker hjertevolum (ved å øke slagvolumet); og gir en liten reduksjon eller ingen endring i hjertefrekvensen. Under dynamisk trening hemmes økninger i diastolisk trykk, mens maksimalt oppnåelig systolisk trykk vanligvis reduseres. Kronisk behandling med diltiazemhydroklorid depotkapsler USP (en gang daglig dosering) gir ingen endring eller økning i plasmakatekolaminer. Ingen økt aktivitet av renin-angiotensin-aldosteron-aksen er observert. Diltiazemhydroklorid depotkapsler USP (en gang daglig dosering) reduserer nyre- og perifere effekter av angiotensin II. Hypertensive dyremodeller reagerer på diltiazem med reduksjoner i blodtrykk og økt urinproduksjon og natriurese uten endring i natrium/kalium-forholdet i urinen.
en dobbeltblind, parallell dose-respons-studie av doser fra 60 mg til 480 mg én gang daglig, økte diltiazemhydroklorid kapsel med forlenget frigivelse (dosering én gang daglig) tiden til avslutning av treningen på en lineær måte over hele dosen rekkevidde studert. Forbedringen i tid til avslutning av trening ved bruk av en Bruce treningsprotokoll, målt ved bunnen, for placebo, 60 mg, 120 mg, 240 mg, 360 mg og 480 mg var 29, 40, 56, 51, 69 og 68 sekunder , henholdsvis. Etter hvert som doser av diltiazemhydroklorid depotkapsel (dosering én gang daglig) ble økt, ble den generelle anginafrekvensen redusert. Diltiazemhydroklorid depotkapsel (dosering én gang daglig), 180 mg én gang daglig, eller placebo ble administrert i en dobbeltblind studie til pasienter som fikk samtidig behandling med langtidsvirkende nitrater og/eller betablokkere. En signifikant økning i tid til avslutning av trening og en signifikant reduksjon i total anginafrekvens ble observert. I denne studien var den totale frekvensen av bivirkninger i behandlingsgruppen med diltiazemhydroklorid depotkapsel (en gang daglig dosering) den samme som i placebogruppen.
Intravenøs diltiazem i doser på 20 mg forlenger AH-ledningstiden og AV-knutefunksjonelle og effektive refraktære perioder med ca. 20 %. I en studie som involverte orale enkeltdoser på 300 mg diltiazemhydroklorid hos seks normale frivillige, var den gjennomsnittlige maksimale PR-forlengelsen 14 % uten tilfeller av større enn førstegrads AV-blokkering. Diltiazem-assosiert forlengelse av AH-intervallet er ikke mer uttalt hos pasienter med førstegrads hjerteblokk. Hos pasienter med sick sinus-syndrom forlenger diltiazem sinussykluslengden betydelig (opptil 50 % i noen tilfeller).
Kronisk oral administrering av diltiazemhydroklorid til pasienter i doser på opptil 540 mg/dag har resultert i små økninger i PR-intervall og kan av og til gi unormal forlengelse (se ADVARSLER ).
Farmakokinetikk og metabolisme
Diltiazem absorberes godt fra mage-tarmkanalen og er utsatt for en omfattende first-pass effekt, noe som gir en absolutt biotilgjengelighet (sammenlignet med intravenøs administrering) på ca. 40 %. Diltiazem gjennomgår omfattende metabolisme der bare 2% til 4% av det uendrede legemidlet vises i urinen. Legemidler som induserer eller hemmer levermikrosomale enzymer kan endre disposisjonen for diltiazem.
Total radioaktivitetsmåling etter kort IV-administrasjon hos friske frivillige tyder på tilstedeværelsen av andre uidentifiserte metabolitter, som oppnår høyere konsentrasjoner enn diltiazem og elimineres langsommere; halveringstid for total radioaktivitet er ca. 20 timer sammenlignet med 2 til 5 timer for diltiazem.
In vitro bindingsstudier viser at diltiazem er 70 % til 80 % bundet til plasmaproteiner. Konkurrerende in vitro ligandbindingsstudier har også vist at diltiazembinding ikke endres av terapeutiske konsentrasjoner av digoksin, hydroklortiazid, fenylbutazon, propranolol, salisylsyre eller warfarin. Plasmaeliminasjonshalveringstiden etter administrering av én eller flere legemidler er ca. 3,0 til 4,5 timer. Desacetyldiltiazem er også tilstede i plasma i nivåer på 10 % til 20 % av det opprinnelige legemidlet og er 25 % til 50 % like potent som en koronar vasodilator som diltiazem. Minimum terapeutiske plasmadiltiazemkonsentrasjoner ser ut til å være i området 50 til 200 ng/ml. Det er en avvik fra linearitet når dosestyrker økes; halveringstiden økes litt med dose. En studie som sammenlignet pasienter med normal leverfunksjon med pasienter med cirrhose fant en økning i halveringstid og en 69 % økning i biotilgjengelighet hos pasienter med nedsatt leverfunksjon. En enkelt studie med ni pasienter med alvorlig nedsatt nyrefunksjon viste ingen forskjell i den farmakokinetiske profilen til diltiazem sammenlignet med pasienter med normal nyrefunksjon.
Diltiazem Hydrochloride Extended-Release Capsules (en gang daglig dosering)
Sammenlignet med et regime med diltiazem-tabletter ved steady-state, absorberes mer enn 95 % av legemidlet fra formuleringen med diltiazemhydroklorid med forlenget frigivelse (en gang daglig dosering). En enkelt dose på 360 mg av kapselen resulterer i påvisbare plasmanivåer innen 2 timer og maksimale plasmanivåer mellom 10 og 14 timer; absorpsjon skjer gjennom hele doseringsintervallet. Når diltiazemhydroklorid depotkapsel (dosering én gang daglig) ble administrert samtidig med en frokost med høyt fettinnhold, ble ikke omfanget av diltiazemabsorpsjon påvirket. Dosedumping forekommer ikke. Den tilsynelatende eliminasjonshalveringstiden etter en eller flere doser er 5 til 8 timer. En avvik fra linearitet lik den som sees med diltiazemtabletter og diltiazemhydrokloridkapsler (to ganger daglig) er observert. Ettersom dosen av diltiazemhydroklorid depotkapsler (en gang daglig dosering) økes fra en daglig dose på 120 mg til 240 mg, er det en økning i arealet under kurven på 2,7 ganger. Når dosen økes fra 240 mg til 360 mg, er det en økning i arealet under kurven på 1,6 ganger.
PASIENTINFORMASJON
Ingen informasjon gitt. Vennligst referer til ADVARSLER og FORHOLDSREGLER seksjoner.
