Proair Inhaler 100mcg Salbutamol Bruk, bivirkninger og dosering. Pris i nettapotek. Generisk medisin uten resept.
Hva er ProAir og hvordan brukes det?
ProAir er et reseptbelagt legemiddel som brukes til å behandle symptomene på akutt, alvorlig eller anstrengelsesutløst astma (bronkospasme). ProAir kan brukes alene eller sammen med andre medisiner.
ProAir tilhører en klasse legemidler kalt PAH, PDE-5-hemmere, fosfodiesterase-5-enzymhemmere.
Det er ikke kjent om ProAir er trygt og effektivt hos barn under 4 år.
Hva er de mulige bivirkningene av ProAir?
ProAir kan forårsake alvorlige bivirkninger, inkludert:
- . hvesing, . kveles, . andre pusteproblemer, . brystsmerter, . rask puls, . bankende hjerteslag eller flagrende i brystet, . alvorlig hodepine, . dunker i nakken eller ørene, . smerte eller svie når du tisser, . økt tørst, . økt vannlating, . tørr i munnen, . lukt av fruktig pust, . kramper i benet, . forstoppelse, . uregelmessige hjerteslag, . økt tørste eller vannlating, . nummenhet eller prikking, og . muskelsvakhet eller slapp følelse
Få medisinsk hjelp med en gang hvis du har noen av symptomene nevnt ovenfor.
De vanligste bivirkningene av ProAir inkluderer:
- . brystsmerter, . raske eller bankende hjerteslag, . svimmelhet, . føler seg skjelven eller nervøs, . hodepine, . ryggsmerte, . Smerter i kroppen, . urolig mage, . sår hals, . bihulesmerter, og . rennende eller tett nese
Fortell legen dersom du har noen bivirkninger som plager deg eller som ikke går over.
Dette er ikke alle mulige bivirkninger av ProAir. Spør legen din eller apoteket for mer informasjon.
Ring legen din for medisinsk råd om bivirkninger. Du kan rapportere bivirkninger til FDA på 1-800-FDA-1088.
BESKRIVELSE
Den aktive ingrediensen i ProAir HFA (albuterolsulfat) inhalasjonsaerosol er albuterolsulfat, et racemisk salt av albuterol. Albuterolsulfat har det kjemiske navnet α -[(tert-butylamino) methyl]-4-hydroksy-m-xylen-α,α'-diol sulfate (2:1) (salt), og har følgende kjemiske struktur:
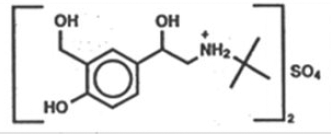
Molekylvekten til albuterolsulfat er 576,7, og den empiriske formelen er (C13H21NO3)2 •H2SO4. Albuterolsulfat er et hvitt til off-white krystallinsk pulver. Det er løselig i vann og litt løselig i etanol. Albuterolsulfat er det offisielle generiske navnet i USA, og salbutamolsulfat er Verdens helseorganisasjons anbefalte generiske navn. ProAir HFA inhalasjonsaerosol er en trykksatt aerosolenhet med målt dose med doseteller. ProAir HFA er kun for oral inhalasjon. Den inneholder en mikrokrystallinsk suspensjon av albuterolsulfat i drivmiddel HFA-134a (1, 1, 1, 2-tetrafluoretan) og etanol.
Prime inhalatoren før bruk for første gang og i tilfeller der inhalatoren ikke har vært brukt på mer enn 2 uker ved å slippe tre sprayer i luften, vekk fra ansiktet. Etter priming leverer hver aktivering 108 mcg albuterolsulfat, fra aktuatormunnstykket (tilsvarer 90 mcg albuterolbase). Hver beholder gir 200 aktiveringer (inhalasjoner).
Dette produktet inneholder ikke klorfluorkarboner (KFK) som drivmiddel.
INDIKASJONER
Bronkospasme
PROAIR HFA inhalasjonsaerosol er indisert for behandling eller forebygging av bronkospasme hos pasienter 4 år og eldre med reversibel obstruktiv luftveissykdom.
Anstrengelsesutløst bronkospasme
PROAIR HFA inhalasjonsaerosol er indisert for forebygging av anstrengelsesutløst bronkospasme hos pasienter 4 år og eldre.
DOSERING OG ADMINISTRASJON
Bronkospasme
For behandling av akutte episoder med bronkospasme eller forebygging av symptomer assosiert med bronkospasme, er den vanlige dosen for voksne og barn 4 år og eldre to inhalasjoner som gjentas hver 4. til 6. time. Hyppigere administrering eller et større antall inhalasjoner anbefales ikke. Hos noen pasienter kan én inhalasjon hver 4. time være tilstrekkelig.
Anstrengelsesutløst bronkospasme
Den vanlige dosen for voksne og barn 4 år eller eldre er to inhalasjoner 15 til 30 minutter før trening.
Administrasjonsinformasjon
Administrer PROAIR HFA kun ved oral inhalasjon. Rist godt før hver spray. For å opprettholde riktig bruk av dette produktet og for å forhindre oppbygging av medisiner og blokkering, er det viktig å følge rengjøringsanvisningene nøye.
Grunning
Prime inhalatoren før bruk for første gang og i tilfeller der inhalatoren ikke har vært brukt på mer enn 2 uker ved å slippe tre sprayer i luften, vekk fra ansiktet.
Rengjøring
Som med alle HFA-holdige albuterol-inhalatorer, er det viktig å rengjøre plastmunnstykket regelmessig for å opprettholde riktig bruk av dette produktet og for å forhindre oppbygging av medisiner og blokkering. Inhalatoren kan slutte å levere medisiner hvis plastaktuatormunnstykket ikke er ordentlig rengjort og tørket. Rengjøring: Vask plastmunnstykket med varmt rennende vann i 30 sekunder, rist av overflødig vann og lufttørk grundig minst en gang i uken. Hvis pasienten har mer enn én PROAIR HFA-inhalator, bør pasienten vaske hver enkelt separat for å unngå å feste feil beholder til feil plastaktuator. På denne måten kan pasienten være sikker på å alltid vite riktig antall gjenværende doser. Fest aldri en beholder med medisiner fra noen annen inhalator til PROAIR HFA-aktuatoren, og fest aldri PROAIR HFA-beholderen til en aktuator fra noen annen inhalator. Hvis munnstykket blir blokkert, vil vask av munnstykket fjerne blokkeringen. Hvis det er nødvendig å bruke inhalatoren før den er helt tørr, rist av overflødig vann, bytt beholderen, spray to ganger i luften vekk fra ansiktet og ta den foreskrevne dosen. Etter slik bruk bør munnstykket vaskes på nytt og lufttørke grundig. [se FDA-godkjent pasientmerking ].
Doseteller
PROAIR HFA har en doseteller festet til aktuatoren. Når pasienten mottar inhalatoren, vil en svart prikk vises i visningsvinduet til den har blitt primet 3 ganger, hvoretter tallet 200 vises. Dosetelleren vil telle ned hver gang en spray slippes ut. Når dosetelleren når 20, vil fargen på tallene endres til rød for å minne pasienten på å kontakte apoteket for påfyll av medisiner eller konsultere legen sin for å få resept.
Når dosetelleren når 0, endres bakgrunnen til konstant rød. PROAIR HFA-inhalator skal kasseres når dosetelleren viser 0 eller etter utløpsdatoen på produktet, avhengig av hva som kommer først.
HVORDAN LEVERES
Doseringsformer og styrker
PROAIR HFA er en inhalasjonsaerosol. PROAIR HFA leveres som en 8,5 g/200 aktuasjoner trykksatt aluminiumsbeholder med en rød plastaktuator med doseteller og hvit støvhette hver i esker med én. Hver aktivering leverer 120 mcg albuterolsulfat fra beholderventilen og 108 mcg albuterolsulfat fra aktuatormunnstykket (tilsvarer 90 mcg albuterolbase).
Oppbevaring og håndtering
PROAIR HFA (albuterolsulfat) Innånding Aerosol leveres som trykksatt aluminiumsbeholder med rød plastaktuator med doseteller og hvit støvhette hver i esker à én. Hver beholder inneholder 8,5 g av formuleringen og gir 200 aktiveringer ( NDC 59310-579-22). Hver aktivering leverer 120 mcg albuterolsulfat fra beholderventilen og 108 mcg albuterolsulfat fra aktuatormunnstykket (tilsvarer 90 mcg albuterolbase).
RIST GODT FØR BRUK. Oppbevares mellom 15° og 25°C (59° og 77°F). Innhold under press. Ikke punkter eller brenn. Beskytt mot kuldegrader og langvarig eksponering for direkte sollys. Eksponering for temperaturer over 120°F kan føre til sprengning. For best resultat bør beholderen være i romtemperatur før bruk. Unngå spraying i øynene. Oppbevares utilgjengelig for barn.
Se FDA-godkjent pasientmerking for grunning og rengjøringsinstruksjoner.
Den røde aktuatoren som følger med PROAIR HFA inhalasjonsaerosol skal ikke brukes med beholderen fra andre inhalasjonsaerosolprodukter. PROAIR HFA inhalasjonsaerosolbeholderen skal ikke brukes med aktuatoren fra andre inhalasjonsaerosolprodukter.
PROAIR HFA-inhalatoren har en doseteller festet til aktuatoren. Pasienter bør aldri prøve å endre tallene for dosetelleren eller tukle med pinnemekanismen inne i aktuatoren. Kast PROAIR HFA-inhalatoren når telleren viser 0 eller etter utløpsdatoen på produktet, avhengig av hva som kommer først. Den merkede mengden medikamenter i hver aktivering kan ikke garanteres etter at telleren viser 0, selv om beholderen ikke er helt tom og vil fortsette å fungere. Senk aldri beholderen i vann for å finne ut hvor full beholderen er ("flyttest").
PROAIR HFA Innånding Aerosol inneholder ikke klorfluorkarboner (KFK) som drivmiddel.
Produsert av: Teva Respiratory, LLC, Frazer, PA 19355. Produsert av: IVAX Pharmaceuticals Ireland Waterford, Irland. Revidert: februar 2019
BIVIRKNINGER
Bruk av PROAIR HFA kan være assosiert med følgende:
- . Paradoksal bronkospasme [se ADVARSLER OG FORHOLDSREGLER ] . Kardiovaskulære effekter [se ADVARSLER OG FORHOLDSREGLER ] . Umiddelbare overfølsomhetsreaksjoner [se ADVARSLER OG FORHOLDSREGLER ] . Hypokalemi [se ADVARSLER OG FORHOLDSREGLER ]
Erfaring fra kliniske forsøk
Totalt 1090 forsøkspersoner ble behandlet med PROAIR HFA inhalasjonsaerosol, eller med samme formulering av albuterol som i PROAIR HFA inhalasjonsaerosol, under det verdensomspennende kliniske utviklingsprogrammet.
Fordi kliniske studier utføres under vidt forskjellige forhold, kan bivirkningsrater observert i kliniske studier av et medikament ikke sammenlignes direkte med rater i kliniske studier av et annet medikament og gjenspeiler kanskje ikke hyppighetene observert i praksis.
Voksen og ungdom 12 år og eldre
Bivirkningsinformasjonen presentert i tabellen nedenfor angående PROAIR HFA inhalasjonsaerosol er avledet fra en 6-ukers, blind studie som sammenlignet PROAIR HFA inhalasjonsaerosol (180 mcg fire ganger daglig) med en dobbeltblind matchet placebo HFA-inhalasjonsaerosol og en evaluator-blindet markedsført aktiv komparator HFA-134a albuterol inhalator hos 172 astmatiske pasienter i alderen 12 til 76 år. Tabellen viser forekomsten av alle uønskede hendelser (enten de vurderes av etterforskerens medikamentrelaterte eller ikke-relaterte medikamenter) fra denne studien som skjedde med en hastighet på 3 % eller høyere i PROAIR HFA-inhalasjonsaerosol-behandlingsgruppen og hyppigere i PROAIR HFA Inhalasjon Aerosolbehandlingsgruppe enn i den matchede placebogruppen. Samlet sett var forekomsten og arten av bivirkningene rapportert for PROAIR HFA inhalasjonsaerosol og den markedsførte aktive komparatoren HFA-134a albuterol inhalatoren sammenlignbar.
Forekomster av uønskede opplevelser (% av pasientene) i en seks-ukers klinisk studie*
Bivirkninger rapportert av mindre enn 3 % av pasientene som fikk PROAIR HFA inhalasjonsaerosol, men av en større andel av PROAIR HFA inhalasjonsaerosolpasienter enn de matchede placebopasientene, som har potensial til å være relatert til PROAIR HFA inhalasjonsaerosol, inkluderte brystsmerter, infeksjon, diaré, glossitt, utilsiktet skade (nervesystemet), angst, dyspné, øresykdommer, øresmerter og urinveisinfeksjon.
I studier med små kumulative doser var tremor, nervøsitet og hodepine de hyppigst forekommende bivirkningene.
Pediatriske pasienter i alderen 4 til 11 år
Bivirkninger rapportert i en 3-ukers pediatrisk klinisk studie som sammenlignet den samme formuleringen av albuterol som i PROAIR HFA inhalasjonsaerosol (180 mcg albuterol fire ganger daglig) med en matchende placebo HFA inhalasjonsaerosol forekom med lav forekomst (ikke mer enn 2 % i den aktive behandlingsgruppen) og var lik de som ble sett i studier for voksne og ungdom.
Postmarketing-erfaring
Følgende bivirkninger er identifisert under bruk av PROAIR HFA etter godkjenning. Fordi disse reaksjonene rapporteres frivillig fra en populasjon av usikker størrelse, er det ikke alltid mulig å pålitelig estimere frekvensen deres eller etablere en årsakssammenheng med legemiddeleksponering. Rapporter har inkludert sjeldne tilfeller av forverret bronkospasme, manglende effekt, astmaforverring (rapportert dødelig i ett tilfelle), muskelkramper og ulike orofaryngeale bivirkninger som halsirritasjon, endret smak, glossitt, tungesår og knebling.
Følgende bivirkninger er observert ved bruk av inhalert albuterol etter godkjenning: urticaria, angioødem, utslett, bronkospasme, heshet, orofaryngealt ødem og arytmier (inkludert atrieflimmer, supraventrikulær takykardi, ekstrasystoler). I tillegg kan albuterol, som andre sympatomimetiske midler, forårsake bivirkninger som: angina, hypertensjon eller hypotensjon, hjertebank, sentralnervesystemstimulering, søvnløshet, hodepine, nervøsitet, skjelving, muskelkramper, uttørking eller irritasjon av orofarynx, hypokalemi, hyperglykemi og metabolsk acidose.
NARKOTIKAHANDEL
Andre korttidsvirkende sympatomimetiske bronkodilatatorer i aerosol bør ikke brukes samtidig med PROAIR HFA inhalasjonsaerosol. Hvis ytterligere adrenerge legemidler skal administreres på en hvilken som helst måte, bør de brukes med forsiktighet for å unngå skadelige kardiovaskulære effekter.
Betablokkere
Beta-adrenerge reseptorblokkere blokkerer ikke bare lungeeffekten til beta-agonister, slik som PROAIR HFA inhalasjonsaerosol, men kan gi alvorlig bronkospasme hos astmatiske pasienter. Pasienter med astma bør derfor normalt ikke behandles med betablokkere. Under visse omstendigheter, f.eks. som profylakse etter hjerteinfarkt, kan det imidlertid ikke være akseptable alternativer til bruk av beta-adrenerge blokkerende midler hos pasienter med astma. I denne innstillingen bør du vurdere kardioselektive betablokkere, selv om de bør administreres med forsiktighet.
Diuretika
EKG-endringene og/eller hypokalemi som kan oppstå ved administrering av ikke-kaliumsparende diuretika (som loop- eller tiaziddiuretika) kan forverres akutt av beta-agonister, spesielt når den anbefalte dosen av beta-agonisten overskrides. Selv om den kliniske betydningen av disse effektene ikke er kjent, anbefales forsiktighet ved samtidig administrering av beta-agonister og ikke-kaliumsparende diuretika. Vurder å overvåke kaliumnivåer.
Digoksin
Gjennomsnittlig reduksjon på 16 % og 22 % i serumdigoksinnivåer ble vist etter intravenøs enkeltdose og oral administrering av albuterol til normale frivillige som hadde fått digoksin i 10 dager. Den kliniske betydningen av disse funnene for pasienter med obstruktiv luftveissykdom som får albuterol og digoksin på kronisk basis er uklar. Ikke desto mindre vil det være klokt å nøye evaluere serumdigoksinnivåene hos pasienter som for tiden får digoksin og PROAIR HFA inhalasjonsaerosol.
Monoaminoksidasehemmere eller trisykliske antidepressiva
PROAIR HFA Inhalasjon Aerosol bør administreres med ekstrem forsiktighet til pasienter som behandles med monoaminoksidasehemmere eller trisykliske antidepressiva, eller innen 2 uker etter seponering av slike midler, fordi virkningen av albuterol på det kardiovaskulære systemet kan potenseres. Vurder alternativ behandling hos pasienter som tar MAO-hemmere eller trisykliske antidepressiva.
ADVARSLER
Inkludert som en del av FORHOLDSREGLER seksjon.
FORHOLDSREGLER
Paradoksal bronkospasme
PROAIR HFA Inhalering Aerosol kan produsere paradoksale bronkospasmer som kan være livstruende. Hvis paradoksal bronkospasme oppstår, bør PROAIR HFA inhalasjonsaerosol seponeres umiddelbart og alternativ behandling settes i gang. Det bør erkjennes at paradoksal bronkospasme, når assosiert med inhalerte formuleringer, ofte oppstår ved første gangs bruk av en ny beholder.
Forverring av astma
Astma kan forverres akutt over en periode på timer eller kronisk over flere dager eller lenger. Hvis pasienten trenger flere doser PROAIR HFA inhalasjonsaerosol enn vanlig, kan dette være en markør for destabilisering av astma og krever revurdering av pasienten og behandlingsregimet, med spesiell vurdering av det mulige behovet for antiinflammatorisk behandling, f.eks. kortikosteroider.
Bruk av antiinflammatoriske midler
Bruk av beta-adrenerge agonister bronkodilatatorer alene er kanskje ikke tilstrekkelig for å kontrollere astma hos mange pasienter. Det bør vurderes tidlig å legge til antiinflammatoriske midler, f.eks. kortikosteroider, til det terapeutiske regimet.
Kardiovaskulære effekter
PROAIR HFA inhalasjonsaerosol, som andre beta-adrenerge agonister, kan gi klinisk signifikante kardiovaskulære effekter hos noen pasienter målt ved puls, blodtrykk og/eller symptomer. Selv om slike effekter er uvanlige etter administrering av PROAIR HFA inhalasjonsaerosol i anbefalte doser, kan det hende at legemidlet må seponeres hvis de oppstår. I tillegg er det rapportert at beta-agonister produserer EKG-endringer, som utflating av T-bølgen, forlengelse av QTc-intervallet og ST-segmentdepresjon. Den kliniske betydningen av disse funnene er ukjent. Derfor bør PROAIR HFA inhalasjonsaerosol, som alle sympatomimetiske aminer, brukes med forsiktighet hos pasienter med kardiovaskulære lidelser, spesielt koronar insuffisiens, hjertearytmier og hypertensjon.
Ikke overskrid anbefalt dose
Dødsfall er rapportert i forbindelse med overdreven bruk av inhalerte sympatomimetika hos pasienter med astma. Den eksakte dødsårsaken er ukjent, men det er mistanke om hjertestans etter en uventet utvikling av en alvorlig akutt astmatisk krise og påfølgende hypoksi.
Umiddelbare overfølsomhetsreaksjoner
Umiddelbare overfølsomhetsreaksjoner kan oppstå etter administrering av albuterolsulfat, som vist ved sjeldne tilfeller av urticaria, angioødem, utslett, bronkospasme, anafylaksi og orofaryngealt ødem. Potensialet for overfølsomhet må vurderes i den kliniske evalueringen av pasienter som opplever umiddelbare overfølsomhetsreaksjoner mens de får PROAIR HFA inhalasjonsaerosol.
Sameksisterende forhold
PROAIR HFA inhalasjonsaerosol, som alle sympatomimetiske aminer, bør brukes med forsiktighet hos pasienter med kardiovaskulære lidelser, spesielt koronar insuffisiens, hjertearytmier og hypertensjon; hos pasienter med konvulsive lidelser, hypertyreose eller diabetes mellitus; og hos pasienter som er uvanlig responsive på sympatomimetiske aminer. Klinisk signifikante endringer i systolisk og diastolisk blodtrykk har blitt sett hos individuelle pasienter og kan forventes å oppstå hos noen pasienter etter bruk av beta-adrenerge bronkodilatatorer. Store doser av intravenøs albuterol er rapportert å forverre eksisterende diabetes mellitus og ketoacidose.
Hypokalemi
Som med andre beta-agonister, kan PROAIR HFA inhalasjonsaerosol gi betydelig hypokalemi hos noen pasienter, muligens gjennom intracellulær shunting, som har potensial til å gi uønskede kardiovaskulære effekter. Nedgangen er vanligvis forbigående og krever ikke tilskudd.
Informasjon om pasientveiledning
Se FDA-godkjent pasientmerking
Pasienter bør gis følgende informasjon:
Bruksfrekvens
Virkningen av PROAIR HFA inhalasjonsaerosol skal vare i 4 til 6 timer. Ikke bruk PROAIR HFA inhalasjonsaerosol oftere enn anbefalt. Instruer pasienter om å ikke øke dosen eller frekvensen av doser av PROAIR HFA inhalasjonsaerosol uten å konsultere legen. Hvis pasienter opplever at behandling med PROAIR HFA inhalasjonsaerosol blir mindre effektiv for symptomatisk lindring, symptomene blir verre og/eller de trenger å bruke produktet oftere enn vanlig, bør de oppsøke lege umiddelbart.
Grunning og rengjøring
Grunning
Priming er avgjørende for å sikre passende albuterolinnhold i hver aktivering. Instruer pasienter om å prime inhalatoren før bruk for første gang og i tilfeller der inhalatoren ikke har vært brukt på mer enn 2 uker ved å slippe tre sprayer ut i luften, vekk fra ansiktet.
Rengjøring
For å sikre riktig dosering og forhindre blokkering av aktuatoråpningen, instruer pasientene om å vaske det røde plastaktuatormunnstykket og tørke grundig minst en gang i uken. Instruer pasienter om at hvis de har mer enn én PROAIR HFA-inhalator, bør de vaske hver av dem til forskjellige tider for å unngå å feste feil beholder til feil plastaktuator. På denne måten kan de være sikre på at de alltid vil vite riktig antall gjenværende doser. Pasienter bør instrueres om å aldri feste en beholder med medisin fra noen annen inhalator til PROAIR HFA-aktuatoren og aldri feste PROAIR HFA-beholderen til en aktuator fra noen annen inhalator. Pasienter bør ikke fjerne beholderen fra aktuatoren unntatt under rengjøring fordi gjenfesting kan frigjøre en dose i luften og dosetelleren vil telle ned hver gang en spray slippes ut. Detaljerte rengjøringsinstruksjoner er inkludert i den illustrerte informasjonen til pasientvedlegget.
Doseteller
Pasienter bør informeres om at PROAIR HFA har en doseteller festet til aktuatoren. Når pasienten mottar inhalatoren, vil en svart prikk vises i visningsvinduet til den har blitt primet 3 ganger, hvoretter tallet 200 vises. Dosetelleren vil telle ned hver gang en spray slippes ut. Dosetellervinduet viser antall spray som er igjen i inhalatoren i enheter på to (f.eks. 200, 198, 196 osv.). Når telleren viser 20, vil fargen på tallene endres til rød for å minne pasienten på å kontakte apoteket for å få påfyll av medisiner eller konsultere legen sin for å få resept. Når dosetelleren når 0, endres bakgrunnen til konstant rød. Pasienter bør informeres om å kaste PROAIR HFA-inhalatoren når dosetelleren viser 0 eller etter utløpsdatoen på produktet, avhengig av hva som kommer først.
Paradoksal bronkospasme
Informer pasienter om at PROAIR HFA inhalasjonsaerosol kan gi paradoksal bronkospasme. Instruer pasienter om å seponere PROAIR HFA inhalasjonsaerosol hvis paradoksal bronkospasme oppstår.
Samtidig legemiddelbruk
Mens pasienter tar PROAIR HFA inhalasjonsaerosol, bør andre inhalasjonsmedisiner og astmamedisiner kun tas som anvist av en lege.
Vanlige uønskede hendelser
Vanlige bivirkninger av behandling med inhalert albuterol inkluderer hjertebank, brystsmerter, rask hjertefrekvens, skjelving eller nervøsitet.
Svangerskap
Pasienter som er gravide eller ammer bør kontakte legen sin om bruk av PROAIR HFA inhalasjonsaerosol.
Det er et graviditetseksponeringsregister som overvåker graviditetsutfall hos kvinner som er utsatt for astmamedisiner under graviditet [se Bruk i spesifikke populasjoner ].
Generell informasjon om bruk
Effektiv og sikker bruk av PROAIR HFA inhalasjonsaerosol inkluderer en forståelse av måten den skal administreres på.
Rist godt før hver spray.
Bruk PROAIR HFA inhalasjonsaerosol kun med aktuatoren som følger med produktet. Kast PROAIR HFA-inhalatoren når dosetelleren viser 0 eller etter utløpsdatoen på produktet, avhengig av hva som kommer først. Senk aldri beholderen i vann for å finne ut hvor full beholderen er ("flyttest").
Generelt er teknikken for å administrere PROAIR HFA inhalasjonsaerosol til barn lik den for voksne. Barn bør bruke PROAIR HFA inhalasjonsaerosol under tilsyn av voksne, som instruert av pasientens lege.
FDA-godkjent pasientmerking
Se avrivning illustrert Informasjon til pasienten brosjyre.
Ikke-klinisk toksikologi
Karsinogenese, mutagenese, svekkelse av fruktbarhet
en 2-årig studie på Sprague-Dawley-rotter forårsaket albuterolsulfat en doserelatert økning i forekomsten av benigne leiomyomer i mesovarium ved og over diettdoser på 2 mg/kg (omtrent 15 ganger og 6 ganger maksimalt anbefalt menneskelig daglig inhalasjonsdose (MRHDID) for henholdsvis voksne og barn, på mg/m² basis). I en annen studie ble denne effekten blokkert av samtidig administrering av propranolol, en ikke-selektiv beta-adrenerg antagonist. I en 18-måneders studie på CD-1-mus, viste albuterolsulfat ingen tegn på tumorigenisitet ved diettdoser på opptil 500 mg/kg (omtrent 1900 ganger og 740 ganger MRHDID for henholdsvis voksne og barn på en mg/m²) basis). I en 22-måneders studie i gylne hamstere, viste albuterolsulfat ingen tegn på tumorgenisitet ved diettdoser på opptil 50 mg/kg (omtrent 250 ganger og 100 ganger MRHDID for henholdsvis voksne og barn, på mg/m²-basis) .
Albuterolsulfat var ikke mutagent i Ames-testen eller en mutasjonstest i gjær. Albuterolsulfat var ikke klastogent i en human perifer lymfocyttanalyse eller i en AH1-stamme mikronukleusanalyse.
Reproduksjonsstudier på rotter viste ingen tegn på nedsatt fertilitet ved orale doser opp til 50 mg/kg (omtrent 380 ganger MRHDID for voksne på mg/m²-basis).
Bruk i spesifikke populasjoner
Svangerskap
Eksponeringsregister for graviditet
Det er et graviditetseksponeringsregister som overvåker graviditetsutfall hos kvinner som er utsatt for astmamedisiner under graviditet. For mer informasjon, kontakt Mothers To Baby Pregnancy Studies utført av Organisation of Teratology Information Specialists på 1-877-311-8972 eller besøk http://mothertobaby.org/pregnancystudies/.
Risikosammendrag
Det er ingen randomiserte kliniske studier av bruk av albuterol under graviditet. Tilgjengelige data fra publiserte epidemiologiske studier og kasusrapporter etter markedsføring av graviditetsutfall etter bruk av inhalert albuterol viser ikke konsekvent en risiko for alvorlige fødselsskader eller spontanabort. Det er kliniske hensyn ved bruk av albuterol hos gravide kvinner [se Kliniske betraktninger ]. I dyrereproduksjonsstudier, når albuterolsulfat ble administrert subkutant til gravide mus, var det tegn på ganespalte ved mindre enn og opptil 9 ganger den maksimale anbefalte daglige inhalasjonsdosen for mennesker (MRHDID) [se Data ].
Estimert bakgrunnsrisiko for alvorlige fødselsskader og spontanabort for den eller de angitte populasjonene er ukjent. I den generelle befolkningen i USA er den estimerte risikoen for alvorlige fødselsskader og spontanabort i klinisk anerkjente svangerskap henholdsvis 2 til 4 % og 15 til 20 %.
Kliniske betraktninger
Sykdomsassosiert mors- og/eller embryo-/fosterrisiko
Hos kvinner med dårlig eller moderat kontrollert astma er det økt risiko for svangerskapsforgiftning hos mor og prematuritet, lav fødselsvekt og liten for svangerskapsalderen hos nyfødt. Gravide kvinner bør overvåkes nøye og medisinen justeres etter behov for å opprettholde optimal kontroll.
Arbeid eller levering
På grunn av potensialet for beta-agonistinterferens med uterin kontraktilitet, bør bruk av PROAIR HFA inhalasjonsaerosol for lindring av bronkospasme under fødsel begrenses til de pasientene hvor fordelene klart oppveier risikoen. PROAIR HFA inhalasjonsaerosol er ikke godkjent for behandling av for tidlig fødsel. Alvorlige bivirkninger, inkludert lungeødem, er rapportert under eller etter behandling av prematur fødsel med beta2-agonister, inkludert albuterol.
Data
Dyredata
en reproduksjonsstudie med mus ga subkutant administrert albuterolsulfat dannelse av ganespalte hos 5 av 111 (4,5 %) fostre ved en eksponering på ni tideler av MRHDID for voksne (på mg/m² basis ved en maternell dose på 0,25 mg/kg) ) og hos 10 av 108 (9,3 %) fostre med omtrent 9 ganger MRHDID (på mg/m² basis ved en maternell dose på 2,5 mg/kg). Lignende effekter ble ikke observert ved omtrent en ellevtedel av MRHDID for voksne (på mg/m² basis ved en maternell dose på 0,025 mg/kg). Ganespalte forekom også hos 22 av 72 (30,5 %) fostre fra kvinner som ble behandlet subkutant med isoproterenol (positiv kontroll).
I en reproduksjonsstudie med kanin induserte oralt administrert albuterolsulfat kranioschise hos 7 av 19 fostre (37 %) ved omtrent 750 ganger MRHDID (på mg/m² basis ved en maternell dose på 50 mg/kg).
en reproduksjonsstudie av rotter ga en albuterolsulfat/HFA-134a-formulering administrert ved inhalasjon ingen teratogene effekter ved eksponeringer på omtrent 80 ganger MRHDID (på mg/m² basis ved en maternal dose på 10,5 mg/kg).
En studie der gravide rotter ble doseret med radiomerket albuterolsulfat viste at medikamentrelatert materiale overføres fra mors sirkulasjon til fosteret.
Amming
Risikosammendrag
Det er ingen tilgjengelige data om tilstedeværelsen av albuterol i morsmelk, effekten på barnet som ammes, eller effekten på melkeproduksjonen. Imidlertid er plasmanivåer av albuterol etter inhalerte terapeutiske doser lave hos mennesker, og hvis det finnes i morsmelk, har albuterol lav oral biotilgjengelighet [se KLINISK FARMAKOLOGI ].
De utviklingsmessige og helsemessige fordelene ved amming bør vurderes sammen med morens kliniske behov for albuterol og eventuelle skadelige effekter på det ammede barnet fra albuterol eller fra den underliggende mors tilstand.
Pediatrisk bruk
Sikkerheten og effektiviteten til PROAIR HFA inhalasjonsaerosol for behandling eller forebygging av bronkospasme hos barn 12 år og eldre med reversibel obstruktiv luftveissykdom er basert på en 6-ukers klinisk studie med 116 pasienter 12 år og eldre med astma sammenlignet doser på 180 mcg fire ganger daglig med placebo, og en enkeltdose crossover-studie som sammenlignet doser på 90, 180 og 270 mcg med placebo hos 58 pasienter [se Kliniske studier ]. Sikkerheten og effektiviteten til PROAIR HFA inhalasjonsaerosol for behandling av anstrengelsesutløst bronkospasme hos barn 12 år og eldre er basert på én enkeltdose-crossover-studie hos 24 voksne og ungdom med anstrengelsesutløst bronkospasme som sammenlignet doser på 180 mikrogram med placebo [se Kliniske studier ].
Sikkerheten til PROAIR HFA inhalasjonsaerosol hos barn i alderen 4 til 11 år er basert på en 3-ukers klinisk studie med 50 pasienter i alderen 4 til 11 år med astma ved bruk av samme formulering av albuterol som i PROAIR HFA inhalasjonsaerosol som sammenligner doser av 180 mcg fire ganger daglig med placebo. Effektiviteten av PROAIR HFA inhalasjonsaerosol hos barn i alderen 4 til 11 år er ekstrapolert fra kliniske studier hos pasienter 12 år og eldre med astma og anstrengelsesutløst bronkospasme, basert på data fra en enkeltdosestudie som sammenligner den bronkodilaterende effekten av PROAIR HFA 90 mcg og 180 mcg med placebo hos 55 pasienter med astma og en 3-ukers klinisk studie med samme formulering av albuterol som i PROAIR HFA inhalasjonsaerosol hos 95 astmatiske barn 4 til 11 år, sammenlignet en dose på 180 mcg albuterol fire ganger daglig med placebo [se Kliniske studier ].
Sikkerheten og effektiviteten til PROAIR HFA inhalasjonsaerosol hos pediatriske pasienter under 4 år har ikke blitt fastslått.
Geriatrisk bruk
Kliniske studier av PROAIR HFA inhalasjonsaerosol inkluderte ikke tilstrekkelig antall pasienter i alderen 65 år og over til å avgjøre om de responderer annerledes enn yngre pasienter. Annen rapportert klinisk erfaring har ikke identifisert forskjeller i respons mellom eldre og yngre pasienter. Generelt bør dosevalg for en eldre pasient være forsiktig, vanligvis med start i den lave enden av doseringsområdet, noe som gjenspeiler den høyere frekvensen av nedsatt lever-, nyre- eller hjertefunksjon, og samtidig sykdom eller annen medikamentell behandling [se ADVARSLER OG FORHOLDSREGLER ].
Alle beta2-adrenerge agonister, inkludert albuterol, er kjent for å bli vesentlig utskilt av nyrene, og risikoen for toksiske reaksjoner kan være større hos pasienter med nedsatt nyrefunksjon. Fordi eldre pasienter har større sannsynlighet for å ha nedsatt nyrefunksjon, bør det utvises forsiktighet ved dosevalg, og det kan være nyttig å overvåke nyrefunksjonen.
OVERDOSE
De forventede symptomene ved overdosering er overdreven betaadrenerg stimulering og/eller forekomst eller overdrivelse av noen av symptomene oppført under BIVIRKNINGER, f.eks. anfall, angina, hypertensjon eller hypotensjon, takykardi med hastigheter på opptil 200 slag per minutt, arytmier, nervøsitet , hodepine, skjelving, munntørrhet, hjertebank, kvalme, svimmelhet, tretthet, ubehag og søvnløshet.
Hypokalemi kan også forekomme. Som med alle sympatomimetiske medisiner, kan hjertestans og til og med død være assosiert med misbruk av PROAIR HFA inhalasjonsaerosol.
Behandlingen består av seponering av PROAIR HFA inhalasjonsaerosol sammen med passende symptomatisk behandling. En fornuftig bruk av en kardioselektiv beta-reseptorblokker kan vurderes, med tanke på at slik medisin kan gi bronkospasme. Det er utilstrekkelig bevis for å avgjøre om dialyse er fordelaktig for overdosering av PROAIR HFA inhalasjonsaerosol.
Den orale dødelige dosen av albuterolsulfat hos mus er større enn 2000 mg/kg (omtrent 6800 ganger den maksimale anbefalte daglige inhalasjonsdosen for voksne på mg/m²-basis og omtrent 3200 ganger den maksimale anbefalte daglige inhalasjonsdosen for barn på en mg /m² basis). Hos modne rotter er den subkutane median dødelige dosen av albuterolsulfat omtrent 450 mg/kg (omtrent 3000 ganger den maksimale anbefalte daglige inhalasjonsdosen for voksne på mg/m² basis og omtrent 1400 ganger den maksimale anbefalte daglige inhalasjonsdosen for barn på en mg/m² basis). Hos unge rotter er den subkutane median dødelige dosen omtrent 2 000 mg/kg (omtrent 14 000 ganger maksimal anbefalt daglig inhalasjonsdose for voksne på mg/m²-basis og omtrent 6 400 ganger maksimal anbefalt daglig inhalasjonsdose for barn på en mg/m² basis). Median dødelig dose ved inhalasjon er ikke bestemt hos dyr.
KONTRAINDIKASJONER
PROAIR HFA inhalasjonsaerosol er kontraindisert hos pasienter med en historie med overfølsomhet overfor albuterol og andre PROAIR HFA inhalasjonsaerosolkomponenter. Sjeldne tilfeller av overfølsomhetsreaksjoner, inkludert urticaria, angioødem og utslett er rapportert etter bruk av albuterolsulfat [se ADVARSLER OG FORHOLDSREGLER ].
KLINISK FARMAKOLOGI
Virkningsmekanismen
Albuterolsulfat er en beta 2-adrenerg agonist. De farmakologiske effektene av albuterolsulfat kan tilskrives aktivering av beta 2-adrenerge reseptorer på glatt muskulatur i luftveiene. Aktivering av beta2-adrenerge reseptorer fører til aktivering av adenylcyklase og til en økning i den intracellulære konsentrasjonen av syklisk-3', 5'-adenosinmonofosfat (syklisk AMP). Denne økningen av syklisk AMP er assosiert med aktiveringen av proteinkinase A, som igjen hemmer fosforyleringen av myosin og senker intracellulære ioniske kalsiumkonsentrasjoner, noe som resulterer i muskelavslapning. Albuterol slapper av den glatte muskulaturen i alle luftveier, fra luftrøret til de terminale bronkiolene. Albuterol fungerer som en funksjonell antagonist for å slappe av luftveiene uavhengig av spasmogenet som er involvert, og beskytter dermed mot alle bronkokonstriktorutfordringer. Økte sykliske AMP-konsentrasjoner er også assosiert med hemming av frigjøring av mediatorer fra mastceller i luftveiene. Selv om det er anerkjent at beta2adrenerge reseptorer er de dominerende reseptorene på bronkial glatt muskulatur, indikerer data at det er betareseptorer i det menneskelige hjertet, hvorav 10 % til 50 % er hjertebeta2-adrenerge reseptorer. Den nøyaktige funksjonen til disse reseptorene er ikke fastslått [se ADVARSLER OG FORHOLDSREGLER ].
Albuterol har vist seg i de fleste kontrollerte kliniske studier å ha mer effekt på luftveiene, i form av bronkial glattmuskelavslapning, enn isoproterenol ved sammenlignbare doser samtidig som det gir færre kardiovaskulære effekter. Imidlertid kan inhalert albuterol, som andre beta-adrenerge agonister, gi en betydelig kardiovaskulær effekt hos noen pasienter, målt ved pulsfrekvens, blodtrykk, symptomer og/eller elektrokardiografiske endringer [se ADVARSLER OG FORHOLDSREGLER ].
Farmakokinetikk
De systemiske nivåene av albuterol er lave etter inhalering av anbefalte doser. I en crossover-studie utført på friske mannlige og kvinnelige frivillige, ga høye kumulative doser av PROAIR HFA inhalasjonsaerosol (1080 mcg albuterolbase administrert over en time) gjennomsnittlig maksimal plasmakonsentrasjon (Cmax) og systemisk eksponering (AUCinf) på omtrent 4100 pg/ mL og 28.426 pg/mL*time, sammenlignet med henholdsvis ca. 3.900 pg/mL og 28.395 pg/mL*time, etter samme dose av en aktiv HFA-134a albuterol inhalator komparator. Den terminale plasmahalveringstiden for albuterol levert av PROAIR HFA inhalasjonsaerosol var ca. 6 timer. Sammenligning av farmakokinetiske parametere viste ingen forskjeller mellom produktene.
Den farmakokinetiske profilen til PROAIR HFA inhalasjonsaerosol ble evaluert i en toveis cross-over-studie med 11 friske pediatriske frivillige i alderen 4 til 11 år. En enkeltdoseadministrasjon av PROAIR HFA inhalasjonsaerosol (180 mcg albuterolbase) ga et minste kvadratmiddel (SE) Cmax og AUC0-∞ på henholdsvis 1100 (1,18) pg/mL og 5120 (1,15) pg/mL*time. Den minste kvadratiske gjennomsnittlige (SE) terminale plasmahalveringstiden for albuterol levert av PROAIR HFA inhalasjonsaerosol var 166 (7,8) minutter.
Metabolisme og eliminering
Informasjon tilgjengelig i den publiserte litteraturen tyder på at det primære enzymet som er ansvarlig for metabolismen av albuterol hos mennesker er SULTIA3 (sulfotransferase). Når racemisk albuterol ble administrert enten intravenøst eller via inhalasjon etter oral kulladministrasjon, var det en 3- til 4 ganger forskjell i området under konsentrasjon-tidskurvene mellom (R)- og (S)albuterol-enantiomerene, med (S) )-albuterolkonsentrasjoner er konsekvent høyere. Uten forbehandling med kull, etter enten oral eller inhalasjonsadministrering, var forskjellene 8 til 24 ganger, noe som tyder på at (R)-albuterol fortrinnsvis metaboliseres i mage-tarmkanalen, antagelig av SULTIA3.
Den primære eliminasjonsveien for albuterol er gjennom nyreutskillelse (80 % til 100 %) av enten moderforbindelsen eller den primære metabolitten. Mindre enn 20 % av stoffet påvises i avføringen. Etter intravenøs administrering av racemisk albuterol ble mellom 25 % og 46 % av (R)-albuterolfraksjonen av dosen utskilt som uendret (R)-albuterol i urinen.
Geriatrisk, pediatrisk, nedsatt lever/nyrefunksjon
Ingen farmakokinetiske studier for PROAIR HFA inhalasjonsaerosol er utført hos nyfødte eller eldre personer.
Effekten av nedsatt leverfunksjon på farmakokinetikken til PROAIR HFA inhalasjonsaerosol har ikke blitt evaluert.
Effekten av nedsatt nyrefunksjon på farmakokinetikken til albuterol ble evaluert hos 5 personer med kreatininclearance på 7 til 53 ml/min, og resultatene ble sammenlignet med resultatene fra friske frivillige. Nyresykdom hadde ingen effekt på halveringstiden, men det var en 67 % reduksjon i albuterolclearance. Forsiktighet bør utvises ved administrering av høye doser PROAIR HFA inhalasjonsaerosol til pasienter med nedsatt nyrefunksjon [se Bruk i spesifikke populasjoner ].
Dyretoksikologi og/eller farmakologi
Preklinisk
Intravenøse studier på rotter med albuterolsulfat har vist at albuterol krysser blod-hjerne-barrieren og når hjernekonsentrasjoner som utgjør omtrent 5 % av plasmakonsentrasjonene. I strukturer utenfor blod-hjerne-barrieren (pineal- og hypofysen) ble albuterolkonsentrasjonen funnet å være 100 ganger høyere enn i hele hjernen.
Studier på laboratoriedyr (minigriser, gnagere og hunder) har vist forekomsten av hjertearytmier og plutselig død (med histologiske tegn på myokardnekrose) når β-agonister og metylxantiner ble administrert samtidig. Den kliniske betydningen av disse funnene er ukjent.
Drivmiddel HFA-134a er uten farmakologisk aktivitet bortsett fra ved svært høye doser hos dyr (380-1300 ganger den maksimale humane eksponeringen basert på sammenligninger av AUC-verdier), og produserer primært ataksi, skjelvinger, dyspné eller spyttutslipp. Disse ligner på effekter produsert av de strukturelt beslektede klorfluorkarbonene (KFK), som har blitt mye brukt i inhalatorer med oppmålte doser.
Hos dyr og mennesker ble drivmiddel HFA-134a funnet å bli raskt absorbert og raskt eliminert, med en eliminasjonshalveringstid på 3-27 minutter hos dyr og 5-7 minutter hos mennesker. Tid til maksimal plasmakonsentrasjon (Tmax) og gjennomsnittlig oppholdstid er begge ekstremt korte, noe som fører til et forbigående utseende av HFA-134a i blodet uten tegn på akkumulering.
Kliniske studier
Bronkospasme assosiert med astma
Voksne og ungdomspasienter 12 år og eldre
I en 6-ukers, randomisert, dobbeltblind, placebokontrollert studie ble PROAIR HFA inhalasjonsaerosol (58 pasienter) sammenlignet med en matchet placebo HFA inhalasjonsaerosol (58 pasienter) hos astmatiske pasienter 12 til 76 år i en dose på 180 mcg albuterol fire ganger daglig. En evaluator-blind markedsført aktiv komparator HFA-134a albuterol inhalatorarm (56 pasienter) ble inkludert.
Serielle FEV1-målinger, vist nedenfor som prosent endring fra testdagens baseline på dag 1 og på dag 43, viste at to inhalasjoner av PROAIR HFA inhalasjonsaerosol ga signifikant større forbedring i FEV1 i forhold til førbehandlingsverdien enn den matchede placeboen, samt en sammenlignbar bronkodilaterende effekt med den markedsførte aktive komparatoren HFA-134a albuterol inhalator.
FEV1 som gjennomsnittlig prosentvis endring fra testdag før dose i en 6-ukers klinisk prøvedag 1
PASIENTINFORMASJON
PROAIR® HFA (pro' ar) (albuterolsulfat) Innånding Aerosol
Les denne pasientinformasjonen før du begynner å bruke PROAIR HFA og hver gang du får påfyll. Det kan komme ny informasjon. Denne informasjonen erstatter ikke å snakke med legen din om din medisinske tilstand eller din behandling.
Hva er PROAIR HFA?
PROAIR HFA er en reseptbelagt medisin som brukes til personer 4 år og eldre for å:
- . behandle eller forebygge bronkospasme hos personer som har reversibel obstruktiv luftveissykdom . forhindre treningsindusert bronkospasme
Det er ikke kjent om PROAIR HFA er trygt og effektivt hos barn under 4 år.
Hvem bør ikke bruke PROAIR HFA?
Ikke bruk PROAIR HFA hvis du er allergisk mot albuterolsulfat eller noen av ingrediensene i PROAIR HFA. Se slutten av dette pakningsvedlegget for en fullstendig liste over ingredienser i PROAIR HFA.
Hva bør jeg fortelle legen min før jeg bruker PROAIR HFA?
Før du bruker PROAIR HFA, fortell legen din dersom du:
- . har hjerteproblemer . har høyt blodtrykk (hypertensjon) . har kramper (anfall) . har problemer med skjoldbruskkjertelen . har diabetes . har lave kaliumnivåer i blodet . er gravid eller planlegger å bli gravid. Det er ikke kjent om PROAIR HFA vil skade det ufødte barnet ditt. Snakk med legen din dersom du er gravid eller planlegger å bli gravid. . ammer eller planlegger å amme. Det er ikke kjent om PROAIR HFA går over i morsmelk. Snakk med legen din om den beste måten å mate babyen din på hvis du bruker PROAIR HFA.
Fortell legen din om alle medisinene du tar, inkludert reseptbelagte og reseptfrie medisiner, vitaminer og urtetilskudd.
PROAIR HFA og andre medisiner kan påvirke hverandre og forårsake bivirkninger. PROAIR HFA kan påvirke måten andre medisiner virker på, og andre medisiner kan påvirke måten PROAIR HFA virker.
Fortell legen din spesielt hvis du tar:
- . andre inhalasjonsmedisiner eller astmamedisiner . betablokkermedisiner . diuretika . digoksin . monoaminoksidasehemmere . trisykliske antidepressiva
Spør legen din eller apoteket om en liste over disse legemidlene hvis du er usikker.
Kjenn til medisinene du tar. Hold en liste over dem for å vise legen din og apoteket når du får en ny medisin.
Hvordan bør jeg bruke PROAIR HFA?
- . For detaljerte instruksjoner, se "Instruksjoner for bruk" på slutten av denne pasientinformasjonen. . Bruk PROAIR HFA nøyaktig slik legen din sier at du skal bruke det. . Hvis barnet ditt trenger å bruke PROAIR HFA, følg barnet nøye for å sikre at barnet bruker inhalatoren riktig. Legen din vil vise deg hvordan barnet ditt bør bruke PROAIR HFA. . Hver dose PROAIR HFA bør vare opptil 4 timer til 6 timer. . Ikke øke dosen eller ta ekstra doser PROAIR HFA uten først å snakke med legen din. . Få medisinsk hjelp med en gang hvis PROAIR HFA ikke lenger hjelper på symptomene dine. . Få medisinsk hjelp med en gang hvis symptomene dine blir verre eller hvis du trenger å bruke inhalatoren oftere. . Mens du bruker PROAIR HFA, ikke bruk andre inhalerte redningsmedisiner og astmamedisiner med mindre legen din ber deg gjøre det. . Ring legen din hvis astmasymptomene dine som hvesing og pusteproblemer blir verre i løpet av noen timer eller dager. Legen din må kanskje gi deg et annet legemiddel (for eksempel kortikosteroider) for å behandle symptomene dine.
Hva er de mulige bivirkningene av PROAIR HFA?
PROAIR HFA kan forårsake alvorlige bivirkninger, inkludert:
- . forverrede pusteproblemer, hoste og hvesing (paradoksal bronkospasme). Hvis dette skjer, slutt å bruke PROAIR HFA og ring legen din eller få akutthjelp umiddelbart. Det er mer sannsynlig at paradoksal bronkospasme oppstår ved første gangs bruk av en ny beholder med medisin. . hjerteproblemer inkludert raskere hjertefrekvens og høyere blodtrykk . mulig død hos personer med astma som bruker for mye PROAIR HFA . allergiske reaksjoner. Ring legen din med en gang hvis du har følgende symptomer på en allergisk reaksjon:
- . kløende hud . hevelse under huden eller i halsen . utslett . forverrede pusteproblemer
De vanligste bivirkningene av PROAIR HFA inkluderer:
- . hjertet ditt føles som om det banker eller banker (hjertebank) . brystsmerter . rask puls . skjelving . nervøsitet . hodepine . svimmelhet . sår hals . rennende nese
Fortell legen din dersom du har noen bivirkninger som plager deg eller som ikke går over.
Dette er ikke alle de mulige bivirkningene av PROAIR HFA. Spør legen din eller apoteket for mer informasjon.
Ring legen din for medisinsk råd om bivirkninger. Du kan rapportere bivirkninger til FDA på 1-800-FDA-1088.
Hvordan bør jeg oppbevare PROAIR HFA?
- . Oppbevar PROAIR HFA ved romtemperatur mellom 59 ° F og 77 ° F (15 ° C og 25 ° C). . Unngå eksponering for ekstrem varme og kulde. . Rist PROAIR HFA-beholderen godt før bruk. . Ikke punktere PROAIR HFA-beholderen. . Ikke oppbevar PROAIR HFA-beholderen nær varme eller en flamme. Temperaturer over 120 ° F kan føre til at beholderen sprekker. . Ikke kast PROAIR HFA-beholderen inn i et bål eller en forbrenningsovn. . Unngå å spraye PROAIR HFA i øynene.
Oppbevar PROAIR HFA og alle legemidler utilgjengelig for barn.
Generell informasjon om sikker og effektiv bruk av PROAIR HFA
Medisiner er noen ganger foreskrevet for andre formål enn de som er oppført i en medisinveiledning. Ikke bruk PROAIR HFA for en tilstand det ikke er foreskrevet for. Ikke gi PROAIR HFA til andre mennesker, selv om de har de samme symptomene som du har. Det kan skade dem.
Denne pasientinformasjonen oppsummerer den viktigste informasjonen om PROAIR HFA. Hvis du vil ha mer informasjon, snakk med legen din. Du kan spørre apoteket eller legen om informasjon om PROAIR HFA som er skrevet for helsepersonell.
For mer informasjon, gå til www.ProAirHFA.com eller ring 1-888-482-9522.
Hva er ingrediensene i PROAIR HFA?
Aktiv ingrediens: albuterolsulfat
Inaktive ingredienser: drivmiddel HFA-134a og etanol.
Instruksjoner for bruk
PROAIR® HFA (pro' ar) (albuterolsulfat) Innånding Aerosol
Les denne bruksanvisningen før du begynner å bruke PROAIR HFA og hver gang du får påfyll. Det kan komme ny informasjon. Denne informasjonen erstatter ikke å snakke med legen din om din medisinske tilstand eller din behandling.
Delene til PROAIR HFA-inhalatoren:
Det er 2 hoveddeler av PROAIR HFA-inhalatoren, inkludert en:
- . rød plastaktuator som sprayer medisinen fra beholderen. Se figur A. . beskyttende støvhette som dekker munnstykket til aktuatoren. Se figur A.
Det er også en metallbeholder som inneholder medisinen. Se figur A.
Det er også en doseteller festet på baksiden av aktuatoren med et visningsvindu som viser deg hvor mange sprayer med medisin du har igjen. Se figur B.
Du vil se en svart prikk i visningsvinduet på aktuatoren inntil enheten har blitt primet 3 ganger. Se figur B og "Priming av PROAIR HFA-enheten" nedenfor.
Figur A og Figur B 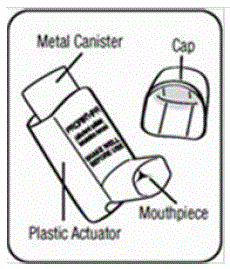
- . Ikke bruk PROAIR HFA-aktuatoren med en beholder med medisin fra en hvilken som helst annen inhalator. . Ikke bruk en PROAIR HFA-beholder med en aktuator fra en hvilken som helst annen inhalator, inkludert en annen PROAIR HFA-inhalator.
Klargjøring av PROAIR HFA-enheten:
PROAIR-enheten din må primes før du bruker den for første gang, eller hvis enheten ikke har vært brukt i mer enn 14 dager på rad. Ikke fyll PROAIR HFA-enheten din hver dag.
- . Ta PROAIR HFA-enheten ut av pakken. . Fjern den beskyttende støvhetten fra munnstykket. . Rist inhalatoren godt, og spray den ut i luften vekk fra ansiktet ditt. Se figur C.
Figur C 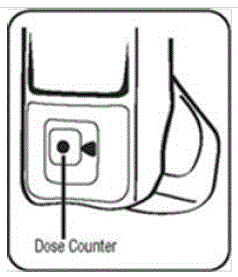
- . Rist og spray inhalatoren slik 2 ganger til for å fullføre grunningen. Dosetelleren på aktuatoren skal vise tallet 200 etter at du fyller aktuatoren for første gang. Se figur D.
Figur D 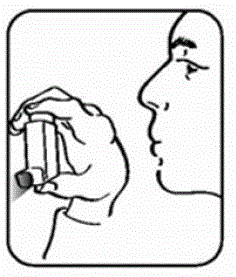
Hver gang du bruker PROAIR HFA-enheten:
- . Sørg for at beholderen passer godt inn i plastaktuatoren. . Se inn i munnstykket for å sikre at det ikke er fremmedlegemer der, spesielt hvis hetten ikke har blitt brukt til å dekke munnstykket.
Lese dosetelleren på PROAIR HFA-aktuatoren
- . Dosetelleren vil telle ned hver gang en spray slippes ut. Dosetellervinduet viser antall spray som er igjen i inhalatoren i enheter på 2 sprayer. For eksempel er det 190 sprayer igjen hvis pilen er nøyaktig motsatt tallet 190, eller 189 sprayer igjen hvis pilen peker mellom 190 og 188. Se figur D. . Når dosetelleren når 0, vil den fortsette å vise 0, og du bør bytte ut PROAIR HFA-enheten. . Dosetelleren kan ikke tilbakestilles og er permanent festet til aktuatoren. Endre aldri tallene for dosetelleren eller berør pinnen inne i aktuatoren. . Ikke fjern beholderen fra plastaktuatoren unntatt under rengjøring. Å feste beholderen til aktuatoren igjen kan ved et uhell slippe ut en dose PROAIR HFA i luften. Dosetelleren vil telle ned hver gang en spray slippes ut.
Bruke din PROAIR HFA-enhet:
Trinn 1. Rist inhalatoren godt før hver spray. Ta hetten av munnstykket til aktuatoren.
Trinn 2. Hold inhalatoren med munnstykket nede. Se figur E.
Figur E 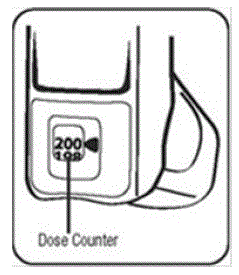
Trinn 3. Pust ut gjennom munnen og skyv så mye luft fra lungene du kan. Sett munnstykket i munnen og lukk leppene rundt det. Se figur F.
Trinn 4. Skyv toppen av beholderen helt ned mens du puster dypt og sakte inn gjennom munnen. Se figur F.
Figur F 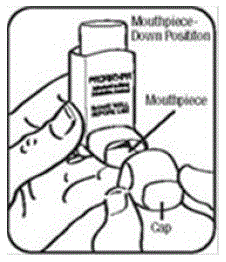
Trinn 5. Rett etter at sprayen kommer ut, ta fingeren av beholderen. Etter at du har pustet helt inn, ta inhalatoren ut av munnen og lukk munnen.
Trinn 6. Hold pusten så lenge du kan, opptil 10 sekunder, pust deretter normalt.
Hvis legen din har fortalt deg å bruke flere sprayer, vent 1 minutt og rist inhalatoren igjen. Gjenta trinn 2 til trinn 6.
Trinn 7. Sett hetten tilbake på munnstykket hver gang du bruker inhalatoren. Pass på at hetten klikker godt på plass.
Rengjøring av PROAIR HFA-enheten:
Det er svært viktig å holde plastaktuatoren ren slik at medisinen ikke bygger seg opp og blokkerer sprayen. Se figur G og figur H.
Figur G og Figur H 
- . Ikke prøv å rengjøre metallbeholderen eller la den bli våt. Inhalatoren kan slutte å spraye hvis den ikke rengjøres på riktig måte. . Hvis du har mer enn 1 PROAIR HFA-inhalator, vask hver enhet til forskjellige tider for å unngå å sette feil beholder sammen med feil plastaktuator. På denne måten kan du være sikker på at du alltid vil vite riktig antall gjenværende doser av PROAIR HFA. . Vask aktuatoren minst 1 gang hver uke som følger:
- . Ta beholderen ut av aktuatoren, og ta hetten av munnstykket. . Hold aktuatoren under kranen og kjør varmt vann gjennom den i ca. 30 sekunder. Se figur I.
Figur I 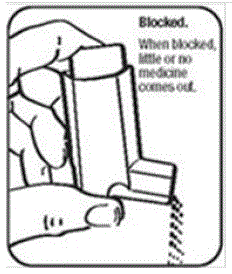
- . Snu aktuatoren opp ned og kjør varmt vann gjennom munnstykket i ca. 30 sekunder. Se figur J.
Figur J 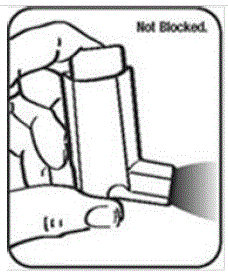
- . Rist av så mye vann fra aktuatoren som mulig. Se inn i munnstykket for å forsikre deg om at eventuell opphopning av medisin er helt vasket bort. Hvis det er opphopning, gjenta vaskeanvisningen. . La aktuatoren lufttørke helt, for eksempel over natten. Se figur K.
Figur K 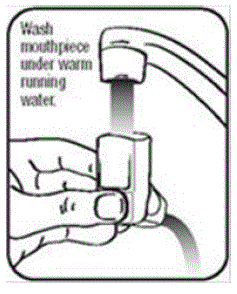
- . Når aktuatoren er tørr, setter du beholderen i aktuatoren og kontrollerer at den sitter godt. Rist inhalatoren godt og spray den to ganger ut i luften vekk fra ansiktet ditt. Sett hetten tilbake på munnstykket.
Hvis du trenger å bruke inhalatoren før aktuatoren er helt tørr:
- . Rist så mye vann av aktuatoren som mulig. . Sett beholderen i aktuatoren og sørg for at den sitter godt. . Rist inhalatoren godt og spray den to ganger ut i luften vekk fra ansiktet ditt. . Ta din PROAIR HFA-dose som foreskrevet. . Følg rengjøringsinstruksjonene ovenfor.
Bytte ut din PROAIR HFA-enhet
- . Når dosetelleren på aktuatoren sier tallet 20, fargen på tallene vil endres til rød. De røde tallene er for å minne deg på å fylle på resept eller be legen din om en annen resept for PROAIR HFA. Når dosetelleren når 0, vil bakgrunnsfargen endres til konstant rød. . Kast PROAIR HFA-inhalatoren så snart dosetelleren sier 0 eller etter utløpsdatoen på PROAIR HFA-emballasjen, avhengig av hva som kommer først. Du bør ikke fortsette å bruke inhalatoren etter 200 spray, selv om beholderen kanskje ikke er helt tom. Du kan ikke være sikker på at du får noen medisin etter å ha brukt 200 sprayer. . Ikke bruk inhalatoren etter utløpsdatoen på PROAIR HFA-emballasjen.
Denne pasientinformasjonen og bruksanvisningen er godkjent av US Food and Drug Administration.
