Reglan 10mg Metoclopramide Bruk, bivirkninger og dosering. Pris i nettapotek. Generisk medisin uten resept.
Hva er Reglan 10mg og hvordan brukes det?
Reglan 10mg er et reseptbelagt legemiddel som brukes til å behandle symptomer på gastroøsofageal reflukssykdom (GERD), kvalme og oppkast forårsaket av kjemoterapi, diabetisk gastroparese og under røntgen av den øvre mage-tarmkanalen. Reglan 10mg kan brukes alene eller sammen med andre medisiner.
Reglan 10mg tilhører en klasse legemidler kalt antiemetiske midler; Prokinetiske midler.
Hva er de mulige bivirkningene av Reglan 10mg?
Reglan kan forårsake alvorlige bivirkninger, inkludert:
- . skjelvinger eller risting i armer eller ben, . forvirring, . depresjon, . tanker om selvmord eller å skade deg selv, . langsomme eller rykende muskelbevegelser i ansiktet ditt, . kramper (anfall), . angst, . opphisselse, . nervøs følelse, . problemer med å holde seg i ro, . søvnproblemer (søvnløshet), . opphovning, . kortpustethet, . rask vektøkning, . veldig stive eller stive muskler, . høy feber, . svette, . forvirring, . raske eller ujevne hjerteslag, og . svimmelhet
Få medisinsk hjelp med en gang hvis du har noen av symptomene nevnt ovenfor.
De vanligste bivirkningene av Reglan 10mg inkluderer:
- . rastløshet, . døsighet, . lite energi, . kvalme, . oppkast, . hodepine, . forvirring, og . søvnproblemer (søvnløshet)
Fortell legen dersom du har noen bivirkninger som plager deg eller som ikke går over.
Dette er ikke alle mulige bivirkninger av Reglan. Spør legen din eller apoteket for mer informasjon.
Ring legen din for medisinsk råd om bivirkninger. Du kan rapportere bivirkninger til FDA på 1-800-FDA-1088.
ADVARSEL
TARDIV DYSKINESIA
Behandling med metoklopramid kan forårsake tardiv dyskinesi, en alvorlig bevegelsesforstyrrelse som ofte er irreversibel. Risikoen for å utvikle tardiv dyskinesi øker med behandlingens varighet og total kumulativ dose.
Behandling med metoklopramid bør seponeres hos pasienter som utvikler tegn eller symptomer på tardiv dyskinesi. Det er ingen kjent behandling for tardiv dyskinesi. Hos noen pasienter kan symptomene avta eller forsvinne etter at metoklopramidbehandling er stoppet.
Behandling med metoklopramid i mer enn 12 uker bør unngås i alle unntatt sjeldne tilfeller der terapeutiske fordeler antas å oppveie risikoen for å utvikle tardiv dyskinesi.
Se ADVARSLER
BESKRIVELSE
For oral administrering er reglan®-tabletter (metoklopramidtabletter, USP) 10 mg hvite, kapselformede tabletter med delestrek, merket med "REGLAN" på den ene siden og "ANI 10" på motsatt side.
Hver tablett inneholder:
Metoklopramidbase 10 mg (som monohydrokloridmonohydrat)
Inaktive ingredienser
Magnesiumstearat, mannitol, mikrokrystallinsk cellulose, stearinsyre.
reglan® tabletter (metoklopramid tabletter, USP) 5 mg er grønne, elliptiske tabletter merket med “REGLAN” over “5” på den ene siden og “ANI” på motsatt side.
Hver tablett inneholder:
Metoklopramidbase 5 mg (som monohydrokloridmonohydrat)
Inaktive ingredienser
Maisstivelse, D&C Yellow 10 Aluminium Lake, FD&C Blue 1 Aluminium Lake, Laktose, Mikrokrystallinsk Cellulose, Silisiumdioksid, Stearinsyre.
Metoklopramidhydroklorid er et hvitt krystallinsk, luktfritt stoff, fritt løselig i vann. Kjemisk er det 4-amino-5-klor-N-[2-(dietylamino)etyl]-2-metoksybenzamidmonohydrokloridmonohydrat. Dens molekylformel er C14H22ClN3O2 • HCl • H2O. Dens molekylvekt er 354,3.
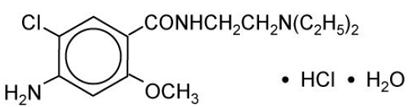
INDIKASJONER
Bruk av reglan® tabletter anbefales kun for voksne. Behandlingen bør ikke overstige 12 uker.
Symptomatisk gastroøsofageal refluks
reglan® tabletter er indisert som korttidsbehandling (4 til 12 uker) for voksne med symptomatisk, dokumentert gastroøsofageal refluks som ikke responderer på konvensjonell behandling.
Den viktigste effekten av metoklopramid er på symptomer på halsbrann etter måltid og dagtid med mindre observert effekt på nattlige symptomer. Hvis symptomene er begrenset til spesielle situasjoner, som etter kveldsmåltidet, bør bruk av metoklopramid som enkeltdoser før den provoserende situasjonen vurderes, i stedet for å bruke stoffet hele dagen. Tilheling av esophageal ulcera og erosjoner er påvist endoskopisk ved slutten av en 12-ukers studie med doser på 15 mg qid Siden det ikke er dokumentert sammenheng mellom symptomer og tilheling av esophageal lesjoner, bør pasienter med dokumenterte lesjoner overvåkes endoskopisk.
Diabetisk gastroparese (diabetisk gastrisk stasis)
reglan® tabletter (metoklopramid tabletter, USP) er indisert for lindring av symptomer assosiert med akutt og tilbakevendende diabetisk gastrisk stase. De vanlige manifestasjonene av forsinket gastrisk tømming (f.eks. kvalme, oppkast, halsbrann, vedvarende fylde etter måltider og anoreksi) ser ut til å reagere på reglan® innen forskjellige tidsintervaller. Betydelig lindring av kvalme oppstår tidlig og fortsetter å forbedre seg over en treukers periode. Lindring av oppkast og anoreksi kan gå før lindring av abdominal fylde med en uke eller mer.
DOSERING OG ADMINISTRASJON
Behandling med reglan® tabletter bør ikke vare mer enn 12 uker.
For lindring av symptomatisk gastroøsofageal refluks
Administrer fra 10 mg til 15 mg reglan® (metoklopramidhydroklorid, USP) oralt opptil qid 30 minutter før hvert måltid og ved sengetid, avhengig av symptomene som behandles og klinisk respons (se KLINISK FARMAKOLOGI og INDIKASJONER OG BRUK ). Hvis symptomene bare oppstår intermitterende eller til bestemte tider på dagen, kan bruk av metoklopramid i enkeltdoser på opptil 20 mg før den provoserende situasjonen foretrekkes fremfor kontinuerlig behandling. Noen ganger vil pasienter (som eldre pasienter) som er mer følsomme for de terapeutiske eller uønskede effektene av metoklopramid, bare trenge 5 mg per dose.
Erfaring med esophageal erosjoner og ulcerasjoner er begrenset, men tilheling har så langt blitt dokumentert i en kontrollert studie med qid-terapi ved 15 mg/dose, og dette regimet bør brukes når lesjoner er tilstede, så lenge det tolereres (se BIVIRKNINGER ). På grunn av den dårlige korrelasjonen mellom symptomer og endoskopisk utseende av spiserøret, er terapi rettet mot spiserørslesjoner best veiledet av endoskopisk evaluering.
Behandling over 12 uker er ikke evaluert og kan ikke anbefales.
For lindring av symptomene Som assosiert med diabetisk gastropares er (diabetisk gas tric stas er) Administrer 10 mg metoklopramid 30 minutter før hvert måltid og ved sengetid i to til åtte uker, avhengig av respons og sannsynligheten for fortsatt velvære ved seponering av medikamentet.
Den første administrasjonsveien bør bestemmes av alvorlighetsgraden av symptomene. Hvis bare de tidligste manifestasjonene av diabetisk gastrisk stase er tilstede, kan oral administrering av reglan® startes. Men hvis alvorlige symptomer er tilstede, bør behandlingen begynne med metoklopramidinjeksjon (se merking av injeksjonen før parenteral administrering startes).
Administrering av metoklopramid-injeksjon i opptil 10 dager kan være nødvendig før symptomene avtar, da oral administrering kan settes i gang. Siden diabetisk gastrisk stase er ofte tilbakevendende, bør reglan®-behandling gjenopptas ved tidligste manifestasjon.
Bruk hos pasienter med nedsatt nyre- eller leverfunksjon
Siden metoklopramid hovedsakelig skilles ut gjennom nyrene, bør behandlingen startes med omtrent halvparten av den anbefalte dosen hos pasienter med kreatininclearance under 40 ml/min. Avhengig av klinisk effekt og sikkerhetshensyn, kan dosen økes eller reduseres etter behov.
Se OVERDOSE seksjon for informasjon om dialyse.
Metoklopramid gjennomgår minimal levermetabolisme, bortsett fra enkel konjugering. Trygg bruk er beskrevet hos pasienter med avansert leversykdom med normal nyrefunksjon.
HVORDAN LEVERES
Hver hvit, kapselformet reglan®-tablett med delestrek (metoklopramidtabletter, USP) inneholder 10 mg metoklopramidbase (som monohydrokloridmonohydrat). Tilgjengelig i:
Flasker med 100 tabletter ( NDC 62559-166-01)
Hver grønn, elliptisk formet reglan®-tablett (metoklopramidtabletter, USP) inneholder 5 mg metoklopramidbase (som monohydrokloridmonohydrat). Tilgjengelig i:
Flasker med 100 tabletter ( NDC 62559-165-01)
Dispenser tabletter i tett, lysbestandig beholder.
Tabletter bør oppbevares ved kontrollert romtemperatur, mellom 20°C og 25°C (68°F og 77°F).
Produsert av: ANI Pharmaceuticals, Inc. Baudette, MN 56623. Revidert: Des 2014
BIVIRKNINGER
Generelt korrelerer forekomsten av bivirkninger med dosen og varigheten av administrering av metoklopramid. Følgende reaksjoner er rapportert, selv om data i de fleste tilfeller ikke tillater et estimat av frekvens:
CNS effekter
Rastløshet, døsighet, tretthet og slapphet forekommer hos omtrent 10 % av pasientene som får den mest foreskrevne dosen på 10 mg qid (se FORHOLDSREGLER ). Søvnløshet, hodepine, forvirring, svimmelhet eller mental depresjon med selvmordstanker (se ADVARSLER forekommer sjeldnere. Forekomsten av døsighet er større ved høyere doser. Det er isolerte rapporter om krampeanfall uten en klar sammenheng med metoklopramid. Sjelden har hallusinasjoner blitt rapportert.
Ekstrapyramidale reaksjoner (EPS)
Akutte dystoniske reaksjoner, den vanligste typen EPS assosiert med metoklopramid, forekommer hos omtrent 0,2 % av pasientene (1 av 500) behandlet med 30 til 40 mg metoklopramid per dag. Symptomer inkluderer ufrivillige bevegelser av lemmer, ansiktsgrimasering, torticollis, okulogyrisk krise, rytmisk fremspring av tungen, bulbar type tale, trismus, opisthotonus (tetanuslignende reaksjoner), og sjelden, stridor og dyspné, muligens på grunn av laryngospasme; vanligvis reverseres disse symptomene lett av difenhydramin (se ADVARSLER ).
Parkinson-lignende symptomer kan omfatte bradykinesi, skjelving, tannhjulstivhet, maskelignende ansikter (se ADVARSLER ).
Tardiv dyskinesi er oftest preget av ufrivillige bevegelser av tungen, ansiktet, munnen eller kjeven, og noen ganger av ufrivillige bevegelser av stammen og/eller ekstremiteter; bevegelser kan være koreoatetiske i utseende (se ADVARSLER ).
Motorisk rastløshet (akatisi) kan bestå av følelser av angst, agitasjon, nervøsitet og søvnløshet, samt manglende evne til å sitte stille, tempo, banking med foten. Disse symptomene kan forsvinne spontant eller reagere på en dosereduksjon.
Malignt nevroleptikasyndrom
Sjeldne forekomster av malignt neuroleptisk syndrom (NMS) er rapportert. Dette potensielt dødelige syndromet består av symptomkomplekset hypertermi, endret bevissthet, muskelstivhet og autonom dysfunksjon (se ADVARSLER ).
Endokrine forstyrrelser
Galaktoré, amenoré, gynekomasti, impotens sekundært til hyperprolaktinemi (se FORHOLDSREGLER ). Væskeretensjon sekundært til forbigående økning av aldosteron (se KLINISK FARMAKOLOGI ).
Kardiovaskulær
Hypotensjon, hypertensjon, supraventrikulær takykardi, bradykardi, væskeretensjon, akutt kongestiv hjertesvikt og mulig AV-blokk (se KONTRAINDIKASJONER og FORHOLDSREGLER ).
Gastrointestinale
Kvalme og tarmforstyrrelser, primært diaré.
Hepatisk
Sjeldne tilfeller av levertoksisitet, karakterisert ved funn som gulsott og endrede leverfunksjonstester, når metoklopramid ble administrert sammen med andre legemidler med kjent levertoksisk potensial.
Nyre
Urinfrekvens og inkontinens.
Hematologisk
Noen få tilfeller av nøytropeni, leukopeni eller agranulocytose, vanligvis uten entydig sammenheng med metoklopramid. Methemoglobinemi, hos voksne og spesielt med overdosering hos nyfødte (se OVERDOSE ). Sulfhemoglobinemi hos voksne.
Allergiske reaksjoner
Noen få tilfeller av utslett, urticaria eller bronkospasme, spesielt hos pasienter med astma i anamnesen. Sjelden angioneurotisk ødem, inkludert glossalt eller larynxødem.
Diverse
Synsforstyrrelser. Porfyri.
NARKOTIKAHANDEL
Effekten av metoklopramid på gastrointestinal motilitet motvirkes av antikolinerge medisiner og narkotiske analgetika. Additive beroligende effekter kan oppstå når metoklopramid gis med alkohol, beroligende midler, hypnotika, narkotiske midler eller beroligende midler.
Funnet om at metoklopramid frigjør katekolaminer hos pasienter med essensiell hypertensjon antyder at det bør brukes med forsiktighet, om i det hele tatt, hos pasienter som får monoaminoksidasehemmere.
Absorpsjon av legemidler fra magen kan reduseres (f.eks. digoksin) av metoklopramid, mens hastigheten og/eller omfanget av absorpsjon av legemidler fra tynntarmen kan øke (f.eks. paracetamol, tetracyklin, levodopa, etanol, ciklosporin).
Gastroparese (gastrisk stase) kan være ansvarlig for dårlig diabeteskontroll hos noen pasienter. Eksogent administrert insulin kan begynne å virke før maten har forlatt magen og føre til hypoglykemi. Fordi virkningen av metoklopramid vil påvirke tilførselen av mat til tarmen og dermed absorpsjonshastigheten, kan insulindosering eller doseringstidspunkt kreve justering.
ADVARSLER
Psykisk depresjon har forekommet hos pasienter med og uten tidligere depresjonshistorie. Symptomene har variert fra milde til alvorlige og har inkludert selvmordstanker og selvmord. Metoklopramid bør kun gis til pasienter med tidligere depresjonshistorie dersom de forventede fordelene oppveier de potensielle risikoene.
Ekstrapyramidale symptomer, manifestert primært som akutte dystoniske reaksjoner, forekommer hos ca. 1 av 500 pasienter som behandles med vanlige voksne doser på 30 til 40 mg/dag av metoklopramid. Disse ses vanligvis i løpet av de første 24 til 48 timene av behandlingen med metoklopramid, forekommer hyppigere hos pediatriske pasienter og voksne pasienter under 30 år og er enda hyppigere ved høyere doser. Disse symptomene kan omfatte ufrivillige bevegelser av lemmer og ansiktsgrimasering, torticollis, okulogyrisk krise, rytmisk fremspring av tungen, bulbar type tale, trismus eller dystoniske reaksjoner som ligner tetanus. I sjeldne tilfeller kan dystoniske reaksjoner oppstå som stridor og dyspné, muligens på grunn av laryngospasme. Hvis disse symptomene skulle oppstå, injiser 50 mg difenhydraminhydroklorid intramuskulært, og de vil vanligvis avta. Benztropinmesylat, 1 til 2 mg intramuskulært, kan også brukes for å reversere disse reaksjonene.
Parkinson-lignende symptomer har oppstått, mer vanlig i løpet av de første 6 månedene etter påbegynt behandling med metoklopramid, men noen ganger etter lengre perioder. Disse symptomene avtar vanligvis innen 2 til 3 måneder etter seponering av metoklopramid. Pasienter med allerede eksisterende Parkinsons sykdom bør gis metoklopramid med forsiktighet, hvis i det hele tatt, siden slike pasienter kan oppleve forverring av parkinsonsymptomer når de tar metoklopramid.
Tardiv dyskinesi
(Se BOKS ADVARSEL)
Behandling med metoklopramid kan forårsake tardiv dyskinesi (TD), en potensielt irreversibel og skjemmende lidelse preget av ufrivillige bevegelser av ansikt, tunge eller ekstremiteter. Risikoen for å utvikle tardiv dyskinesi øker med behandlingens varighet og den totale kumulative dosen. En analyse av bruksmønstre viste at omtrent 20 % av pasientene som brukte metoklopramid tok det i mer enn 12 uker. Behandling med metoklopramid i lengre tid enn de anbefalte 12 ukene bør unngås i alle unntatt sjeldne tilfeller der terapeutiske fordeler antas å oppveie risikoen for å utvikle TD.
Selv om risikoen for å utvikle TD i den generelle befolkningen kan være økt blant eldre, kvinner og diabetikere, er det ikke mulig å forutsi hvilke pasienter som vil utvikle metoklopramid-indusert TD. Både risikoen for å utvikle TD og sannsynligheten for at TD blir irreversibel øker med behandlingsvarighet og total kumulativ dose.
Metoklopramid bør seponeres hos pasienter som utvikler tegn eller symptomer på TD. Det er ingen kjent effektiv behandling for etablerte tilfeller av TD, selv om TD hos noen pasienter kan remittere, delvis eller fullstendig, innen flere uker til måneder etter at metoklopramid er trukket tilbake.
Metoklopramid i seg selv kan undertrykke, eller delvis undertrykke, tegnene på TD, og dermed maskere den underliggende sykdomsprosessen. Effekten av denne symptomatiske undertrykkelsen på det langsiktige forløpet av TD er ukjent. Metoklopramid bør derfor ikke brukes til symptomatisk kontroll av TD.
Malignt nevroleptikasyndrom (NMS)
Det har vært sjeldne rapporter om et uvanlig, men potensielt dødelig symptomkompleks, noen ganger referert til som malignt nevroleptisk syndrom (NMS) assosiert med metoklopramid. Kliniske manifestasjoner av NMS inkluderer hypertermi, muskelstivhet, endret bevissthet og bevis på autonom ustabilitet (uregelmessig puls eller blodtrykk, takykardi, diaforese og hjertearytmier).
Den diagnostiske evalueringen av pasienter med dette syndromet er komplisert. For å komme frem til en diagnose er det viktig å identifisere tilfeller der den kliniske presentasjonen inkluderer både alvorlig medisinsk sykdom (f.eks. lungebetennelse, systemisk infeksjon, etc.) og ubehandlede eller utilstrekkelig behandlede ekstrapyramidale tegn og symptomer (EPS). Andre viktige hensyn i differensialdiagnosen inkluderer sentral antikolinergisk toksisitet, heteslag, ondartet hypertermi, medikamentfeber og primær sentralnervesystem (CNS) patologi.
Behandlingen av NMS bør omfatte 1) umiddelbar seponering av metoklopramid og andre legemidler som ikke er nødvendige for samtidig behandling, 2) intensiv symptomatisk behandling og medisinsk overvåking, og 3) behandling av eventuelle samtidige alvorlige medisinske problemer som spesifikke behandlinger er tilgjengelige for. Bromokriptin og dantrolennatrium har blitt brukt i behandling av NMS, men deres effektivitet er ikke fastslått (se BIVIRKNINGER ).
FORHOLDSREGLER
Generell
I en studie på hypertensive pasienter ble intravenøst administrert metoklopramid vist å frigjøre katekolaminer; derfor bør det utvises forsiktighet når metoklopramid brukes hos pasienter med hypertensjon.
Fordi metoklopramid gir en forbigående økning i plasmaaldosteron, kan enkelte pasienter, spesielt de med cirrhose eller kongestiv hjertesvikt, ha risiko for å utvikle væskeretensjon og volumoverbelastning. Hvis disse bivirkningene oppstår når som helst under metoklopramidbehandling, bør stoffet seponeres.
Bivirkninger, spesielt de som involverer nervesystemet, kan oppstå etter avsluttet bruk av reglan®. Et lite antall pasienter kan oppleve en abstinensperiode etter seponering av reglan® som kan omfatte svimmelhet, nervøsitet og/eller hodepine.
Informasjon til pasienter
Bruk av reglan® anbefales kun for voksne. Metoklopramid kan svekke de mentale og/eller fysiske evnene som kreves for å utføre farlige oppgaver som å betjene maskiner eller kjøre motorkjøretøy. Den ambulerende pasienten bør advares tilsvarende.
For ytterligere informasjon bør pasienter instrueres om å se Medisineringsveiledningen for reglan®-tabletter.

Karsinogenese, mutagenese, svekkelse av fruktbarhet
En 77-ukers studie ble utført på rotter med orale doser opptil ca. 40 ganger den maksimale anbefalte daglige dosen til mennesker. Metoklopramid øker prolaktinnivået og økningen vedvarer under kronisk administrering. Vevskultureksperimenter indikerer at omtrent en tredjedel av brystkreft hos mennesker er prolaktinavhengig in vitro, en faktor av potensiell betydning dersom forskrivning av metoklopramid vurderes til en pasient med tidligere påvist brystkreft. Selv om forstyrrelser som galaktoré, amenoré, gynekomasti og impotens er rapportert med prolaktinøkende legemidler, er den kliniske betydningen av forhøyede serumprolaktinnivåer ukjent for de fleste pasienter. En økning i brystneoplasmer er funnet hos gnagere etter kronisk administrering av prolaktinstimulerende nevroleptika og metoklopramid. Verken kliniske studier eller epidemiologiske studier utført til dags dato har imidlertid vist en sammenheng mellom kronisk administrering av disse legemidlene og brystsvulstdannelse; det tilgjengelige beviset er for begrenset til å være avgjørende på dette tidspunktet.
En Ames mutagenitetstest utført på metoklopramid var negativ.
Graviditetskategori B
Reproduksjonsstudier utført på rotter, mus og kaniner ved IV, IM, SC og oral vei ved maksimale nivåer fra 12 til 250 ganger human dose, har ikke vist noen svekkelse av fertilitet eller betydelig skade på fosteret på grunn av metoklopramid. Det finnes imidlertid ingen tilstrekkelige og godt kontrollerte studier på gravide kvinner. Fordi reproduksjonsstudier på dyr ikke alltid er prediktive for menneskelig respons, bør dette legemidlet kun brukes under graviditet hvis det er klart nødvendig.
Ammende mødre
Metoklopramid skilles ut i morsmelk. Forsiktighet bør utvises når metoklopramid gis til en ammende mor.
Pediatrisk bruk
Sikkerhet og effektivitet hos pediatriske pasienter er ikke fastslått (se OVERDOSE ).
Forsiktighet bør utvises ved administrering av metoklopramid til nyfødte siden forlenget clearance kan gi for høye serumkonsentrasjoner (se KLINISK FARMAKOLOGI - Farmakokinetikk ). I tillegg har nyfødte reduserte nivåer av NADH-cytokrom b5-reduktase som, i kombinasjon med de nevnte farmakokinetiske faktorene, gjør nyfødte mer utsatt for methemoglobinemi (se OVERDOSE ).
Sikkerhetsprofilen til metoklopramid hos voksne kan ikke ekstrapoleres til pediatriske pasienter. Dystonier og andre ekstrapyramidale reaksjoner assosiert med metoklopramid er mer vanlig i den pediatriske befolkningen enn hos voksne. (Se ADVARSLER og BIVIRKNINGER - Ekstrapyramidale reaksjoner. )
Geriatrisk bruk
Kliniske studier av reglan® inkluderte ikke tilstrekkelig antall forsøkspersoner i alderen 65 år og over til å avgjøre om eldre forsøkspersoner responderer annerledes enn yngre forsøkspersoner.
Risikoen for å utvikle parkinsonlignende bivirkninger øker med stigende dose. Geriatriske pasienter bør få den laveste dosen av reglan® som er effektiv. Hvis parkinson-lignende symptomer utvikles hos en geriatrisk pasient som får reglan®, bør reglan® vanligvis seponeres før du starter noen spesifikke anti-parkinsonmidler (se ADVARSLER og DOSERING OG ADMINISTRASJON – For lindring av symptomatisk gastroes ophageal refluks ).
Eldre kan ha større risiko for tardiv dyskinesi (se ADVARSLER – Tardiv dys kinesia ).
Sedasjon er rapportert hos reglan®-brukere. Sedasjon kan forårsake forvirring og manifestere seg som oversedasjon hos eldre (se KLINISK FARMAKOLOGI , FORHOLDSREGLER – Informasjon til pasienter og BIVIRKNINGER – CNS-effekter ).
reglan® er kjent for å utskilles vesentlig av nyrene, og risikoen for toksiske reaksjoner på dette legemidlet kan være større hos pasienter med nedsatt nyrefunksjon (se DOSERING OG ADMINISTRASJON – Bruk hos pasienter med nedsatt nyre- eller leverfunksjon ).
Av disse grunner bør dosevalg for en eldre pasient være forsiktig, vanligvis med start i den lave enden av doseringsområdet, noe som gjenspeiler den høyere frekvensen av nedsatt nyrefunksjon, samtidig sykdom eller annen medikamentell behandling hos eldre (se DOSERING OG ADMINISTRASJON – For lindring av symptomatisk gastroøsofageal refluks og bruk hos pasienter med nedsatt nyre- eller leverfunksjon ).
Andre spesielle populasjoner
Pasienter med NADH-cytokrom b5-reduktasemangel har økt risiko for å utvikle methemoglobinemi og/eller sulfhemoglobinemi når metoklopramid administreres. Hos pasienter med G6PD-mangel som opplever metoklopramidindusert methemoglobinemi, anbefales ikke behandling med metylenblått (se OVERDOSE ).
OVERDOSE
Symptomer på overdosering kan omfatte døsighet, desorientering og ekstrapyramidale reaksjoner. Antikolinerge eller antiparkinsonmedisiner eller antihistaminer med antikolinerge egenskaper kan være nyttige for å kontrollere de ekstrapyramidale reaksjonene. Symptomene er selvbegrensende og forsvinner vanligvis innen 24 timer.
Hemodialyse fjerner relativt lite metoklopramid, sannsynligvis på grunn av den lille mengden av stoffet i blodet i forhold til vev. På samme måte fjerner ikke kontinuerlig ambulatorisk peritonealdialyse betydelige mengder medikament. Det er usannsynlig at dosen må justeres for å kompensere for tap gjennom dialyse. Dialyse vil sannsynligvis ikke være en effektiv metode for fjerning av medikamenter i overdosesituasjoner.
Utilsiktet overdosering på grunn av feiladministrasjon er rapportert hos spedbarn og barn med bruk av metoklopramid mikstur. Selv om det ikke var noe konsistent mønster i rapportene knyttet til disse overdosene, inkluderte hendelsene anfall, ekstrapyramidale reaksjoner og sløvhet.
Methemoglobinemi har forekommet hos premature og fullbårne nyfødte som ble gitt overdoser av metoklopramid (1 til 4 mg/kg/dag oralt, intramuskulært eller intravenøst i 1 til 3 eller flere dager). Methemoglobinemi kan reverseres ved intravenøs administrering av metylenblått. Imidlertid kan metylenblått forårsake hemolytisk anemi hos pasienter med G6PD-mangel, som kan være dødelig (se FORHOLDSREGLER – Andre spesielle populasjoner ).
KONTRAINDIKASJONER
Metoklopramid bør ikke brukes når stimulering av gastrointestinal motilitet kan være farlig, f.eks. ved gastrointestinal blødning, mekanisk obstruksjon eller perforering.
Metoklopramid er kontraindisert hos pasienter med feokromocytom fordi stoffet kan forårsake en hypertensiv krise, sannsynligvis på grunn av frigjøring av katekolaminer fra svulsten. Slike hypertensive kriser kan kontrolleres av fentolamin.
Metoklopramid er kontraindisert hos pasienter med kjent følsomhet eller intoleranse overfor stoffet. Metoklopramid bør ikke brukes hos epileptikere eller pasienter som får andre legemidler som sannsynligvis vil forårsake ekstrapyramidale reaksjoner, siden frekvensen og alvorlighetsgraden av anfall eller ekstrapyramidale reaksjoner kan øke.
KLINISK FARMAKOLOGI
Metoklopramid stimulerer motiliteten i den øvre mage-tarmkanalen uten å stimulere mage-, galle- eller bukspyttkjertelsekresjoner. Virkemåten er uklar. Det ser ut til å sensibilisere vev for virkningen av acetylkolin. Effekten av metoklopramid på motilitet er ikke avhengig av intakt vagal innervasjon, men den kan oppheves med antikolinerge medisiner.
Metoklopramid øker tonus og amplitude av gastriske (spesielt antrale) sammentrekninger, slapper av den pyloriske lukkemuskelen og tolvfingertarmen, og øker peristaltikken av tolvfingertarmen og jejunum, noe som resulterer i akselerert gastrisk tømming og intestinal transitt. Det øker hviletonen i den nedre esophageal sphincter. Det har liten, om noen, effekt på motiliteten til tykktarmen eller galleblæren.
Hos pasienter med gastroøsofageal refluks og lav LESP (lavere esophageal sphincter-trykk), gir enkelt orale doser av metoklopramid doserelaterte økninger i LESP. Effekten begynner ved ca. 5 mg og øker til 20 mg (den største dosen som er testet). Økningen i LESP fra en dose på 5 mg varer i ca. 45 minutter, og økningen på 20 mg varer mellom 2 og 3 timer. Økt magetømmingshastighet er observert med orale enkeltdoser på 10 mg.
De antiemetiske egenskapene til metoklopramid ser ut til å være et resultat av dets antagonisme av sentrale og perifere dopaminreseptorer. Dopamin produserer kvalme og oppkast ved stimulering av den medullære kjemoreseptorutløsersonen (CTZ), og metoklopramid blokkerer stimulering av CTZ av midler som ldopa eller apomorfin som er kjent for å øke dopaminnivået eller ha dopaminlignende effekter. Metoklopramid opphever også senkingen av magetømming forårsaket av apomorfin.
I likhet med fenotiaziner og relaterte legemidler, som også er dopaminantagonister, produserer metoklopramid sedasjon og kan gi ekstrapyramidale reaksjoner, selv om disse er relativt sjeldne (se ADVARSLER ). Metoklopramid hemmer de sentrale og perifere effektene av apomorfin, induserer frigjøring av prolaktin og forårsaker en forbigående økning i sirkulerende aldosteronnivåer, som kan være assosiert med forbigående væskeretensjon.
Begynnelsen av den farmakologiske virkningen av metoklopramid er 1 til 3 minutter etter en intravenøs dose, 10 til 15 minutter etter intramuskulær administrering og 30 til 60 minutter etter en oral dose; farmakologiske effekter vedvarer i 1 til 2 timer.
Farmakokinetikk
Metoklopramid absorberes raskt og godt. I forhold til en intravenøs dose på 20 mg er den absolutte orale biotilgjengeligheten av metoklopramid 80 % ± 15,5 %, som vist i en crossover-studie med 18 personer. Maksimal plasmakonsentrasjon oppstår ca. 1 til 2 timer etter en enkelt oral dose. Tilsvarende tid til topp er observert etter individuelle doser ved steady state.
en enkeltdosestudie med 12 forsøkspersoner øker arealet under legemiddelkonsentrasjon-tid-kurven lineært med doser fra 20 til 100 mg. Toppkonsentrasjoner øker lineært med dose; tiden til toppkonsentrasjoner forblir den samme; hele kroppens klaring er uendret; og eliminasjonsraten forblir den samme. Gjennomsnittlig eliminasjonshalveringstid hos personer med normal nyrefunksjon er 5 til 6 timer. Lineære kinetiske prosesser beskriver tilstrekkelig absorpsjon og eliminering av metoklopramid.
Omtrent 85 % av radioaktiviteten til en oral administrert dose vises i urinen innen 72 timer. Av de 85 % som elimineres i urinen, er omtrent halvparten til stede som fritt eller konjugert metoklopramid.
Legemidlet er ikke i stor grad bundet til plasmaproteiner (ca. 30%). Hele kroppsfordelingsvolumet er høyt (ca. 3,5 l/kg), noe som tyder på omfattende distribusjon av medikament til vevet.
Nedsatt nyrefunksjon påvirker clearance av metoklopramid. I en studie med pasienter med varierende grad av nedsatt nyrefunksjon, var en reduksjon i kreatininclearance korrelert med reduksjon i plasmaclearance, renal clearance, non-renal clearance og økning i eliminasjonshalveringstid. Kinetikken til metoklopramid i nærvær av nedsatt nyrefunksjon forble imidlertid lineær. Reduksjonen i clearance som følge av nedsatt nyrefunksjon antyder at vedlikeholdsdosen bør justeres ned for å unngå akkumulering av legemidler.
Farmakokinetiske data for voksne
Hos pediatriske pasienter er farmakodynamikken til metoklopramid etter oral og intravenøs administrering svært varierende og en konsentrasjon-effekt-sammenheng er ikke etablert.
Det er utilstrekkelig pålitelige data til å konkludere om farmakokinetikken til metoklopramid hos voksne og den pediatriske populasjonen er lik. Selv om det ikke er tilstrekkelige data til å støtte effekten av metoklopramid hos pediatriske pasienter med symptomatisk gastroøsofageal refluks (GER) eller kreftkjemoterapirelatert kvalme og oppkast, har dets farmakokinetikk blitt studert i disse pasientpopulasjonene.
en åpen studie fikk seks pediatriske pasienter (aldersintervall, 3,5 uker til 5,4 måneder) med GER metoklopramid 0,15 mg/kg mikstur hver 6. time i 10 doser. Den gjennomsnittlige maksimale plasmakonsentrasjonen av metoklopramid etter den tiende dosen var 2 ganger (56,8 μg/L) høyere sammenlignet med det som ble observert etter den første dosen (29 μg/L), noe som indikerte legemiddelakkumulering ved gjentatt dosering. Etter den tiende dosen var gjennomsnittlig tid for å nå toppkonsentrasjoner (2,2 timer), halveringstid (4,1 timer), clearance (0,67 l/time/kg) og distribusjonsvolum (4,4 l/kg) av metoklopramid tilsvarende som de observert etter den første dosen. Hos den yngste pasienten (alder, 3,5 uker) var halveringstiden for metoklopramid etter første og tiende dose (henholdsvis 23,1 og 10,3 timer) signifikant lengre sammenlignet med andre spedbarn på grunn av redusert clearance. Dette kan tilskrives umodne lever- og nyresystemer ved fødselen.
Enkelte intravenøse doser av metoklopramid 0,22 til 0,46 mg/kg (gjennomsnittlig 0,35 mg/kg) ble administrert over 5 minutter til 9 pediatriske kreftpasienter som fikk kjemoterapi (gjennomsnittsalder 11,7 år; område 7 til 14 år) for profylakse av cytotoksisk- indusert brekninger. Metoklopramidplasmakonsentrasjonene ekstrapolert til null varierte fra 65 til 395 μg/L (gjennomsnittlig 152 μg/L). Gjennomsnittlig eliminasjonshalveringstid, clearance og distribusjonsvolum for metoklopramid var 4,4 timer (område 1,7 til 8,3 timer), 0,56 l/t/kg (område 0,12 til 1,20 l/t/kg) og 3,0 l/t/kg kg (rekkevidde, henholdsvis 1,0 til 4,8 L/kg).
en annen studie mottok ni pediatriske kreftpasienter (aldersgruppe, 1 til 9 år) 4 til 5 intravenøse infusjoner (over 30 minutter) av metoklopramid i en dose på 2 mg/kg for å kontrollere emesis. Etter siste dose varierte de maksimale serumkonsentrasjonene av metoklopramid fra 1060 til 5680 μg/L. Gjennomsnittlig eliminasjonshalveringstid, clearance og distribusjonsvolum for metoklopramid var 4,5 timer (område, 2,0 til 12,5 timer), 0,37 l/t/kg (område, 0,10 til 1,24 l/t/kg) og 1,93 l/ kg (rekkevidde, henholdsvis 0,95 til 5,50 L/kg).
PASIENTINFORMASJON
REGLAN (REG-lan) (metoklopramid tabletter ) Tabletter
Les Medisinguiden som følger med REGLAN før du begynner å ta den og hver gang du får påfyll. Det kan komme ny informasjon. Hvis du tar et annet produkt som inneholder metoklopramid (som REGLAN 10mg injeksjon, REGLAN ODT eller metoklopramid mikstur), bør du lese medisinveiledningen som følger med det produktet. Noe av informasjonen kan være annerledes. Denne medisinveiledningen erstatter ikke å snakke med legen din om din medisinske tilstand eller din behandling.
Hva er den viktigste informasjonen jeg bør vite om REGLAN?
REGLAN kan forårsake alvorlige bivirkninger, inkludert:
Tardiv dyskinesi (unormale muskelbevegelser). Disse bevegelsene skjer hovedsakelig i ansiktsmusklene. Du kan ikke kontrollere disse bevegelsene. De forsvinner kanskje ikke selv etter å ha stoppet REGLAN. Det finnes ingen behandling for tardiv dyskinesi, men symptomene kan reduseres eller forsvinne over tid etter at du slutter å ta REGLAN.
Sjansene dine for å få tardiv dyskinesi øker:
- . jo lenger du tar REGLAN 10mg og jo mer REGLAN 10mg tar du. Du bør ikke ta REGLAN 10mg i mer enn 12 uker. . hvis du er eldre, spesielt hvis du er kvinne . hvis du har diabetes
Det er ikke mulig for legen din å vite om du vil få tardiv dyskinesi hvis du tar REGLAN.
Ring legen din med en gang hvis du får bevegelser du ikke kan stoppe eller kontrollere, for eksempel:
- . leppesmakking, tygging eller rynker i munnen . rynker eller skulende panner . stikker ut tungen . blunker og beveger øynene . risting av armer og ben
Se avsnittet "Hva er de mulige bivirkningene av REGLAN 10mg?" for mer informasjon om bivirkninger.
Hva er REGLAN 10mg?
REGLAN 10mg er en reseptbelagt medisin som brukes:
- . hos voksne i 4 til 12 uker for å lindre halsbrannsymptomer med gastroøsofageal reflukssykdom (GERD) når visse andre behandlinger ikke virker. REGLAN lindrer halsbrann på dagtid og halsbrann etter måltider. Det hjelper også sår i spiserøret å gro. . for å lindre symptomer på langsom magetømming hos personer med diabetes. REGLAN hjelper til med å behandle symptomer som kvalme, oppkast, halsbrann, metthetsfølelse lenge etter et måltid og tap av matlyst. Ikke alle disse symptomene blir bedre samtidig.
Det er ikke kjent om REGLAN er trygt og virker på barn.
Hvem bør ikke ta REGLAN 10mg?
Ikke bruk REGLAN hvis du:
- . har mage- eller tarmproblemer som kan bli verre med REGLAN, som blødning, blokkering eller rift i magen eller tarmveggen . har en svulst i binyrene kalt feokromocytom . er allergisk mot REGLAN 10mg eller noe i den. Se slutten av denne medisinveiledningen for en liste over ingredienser i REGLAN. . ta medisiner som kan forårsake ukontrollerte bevegelser, som medisiner mot psykiske lidelser har anfall
Hva bør jeg fortelle legen min før jeg tar REGLAN?
Fortell legen din om alle dine medisinske tilstander, inkludert hvis du har:
- . depresjon . Parkinsons sykdom . høyt blodtrykk . nyreproblemer. Legen din kan starte med en lavere dose. . leverproblemer eller hjertesvikt. REGLAN kan føre til at kroppen din holder på væske. . diabetes. Din insulindose må kanskje endres. . brystkreft . du er gravid eller planlegger å bli gravid. Det er ikke kjent om REGLAN 10mg vil skade det ufødte barnet ditt. . du ammer. REGLAN 10mg kan gå over i morsmelk og kan skade babyen din. Snakk med legen din om den beste måten å mate babyen din på hvis du tar REGLAN.
Fortell legen din om alle medisinene du tar, inkludert reseptbelagte og reseptfrie medisiner, vitaminer og urtetilskudd. REGLAN og noen andre legemidler kan interagere med hverandre og virker kanskje ikke like bra, eller forårsake mulige bivirkninger. Ikke start noen nye medisiner mens du tar REGLAN 10mg før du har snakket med legen din.
Fortell legen din spesielt hvis du tar:
- . et annet legemiddel som inneholder metoklopramid, for eksempel REGLAN 10mg ODT, eller metoklopramid mikstur . en blodtrykksmedisin . et legemiddel mot depresjon, spesielt en monoaminoksidasehemmer (MAOI) . insulin . en medisin som kan gjøre deg søvnig, for eksempel angstdempende medisiner, sovemedisiner og narkotika.
Spør legen din eller apoteket hvis du ikke er sikker på om medisinen din er oppført ovenfor.
Kjenn til medisinene du tar. Hold en liste over dem og vis den til legen din og apoteket når du får en ny medisin.
Hvordan skal jeg ta REGLAN?
- . REGLAN 10mg kommer som en tablett du tar gjennom munnen. . Ta REGLAN nøyaktig slik legen din har fortalt deg. Ikke endre dosen med mindre legen din forteller deg det. . Du bør ikke ta REGLAN i mer enn 12 uker. . Hvis du tar for mye REGLAN 10mg, ring legen din eller giftkontrollsenteret med en gang.
Hva bør jeg unngå mens jeg tar REGLAN?
- . Ikke drikk alkohol mens du tar REGLAN. Alkohol kan gjøre noen bivirkninger av REGLAN 10mg verre, for eksempel søvnighet. . Ikke kjør bil, arbeid med maskiner eller gjør farlige oppgaver før du vet hvordan REGLAN påvirker deg. REGLAN kan forårsake søvnighet.
Hva er de mulige bivirkningene av REGLAN?
Reglan kan forårsake alvorlige bivirkninger, inkludert:
- . Tardiv dyskinesi (unormale muskelbevegelser). Se "Hva er den viktigste informasjonen jeg trenger å vite om REGLAN?" . Ukontrollerte spasmer i ansikts- og nakkemusklene, eller muskler i kropp, armer og ben (dystoni). Disse muskelspasmene kan forårsake unormale bevegelser og kroppsstillinger. Disse spasmene starter vanligvis innen de første 2 dagene av behandlingen. Disse spasmene skjer oftere hos barn og voksne under 30 år. . Depresjon, tanker om selvmord og selvmord. Noen mennesker som tar REGLAN blir deprimerte. Du kan ha tanker om å skade eller ta livet av deg selv. Noen mennesker som tar Reglan har avsluttet sitt eget liv (selvmord). . Malignt nevroleptikasyndrom (NMS). NMS er en svært sjelden, men svært alvorlig tilstand som kan skje med Reglan. NMS kan forårsake død og må behandles på sykehus. Symptomer på NMS inkluderer: høy feber, stive muskler, problemer med å tenke, svært rask eller ujevn hjerterytme og økt svette. . Parkinsonisme. Symptomer inkluderer lett skjelving, stivhet i kroppen, problemer med å bevege seg eller holde balansen. Hvis du allerede har Parkinsons sykdom, kan symptomene dine bli verre mens du får REGLAN.
Ring legen din og få medisinsk hjelp umiddelbart hvis du:
- . føler deg deprimert eller har tanker om å skade eller begå selvmord . har høy feber, stive muskler, problemer med å tenke, svært rask eller ujevn hjerterytme og økt svette . har muskelbevegelser du ikke kan stoppe eller kontrollere . har muskelbevegelser som er nye eller uvanlige
Vanlige bivirkninger av Reglan 10mg inkluderer:
- . føler seg rastløs, trøtt, trøtt, svimmel eller utmattet . hodepine . forvirring . problemer med å sove
Du kan få flere bivirkninger jo lenger du tar REGLAN og jo mer REGLAN du tar.
Du kan fortsatt ha bivirkninger etter at du har sluttet med REGLAN. Du kan ha symptomer fra å slutte (abstinens) av REGLAN 10mg som hodepine og følelse av svimmelhet eller nervøsitet.
Fortell legen din om eventuelle bivirkninger som plager deg eller som ikke forsvinner. Dette er ikke alle mulige bivirkninger av REGLAN.
Ring legen din for medisinsk råd om bivirkninger. Du kan rapportere bivirkninger til FDA på 1-800-FDA-1088.
Hvordan skal jeg oppbevare REGLAN?
- . Oppbevar REGLAN i romtemperatur mellom 68 °F til 77 °F (20 °C til 25 °C). . Oppbevar REGLAN 10mg i flasken den kommer i. Hold flasken tett lukket.
Oppbevar REGLAN 10mg og alle legemidler utilgjengelig for barn.
Generell informasjon om REGLAN
Medisiner er noen ganger foreskrevet for andre formål enn de som er oppført i en medisinveiledning. Ikke bruk REGLAN for en tilstand det ikke er foreskrevet for. Ikke gi REGLAN 10mg til andre mennesker, selv om de har de samme symptomene som du har. Det kan skade dem.
Denne medisinguiden oppsummerer den viktigste informasjonen om REGLAN. Hvis du vil ha mer informasjon, snakk med legen din. Du kan spørre legen din eller apoteket om informasjon om REGLAN 10mg som er skrevet for helsepersonell. For mer informasjon, gå til www.anipharmaceuticals.com eller ring gratis på 1-800-308-6755.
Hva er ingrediensene i REGLAN?
Aktiv ingrediens: metoklopramid
Inaktive ingredienser:
REGLAN 10 mg tabletter: magnesiumstearat, mannitol, mikrokrystallinsk cellulose, stearinsyre
REGLAN 5 mg tabletter: maisstivelse, D&C yellow 10 aluminium lake, FD&C blue 1 aluminium lake, laktose, mikrokrystallinsk cellulose, silisiumdioksid, stearinsyre
