Anafranil 10mg, 25mg, 50mg Clomipramine Bruk, bivirkninger og dosering. Pris i nettapotek. Generisk medisin uten resept.
Hva er Anafranil 10mg og hvordan brukes det?
Anafranil 50mg er et reseptbelagt legemiddel som brukes til å behandle symptomene på tvangslidelser. Anafranil 50mg kan brukes alene eller sammen med andre medisiner.
Anafranil tilhører en klasse legemidler som kalles antidepressiva, TCA.
Det er ikke kjent om Anafranil 50mg er trygt og effektivt hos barn yngre enn 10 år.
Hva er de mulige bivirkningene av Anafranil 25mg?
Anafranil 50mg kan forårsake alvorlige bivirkninger inkludert:
- . hudutslett, . feber, . hovne kjertler, . influensalignende symptomer, . muskelsmerter, . alvorlig svakhet, . uvanlige blåmerker, . gulfarging av hud og øyne (gulsott), . atferdsendringer, . angst, . panikk anfall, . problemer med å sove, . impulsiv oppførsel, . irritabilitet, . opphisselse, . fiendtlighet, . aggressivitet, . hyperaktiv (psykisk eller fysisk), . depresjon, . selvmordstanker, . tåkesyn, . tunnelsyn, . øyesmerter eller hevelse, . ser glorier rundt lys, . rask hjertefrekvens, . skjelvinger eller skjelvinger, . forvirring, . ekstrem frykt, . smertefull eller vanskelig vannlating, . anfall, . feber, . hallusinasjoner, . svette, . skjelver, . rask puls, . muskelstivhet, . rykninger, . tap av koordinasjon, . kvalme, . oppkast, og . diaré
Få medisinsk hjelp med en gang hvis du har noen av symptomene nevnt ovenfor.
De vanligste bivirkningene av Anafranil inkluderer:
- . tørr i munnen, . kvalme, . urolig mage, . tap av Appetit, . forstoppelse, . føler angst, . svimmel, . døsighet, . trett, . søvnproblemer, . appetitt eller vektendringer, . hukommelsesproblemer, . problemer med å konsentrere seg, . økt svette, . nummenhet eller prikking, . synsforandringer, . redusert sexlyst, . impotens, og . problemer med å få orgasme
Fortell legen dersom du har noen bivirkninger som plager deg eller som ikke går over.
Dette er ikke alle mulige bivirkninger av Anafranil. Spør legen din eller apoteket for mer informasjon.
Ring legen din for medisinsk råd om bivirkninger. Du kan rapportere bivirkninger til FDA på 1-800-FDA-1088.
ADVARSEL
Suicidalitet og antidepressiva
Antidepressiva økte risikoen sammenlignet med placebo for selvmordstenkning og -adferd (suicidalitet) hos barn, ungdom og unge voksne i korttidsstudier av alvorlig depressiv lidelse (MDD) og andre psykiatriske lidelser. Alle som vurderer bruk av klomipraminhydroklorid eller andre antidepressiva hos et barn, ungdom eller ung voksen må balansere denne risikoen med det kliniske behovet. Korttidsstudier viste ikke en økning i risikoen for suicidalitet med antidepressiva sammenlignet med placebo hos voksne over 24 år; det var en reduksjon i risiko med antidepressiva sammenlignet med placebo hos voksne i alderen 65 år og eldre. Depresjon og visse andre psykiatriske lidelser er i seg selv assosiert med økt risiko for selvmord. Pasienter i alle aldre som starter på antidepressiv behandling bør overvåkes på passende måte og observeres nøye for klinisk forverring, suicidalitet eller uvanlige endringer i atferd. Familier og omsorgspersoner bør informeres om behovet for tett observasjon og kommunikasjon med forskriveren. Klomipraminhydroklorid er ikke godkjent for bruk hos pediatriske pasienter bortsett fra pasienter med obsessiv-kompulsiv lidelse (OCD) (se ADVARSLER , Klinisk forverring og selvmordsrisiko ; PASIENTINFORMASJON ; og FORHOLDSREGLER , Pediatrisk bruk ).
BESKRIVELSE
Anafranil™ (klomipraminhydroklorid) kapsler USP er et antiobsessionelt medikament som tilhører klassen (dibenzazepin) av farmakologiske midler kjent som trisykliske antidepressiva. Anafranil er tilgjengelig som kapsler på 25, 50 og 75 mg for oral administrering.
Klomipraminhydroklorid USP er 3-klor-5-[3-(dimetylamino)propyl]-10,11-dihydro5H-dibenz[b,f]azepinmonohydroklorid, og dets strukturformel er:
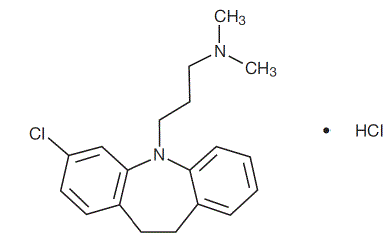
C19H23ClN2 • HCl MW = 351,31
Clomipramine hydrochloride USP er et hvitt til off-white krystallinsk pulver. Det er fritt løselig i vann, i metanol og i metylenklorid, og uløselig i etyleter og i heksan.
Inaktive ingredienser. D&C Red No. 33 (kun 25 mg kapsler), D&C Yellow No. 10, FD&C Blue No. 1 (kun 50 mg kapsler), FD&C Yellow No. 6, gelatin, magnesiumstearat, metylparaben, propylparaben, stivelse (mais), og titandioksid.
INDIKASJONER
Anafranil™ (klomipraminhydroklorid) kapsler USP er indisert for behandling av tvangstanker og tvangshandlinger hos pasienter med obsessiv-kompulsiv lidelse (OCD). Tvangstankene eller tvangshandlingene må forårsake markert plager, være tidkrevende eller i betydelig grad forstyrre sosial eller yrkesmessig funksjon, for å møte DSM-III-R (ca. 1989) diagnosen OCD.
Tvangstanker er tilbakevendende, vedvarende ideer, tanker, bilder eller impulser som er ego-dystoniske. Tvangshandlinger er repeterende, målrettet og tilsiktet atferd utført som svar på en besettelse eller på en stereotyp måte, og gjenkjennes av personen som overdreven eller urimelig.
Effektiviteten av Anafranil 25 mg for behandling av OCD ble demonstrert i multisenter, placebokontrollerte parallellgruppestudier, inkludert to 10-ukers studier på voksne og en 8-ukers studie på barn og ungdom i alderen 10 til 17 år. Pasienter i alle studiene hadde moderat til alvorlig OCD (DSM-III), med gjennomsnittlig baseline-vurdering på Yale-Brown Obsessive Compulsive Scale (YBOCS) fra 26 til 28 og en gjennomsnittlig baseline-vurdering på 10 på NIMH Clinical Global Obsessive Compulsive Scale (NIMH-OC). Pasienter som tok CMI opplevde en gjennomsnittlig reduksjon på omtrent 10 på YBOCS, noe som representerer en gjennomsnittlig forbedring på denne skalaen på 35 % til 42 % blant voksne og 37 % blant barn og ungdom. CMI-behandlede pasienter opplevde en reduksjon på 3,5 enheter på NIMH-OC. Pasienter på placebo viste ingen viktig klinisk respons på noen av skalaene. Maksimal dose var 250 mg/dag for de fleste voksne og 3 mg/kg/dag (opptil 200 mg) for alle barn og ungdom.
Effektiviteten av Anafranil 25 mg for langtidsbruk (dvs. i mer enn 10 uker) har ikke blitt systematisk evaluert i placebokontrollerte studier. Legen som velger å bruke Anafranil 10mg i lengre perioder bør med jevne mellomrom revurdere den langsiktige nytten av stoffet for den enkelte pasient (se DOSERING OG ADMINISTRASJON ).
DOSERING OG ADMINISTRASJON
Behandlingsregimene beskrevet nedenfor er basert på de som ble brukt i kontrollerte kliniske studier av Anafranil 50 mg hos 520 voksne og 91 barn og ungdom med OCD. Under initial titrering bør Anafranil gis i delte doser med måltider for å redusere gastrointestinale bivirkninger. Målet med denne innledende titreringsfasen er å minimere bivirkninger ved å la toleranse for bivirkninger utvikle seg eller gi pasienten tid til å tilpasse seg dersom toleranse ikke utvikles.
Fordi både CMI og dens aktive metabolitt, DMI, har lange eliminasjonshalveringstider, bør forskriveren ta hensyn til at steady-state plasmanivåer ikke kan oppnås før 2 til 3 uker etter doseendring (se KLINISK FARMAKOLOGI ). Etter initial titrering kan det derfor være aktuelt å vente 2 til 3 uker mellom ytterligere dosejusteringer.
Innledende behandling/dosejustering (voksne)
Behandling med Anafranil 25 mg bør startes med en dose på 25 mg daglig og gradvis økes, ettersom det tolereres, til ca. 100 mg i løpet av de første 2 ukene. Under initial titrering bør Anafranil 50 mg gis i delte doser med måltider for å redusere gastrointestinale bivirkninger. Deretter kan dosen økes gradvis i løpet av de neste ukene, opp til maksimalt 250 mg daglig. Etter titrering kan den totale daglige dosen gis én gang daglig ved sengetid for å minimere sedasjon på dagtid.
Innledende behandling/dosejustering (barn og ungdom)
Som for voksne er startdosen 25 mg daglig og bør økes gradvis (også gis i delte doser med måltider for å redusere gastrointestinale bivirkninger) i løpet av de første 2 ukene, som tolerert, opp til et daglig maksimum på 3 mg/kg eller 100 mg, avhengig av hva som er minst. Deretter kan dosen økes gradvis i løpet av de neste ukene opp til et daglig maksimum på 3 mg/kg eller 200 mg, avhengig av hva som er minst (se FORHOLDSREGLER , Pediatrisk bruk ). Som for voksne, etter titrering, kan den totale daglige dosen gis én gang daglig ved sengetid for å minimere sedasjon på dagtid.
Vedlikehold/fortsatt behandling (voksne, barn og ungdom)
Selv om det ikke er noen systematiske studier som svarer på spørsmålet om hvor lenge man skal fortsette Anafranil 10mg, er OCD en kronisk tilstand og det er rimelig å vurdere fortsettelse for en responderende pasient. Selv om effekten av Anafranil 50 mg etter 10 uker ikke er dokumentert i kontrollerte studier, har pasienter fortsatt i terapi under dobbeltblinde tilstander i opptil 1 år uten tap av nytte. Dosejusteringer bør imidlertid gjøres for å holde pasienten på den laveste effektive dosen, og pasienter bør periodisk revurderes for å fastslå behovet for behandling. Under vedlikehold kan den totale daglige dosen gis én gang daglig ved sengetid.
Bytte en pasient til eller fra en monoaminoksidasehemmer (MAOI) beregnet på å behandle psykiatriske lidelser
Det bør gå minst 14 dager mellom seponering av en MAO-hemmer beregnet på å behandle psykiatriske lidelser og oppstart av behandling med Anafranil. Omvendt bør det tillates minst 14 dager etter seponering av Anafranil før man starter en MAO-hemmer beregnet på å behandle psykiatriske lidelser (se KONTRAINDIKASJONER ).
Bruk av Anafranil 25mg med andre MAO-hemmere, som linezolid eller metylenblått
Ikke start Anafranil 50 mg hos en pasient som behandles med linezolid eller intravenøs metylenblått fordi det er økt risiko for serotonergt syndrom. Hos en pasient som trenger mer akutt behandling av en psykiatrisk tilstand, bør andre intervensjoner, inkludert sykehusinnleggelse, vurderes (se KONTRAINDIKASJONER ).
noen tilfeller kan en pasient som allerede får Anafranil 25 mg-behandling kreve akutt behandling med linezolid eller intravenøs metylenblått. Hvis akseptable alternativer til linezolid eller intravenøs behandling med metylenblått ikke er tilgjengelig og de potensielle fordelene ved behandling med linezolid eller intravenøs metylenblått vurderes å oppveie risikoen for serotonergt syndrom hos en bestemt pasient, bør Anafranil seponeres umiddelbart, og linezolid eller intravenøs metylenblått kan administreres. Pasienten bør overvåkes for symptomer på serotonergt syndrom i to uker eller inntil 24 timer etter siste dose linezolid eller intravenøs metylenblått, avhengig av hva som kommer først. Behandling med Anafranil kan gjenopptas 24 timer etter siste dose linezolid eller intravenøs metylenblått (se ADVARSLER ).
Risikoen for å administrere metylenblått på ikke-intravenøse veier (som orale tabletter eller ved lokal injeksjon) eller i intravenøse doser mye lavere enn 1 mg/kg med Anafranil 50 mg er uklar. Legen bør likevel være klar over muligheten for nye symptomer på serotonergt syndrom ved slik bruk (se ADVARSLER ).
HVORDAN LEVERES
Anafranil™ (klomipraminhydroklorid) kapsler USP
Kapsler 25 mg – elfenbensfarget kropp merket i svart med "M" og melon-gul hette merket i svart med "ANAFRANIL 25 mg"
Flasker på 30………....………...……….....……… … NDC 0406-9906-03
Kapsler 50 mg – elfenbensfarget kropp merket i svart med "M" og vannblå hette merket i svart med "ANAFRANIL 50 mg"
Flasker på 30………..………....………...………... ..…NDC 0406-9907-03
Kapsler 75 mg – elfenbenskjold merket med "M" i svart og gul hette merket i svart med "ANAFRANIL 75 mg"
Flasker på 30………..………...……….....……….. ..…NDC 0406-9908-03
Oppbevaring
Oppbevares ved 20° til 25°C (68° til 77°F) [se USP kontrollert romtemperatur ].
Dispenser i godt lukkede beholdere med barnesikret lukking. Beskytt mot fuktighet.
dyretoksikologi
Fosfolipidose og testikkelforandringer, ofte assosiert med trisykliske forbindelser, har blitt observert med Anafranil. I kroniske rottestudier besto endringer relatert til Anafranil 50 mg av systemisk fosfolipidose, endringer i testiklene (atrofi, mineralisering) og sekundære endringer i annet vev. I tillegg ble hjertetrombose og dermatitt/keratitt observert hos rotter behandlet i 2 år med doser som var henholdsvis 24 og 10 ganger den maksimale anbefalte daglige dosen for mennesker (MRHD), på mg/kg-basis, og 4 og 1,5 ganger MRHD på mg/m²-basis.
Mallinckrodt, "M"-merkemerket, Mallinckrodt Pharmaceuticals-logoen, M Â og andre merker er varemerker for et Mallinckrodt-selskap.
Produsert av: Patheon Inc., Whitby, Ontario, Canada, L1N 5Z5 for SpecGx LLC, Webster Groves, MO 63119 USA. Revidert: mars 2019
BIVIRKNINGER
Vanlig observert
De vanligst observerte bivirkningene assosiert med bruk av Anafranil 10 mg og som ikke er sett med tilsvarende forekomst blant placebo-behandlede pasienter, var gastrointestinale plager, inkludert munntørrhet, forstoppelse, kvalme, dyspepsi og anoreksi; nervesystemplager, inkludert søvnighet, skjelving, svimmelhet, nervøsitet og myoklonus; genitourinære plager, inkludert endret libido, ejakulasjonssvikt, impotens og vannlatingsforstyrrelse; og andre diverse plager, inkludert tretthet, svette, økt appetitt, vektøkning og visuelle endringer.
Fører til seponering av behandling
Omtrent 20 % av 3616 pasienter som fikk Anafranil i kliniske studier før markedsføring i USA, avbrøt behandlingen på grunn av en bivirkning. Omtrent halvparten av pasientene som sluttet (9 % av totalen) hadde flere plager, hvorav ingen kunne klassifiseres som primære. Der en primær årsak til seponering kunne identifiseres, avbrøt de fleste pasientene på grunn av nervesystemplager (5,4 %), primært somnolens. Den nest hyppigste årsaken til seponering var plager i fordøyelsessystemet (1,3 %), primært oppkast og kvalme.
Det var ingen tilsynelatende sammenheng mellom bivirkningene og forhøyede plasmakonsentrasjoner av legemidler.
Forekomst i kontrollerte kliniske studier
Følgende tabell oppregner bivirkninger som oppstod med en forekomst på 1 % eller mer blant pasienter med OCD som fikk Anafranil 10 mg i placebokontrollerte kliniske studier for voksne eller barn. Frekvensene ble hentet fra sammenslåtte data fra kliniske studier som involverte enten voksne som fikk Anafranil (N=322) eller placebo (N=319) eller barn behandlet med Anafranil (N=46) eller placebo (N=44). Forskriveren bør være klar over at disse tallene ikke kan brukes til å forutsi forekomsten av bivirkninger i løpet av vanlig medisinsk praksis, der pasientkarakteristikker og andre faktorer avviker fra de som var fremherskende i de kliniske forsøkene. Tilsvarende kan de siterte frekvensene ikke sammenlignes med tall hentet fra andre kliniske undersøkelser som involverer ulike behandlinger, bruksområder og etterforskere. De siterte tallene gir imidlertid legen et grunnlag for å estimere det relative bidraget til medikamentelle og ikke-medikamentelle faktorer til forekomsten av bivirkninger i populasjonene som ble studert.
Forekomst av behandlingsoppstått uønsket opplevelse i placebokontrollerte kliniske studier (prosentandel av pasienter som rapporterer hendelse)
Andre hendelser observert under evalueringen av Anafranil før markedsføring
Under klinisk testing i USA ble flere doser Anafranil 50 mg administrert til ca. 3600 personer. Uheldige hendelser knyttet til denne eksponeringen ble registrert av kliniske etterforskere ved å bruke terminologi etter eget valg. Følgelig er det ikke mulig å gi et meningsfullt estimat av andelen individer som opplever uønskede hendelser uten først å gruppere lignende typer uheldige hendelser i et mindre antall standardiserte hendelseskategorier.
tabellene som følger har en modifisert terminologiordbok fra Verdens helseorganisasjon blitt brukt til å klassifisere rapporterte uønskede hendelser. Frekvensene som presenteres representerer derfor andelen av de 3525 individene som ble eksponert for Anafranil som opplevde en hendelse av typen nevnt ved minst én anledning mens de fikk Anafranil. Alle hendelser er inkludert bortsett fra de som allerede er oppført i forrige tabell, de som er rapportert i termer som er så generelle at de er uinformative, og de der en assosiasjon med stoffet var fjern. Det er viktig å understreke at selv om de rapporterte hendelsene skjedde under behandling med Anafranil, var de ikke nødvendigvis forårsaket av det.
Hendelser er videre kategorisert etter kroppssystem og oppført i rekkefølge etter avtagende frekvens i henhold til følgende definisjoner: hyppige bivirkninger er de som forekommer ved en eller flere anledninger hos minst 1/100 pasienter; sjeldne bivirkninger er de som forekommer hos 1/100 til 1/1000 pasienter; sjeldne hendelser er de som forekommer hos mindre enn 1/1000 pasienter.
Kroppen som helhet - Sjelden - generelt ødem, økt mottakelighet for infeksjon, ubehag. Sjelden - avhengig ødem, abstinenssyndrom.
Sirkulasjonssystem - Sjeldne - unormalt EKG, arytmi, bradykardi, hjertestans, ekstrasystoler, blekhet. Sjeldne - aneurisme, atrieflutter, grenblokk, hjertesvikt, hjerneblødning, hjerteblokk, hjerteinfarkt, myokardiskemi, perifer iskemi, tromboflebitt, vasospasme, ventrikulær takykardi.
Fordøyelsessystemet - Sjeldne - unormal leverfunksjon, blod i avføring, kolitt, duodenitt, magesår, gastritt, gastroøsofageal refluks, gingivitt, glossitt, hemoroider, hepatitt, økt spytt, irritabel tarm, magesår, rektal blødning, sårdannelse i tungen,. Sjeldne - cheilitt, kronisk enteritt, misfarget avføring, gastrisk dilatasjon, gingival blødning, hikke, intestinal obstruksjon, oral/faryngealt ødem, paralytisk ileus, spyttkjertelforstørrelse.
Endokrine system - Sjelden - hypotyreose. Sjelden - struma, gynekomasti, hypertyreose.
Hemisk og lymfesystem - Sjelden - lymfadenopati. Sjelden - leukemoid reaksjon, lymfomlignende lidelse, margdepresjon.
Metabolsk og ernæringsforstyrrelse - Sjelden - dehydrering, diabetes mellitus, gikt, hyperkolesterolemi, hyperglykemi, hyperurikemi, hypokalemi. Sjelden - fettintoleranse, glykosuri.
Muskel- og skjelettsystemet - Sjelden - artrose. Sjeldne - dystoni, eksostose, lupus erythematosus utslett, blåmerker, myopati, myositt, polyarteritis nodosa, torticollis.
nervesystemet - Hyppig - unormal tenkning, vertigo. Sjeldne - unormal koordinering, unormal EEG, unormal gang, apati, ataksi, koma, kramper, delirium, vrangforestillinger, dyskinesi, dysfoni, encefalopati, eufori, ekstrapyramidal lidelse, hallusinasjoner, fiendtlighet, hyperkinesi, hypnagogiske hallusinasjoner, leggreaksjoner, benreaksjoner. , nevralgi, paranoia, fobisk lidelse, psykose, sanseforstyrrelser, somnambulisme, stimulering, selvmordstanker, selvmordsforsøk, tanngnissing. Sjelden - antikolinergt syndrom, afasi, apraksi, katalepsi, kolinergt syndrom, koreoatetose, generalisert spasmer, hemiparese, hyperestesi, hyperrefleksi, hypoestesi, illusjon, nedsatt impulskontroll, ubesluttsomhet, mutisme, nevromusisk krise, o nyskulisk motorisk reaksjon, oc, nyskulisk motorisk reaksjon , stupor, selvmord.
Luftveiene - Sjelden - bronkitt, hyperventilering, økt sputum, lungebetennelse. Sjelden - cyanose, hemoptyse, hypoventilasjon, laryngisme.
Hud og vedheng - Sjeldne - alopecia, cellulitt, cyste, eksem, erytematøst utslett, genital pruritus, makulopapulært utslett, lysfølsomhetsreaksjon, psoriasis, pustulært utslett, misfarging av huden. Sjeldne - kloasma, follikulitt, hypertrikose, piloereksjon, seboré, hudhypertrofi, hudsår.
Spesielle sanser - Sjelden - unormal overnatting, døvhet, diplopi, øreverk, øyesmerter, fremmedlegemefølelse, hyperakusis, parosmi, fotofobi, skleritt, smakstap. Sjeldne - blefaritt, kromatopsi, konjunktival blødning, eksoftalmos, glaukom, keratitt, labyrintforstyrrelse, nattblindhet, retinal lidelse, skjeling, synsfeltdefekt.
Urogenital system - Sjeldne - endometriose, epididymitt, hematuri, nokturi, oliguri, ovariecyste, perineal smerte, polyuri, prostatasykdom, nyresten, nyresmerter, urinrørsforstyrrelse, urininkontinens, livmorblødning, vaginal blødning. Sjeldne - albuminuri, anorgasmi, brystoverfylling, brystfibroadenose, cervikal dysplasi, endometriehyperplasi, for tidlig utløsning, pyelonefritt, pyuri, nyrecyste, livmorbetennelse, vulvalidelse.
Postmarketing-erfaring
Følgende bivirkning er rapportert under bruk av Anafranil etter godkjenning. Fordi denne reaksjonen rapporteres frivillig fra en populasjon av usikker størrelse, er det ikke alltid mulig å pålitelig estimere frekvensen.
Øyelidelser - Vinkellukkende glaukom.
Forstyrrelser i immunsystemet - Legemiddelutslett med eosinofili og systemiske symptomer (DRESS).
Metabolisme og ernæringsforstyrrelser - Hyponatremi.
Endokrine lidelser - Syndrom av upassende antidiuretisk hormonsekresjon (SIADH).
NARKOTIKAHANDEL
Risikoen ved bruk av Anafranil i kombinasjon med andre legemidler har ikke blitt systematisk evaluert. Gitt de primære CNS-effektene av Anafranil, anbefales det å utvise forsiktighet ved bruk av det samtidig med andre CNS-aktive legemidler (se TÅLMODIG INFORMASJON ). Anafranil skal ikke brukes sammen med MAO-hemmere (se KONTRAINDIKASJONER ).
Nøye tilsyn og nøye justering av dosen er nødvendig når Anafranil administreres sammen med antikolinerge eller sympatomimetika.
Flere trisykliske antidepressiva er rapportert å blokkere de farmakologiske effektene av guanethidin, klonidin eller lignende midler, og en slik effekt kan forventes med CMI på grunn av dens strukturelle likhet med andre trisykliske antidepressiva.
Plasmakonsentrasjonen av CMI er rapportert å øke ved samtidig administrering av haloperidol; plasmanivåer av flere nært beslektede trisykliske antidepressiva er rapportert å øke ved samtidig administrering av metylfenidat eller leverenzyminhibitorer (f.eks. cimetidin, fluoksetin) og redusert ved samtidig administrering av leverenzyminduktorer (f.eks. barbiturater, fenytoin), og en slik effekt kan også forventes med CMI. Administrering av CMI er rapportert å øke plasmanivåene av fenobarbital, dersom det gis samtidig (se KLINISK FARMAKOLOGI , Interaksjoner ).
Legemidler metabolisert av P450 2D6
Den biokjemiske aktiviteten til legemiddelmetaboliserende isozym cytokrom P450 2D6 (debrisoquinhydroksylase) er redusert i en undergruppe av den kaukasiske befolkningen (omtrent 7 % til 10 % av kaukasiere er såkalte "dårlige metabolisatorer"); pålitelige estimater av prevalensen av redusert P450 2D6 isozymaktivitet blant asiatiske, afrikanske og andre populasjoner er ennå ikke tilgjengelig. Dårlige metabolisatorer har høyere enn forventet plasmakonsentrasjoner av trisykliske antidepressiva (TCA) når de gis vanlige doser. Avhengig av andelen legemiddel som metaboliseres av P450 2D6, kan økningen i plasmakonsentrasjon være liten eller ganske stor (8 ganger økning i plasma AUC for TCA). I tillegg hemmer visse legemidler aktiviteten til dette isozymet og får normale metabolisatorer til å ligne dårlige metabolisatorer. Et individ som er stabilt på en gitt dose TCA kan bli brått giftig når det gis en av disse hemmende medikamentene som samtidig behandling. Legemidlene som hemmer cytokrom P450 2D6 inkluderer noen som ikke metaboliseres av enzymet (kinidin; cimetidin) og mange som er substrater for P450 2D6 (mange andre antidepressiva, fenotiaziner og Type 1C antiarytmika propafenon og flekainid). Mens alle selektive serotoninreopptakshemmere (SSRI), f.eks. fluoksetin, sertralin, paroksetin og fluvoksamin, hemmer P450 2D6, kan de variere i hemmingsgrad. Fluvoxamine har også vist seg å hemme P450 1A2, en isoform som også er involvert i TCA-metabolismen. I hvilken grad SSRI-TCA-interaksjoner kan gi kliniske problemer, vil avhenge av graden av hemming og farmakokinetikken til den involverte SSRI. Likevel er forsiktighet indikert ved samtidig administrering av TCA med noen av SSRIene og også ved bytte fra en klasse til en annen. Det er spesielt viktig at det må gå tilstrekkelig tid før TCA-behandling igangsettes hos en pasient som seponeres fra fluoksetin, gitt den lange halveringstiden til forelderen og den aktive metabolitten (minst 5 uker kan være nødvendig). Samtidig bruk av midler i den trisykliske antidepressiva-klassen (som inkluderer Anafranil) med legemidler som kan hemme cytokrom P450 2D6 kan kreve lavere doser enn det som vanligvis er foreskrevet for enten det trisykliske antidepressiva eller det andre legemidlet. Videre, hver gang et av disse legemidlene trekkes ut av samtidig behandling, kan det være nødvendig med en økt dose trisykliske antidepressiva. Det er ønskelig å overvåke TCA-plasmanivåer når et middel av den trisykliske antidepressiva-klassen, inkludert Anafranil, skal gis samtidig med et annet legemiddel som er kjent for å være en hemmer av P450 2D6 (og/eller P450 1A2).
Fordi Anafranil er sterkt bundet til serumprotein, kan administrering av Anafranil til pasienter som tar andre legemidler som er sterkt bundet til protein (f.eks. warfarin, digoksin) forårsake en økning i plasmakonsentrasjonen av disse legemidlene, som potensielt kan resultere i bivirkninger. Omvendt kan bivirkninger skyldes fortrengning av proteinbundet Anafranil med andre sterkt bundne legemidler (se KLINISK FARMAKOLOGI , Fordeling ).
Monoaminoksidasehemmere (MAO-hemmere)
(Se KONTRAINDIKASJONER , ADVARSLER , og DOSERING OG ADMINISTRASJON .)
Serotonerge legemidler
(Se KONTRAINDIKASJONER , ADVARSLER , og DOSERING OG ADMINISTRASJON .)
Narkotikamisbruk og avhengighet
Anafranil har ikke blitt systematisk studert hos dyr eller mennesker for potensialet for misbruk, toleranse eller fysisk avhengighet. Mens en rekke abstinenssymptomer er beskrevet i forbindelse med seponering av Anafranil 50 mg (se FORHOLDSREGLER , Abstinenssymptomer ), er det ingen bevis for narkotikasøkende atferd, bortsett fra en enkelt rapport om potensielt Anafranil-misbruk av en pasient med en historie med avhengighet av kodein, benzodiazepiner og flere psykoaktive stoffer. Pasienten fikk Anafranil for depresjon og panikkanfall og så ut til å bli avhengig etter utskrivning fra sykehus.
Til tross for mangelen på bevis som tyder på et misbruksansvar for Anafranil i utenlandsk markedsføring, er det ikke mulig å forutsi i hvilken grad Anafranil kan bli misbrukt eller misbrukt når det først er markedsført i USA. Følgelig bør leger nøye vurdere pasienter for en historie med narkotikamisbruk og følge slike pasienter nøye.
ADVARSLER
Klinisk forverring og selvmordsrisiko
Pasienter med alvorlig depressiv lidelse (MDD), både voksne og barn, kan oppleve forverring av depresjonen og/eller fremveksten av selvmordstanker og -adferd (suicidalitet) eller uvanlige endringer i atferd, enten de tar antidepressive medisiner eller ikke, og dette risikoen kan vedvare inntil betydelig remisjon oppstår. Selvmord er en kjent risiko for depresjon og visse andre psykiatriske lidelser, og disse lidelsene er i seg selv de sterkeste prediktorene for selvmord. Det har imidlertid vært en langvarig bekymring for at antidepressiva kan ha en rolle i å indusere forverring av depresjon og fremveksten av suicidalitet hos visse pasienter i de tidlige faser av behandlingen. Samlede analyser av kortsiktige placebokontrollerte studier av antidepressiva (SSRI og andre) viste at disse medikamentene øker risikoen for suicidal tenkning og atferd (suicidalitet) hos barn, ungdom og unge voksne (alder 18 til 24) med alvorlig depressiv sykdom. lidelse (MDD) og andre psykiatriske lidelser. Korttidsstudier viste ikke en økning i risikoen for suicidalitet med antidepressiva sammenlignet med placebo hos voksne over 24 år; det var en reduksjon med antidepressiva sammenlignet med placebo hos voksne i alderen 65 år og eldre.
De samlede analysene av placebokontrollerte studier hos barn og ungdom med MDD, tvangslidelse (OCD) eller andre psykiatriske lidelser inkluderte totalt 24 korttidsstudier av 9 antidepressiva med over 4400 pasienter. De samlede analysene av placebokontrollerte studier hos voksne med MDD eller andre psykiatriske lidelser inkluderte totalt 295 korttidsstudier (median varighet på 2 måneder) med 11 antidepressiva med over 77 000 pasienter. Det var betydelig variasjon i risiko for suicidalitet blant legemidler, men en tendens til en økning i yngre pasienter for nesten alle legemidler som ble studert. Det var forskjeller i absolutt risiko for suicidalitet på tvers av de forskjellige indikasjonene, med høyest forekomst av MDD. Risikoforskjellene (legemiddel vs placebo) var imidlertid relativt stabile innenfor aldersstrata og på tvers av indikasjoner. Disse risikoforskjellene (drugplacebo-forskjell i antall tilfeller av suicidalitet per 1000 behandlede pasienter) er gitt i tabell 1.
Ingen selvmord skjedde i noen av de pediatriske studiene. Det var selvmord i voksenforsøkene, men antallet var ikke tilstrekkelig til å komme til noen konklusjon om legemiddeleffekt på selvmord.
Det er ukjent om suicidalitetsrisikoen strekker seg til langvarig bruk, dvs. utover flere måneder. Det er imidlertid betydelig bevis fra placebokontrollerte vedlikeholdsforsøk hos voksne med depresjon på at bruk av antidepressiva kan forsinke tilbakefall av depresjon.
Alle pasienter som behandles med antidepressiva for enhver indikasjon bør overvåkes hensiktsmessig og observeres nøye for klinisk forverring, suicidalitet og uvanlige endringer i atferd, spesielt i løpet av de første månedene av en medikamentell behandlingskur, eller ved doseendringer, enten økninger eller synker.
Følgende symptomer, angst, agitasjon, panikkanfall, søvnløshet, irritabilitet, fiendtlighet, aggressivitet, impulsivitet, akatisi (psykomotorisk rastløshet), hypomani og mani, er rapportert hos voksne og pediatriske pasienter som også behandles med antidepressiva for alvorlig depressiv lidelse som for andre indikasjoner, både psykiatriske og ikke-psykiatriske. Selv om det ikke er etablert en årsakssammenheng mellom fremveksten av slike symptomer og enten forverring av depresjon og/eller fremveksten av selvmordsimpulser, er det bekymring for at slike symptomer kan representere forløpere til fremvoksende suicidalitet.
Det bør vurderes å endre det terapeutiske regimet, inkludert eventuelt seponering av medisinen, hos pasienter hvis depresjon er vedvarende verre, eller som opplever ny suicidalitet eller symptomer som kan være forløpere til forverring av depresjon eller suicidalitet, spesielt hvis disse symptomene er alvorlige, brå i debut, eller var ikke en del av pasientens tilstedeværende symptomer.
Familier og omsorgspersoner til pasienter som behandles med antidepressiva for alvorlig depressiv lidelse eller andre indikasjoner, både psykiatriske og ikke-psykiatriske, bør varsles om behovet for å overvåke pasienter for fremveksten av agitasjon, irritabilitet, uvanlige endringer i atferd og de andre symptomene beskrevet ovenfor , samt fremveksten av suicidalitet, og å rapportere slike symptomer umiddelbart til helsepersonell. Slik overvåking bør inkludere daglig observasjon av familier og omsorgspersoner. Resepter for klomipraminhydroklorid bør skrives ut for den minste mengde kapsler i samsvar med god pasientbehandling, for å redusere risikoen for overdosering.
Screening av pasienter for bipolar lidelse
En alvorlig depressiv episode kan være den første presentasjonen av bipolar lidelse. Det er generelt antatt (men ikke etablert i kontrollerte studier) at behandling av en slik episode med et antidepressivum alene kan øke sannsynligheten for utfelling av en blandet/manisk episode hos pasienter med risiko for bipolar lidelse. Hvorvidt noen av symptomene beskrevet ovenfor representerer en slik konvertering er ukjent. Før behandling med et antidepressivum startes, bør imidlertid pasienter med depressive symptomer undersøkes tilstrekkelig for å avgjøre om de har risiko for bipolar lidelse; slik screening bør inkludere en detaljert psykiatrisk historie, inkludert en familiehistorie med selvmord, bipolar lidelse og depresjon. Det skal bemerkes at klomipraminhydroklorid ikke er godkjent for bruk ved behandling av bipolar depresjon.
Serotonin syndrom
Utvikling av et potensielt livstruende serotonergt syndrom er rapportert med SNRI og SSRI, inkludert Anafranil 50 mg, alene, men spesielt ved samtidig bruk av andre serotonerge legemidler (inkludert triptaner, trisykliske antidepressiva, fentanyl, litium, tramadol, tryptofan, johannesurt) og med legemidler som hemmer metabolismen av serotonin (spesielt MAO-hemmere, både de som er beregnet på å behandle psykiatriske lidelser og også andre, som linezolid og intravenøs metylenblått).
Symptomer på serotonergt syndrom kan omfatte endringer i mental status (f.eks. agitasjon, hallusinasjoner, delirium og koma), autonom ustabilitet (f.eks. takykardi, labilt blodtrykk, svimmelhet, diaforese, rødme, hypertermi), nevromuskulære endringer (f.eks. skjelving, rigiditet, myoklonus, hyperrefleksi, inkoordinering), anfall og/eller gastrointestinale symptomer (f.eks. kvalme, oppkast, diaré). Pasienter bør overvåkes for fremveksten av serotonergt syndrom.
Samtidig bruk av Anafranil 10 mg og MAO-hemmere beregnet på å behandle psykiatriske lidelser er kontraindisert. Anafranil 50 mg bør heller ikke startes hos en pasient som behandles med MAO-hemmere som linezolid eller intravenøs metylenblått. Alle rapporter med metylenblått som ga informasjon om administreringsveien involverte intravenøs administrering i doseområdet 1 mg/kg til 8 mg/kg. Ingen rapporter involverte administrering av metylenblått på andre måter (som orale tabletter eller lokal vevsinjeksjon) eller ved lavere doser. Det kan være omstendigheter når det er nødvendig å starte behandling med en MAO-hemmer som linezolid eller intravenøs metylenblått hos en pasient som tar Anafranil. Anafranil bør seponeres før behandling med MAO-hemmeren startes (se KONTRAINDIKASJONER og DOSERING OG ADMINISTRASJON ).
Hvis samtidig bruk av Anafranil 10mg med andre serotonerge legemidler, inkludert triptaner, trisykliske antidepressiva, fentanyl, litium, tramadol, buspiron, tryptofan og johannesurt er klinisk berettiget, bør pasienter gjøres oppmerksomme på en potensiell økt risiko for serotonergt syndrom, spesielt under behandlingsstart og doseøkninger.
Behandling med Anafranil 10 mg og eventuelle samtidige serotonerge midler bør seponeres umiddelbart hvis ovennevnte hendelser inntreffer og støttende symptomatisk behandling bør startes.
Vinkel-lukkende glaukom
Pupilleutvidelsen som oppstår etter bruk av mange antidepressiva, inkludert Anafranil, kan utløse et vinkelangrep hos en pasient med anatomisk smale vinkler som ikke har patentert iridektomi.
Anfall
Under forhåndsmarkedsevaluering ble anfall identifisert som den viktigste risikoen ved bruk av Anafranil.
Den observerte kumulative forekomsten av anfall blant pasienter eksponert for Anafranil 25 mg i doser opp til 300 mg/dag var 0,64 % etter 90 dager, 1,12 % etter 180 dager og 1,45 % etter 365 dager. De kumulative ratene korrigerer råhastigheten på 0,7 % (25 av 3519 pasienter) for den variable eksponeringsvarigheten i kliniske studier.
Selv om dosen ser ut til å være en prediktor for anfall, er det en forvirring av dose og eksponeringsvarighet, noe som gjør det vanskelig å vurdere uavhengig effekt av begge faktorer alene. Evnen til å forutsi forekomsten av anfall hos pasienter som eksponeres for doser med CMI større enn 250 mg er begrenset, gitt at plasmakonsentrasjonen av CMI kan være doseavhengig og kan variere mellom individer som får samme dose. Likevel anbefales forskrivere å begrense den daglige dosen til maksimalt 250 mg hos voksne og 3 mg/kg (eller 200 mg) hos barn og ungdom (se DOSERING OG ADMINISTRASJON ).
Forsiktighet bør utvises ved administrering av Anafranil 50 mg til pasienter med tidligere anfall eller andre disponerende faktorer, f.eks. hjerneskade av varierende etiologi, alkoholisme og samtidig bruk med andre legemidler som senker krampeterskelen.
Sjeldne rapporter om dødsfall i forbindelse med anfall har blitt rapportert av utenlandsk postmarkedsføringsovervåking, men ikke i amerikanske kliniske studier. I noen av disse tilfellene hadde Anafranil blitt administrert sammen med andre epileptogene midler; i andre hadde de involverte pasientene muligens disponerende medisinske tilstander. En årsakssammenheng mellom behandling med Anafranil 25 mg og disse dødsfallene er derfor ikke fastslått.
Leger bør diskutere risikoen ved å ta Anafranil med pasienter mens de deltar i aktiviteter der plutselig tap av bevissthet kan føre til alvorlig skade på pasienten eller andre, f.eks. bruk av komplekse maskiner, kjøring, svømming, klatring.
KJOLE
Sjeldne tilfeller av legemiddelutslett med eosinofili og systemiske symptomer (DRESS) er rapportert ved bruk av klomipramin. Ved alvorlige akutte reaksjoner som DRESS, avbryt klomipraminbehandling umiddelbart og igangsett passende behandling.
FORHOLDSREGLER
Generell
Selvmord
Siden depresjon er et ofte assosiert trekk ved OCD, må risikoen for selvmord vurderes. Resepter for Anafranil bør skrives ut for den minste mengde kapsler i samsvar med god pasientbehandling, for å redusere risikoen for overdosering.
Kardiovaskulære effekter
Beskjeden ortostatisk reduksjon i blodtrykk og beskjeden takykardi ble sett hos ca. 20 % av pasientene som tok Anafranil 10 mg i kliniske studier; men pasientene var ofte asymptomatiske. Blant ca. 1400 pasienter behandlet med CMI i premarketing-erfaringen som hadde EKG, utviklet 1,5 % abnormiteter under behandlingen, sammenlignet med 3,1 % av pasientene som fikk aktive kontrollmedisiner og 0,7 % av pasientene som fikk placebo. De vanligste EKG-forandringene var PVC-er, ST-T-bølgeforandringer og intraventrikulære ledningsavvik. Disse endringene var sjelden forbundet med signifikante kliniske symptomer. Det er likevel nødvendig med forsiktighet ved behandling av pasienter med kjent kardiovaskulær sykdom, og gradvis dosetitrering anbefales.
Psykose, forvirring og andre nevropsykiatriske fenomener
Pasienter behandlet med Anafranil 10 mg har blitt rapportert å vise en rekke nevropsykiatriske tegn og symptomer, inkludert vrangforestillinger, hallusinasjoner, psykotiske episoder, forvirring og paranoia. På grunn av den ukontrollerte naturen til mange av studiene, er det umulig å gi et presist estimat på omfanget av risikoen ved behandling med Anafranil. Som med trisykliske antidepressiva som det er nært beslektet med, kan Anafranil 25 mg utløse en akutt psykotisk episode hos pasienter med ukjent schizofreni.
Mani/hypomani
Under premarketing testing av Anafranil 10 mg hos pasienter med affektiv lidelse ble hypomani eller mani utløst hos flere pasienter. Aktivering av mani eller hypomani er også rapportert hos en liten andel av pasienter med affektiv lidelse behandlet med markedsførte trisykliske antidepressiva, som er nært beslektet med Anafranil.
Hepatiske endringer
Under testing før markedsføring ble Anafranil av og til assosiert med økninger i SGOT og SGPT (sammenslått forekomst på henholdsvis ca. 1 % og 3 %) av potensiell klinisk betydning (dvs. verdier større enn 3 ganger øvre normalgrense). I de aller fleste tilfeller var disse enzymøkningene ikke assosiert med andre kliniske funn som tydet på leverskade; dessuten var ingen gulsott. Sjeldne rapporter om mer alvorlig leverskade, noen dødelige, har blitt registrert i utenlandsk erfaring etter markedsføring. Forsiktighet er indisert ved behandling av pasienter med kjent leversykdom, og periodisk overvåking av leverenzymnivåer anbefales hos slike pasienter.
Hematologiske endringer
Selv om det ikke ble sett noen tilfeller av alvorlig hematologisk toksisitet før markedsføring med Anafranil 25 mg, har det vært rapporter etter markedsføring om leukopeni, agranulocytose, trombocytopeni, anemi og pancytopeni i forbindelse med bruk av Anafranil 50 mg. Som tilfellet er med trisykliske antidepressiva som Anafranil 25 mg er nært beslektet med, bør leukocytt- og differensialblodtellinger innhentes hos pasienter som utvikler feber og sår hals under behandling med Anafranil.
Sentralnervesystemet
Mer enn 30 tilfeller av hypertermi er registrert av overvåkingssystemer etter markedsføring. De fleste tilfellene skjedde når Anafranil ble brukt i kombinasjon med andre legemidler. Når Anafranil 25 mg og et nevroleptika ble brukt samtidig, ble tilfellene noen ganger ansett for å være eksempler på et malignt nevroleptikasyndrom.
Seksuell dysfunksjon
Frekvensen av seksuell dysfunksjon hos mannlige pasienter med OCD som ble behandlet med Anafranil i førmarkedsføringserfaringen var markant økt sammenlignet med placebokontroller (dvs. 42 % opplevde ejakulasjonssvikt og 20 % opplevde impotens, sammenlignet med henholdsvis 2,0 % og 2,6 %, i placebogruppen). Omtrent 85 % av menn med seksuell dysfunksjon valgte å fortsette behandlingen.
Hyponatremi
Hyponatremi har oppstått som følge av behandling med klomipramin. I mange tilfeller ser hyponatremi ut til å være et resultat av syndromet med upassende antidiuretisk hormonsekresjon (SIADH). Eldre pasienter kan ha større risiko for å utvikle hyponatremi med et serotonergt antidepressivum. Pasienter som tar diuretika eller som på annen måte er volumfattige kan ha større risiko. Seponering av Anafranil hos pasienter med symptomatisk hyponatremi og passende medisinsk intervensjon bør iverksettes. Tegn og symptomer på hyponatremi inkluderer hodepine, konsentrasjonsvansker, hukommelsessvikt, forvirring, svakhet og ustabilitet, som kan føre til fall. Mer alvorlige og/eller akutte tilfeller har inkludert hallusinasjoner, synkope, anfall, koma, pustestans og død.
Vektendringer
kontrollerte studier av OCD ble vektøkning rapportert hos 18 % av pasientene som fikk Anafranil, sammenlignet med 1 % av pasientene som fikk placebo. I disse studiene hadde 28 % av pasientene som fikk Anafranil 25 mg en vektøkning på minst 7 % av den opprinnelige kroppsvekten, sammenlignet med 4 % av pasientene som fikk placebo. Flere pasienter hadde vektøkninger på over 25 % av den opprinnelige kroppsvekten. Omvendt hadde 5 % av pasientene som fikk Anafranil og 1 % som fikk placebo vekttap på minst 7 % av den opprinnelige kroppsvekten.
Elektrokonvulsiv terapi
Som med nært beslektede trisykliske antidepressiva, kan samtidig administrering av Anafranil og elektrokonvulsiv terapi øke risikoen; slik behandling bør begrenses til de pasientene som det er viktig for, siden det er begrenset klinisk erfaring.
Kirurgi
Før elektiv kirurgi med generell anestesi, bør behandling med Anafranil 50mg seponeres så lenge det er klinisk mulig, og anestesilegen bør informeres.
Bruk ved samtidig sykdom
. Som med nært beslektede trisykliske antidepressiva, bør Anafranil 10 mg brukes med forsiktighet i følgende: . Hypertyreoideapasienter eller pasienter som får skjoldbruskmedisin, på grunn av muligheten for hjertetoksisitet; . Pasienter med økt intraokulært trykk, en historie med trangvinklet glaukom eller urinretensjon på grunn av legemidlets antikolinerge egenskaper; . Pasienter med svulster i binyremargen (f.eks. feokromocytom, neuroblastom) hvor stoffet kan provosere hypertensive kriser;Pasienter med betydelig nedsatt nyrefunksjon.
Abstinenssymptomer
En rekke abstinenssymptomer er rapportert i forbindelse med brå seponering av Anafranil 50 mg, inkludert svimmelhet, kvalme, oppkast, hodepine, ubehag, søvnforstyrrelser, hypertermi og irritabilitet. I tillegg kan slike pasienter oppleve en forverring av psykiatrisk status. Selv om abstinenseffektene av Anafranil 10 mg ikke har blitt systematisk evaluert i kontrollerte studier, er de velkjente med nært beslektede trisykliske antidepressiva, og det anbefales at dosen trappes ned gradvis og pasienten overvåkes nøye under seponering (se Narkotikamisbruk og avhengighet ).
Informasjon til pasienter
Forskrivere eller annet helsepersonell bør informere pasienter, deres familier og deres omsorgspersoner om fordelene og risikoene forbundet med behandling med klomipraminhydroklorid og bør gi dem råd om riktig bruk. En pasientmedisineringsveiledning om "antidepressive medisiner, depresjon og andre alvorlige psykiske lidelser og selvmordstanker eller handlinger" er tilgjengelig for klomipraminhydroklorid. Forskriveren eller helsepersonell bør instruere pasienter, deres familier og deres omsorgspersoner om å lese medisinveiledningen og bør hjelpe dem med å forstå innholdet. Pasienter bør gis mulighet til å diskutere innholdet i legemiddelveiledningen og få svar på spørsmål de måtte ha. Den fullstendige teksten til medisinveiledningen er skrevet ut på nytt på slutten av dette dokumentet.
Pasienter bør informeres om følgende problemer og bes om å varsle sin forskriver dersom disse oppstår mens de tar klomipraminhydroklorid.
Klinisk forverring og selvmordsrisiko
Pasienter, deres familier og deres omsorgspersoner bør oppmuntres til å være oppmerksomme på fremveksten av angst, agitasjon, panikkanfall, søvnløshet, irritabilitet, fiendtlighet, aggressivitet, impulsivitet, akatisi (psykomotorisk rastløshet), hypomani, mani, andre uvanlige endringer i atferd. , forverring av depresjon og selvmordstanker, spesielt tidlig under antidepressiv behandling og når dosen justeres opp eller ned. Familier og omsorgspersoner til pasienter bør rådes til å se etter forekomsten av slike symptomer på daglig basis, siden endringer kan være brå. Slike symptomer bør rapporteres til pasientens forskriver eller helsepersonell, spesielt hvis de er alvorlige, plutselige eller ikke var en del av pasientens symptomer. Symptomer som disse kan være assosiert med økt risiko for suicidal tenkning og atferd og indikerer behov for svært tett oppfølging og muligens endringer i medisinen.
Leger anbefales å diskutere følgende problemer med pasienter som de foreskriver Anafranil til:
- . Risikoen for anfall (se ADVARSLER ); . Den relativt høye forekomsten av seksuell dysfunksjon blant menn (se Seksuell dysfunksjon ); . Siden Anafranil 50mg kan svekke de mentale og/eller fysiske evnene som kreves for å utføre komplekse oppgaver, og siden Anafranil 25mg er assosiert med en risiko for anfall, bør pasienter advares om utførelse av komplekse og farlige oppgaver (se ADVARSLER ); . Pasienter bør advares om samtidig bruk av alkohol, barbiturater eller andre CNS-dempende midler, siden Anafranil 50 mg kan overdrive deres respons på disse legemidlene; . Pasienter bør varsle legen dersom de blir gravide eller har tenkt å bli gravide under behandlingen; . Pasienter bør varsle legen dersom de ammer.
Pasienter bør informeres om at bruk av Anafranil kan forårsake mild pupilledilatasjon, som hos følsomme personer kan føre til en episode med lukket vinkelglaukom. Eksisterende glaukom er nesten alltid åpenvinklet glaukom fordi vinkel-lukkende glaukom, når diagnostisert, kan behandles definitivt med iridektomi. Åpenvinklet glaukom er ikke en risikofaktor for lukkevinkelglaukom. Pasienter kan ønske å bli undersøkt for å finne ut om de er mottakelige for vinkellukking, og ha en profylaktisk prosedyre (f.eks. iridektomi), hvis de er mottakelige.
Karsinogenese, mutagenese, svekkelse av fruktbarhet
Det ble ikke funnet bevis for karsinogenitet i to 2-årige bioassays på rotter ved doser opp til 100 mg/kg, som er 24 og 4 ganger den maksimale anbefalte daglige dosen for mennesker (MRHD) på henholdsvis mg/kg og mg/m² basis. , eller i en 2-årig bioanalyse på mus i doser opp til 80 mg/kg, som er 20 og 1,5 ganger MRHD på henholdsvis mg/kg og mg/m² basis.
reproduksjonsstudier ble det ikke funnet noen effekter på fertilitet hos rotter gitt opp til 24 mg/kg, som er 6 ganger og omtrent lik MRHD på henholdsvis mg/kg og mg/m² basis.
Graviditetskategori C
Ingen teratogene effekter ble observert i studier utført på rotter og mus ved doser opp til 100 mg/kg, som er 24 ganger den maksimale anbefalte daglige dosen for mennesker (MRHD) på mg/kg-basis og 4 ganger (rotter) og 2 ganger ( mus) MRHD på mg/m²-basis. Små uspesifikke embryo-/føtotoksiske effekter ble sett hos avkom av behandlede rotter som ble gitt 50 og 100 mg/kg og av behandlede mus som ble gitt 100 mg/kg.
Det finnes ingen tilstrekkelige eller godt kontrollerte studier hos gravide kvinner. Abstinenssymptomer, inkludert nervøsitet, skjelving og anfall, er rapportert hos nyfødte hvis mødre hadde tatt Anafranil 50 mg frem til fødselen. Anafranil 10 mg skal kun brukes under graviditet hvis den potensielle fordelen rettferdiggjør den potensielle risikoen for fosteret.
Ammende mødre
Anafranil er funnet i morsmelk. På grunn av potensialet for bivirkninger, bør det tas en beslutning om å avbryte ammingen eller å avbryte medikamentet, tatt i betraktning stoffets betydning for moren.
Pediatrisk bruk
Sikkerhet og effektivitet i den pediatriske populasjonen andre enn pediatriske pasienter med OCD er ikke fastslått (se BOKS ADVARSEL og ADVARSLER , Klinisk forverring og selvmordsrisiko ). Alle som vurderer bruk av Anafranil hos et barn eller en ungdom, må balansere den potensielle risikoen med det kliniske behovet.
I en kontrollert klinisk studie hos barn og ungdom (10 til 17 år) fikk 46 polikliniske pasienter Anafranil 50 mg i opptil 8 uker. I tillegg har 150 ungdomspasienter fått Anafranil 10 mg i åpne protokoller i perioder på flere måneder til flere år. Av de 196 ungdommene som ble studert, var 50 13 år eller yngre og 146 var 14 til 17 år gamle. Bivirkningsprofilen i denne aldersgruppen (se BIVIRKNINGER ) er lik det som er observert hos voksne.
Risikoen, hvis noen, som kan være forbundet med Anafranils utvidede bruk hos barn og ungdom med OCD er ikke systematisk vurdert. Beviset som støtter konklusjonen om at Anafranil 50 mg er trygt for bruk hos barn og ungdom, er avledet fra relativt kortsiktige kliniske studier og fra ekstrapolering av erfaringer fra voksne pasienter. Spesielt er det ingen studier som direkte evaluerer effekten av langtidsbruk av Anafranil 25 mg på vekst, utvikling og modning av barn og ungdom. Selv om det ikke er bevis som tyder på at Anafranil 10 mg påvirker vekst, utvikling eller modning negativt, er fraværet av slike funn ikke tilstrekkelig til å utelukke et potensial for slike effekter ved kronisk bruk.
Sikkerhet og effektivitet hos pediatriske pasienter under 10 år er ikke fastslått. Det kan derfor ikke gis spesifikke anbefalinger for bruk av Anafranil hos pediatriske pasienter under 10 år.
Geriatrisk bruk
Kliniske studier av Anafranil 50 mg inkluderte ikke tilstrekkelig antall forsøkspersoner i alderen 65 år og over til å avgjøre om de responderer annerledes enn yngre forsøkspersoner; 152 pasienter på minst 60 år som deltok i ulike amerikanske kliniske studier fikk Anafranil i perioder på flere måneder til flere år. Ingen uvanlige aldersrelaterte bivirkninger ble identifisert i denne populasjonen. Annen rapportert klinisk erfaring har ikke identifisert forskjeller i respons mellom eldre og yngre pasienter. Generelt bør dosevalg for en eldre pasient være forsiktig, vanligvis med start i den lave enden av doseringsområdet, noe som gjenspeiler den høyere frekvensen av nedsatt lever-, nyre- eller hjertefunksjon og samtidig sykdom eller annen medikamentell behandling.
Anafranil har vært assosiert med tilfeller av klinisk signifikant hyponatremi. Eldre pasienter kan ha større risiko for denne bivirkningen (se FORHOLDSREGLER , Hyponatremi ).
OVERDOSE
Dødsfall kan oppstå på grunn av overdosering med denne klassen medikamenter. Multiple stoffinntak (inkludert alkohol) er vanlig ved bevisst trisyklisk overdose. Siden håndteringen er kompleks og i endring, anbefales det at legen kontakter en giftsentral for å få oppdatert informasjon om behandling. Tegn og symptomer på toksisitet utvikler seg raskt etter trisyklisk overdose. Derfor er sykehusovervåking nødvendig så snart som mulig.
Menneskelig erfaring
amerikanske kliniske studier forekom 2 dødsfall i 12 rapporterte tilfeller av akutt overdosering med Anafranil enten alene eller i kombinasjon med andre legemidler. Ett dødsfall involverte en pasient mistenkt for å ha inntatt en dose på 7000 mg. Det andre dødsfallet involverte en pasient mistenkt for å ha inntatt en dose på 5750 mg. De 10 ikke-dødelige tilfellene involverte doser på opptil 5000 mg, ledsaget av plasmanivåer på opptil 1010 ng/ml. Alle de 10 pasientene ble fullstendig friske. Blant rapporter fra andre land om overdosering av Anafranil, var den laveste dosen assosiert med dødsfall 750 mg. Basert på rapporter etter markedsføring i Storbritannia, anses CMIs dødelighet ved overdosering å være lik den som er rapportert for nært beslektede trisykliske forbindelser markedsført som antidepressiva.
Manifestasjoner
Tegn og symptomer varierer i alvorlighetsgrad avhengig av faktorer som mengden medikament som er absorbert, pasientens alder og tiden som har gått siden legemiddelinntaket. Kritiske manifestasjoner av overdose inkluderer hjertedysrytmier, alvorlig hypotensjon, kramper og CNS-depresjon inkludert koma. Endringer i elektrokardiogrammet, spesielt i QRS-aksen eller -bredden, er klinisk signifikante indikatorer på trisyklisk toksisitet. Andre CNS-manifestasjoner kan inkludere døsighet, stupor, ataksi, rastløshet, agitasjon, delirium, alvorlig svette, hyperaktive reflekser, muskelstivhet og atetoid- og choreiforme bevegelser. Hjerteavvik kan omfatte takykardi, tegn på kongestiv hjertesvikt, og i svært sjeldne tilfeller hjertestans. Respirasjonsdepresjon, cyanose, sjokk, oppkast, hyperpyreksi, mydriasis og oliguri eller anuri kan også være tilstede.
Ledelse
Ta EKG og start hjerteovervåking umiddelbart. Beskytt pasientens luftveier, etablere en intravenøs linje, og start gastrisk dekontaminering. Minimum 6 timers observasjon med hjerteovervåking og observasjon for tegn på CNS eller respirasjonsdepresjon, hypotensjon, hjerterytmeforstyrrelser og/eller ledningsblokker og anfall er nødvendig.
Hvis tegn på toksisitet oppstår når som helst i løpet av denne perioden, er utvidet overvåking nødvendig. Det er kasusrapporter om pasienter som bukker under for fatale dysrytmier sent etter overdose; disse pasientene hadde kliniske bevis på betydelig forgiftning før døden, og de fleste fikk utilstrekkelig gastrointestinal dekontaminering. Overvåking av plasmanivåer av medikamenter bør ikke veilede behandlingen av pasienten.
Gastrointestinal dekontaminering
Alle pasienter som mistenkes for trisyklisk overdose bør få gastrointestinal dekontaminering. Dette bør inkludere store volum mageskylling etterfulgt av aktivt kull. Hvis bevisstheten er svekket, bør luftveiene sikres før skylling. Emesis er kontraindisert.
Kardiovaskulær
En maksimal QRS-lengde på ≥ 0,10 sekunder kan være den beste indikasjonen på alvorlighetsgraden av overdosen. Intravenøst natriumbikarbonat bør brukes for å opprettholde serum-pH i området 7,45 til 7,55. Hvis pH-responsen er utilstrekkelig, kan hyperventilering også brukes. Samtidig bruk av hyperventilering og natriumbikarbonat bør gjøres med ekstrem forsiktighet, med hyppig pH-overvåking. En pH >7,60 eller en pCO2
sjeldne tilfeller kan hemoperfusjon være gunstig ved akutt refraktær kardiovaskulær ustabilitet hos pasienter med akutt toksisitet. Imidlertid har hemodialyse, peritonealdialyse, utvekslingstransfusjoner og tvungen diurese generelt blitt rapportert som ineffektive ved trisykliske forgiftninger.
CNS
Hos pasienter med CNS-depresjon anbefales tidlig intubering på grunn av potensialet for brå forverring. Anfall bør kontrolleres med benzodiazepiner, eller hvis disse er ineffektive, andre antikonvulsiva (f.eks. fenobarbital, fenytoin). Fysiostigmin anbefales ikke unntatt for å behandle livstruende symptomer som ikke har respondert på andre terapier, og da kun i samråd med et giftkontrollsenter.
Psykiatrisk oppfølging
Siden overdosering ofte er bevisst, kan pasienter forsøke selvmord på andre måter i restitusjonsfasen. Psykiatrisk henvisning kan være aktuelt.
Pediatrisk ledelse
Prinsippene for behandling av overdosering av barn og voksne er like. Det anbefales sterkt at legen kontakter det lokale giftkontrollsenteret for spesifikk pediatrisk behandling.
KONTRAINDIKASJONER
Anafranil er kontraindisert hos pasienter med en historie med overfølsomhet overfor Anafranil 25 mg eller andre trisykliske antidepressiva.
Monoaminoksidasehemmere (MAO-hemmere)
Bruk av MAO-hemmere beregnet på å behandle psykiatriske lidelser med Anafranil eller innen 14 dager etter avsluttet behandling med Anafranil er kontraindisert på grunn av økt risiko for serotonergt syndrom. Bruk av Anafranil 10 mg innen 14 dager etter seponering av en MAO-hemmer beregnet på å behandle psykiatriske lidelser er også kontraindisert (se ADVARSLER og DOSERING OG ADMINISTRASJON ).
Å starte Anafranil hos en pasient som behandles med linezolid eller intravenøs metylenblått er også kontraindisert på grunn av økt risiko for serotonergt syndrom (se ADVARSLER og DOSERING OG ADMINISTRASJON ).
Hjerteinfarkt
Anafranil er kontraindisert i den akutte restitusjonsperioden etter et hjerteinfarkt.
KLINISK FARMAKOLOGI
Farmakodynamikk
Klomipramin (CMI) antas å påvirke obsessiv og tvangsmessig atferd gjennom dens effekter på serotonerg nevronal overføring. Den faktiske nevrokjemiske mekanismen er ukjent, men CMIs kapasitet til å hemme gjenopptaket av serotonin (5-HT) antas å være viktig.
Farmakokinetikk
Absorpsjon/Biotilgjengelighet
CMI fra Anafranil 25mg kapsler er like biotilgjengelig som CMI fra en løsning. Biotilgjengeligheten til CMI fra kapsler påvirkes ikke signifikant av mat.
en doseproporsjonalitetsstudie som involverte flere CMI-doser, var steady-state plasmakonsentrasjoner (Css) og area-under-plasma-concentration-time kurver (AUC) av CMI og CMIs viktigste aktive metabolitt, desmethylclomipramin (DMI), ikke proporsjonale med dosen. over de evaluerte områdene, dvs. mellom 25 til 100 mg/dag og mellom 25 til 150 mg/dag, selv om Css og AUC er omtrent lineært relatert til dose mellom 100 og 150 mg/dag. Forholdet mellom dose og CMI/DMI-konsentrasjoner ved høyere daglige doser har ikke blitt systematisk vurdert, men hvis det er betydelig doseavhengighet ved doser over 150 mg/dag, er det potensiale for dramatisk høyere Css og AUC selv for pasienter som doseres innenfor anbefalt rekkevidde. Dette kan utgjøre en potensiell risiko for noen pasienter (se ADVARSLER og NARKOTIKAHANDEL ).
Etter en enkelt oral dose på 50 mg oppstår maksimal plasmakonsentrasjon av CMI innen 2 til 6 timer (gjennomsnittlig 4,7 timer) og varierer fra 56 ng/ml til 154 ng/ml (gjennomsnittlig 92 ng/ml). Etter flere daglige doser på 150 mg Anafranil 25 mg, varierer steady-state maksimale plasmakonsentrasjoner fra 94 ng/ml til 339 ng/ml (gjennomsnittlig 218 ng/ml) for CMI og fra 134 ng/ml til 532 ng/ml ( gjennomsnitt, 274 ng/ml) for DMI. Ytterligere informasjon fra en studie med stigende doser med doser opp til 250 mg antyder at DMI kan utvise ikke-lineær farmakokinetikk over det vanlige doseringsområdet. Ved en dose av Anafranil 200 mg hadde forsøkspersoner som fikk en enkelt blodprøve tatt ca. 9 til 22 timer (median 16 timer), etter dosen plasmakonsentrasjoner på opptil 605 ng/ml for CMI, 781 ng/ml for DMI og 1386 ng/ml for begge.
Fordeling
CMI distribueres til cerebrospinalvæske (CSF) og hjernen og til morsmelk. DMI distribueres også til CSF, med et gjennomsnittlig CSF/plasma-forhold på 2,6. Proteinbindingen til CMI er omtrent 97 %, hovedsakelig til albumin, og er uavhengig av CMI-konsentrasjonen. Interaksjonen mellom CMI og andre sterkt proteinbundne legemidler har ikke blitt fullstendig evaluert, men kan være viktig (se NARKOTIKAHANDEL ).
Metabolisme
CMI er omfattende biotransformert til DMI og andre metabolitter og deres glukuronidkonjugater. DMI er farmakologisk aktiv, men effekten på OCD-atferd er ukjent. Disse metabolittene skilles ut i urin og feces etter galle-eliminering. Etter en 25 mg radiomerket dose av CMI hos to personer ble henholdsvis 60 % og 51 % av dosen gjenfunnet i urinen og henholdsvis 32 % og 24 % i feces. I den samme studien var den kombinerte uringjenvinningen av CMI og DMI bare omtrent 0,8 % til 1,3 % av den administrerte dosen. CMI induserer ikke legemiddelmetaboliserende enzymer, målt ved antipyrinhalveringstid.
Eliminering
Bevis på at Css og AUC for CMI og DMI kan øke uforholdsmessig med økende orale doser, tyder på at metabolismen av CMI og DMI kan være kapasitetsbegrenset. Dette faktum må tas i betraktning ved vurdering av estimatene for de farmakokinetiske parameterne presentert nedenfor, da disse ble oppnådd hos individer som ble eksponert for doser på 150 mg. Hvis farmakokinetikken til CMI og DMI er ikke-lineær ved doser over 150 mg, kan eliminasjonshalveringstidene deres bli betydelig forlenget ved doser nær den øvre enden av det anbefalte doseringsområdet (dvs. 200 mg/dag til 250 mg/dag). Følgelig kan CMI og DMI akkumuleres, og denne akkumuleringen kan øke forekomsten av alle dose- eller plasmakonsentrasjonsavhengige bivirkninger, spesielt anfall (se ADVARSLER ).
Etter en dose på 150 mg varierer halveringstiden til CMI fra 19 timer til 37 timer (gjennomsnittlig 32 timer) og halveringstiden for DMI varierer fra 54 timer til 77 timer (gjennomsnittlig 69 timer). Steady-state-nivåer etter gjentatt dosering nås vanligvis innen 7 til 14 dager for CMI. Plasmakonsentrasjonen av metabolitten overstiger det opprinnelige legemidlet ved gjentatt dosering. Etter gjentatt dosering med 150 mg/dag er akkumuleringsfaktoren for CMI ca. 2,5 og for DMI er 4,6. Viktigere, det kan ta to uker eller lenger å oppnå denne graden av akkumulering ved konstant dosering på grunn av de relativt lange eliminasjonshalveringstidene for CMI og DMI (se DOSERING OG ADMINISTRASJON ). Effekten av nedsatt lever- og nyrefunksjon på disposisjonen av Anafranil er ikke fastslått.
Interaksjoner
Samtidig administrering av haloperidol med CMI øker plasmakonsentrasjonen av CMI. Samtidig administrering av CMI med fenobarbital øker plasmakonsentrasjonen av fenobarbital (se NARKOTIKAHANDEL ). Yngre forsøkspersoner (18 til 40 år) tolererte CMI bedre og hadde signifikant lavere steady-state plasmakonsentrasjoner, sammenlignet med forsøkspersoner over 65 år. Barn under 15 år hadde signifikant lavere plasmakonsentrasjon/doseforhold sammenlignet med voksne. Plasmakonsentrasjoner av CMI var signifikant lavere hos røykere enn hos ikke-røykere.
PASIENTINFORMASJON
Anafranil™ (klomipraminhydroklorid) Kapsler USP
Antidepressive medisiner, depresjon og andre alvorlige psykiske sykdommer, og selvmordstanker eller handlinger
Les medisinveiledningen som følger med deg eller ditt familiemedlems antidepressive medisin. Denne medisinveiledningen handler kun om risikoen for selvmordstanker og -handlinger med antidepressiva. Snakk med din eller familiemedlemmets helsepersonell om:
- . alle risikoer og fordeler ved behandling med antidepressiva . alle behandlingsvalg for depresjon eller annen alvorlig psykisk lidelse
Hva er den viktigste informasjonen jeg bør vite om antidepressive medisiner, depresjon og andre alvorlige psykiske lidelser, og selvmordstanker eller -handlinger?
1. Antidepressiva kan øke selvmordstanker eller -handlinger hos enkelte barn, tenåringer og unge voksne i løpet av de første månedene av behandlingen.
2. Depresjon og andre alvorlige psykiske lidelser er de viktigste årsakene til selvmordstanker og -handlinger. Noen mennesker kan ha en spesielt høy risiko for å ha selvmordstanker eller -handlinger. Disse inkluderer personer som har (eller har en familiehistorie med) bipolar sykdom (også kalt manisk-depressiv sykdom) eller selvmordstanker eller -handlinger.
3. Hvordan kan jeg se etter og prøve å forhindre selvmordstanker og -handlinger hos meg selv eller et familiemedlem?
- . Vær nøye med eventuelle endringer, spesielt plutselige endringer, i humør, atferd, tanker eller følelser. Dette er svært viktig når en antidepressiv medisin startes eller når dosen endres. . Ring helsepersonell med en gang for å rapportere nye eller plutselige endringer i humør, atferd, tanker eller følelser. . Hold alle oppfølgingsbesøk hos helsepersonell som planlagt. Ring helsepersonell mellom besøkene etter behov, spesielt hvis du har bekymringer om symptomer.
Ring en helsepersonell med en gang hvis du eller familiemedlemmet ditt har noen av følgende symptomer, spesielt hvis de er nye, verre eller bekymrer deg:
- . tanker om selvmord eller å dø . forsøk på å begå selvmord . ny eller verre depresjon . ny eller verre angst . føler meg veldig urolig eller rastløs . panikk anfall . problemer med å sove (søvnløshet) . ny eller verre irritabilitet . opptrer aggressivt, er sint eller voldelig . handler på farlige impulser . en ekstrem økning i aktivitet og prat (mani) . andre uvanlige endringer i atferd eller humør
Lavt saltnivå (natrium) i blodet. Eldre mennesker kan ha større risiko for dette. Symptomer kan omfatte:
- . hodepine . svakhet eller ustabilitet . forvirring, problemer med å konsentrere seg eller tenke eller hukommelsesproblemer
Visuelle problemer
- . øyesmerter . endringer i synet . hevelse eller rødhet i eller rundt øyet
Bare noen mennesker er i faresonen for disse problemene. Det kan være lurt å gjennomgå en øyeundersøkelse for å se om du er i faresonen og få forebyggende behandling hvis du er det.
Hvem bør ikke ta Anafranil?
Ikke ta Anafranil hvis du:
- . ta en monoaminoksidasehemmer (MAOI). Spør helsepersonell eller apotek hvis du ikke er sikker på om du tar en MAO-hemmer, inkludert antibiotikum linezolid.
- . Ikke ta en MAO-hemmer innen 2 uker etter å ha sluttet med Anafranil 25mg med mindre legen din har bedt om det. . Ikke start Anafranil hvis du sluttet å ta en MAO-hemmer i løpet av de siste 2 ukene med mindre legen din har bedt om det.
Hva annet trenger jeg å vite om antidepressiva?
- . Slutt aldri en antidepressiv medisin uten først å snakke med en helsepersonell. Å stoppe en antidepressiv medisin plutselig kan forårsake andre symptomer. . Antidepressiva er medisiner som brukes til å behandle depresjon og andre sykdommer. Det er viktig å diskutere alle risikoene ved å behandle depresjon og også risikoen ved å ikke behandle den. Pasienter og deres familier eller andre omsorgspersoner bør diskutere alle behandlingsvalg med helsepersonell, ikke bare bruken av antidepressiva. . Antidepressiva har andre bivirkninger. Snakk med helsepersonell om bivirkningene av medisinen som er foreskrevet for deg eller ditt familiemedlem. . Antidepressiva kan samhandle med andre medisiner. Kjenn til alle medisinene du eller ditt familiemedlem tar. Hold en liste over alle medisiner for å vise helsepersonell. Ikke start nye medisiner uten først å sjekke med helsepersonell. . Ikke alle antidepressive medisiner foreskrevet for barn er FDA-godkjent for bruk hos barn. Snakk med barnets helsepersonell for mer informasjon.
Ring legen din for medisinsk råd om bivirkninger. Du kan rapportere bivirkninger til FDA på 1-800-FDA-1088.
Denne medisinveiledningen er godkjent av US Food and Drug Administration.
