Fosamax 35mg, 70mg Alendronate Bruk, bivirkninger og dosering. Pris i nettapotek. Generisk medisin uten resept.
Hva er Fosamax 70mg og hvordan brukes det?
Fosamax 35mg er et reseptbelagt legemiddel som brukes til å forebygge og behandle visse typer bentap (osteoporose) hos voksne. Fosamax 70mg kan brukes alene eller sammen med andre medisiner.
Fosamax er et kalsiummetabolismemodifikator, bisfosfonatderivater.
Det er ikke kjent om Fosamax er trygt og effektivt hos barn.
Hva er de mulige bivirkningene av Fosamax?
Fosamax kan forårsake alvorlige bivirkninger inkludert:
- . brystsmerter . ny eller forverret halsbrann . smerte eller svie under ribbeina eller i ryggen . alvorlig halsbrann . brennende smerter i øvre del av magen eller hoste opp blod . nye eller uvanlige smerter i låret eller hoften . kjevesmerter . nummenhet . opphovning . alvorlige ledd-, bein- eller muskelsmerter . muskelspasmer eller kramper . nummenhet eller prikking rundt munnen eller i fingrene eller tærne
Få medisinsk hjelp med en gang hvis du har noen av symptomene nevnt ovenfor.
De vanligste bivirkningene av Fosamax inkluderer:
- . halsbrann . urolig mage . magesmerter . kvalme . diaré . forstoppelse . beinsmerter . Muskelsmerte . leddsmerter
Fortell legen dersom du har noen bivirkninger som plager deg eller som ikke går over.
Dette er ikke alle mulige bivirkninger av Fosamax. Spør legen din eller apoteket for mer informasjon.
Ring legen din for medisinsk råd om bivirkninger. Du kan rapportere bivirkninger til FDA på 1-800-FDA-1088.
BESKRIVELSE
FOSAMAX (natriumalendronat) er et bisfosfonat som virker som en spesifikk hemmer av osteoklastmediert benresorpsjon. Bisfosfonater er syntetiske analoger av pyrofosfat som binder seg til hydroksyapatitten som finnes i bein.
Alendronatnatrium er kjemisk beskrevet som (4-amino-1-hydroksybutyliden) bisfosfonsyre mononatriumsalttrihydrat.
Den empiriske formelen for alendronatnatrium er C4H12NNaO7P2 •3H2O og formelvekten er 325,12. Strukturformelen er:
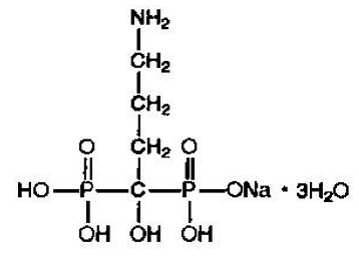
Alendronatnatrium er et hvitt, krystallinsk, ikke-hygroskopisk pulver. Det er løselig i vann, veldig lite løselig i alkohol og praktisk talt uløselig i kloroform.
FOSAMAX 70 mg tabletter for oral administrering inneholder 91,37 mg alendronatmononatriumsalttrihydrat, som er den molare ekvivalenten til 70 mg fri syre, og følgende inaktive ingredienser: mikrokrystallinsk cellulose, vannfri laktose, kroskarmellosenatrium og magnesiumstearat.
INDIKASJONER
Behandling® av osteoporose hos postmenopausale kvinner
FOSAMAX er indisert for behandling av osteoporose hos postmenopausale kvinner. Hos postmenopausale kvinner øker FOSAMAX 70mg beinmassen og reduserer forekomsten av brudd, inkludert brudd i hofte og ryggrad (frakturer av vertebrale kompresjonsbrudd). [Se Kliniske studier ]
Forebygging av osteoporose hos postmenopausale kvinner
FOSAMAX 70mg er indisert for forebygging av postmenopausal osteoporose [se Kliniske studier ].
Behandling for å øke beinmassen hos menn med osteoporose
FOSAMAX er indisert for behandling for å øke beinmassen hos menn med osteoporose [se Kliniske studier ].
Behandling av glukokortikoid-indusert osteoporose
FOSAMAX er indisert for behandling av glukokortikoid-indusert osteoporose hos menn og kvinner som får glukokortikoider i en daglig dose tilsvarende 7,5 mg eller mer av prednison og som har lav bentetthet [se Kliniske studier ].
Behandling av Pagets beinsykdom
FOSAMAX 35mg er indisert for behandling av Pagets bensykdom hos menn og kvinner. Behandling er indisert hos pasienter med Pagets bensykdom som har alkalisk fosfatase minst to ganger øvre normalgrense, eller de som er symptomatiske, eller de som har risiko for fremtidige komplikasjoner fra sykdommen. [Se Kliniske studier ]
Viktige bruksbegrensninger
Den optimale bruksvarigheten er ikke bestemt. Sikkerheten og effektiviteten til FOSAMAX for behandling av osteoporose er basert på kliniske data av fire års varighet. Alle pasienter på bisfosfonatbehandling bør ha behov for fortsatt behandling revurdert med jevne mellomrom. Pasienter med lav risiko for brudd bør vurderes å seponere medikamentet etter 3 til 5 års bruk. Pasienter som avbryter behandlingen bør få revurdert risikoen for fraktur med jevne mellomrom.
DOSERING OG ADMINISTRASJON
Selv om alendronattabletter 5 mg, 10 mg, 35 mg og 40 mg er tilgjengelige på markedet, markedsføres ikke lenger FOSAMAX 35 mg i styrkene 5 mg, 10 mg, 35 mg og 40 mg.
Selv om en mikstur av alendronat kan være tilgjengelig på markedet, markedsføres ikke lenger FOSAMAX 35 mg mikstur.
Behandling av osteoporose hos postmenopausale kvinner
Anbefalt dosering er:
- . én 70 mg tablett én gang i uken eller . en flaske med 70 mg mikstur én gang i uken eller . én 10 mg tablett én gang daglig
Forebygging av osteoporose hos postmenopausale kvinner
Anbefalt dosering er:
- . én 35 mg tablett én gang i uken eller . én 5 mg tablett én gang daglig
Behandling for å øke beinmassen hos menn med osteoporose
Anbefalt dosering er:
- . én 70 mg tablett én gang i uken eller . en flaske med 70 mg mikstur én gang i uken eller . én 10 mg tablett én gang daglig
Behandling av glukokortikoid-indusert osteoporose
Den anbefalte dosen er én 5 mg tablett én gang daglig, bortsett fra for postmenopausale kvinner som ikke får østrogen, for hvem den anbefalte dosen er én 10 mg tablett én gang daglig.
Behandling av Pagets beinsykdom
Anbefalt behandlingsregime er 40 mg én gang daglig i seks måneder.
Re-behandling av Pagets sykdom
Re-behandling med FOSAMAX 35 mg kan vurderes etter en seks måneders evalueringsperiode etter behandling hos pasienter som har fått tilbakefall, basert på økning i serum alkalisk fosfatase, som bør måles med jevne mellomrom. Re-behandling kan også vurderes hos de som ikke klarte å normalisere alkalisk fosfatase i serum.
Viktige administrasjonsinstruksjoner
Instruer pasientene til å gjøre følgende:
- . Ta FOSAMAX minst en halv time før dagens første mat, drikke eller medisinering kun med rent vann [se Informasjon om pasientveiledning ]. Andre drikker (inkludert mineralvann), mat og noen medisiner vil sannsynligvis redusere absorpsjonen av FOSAMAX [se NARKOTIKAHANDEL ]. Å vente mindre enn 30 minutter, eller ta FOSAMAX 70mg sammen med mat, drikke (annet enn vanlig vann) eller andre medisiner vil redusere effekten av FOSAMAX 70mg ved å redusere dets absorpsjon i kroppen. . Ta FOSAMAX når du står opp for dagen. For å lette tilførselen til magesekken og dermed redusere potensialet for esophageal irritasjon, bør en FOSAMAX 35 mg tablett svelges med et fullt glass vann (6-8 unser). For å lette magetømmingen bør FOSAMAX 70 mg mikstur etterfølges av minst 2 unser (en kvart kopp) vann. Pasienter bør ikke legge seg ned i minst 30 minutter og før etter dagens første mat. FOSAMAX bør ikke tas ved sengetid eller før oppreisning for dagen. Unnlatelse av å følge disse instruksjonene kan øke risikoen for uønskede opplevelser i spiserøret [se ADVARSLER OG FORHOLDSREGLER og Informasjon om pasientveiledning ].
Anbefalinger for tilskudd av kalsium og vitamin D
Instruer pasienter om å ta tilskudd av kalsium hvis diettinntaket er utilstrekkelig [se ADVARSLER OG FORHOLDSREGLER ]. Pasienter med økt risiko for vitamin D-mangel (f.eks. over 70 år, sykehjemsbundet eller kronisk syke) kan trenge vitamin D-tilskudd. Pasienter med gastrointestinale malabsorpsjonssyndromer kan kreve høyere doser av vitamin D-tilskudd og måling av 25-hydroksyvitamin D bør vurderes.
Pasienter som behandles med glukokortikoider bør få tilstrekkelige mengder kalsium og vitamin D.
Administrasjonsinstruksjoner for ubesvarte doser
Hvis en ukentlig dose av FOSAMAX glemmes, instruer pasientene om å ta en dose om morgenen etter at de har husket det. De bør ikke ta to doser på samme dag, men bør gå tilbake til å ta én dose en gang i uken, som opprinnelig planlagt på den valgte dagen.
HVORDAN LEVERES
Doseringsformer og styrker
- . 70 mg tabletter er hvite, ovale, ikke-drasjerte tabletter med kode 31 på den ene siden og et omriss av et beinbilde på den andre.
Oppbevaring og håndtering
nr. 3814 - FOSAMAX tabletter, 70 mg, er hvite, ovale, ubestrøede tabletter med kode 31 på den ene siden og en omriss av et beinbilde på den andre:
NDC 0006-0031-44 bruksenhet blisterpakning med 4 stk.
Oppbevaring
FOSAMAX tabletter
Oppbevares i en godt lukket beholder ved romtemperatur, 15-30°C (59-86°F).
Distribuert av: Merck Sharp & Dohme Corp., et datterselskap av MERCK & CO., INC., Whitehouse Station, NJ 08889, USA. Revidert: august 2019
BIVIRKNINGER
Erfaring fra kliniske forsøk
Fordi kliniske studier utføres under vidt forskjellige forhold, kan bivirkningsrater observert i kliniske studier av et medikament ikke sammenlignes direkte med rater i kliniske studier av et annet legemiddel og gjenspeiler kanskje ikke ratene observert i klinisk praksis.
Behandling av osteoporose hos postmenopausale kvinner
Daglig dosering
Sikkerheten til FOSAMAX 35 mg i behandlingen av postmenopausal osteoporose ble vurdert i fire kliniske studier som inkluderte 7453 kvinner i alderen 44-84 år. Studie 1 og studie 2 var identisk designet, treårige, placebokontrollerte, dobbeltblinde, multisenterstudier (USA og multinasjonale n=994); Studie 3 var den treårige vertebrale frakturkohorten til frakturintervensjonsforsøket [FIT] (n=2027) og studie 4 var den fireårige kliniske frakturkohorten til FIT (n=4432). Totalt ble 3620 pasienter eksponert for placebo og 3432 pasienter eksponert for FOSAMAX. Pasienter med eksisterende gastrointestinal sykdom og samtidig bruk av ikke-steroide antiinflammatoriske legemidler ble inkludert i disse kliniske studiene. I studie 1 og studie 2 fikk alle kvinner 500 mg elementært kalsium som karbonat. I studie 3 og studie 4 fikk alle kvinner med kalsiuminntak mindre enn 1000 mg per dag 500 mg kalsium og 250 internasjonale enheter vitamin D per dag.
Blant pasienter behandlet med alendronat 10 mg eller placebo i studie 1 og studie 2, og alle pasienter i studie 3 og studie 4, var forekomsten av dødelighet av alle årsaker 1,8 % i placebogruppen og 1,8 % i FOSAMAX 35 mg-gruppen. Forekomsten av alvorlige bivirkninger var 30,7 % i placebogruppen og 30,9 % i FOSAMAX-gruppen. Prosentandelen av pasienter som avbrøt studien på grunn av en klinisk bivirkning var 9,5 % i placebogruppen og 8,9 % i FOSAMAX 70 mg-gruppen. Bivirkninger fra disse studiene vurdert av etterforskerne som mulig, sannsynligvis eller definitivt medikamentrelatert hos mer enn eller lik 1 % av pasientene behandlet med enten FOSAMAX 35 mg eller placebo er presentert i tabell 1.
Utslett og erytem har oppstått.
Gastrointestinale bivirkninger
En pasient behandlet med FOSAMAX (10 mg/dag), som hadde en historie med magesår og gastrektomi og som samtidig tok aspirin, utviklet et anastomotisk sår med mild blødning, som ble ansett som medikamentrelatert. Aspirin og FOSAMAX ble seponert og pasienten ble frisk. I populasjonene i studie 1 og studie 2 hadde 49–54 % en historie med gastrointestinale lidelser ved baseline og 54–89 % brukte ikke-steroide antiinflammatoriske legemidler eller aspirin på et tidspunkt i løpet av studiene. [Se ADVARSLER OG FORHOLDSREGLER ]
Laboratorietestfunn
I dobbeltblinde, multisenter, kontrollerte studier ble asymptomatiske, milde og forbigående reduksjoner i serumkalsium og fosfat observert hos henholdsvis ca. 18 % og 10 % av pasientene som tok FOSAMAX, mot ca. 12 % og 3 % av de som tok placebo. Imidlertid var forekomsten av reduksjoner i serumkalsium til mindre enn 8,0 mg/dL (2,0 mM) og serumfosfat til mindre enn eller lik 2,0 mg/dL (0,65 mM) lik i begge behandlingsgruppene.
Ukentlig dosering
Sikkerheten til FOSAMAX 70 mg én gang ukentlig for behandling av postmenopausal osteoporose ble vurdert i en ettårig, dobbeltblind multisenterstudie som sammenlignet FOSAMAX 70 mg én gang ukentlig og FOSAMAX 10 mg daglig. De generelle sikkerhets- og tolerabilitetsprofilene for FOSAMAX 70 mg én gang i uken og FOSAMAX 10 mg daglig var like. Bivirkningene ansett av etterforskerne som mulig, sannsynlig eller definitivt medikamentrelatert hos mer enn eller lik 1 % av pasientene i begge behandlingsgruppene er presentert i tabell 2.
Forebygging av osteoporose hos postmenopausale kvinner
Daglig dosering
Sikkerheten til FOSAMAX 5 mg/dag hos postmenopausale kvinner i alderen 40-60 år har blitt evaluert i tre dobbeltblindede, placebokontrollerte studier med over 1400 pasienter randomisert til å motta FOSAMAX i enten to eller tre år. I disse studiene var de generelle sikkerhetsprofilene til FOSAMAX 5 mg/dag og placebo like. Seponering av behandlingen på grunn av en hvilken som helst klinisk bivirkning skjedde hos 7,5 % av 642 pasienter behandlet med FOSAMAX 5 mg/dag og 5,7 % av 648 pasienter behandlet med placebo.
Ukentlig dosering
Sikkerheten til FOSAMAX 35 mg én gang ukentlig sammenlignet med FOSAMAX 5 mg daglig ble evaluert i en ettårig, dobbeltblind multisenterstudie med 723 pasienter. De generelle sikkerhets- og tolerabilitetsprofilene for FOSAMAX 35 mg én gang i uken og FOSAMAX 5 mg daglig var like.
Bivirkningene fra disse studiene vurdert av etterforskerne som mulig, sannsynligvis eller definitivt medikamentrelatert hos mer enn eller lik 1 % av pasientene behandlet med enten FOSAMAX 35 mg én gang i uken, FOSAMAX 5 mg/dag eller placebo er presentert i tabell 3 .
Samtidig bruk med østrogen/hormonerstatningsterapi
I to studier (av ett og to års varighet) av postmenopausale osteoporotiske kvinner (totalt: n=853), var sikkerhets- og tolerabilitetsprofilen for kombinert behandling med FOSAMAX 10 mg én gang daglig og østrogen ± gestagen (n=354) samsvarer med de individuelle behandlingene.
Osteoporose hos menn
to placebokontrollerte, dobbeltblinde multisenterstudier på menn (en toårig studie med FOSAMAX 10 mg/dag og en ettårsstudie med FOSAMAX 70 mg én gang i uken) var frekvensen av seponering av behandlingen på grunn av kliniske bivirkninger. hendelsen var 2,7 % for FOSAMAX 10 mg/dag vs. 10,5 % for placebo, og 6,4 % for FOSAMAX 70 mg én gang i uken vs. 8,6 % for placebo. Bivirkningene ansett av etterforskerne som mulig, sannsynligvis eller definitivt medikamentrelatert hos mer enn eller lik 2 % av pasientene behandlet med enten FOSAMAX 70 mg eller placebo, er presentert i tabell 4.
Glukokortikoid-indusert osteoporose
to, ettårige, placebokontrollerte, dobbeltblinde, multisenterstudier med pasienter som fikk glukokortikoidbehandling, var den generelle sikkerhets- og tolerabilitetsprofilen for FOSAMAX 5 og 10 mg/dag generelt lik den for placebo. Bivirkningene ansett av etterforskerne som mulig, sannsynligvis eller definitivt medikamentrelatert hos mer enn eller lik 1 % av pasientene behandlet med enten FOSAMAX 5 eller 10 mg/dag eller placebo, er presentert i tabell 5.
Den generelle sikkerhets- og tolerabilitetsprofilen i den glukokortikoid-induserte osteoporosepopulasjonen som fortsatte behandlingen i det andre året av studiene (FOSAMAX: n=147) var i samsvar med det som ble observert det første året.
Pagets beinsykdom
kliniske studier (osteoporose og Pagets sykdom) var bivirkninger rapportert hos 175 pasienter som tok FOSAMAX 40 mg/dag i 3-12 måneder lik de hos postmenopausale kvinner behandlet med FOSAMAX 10 mg/dag. Imidlertid var det en tilsynelatende økt forekomst av øvre gastrointestinale bivirkninger hos pasienter som tok FOSAMAX 40 mg/dag (17,7 % FOSAMAX vs. 10,2 % placebo). Ett tilfelle av øsofagitt og to tilfeller av gastritt resulterte i seponering av behandlingen.
tillegg ble muskel- og skjelettsmerter (bein, muskler eller ledd), som er beskrevet hos pasienter med Pagets sykdom behandlet med andre bisfosfonater, av etterforskerne vurdert som mulig, sannsynligvis eller definitivt medikamentrelatert hos omtrent 6 % av pasientene behandlet med FOSAMAX 40 mg/dag versus omtrent 1 % av pasientene behandlet med placebo, men resulterte sjelden i seponering av behandlingen. Seponering av behandlingen på grunn av eventuelle kliniske bivirkninger forekom hos 6,4 % av pasientene med Pagets sykdom behandlet med FOSAMAX 40 mg/dag og 2,4 % av pasientene behandlet med placebo.
Erfaring etter markedsføring
Følgende bivirkninger er identifisert under bruk av FOSAMAX etter godkjenning. Fordi disse reaksjonene rapporteres frivillig fra en populasjon av usikker størrelse, er det ikke alltid mulig å pålitelig estimere frekvensen deres eller etablere en årsakssammenheng med legemiddeleksponering.
Kroppen som helhet: overfølsomhetsreaksjoner inkludert urticaria og angioødem. Forbigående symptomer på myalgi, ubehag, asteni og feber er rapportert med FOSAMAX, vanligvis i forbindelse med oppstart av behandling. Symptomatisk hypokalsemi har forekommet, vanligvis i forbindelse med disponerende tilstander. Perifert ødem.
Gastrointestinale: øsofagitt, esophageal erosjoner, esophageal ulcera, esophageal striktur eller perforation, og orofaryngeal ulceration. Magesår eller duodenalsår, noen alvorlige og med komplikasjoner, er også rapportert [se DOSERING OG ADMINISTRASJON ; ADVARSLER OG FORHOLDSREGLER ].
Lokalisert osteonekrose i kjeven, vanligvis assosiert med tannekstraksjon og/eller lokal infeksjon med forsinket tilheling, er rapportert [se ADVARSLER OG FORHOLDSREGLER ].
Muskuloskeletal: bein-, ledd- og/eller muskelsmerter, noen ganger alvorlige og invalidiserende [se ADVARSLER OG FORHOLDSREGLER ]; leddhevelse; lavenergi femurskaft og subtrokantære frakturer [se ADVARSLER OG FORHOLDSREGLER ].
Nervesystemet: svimmelhet og svimmelhet.
Lunge: akutte astmaforverringer.
Hud: utslett (noen ganger med lysfølsomhet), kløe, alopecia, alvorlige hudreaksjoner, inkludert Stevens-Johnsons syndrom og toksisk epidermal nekrolyse.
Spesielle sanser: uveitt, skleritt eller episkleritt. Kolesteatom i den ytre hørselskanalen (fokal osteonekrose).
NARKOTIKAHANDEL
Kalsiumtilskudd/antacida
Samtidig administrering av FOSAMAX og kalsium, antacida eller orale medisiner som inneholder multivalente kationer vil forstyrre absorpsjonen av FOSAMAX. Instruer derfor pasientene til å vente minst en halv time etter å ha tatt FOSAMAX 35 mg før de tar andre orale medisiner.
Aspirin
I kliniske studier var forekomsten av øvre gastrointestinale bivirkninger økt hos pasienter som fikk samtidig behandling med daglige doser av FOSAMAX 35 mg større enn 10 mg og aspirinholdige produkter.
Ikke-steroide antiinflammatoriske legemidler
FOSAMAX 35 mg kan gis til pasienter som tar ikke-steroide antiinflammatoriske legemidler (NSAIDs). I en 3-årig, kontrollert, klinisk studie (n=2027) der et flertall av pasientene fikk samtidig NSAID, var forekomsten av øvre gastrointestinale bivirkninger lik hos pasienter som tok FOSAMAX 5 eller 10 mg/dag sammenlignet med de som tok placebo. Siden bruk av NSAID er assosiert med gastrointestinal irritasjon, bør det imidlertid utvises forsiktighet ved samtidig bruk med FOSAMAX.
ADVARSLER
Inkludert som en del av FORHOLDSREGLER seksjon.
FORHOLDSREGLER
Øvre gastrointestinale bivirkninger
FOSAMAX 35mg, som andre bisfosfonater administrert oralt, kan forårsake lokal irritasjon av den øvre gastrointestinale slimhinnen. På grunn av disse mulige irriterende effektene og et potensial for forverring av den underliggende sykdommen, bør det utvises forsiktighet når FOSAMAX gis til pasienter med aktive øvre gastrointestinale problemer (som kjent Barretts spiserør, dysfagi, andre spiserørssykdommer, gastritt, duodenitt eller sår).
Uønskede opplevelser i spiserøret, som øsofagitt, esophageal ulcus og esophageal erosjoner, noen ganger med blødning og sjelden etterfulgt av esophageal striktur eller perforasjon, er rapportert hos pasienter som får behandling med orale bisfosfonater inkludert FOSAMAX. I noen tilfeller har disse vært alvorlige og krevd sykehusinnleggelse. Leger bør derfor være oppmerksomme på alle tegn eller symptomer som signaliserer en mulig esophageal reaksjon, og pasienter bør instrueres om å seponere FOSAMAX 70mg og søke legehjelp hvis de utvikler dysfagi, odynofagi, retrosternale smerter eller ny eller forverret halsbrann.
Risikoen for alvorlige øsofagusbivirkninger ser ut til å være større hos pasienter som legger seg etter å ha tatt orale bisfosfonater inkludert FOSAMAX 70 mg og/eller som ikke klarer å svelge orale bisfosfonater inkludert FOSAMAX 35 mg med det anbefalte fulle glasset (6-8 unser) vann, og /eller som fortsetter å ta orale bisfosfonater inkludert FOSAMAX 70 mg etter å ha utviklet symptomer som tyder på irritasjon i spiserøret. Derfor er det svært viktig at de fullstendige doseringsinstruksjonene er gitt til, og forstått av, pasienten [se DOSERING OG ADMINISTRASJON ]. Hos pasienter som ikke kan følge doseringsinstruksjonene på grunn av psykisk funksjonshemming, bør terapi med FOSAMAX brukes under passende tilsyn.
Det har vært rapporter etter markedsføring om magesår og duodenalsår med oral bisfosfonatbruk, noen alvorlige og med komplikasjoner, selv om det ikke ble observert økt risiko i kontrollerte kliniske studier [se BIVIRKNINGER ].
Mineralmetabolisme
Hypokalsemi må korrigeres før behandling med FOSAMAX startes [se KONTRAINDIKASJONER ]. Andre forstyrrelser som påvirker mineralmetabolismen (som vitamin D-mangel) bør også behandles effektivt. Hos pasienter med disse tilstandene bør serumkalsium og symptomer på hypokalsemi overvåkes under behandling med FOSAMAX.
Antagelig på grunn av effekten av FOSAMAX på økende benmineral, kan små, asymptomatiske reduksjoner i serumkalsium og fosfat forekomme, spesielt hos pasienter med Pagets sykdom, hvor forbehandlingshastigheten for beinomsetning kan være sterkt forhøyet, og i pasienter som får glukokortikoider, hvor kalsiumabsorpsjonen kan være redusert.
Å sikre tilstrekkelig kalsium- og vitamin D-inntak er spesielt viktig hos pasienter med Pagets bensykdom og hos pasienter som får glukokortikoider.
Muskel- og skjelettsmerter
Etter markedsføring er det rapportert om alvorlige og til tider invalidiserende bein-, ledd- og/eller muskelsmerter hos pasienter som tar bisfosfonater som er godkjent for forebygging og behandling av osteoporose [se BIVIRKNINGER ]. Denne kategorien medikamenter inkluderer FOSAMAX (alendronat). De fleste av pasientene var postmenopausale kvinner. Tiden til symptomdebut varierte fra én dag til flere måneder etter oppstart av legemidlet. Avbryt bruken hvis det oppstår alvorlige symptomer. De fleste pasientene hadde lindring av symptomene etter å ha stoppet. En undergruppe hadde tilbakefall av symptomer når de ble utsatt for det samme legemidlet eller et annet bisfosfonat.
I placebokontrollerte kliniske studier av FOSAMAX var prosentandelen av pasienter med disse symptomene lik i gruppene FOSAMAX 35 mg og placebo.
Osteonekrose av kjeven
Osteonekrose i kjeven (ONJ), som kan oppstå spontant, er vanligvis assosiert med tannekstraksjon og/eller lokal infeksjon med forsinket tilheling, og har blitt rapportert hos pasienter som tar bisfosfonater, inkludert FOSAMAX. Kjente risikofaktorer for osteonekrose i kjeven inkluderer invasive tannprosedyrer (f.eks. tannekstraksjon, tannimplantater, beinkirurgi), diagnose av kreft, samtidig behandling (f.eks. kjemoterapi, kortikosteroider, angiogenesehemmere), dårlig munnhygiene og komorbid. lidelser (f.eks. periodontal og/eller annen eksisterende tannsykdom, anemi, koagulopati, infeksjon, dårlig tilpassede proteser). Risikoen for ONJ kan øke med varigheten av eksponering for bisfosfonater.
For pasienter som trenger invasive tannprosedyrer, kan seponering av bisfosfonatbehandling redusere risikoen for ONJ. Klinisk vurdering av behandlende lege og/eller oral kirurg bør veilede behandlingsplanen for hver pasient basert på individuell nytte/risikovurdering.
Pasienter som utvikler osteonekrose i kjeven mens de er på bisfosfonatbehandling, bør behandles av en oral kirurg. Hos disse pasientene kan omfattende tannkirurgi for å behandle ONJ forverre tilstanden. Seponering av bisfosfonatbehandling bør vurderes basert på individuell nytte/risikovurdering.
Atypiske subtrokantære og diafysiske lårbensbrudd
Atypiske brudd med lav energi eller lavt traume i lårbensskaftet er rapportert hos pasienter behandlet med bisfosfonater. Disse bruddene kan oppstå hvor som helst i lårbensskaftet fra like under den mindre trochanter til over suprakondylær flare og er tverrgående eller kort skrå i orientering uten tegn på findeling. Årsakssammenheng er ikke fastslått da disse bruddene også forekommer hos osteoporotiske pasienter som ikke har blitt behandlet med bisfosfonater.
Atypiske lårbensbrudd oppstår oftest med minimale eller ingen traumer i det berørte området. De kan være bilaterale, og mange pasienter rapporterer prodromal smerte i det berørte området, vanligvis fremstår som kjedelig, verkende lårsmerter, uker til måneder før et fullstendig brudd oppstår. En rekke rapporter viser at pasienter også fikk behandling med glukokortikoider (f.eks. prednison) på tidspunktet for bruddet.
Enhver pasient med en historie med bisfosfonateksponering som viser seg med lår- eller lyskesmerter bør mistenkes for å ha et atypisk brudd og bør evalueres for å utelukke et ufullstendig lårbensbrudd. Pasienter med atypisk fraktur bør også vurderes for symptomer og tegn på fraktur i det kontralaterale lemmet. Avbrudd av bisfosfonatbehandling bør vurderes, i påvente av en risiko-/nyttevurdering, på individuell basis.
Nedsatt nyrefunksjon
FOSAMAX 35mg anbefales ikke for pasienter med kreatininclearance mindre enn 35 ml/min.
Glukokortikoid-indusert osteoporose
Risiko versus nytte av FOSAMAX for behandling ved daglige doser av glukokortikoider mindre enn 7,5 mg prednison eller tilsvarende er ikke fastslått [se INDIKASJONER OG BRUK ]. Før behandling påbegynnes, bør den gonade hormonstatusen til både menn og kvinner fastslås og passende erstatning vurderes.
En bentetthetsmåling bør gjøres ved oppstart av behandlingen og gjentas etter 6 til 12 måneder med kombinert FOSAMAX- og glukokortikoidbehandling.
Informasjon om pasientveiledning
Råd pasienten til å lese den FDA-godkjente pasientmerkingen ( Medisinveiledning ).
Instruer pasientene om å lese medisinveiledningen før du starter behandling med FOSAMAX og å lese den på nytt hver gang resepten fornyes.
Osteoporose-anbefalinger, inkludert kalsium- og vitamin D-tilskudd
Instruer pasienter om å ta tilskudd av kalsium og vitamin D hvis det daglige kostinntaket er utilstrekkelig. Vektbærende trening bør vurderes sammen med modifisering av visse atferdsfaktorer, for eksempel sigarettrøyking og/eller overdreven alkoholforbruk, hvis disse faktorene eksisterer.
Doseringsinstruksjoner
Instruer pasientene om at de forventede fordelene med FOSAMAX 70 mg bare kan oppnås når det tas med rent vann, det første når det oppstår for dagen minst 30 minutter før dagens første mat, drikke eller medisinering. Selv dosering med appelsinjuice eller kaffe har vist seg å redusere absorpsjonen av FOSAMAX markant [se KLINISK FARMAKOLOGI ].
Instruer pasienter om ikke å tygge eller suge på tabletten på grunn av en mulighet for orofaryngeal sårdannelse.
Instruer pasientene til å svelge hver tablett med FOSAMAX med et fullt glass vann (6-8 gram) for å lette tilførselen til magen og dermed redusere potensialet for esophageal irritasjon. Instruer pasienter om å drikke minst 2 unser (en kvart kopp) vann etter å ha tatt FOSAMAX 70 mg mikstur, for å lette magetømming.
Instruer pasientene til å ikke legge seg ned i minst 30 minutter og før etter dagens første mat.
Instruer pasienter om ikke å ta FOSAMAX ved sengetid eller før de står opp for dagen. Pasienter bør informeres om at unnlatelse av å følge disse instruksjonene kan øke risikoen for esophageal problemer.
Instruer pasienter om at hvis de utvikler symptomer på esophageal sykdom (som svelgevansker eller smerter ved svelging, retrosternale smerter eller ny eller forverret halsbrann), bør de slutte å ta FOSAMAX og konsultere legen sin.
Hvis pasienter glemmer en dose på FOSAMAX 70 mg én gang i uken, instruer pasientene om å ta en dose om morgenen etter at de har husket det. De bør ikke ta to doser på samme dag, men bør gå tilbake til å ta én dose en gang i uken, som opprinnelig planlagt på den valgte dagen.
Ikke-klinisk toksikologi
Karsinogenese, mutagenese, svekkelse av fruktbarhet
Harderian kjertel (en retro-orbital kjertel som ikke finnes hos mennesker) adenomer ble økt hos høydose hunnmus (p=0,003) i en 92-ukers oral karsinogenitetsstudie ved doser av alendronat på 1, 3 og 10 mg/kg/ dag (hanner) eller 1, 2 og 5 mg/kg/dag (kvinner). Disse dosene tilsvarer omtrent 0,1 til 1 ganger den høyeste anbefalte kliniske daglige dosen på 40 mg basert på overflateareal, mg/m². Relevansen av dette funnet for mennesker er ukjent.
Parafollikulære celle (skjoldbruskkjertel) adenomer ble økt hos høydose hannrotter (p=0,003) i en 2-årig oral karsinogenitetsstudie ved doser på 1 og 3,75 mg/kg kroppsvekt. Disse dosene tilsvarer omtrent 0,3 og 1 ganger den kliniske daglige dosen på 40 mg basert på overflateareal, mg/m². Relevansen av dette funnet for mennesker er ukjent.
Alendronat var ikke genotoksisk i in vitro mikrobiell mutageneseanalyse med og uten metabolsk aktivering, i en in vitro pattedyrcellemutageneseanalyse, i en in vitro alkalisk elueringsanalyse i rottehepatocytter og i en in vivo kromosomavviksanalyse hos mus. I en in vitro kromosomavviksanalyse i eggstokkceller fra kinesisk hamster ga imidlertid alendronat tvetydige resultater.
Alendronat hadde ingen effekt på fertilitet (hann eller hunn) hos rotter ved orale doser opptil 5 mg/kg/dag (ca. 1 ganger 40 mg klinisk daglig dose basert på overflateareal, mg/m²).
Bruk i spesifikke populasjoner
Svangerskap
Risikosammendrag
Tilgjengelige data om bruk av FOSAMAX hos gravide kvinner er utilstrekkelige til å informere om en legemiddelrelatert risiko for uønskede utfall hos mor eller foster. Seponer FOSAMAX 35mg når graviditet er anerkjent.
reproduksjonsstudier på dyr viste daglig oral administrering av alendronat til rotter fra før paring til slutten av drektighet eller laktasjon redusert postimplantasjonsoverlevelse og redusert kroppsvektøkning hos valpene som startet med doser tilsvarende mindre enn halvparten av den høyeste anbefalte kliniske daglige dosen på 40 mg ( basert på kroppsoverflate, mg/m²). Oral administrering av alendronat til rotter under organogenese resulterte i redusert fosterforbening med doser 3 ganger 40 mg klinisk daglig dose. Ingen lignende fostereffekter ble observert hos drektige kaniner gitt oralt under organogenese ved doser tilsvarende ca. 10 ganger den kliniske daglige dosen på 40 mg.
Forsinket eller mislykket fødsel av avkom, langvarig fødsel og sen graviditet dødsfall hos mor og foster på grunn av mors hypokalsemi oppstod hos rotter ved orale doser så lave som en tidel av den kliniske daglige dosen på 40 mg (se Data ).
Bisfosfonater er inkorporert i benmatrisen, hvorfra de gradvis frigjøres over en periode på år. Mengden bisfosfonat som er inkorporert i ben hos voksne og tilgjengelig for frigjøring i den systemiske sirkulasjonen er direkte relatert til dosen og varigheten av bisfosfonatbruken. Basert på virkningsmekanismen til bisfosfonater er det følgelig en potensiell risiko for fosterskader, hovedsakelig skjelett, hvis en kvinne blir gravid etter å ha fullført en bisfosfonatbehandlingskur. Effekten av variabler som tid mellom seponering av bisfosfonatterapi til unnfangelse, det bestemte bisfosfonatet som brukes og administreringsveien (intravenøs versus oral) på risikoen er ikke studert.
Estimert bakgrunnsrisiko for alvorlige fødselsskader og spontanabort for den eller de angitte populasjonene er ukjent. Alle graviditeter har en bakgrunnsrisiko for fødselsskader, tap eller andre uheldige utfall. I den generelle befolkningen i USA er den estimerte bakgrunnsrisikoen for alvorlige fødselsskader og spontanabort i klinisk anerkjente svangerskap henholdsvis 2-4 % og 15-20 %.
Data
Dyredata
Reproduksjonsstudier på rotter doseret oralt fra før paring til slutten av drektighet eller laktasjon viste redusert postimplantasjonsoverlevelse fra 2 mg/kg/dag og redusert kroppsvektøkning fra 1 mg/kg/dag, doser tilsvarende mindre enn halvparten av de 40 mg klinisk daglig dose basert på kroppsoverflate, mg/m². Forekomsten av ufullstendig føtal ossifikasjon i vertebrale, hodeskalle og sternebrale bein økte hos rotter som ble doseret oralt under organogenese som startet med 10 mg/kg/dag (omtrent 3 ganger den kliniske daglige dosen på 40 mg). Ingen lignende fostereffekter ble observert hos drektige kaniner gitt oralt under organogenese med opptil 35 mg/kg/dag (tilsvarer ca. 10 ganger den kliniske daglige dosen på 40 mg).
Både totalt og ionisert kalsium reduserte hos gravide rotter som ble doseret oralt med 15 mg/kg/dag alendronat (ca. 4 ganger den kliniske daglige dosen på 40 mg), noe som resulterte i forsinkelser og leveringssvikt. Langvarig fødsel på grunn av maternell hypokalsemi ble observert når rotter ble behandlet fra før paring og fram til svangerskapet startet med 0,5 mg/kg/dag (omtrent en tidel av den kliniske daglige dosen på 40 mg). Maternotoksisitet (dødsfall i sen graviditet) forekom også hos hunnrotter behandlet oralt med 15 mg/kg/dag (ca. 4 ganger den kliniske daglige dosen på 40 mg) i varierende svangerskapsperioder. Disse mødredødsfallene ble redusert, men ikke eliminert ved avslutning av behandlingen. Kalsiumtilskudd i drikkevannet eller med subkutan minipumpe til rotter doseret oralt med 15 mg/kg/dag alendronat kunne ikke lindre hypokalsemien eller forhindre dystokierelaterte mødre- og neonatale dødsfall. Imidlertid forhindret intravenøs kalsiumtilskudd mors, men ikke neonatale dødsfall.
Amming
Risikosammendrag
Det er ikke kjent om alendronat er tilstede i morsmelk hos mennesker, påvirker produksjonen av brystmelk eller har effekter på spedbarn som ammes. De utviklingsmessige og helsemessige fordelene ved amming bør vurderes sammen med morens kliniske behov for FOSAMAX 70mg og eventuelle skadelige effekter på det ammede barnet fra FOSAMAX eller fra den underliggende morstilstanden.
Pediatrisk bruk
FOSAMAX 70mg er ikke indisert for bruk hos pediatriske pasienter.
Sikkerheten og effekten av FOSAMAX ble undersøkt i en randomisert, dobbeltblind, placebokontrollert to-års studie av 139 pediatriske pasienter i alderen 4-18 år med alvorlig osteogenesis imperfecta (OI). Ett hundre og ni pasienter ble randomisert til 5 mg FOSAMAX 35 mg daglig (vekt mindre enn 40 kg) eller 10 mg FOSAMAX 70 mg daglig (vekt større enn eller lik 40 kg) og 30 pasienter til placebo. Gjennomsnittlig baseline lumbalcolumn BMD Z-score for pasientene var -4,5. Gjennomsnittlig endring i lumbalcolumna BMD Z-score fra baseline til måned 24 var 1,3 hos FOSAMAX 35 mg-behandlede pasienter og 0,1 hos placebobehandlede pasienter. Behandling med FOSAMAX 35 mg reduserte ikke risikoen for brudd. 16 prosent av FOSAMAX-pasientene som fikk et radiologisk bekreftet brudd innen måned 12 av studien, hadde forsinket bruddtilheling (callus-remodellering) eller fraktur som ikke var sammenføyd når de ble vurdert radiografisk ved 24. måned sammenlignet med 9 % av de placebobehandlede pasientene. Hos FOSAMAX-behandlede pasienter viste benhistomorfometridata oppnådd ved måned 24 redusert beinomsetning og forsinket mineraliseringstid; det var imidlertid ingen mineraliseringsfeil. Det var ingen statistisk signifikante forskjeller mellom FOSAMAX 35 mg og placebogruppene i reduksjon av beinsmerter. Den orale biotilgjengeligheten hos barn var lik den som ble observert hos voksne.
Den generelle sikkerhetsprofilen til FOSAMAX hos pasienter med osteogenesis imperfecta behandlet i opptil 24 måneder var generelt lik den for voksne med osteoporose behandlet med FOSAMAX. Imidlertid var det en økt forekomst av oppkast hos pasienter med osteogenesis imperfecta behandlet med FOSAMAX sammenlignet med placebo. I løpet av den 24 måneder lange behandlingsperioden ble oppkast observert hos 32 av 109 (29,4 %) pasienter behandlet med FOSAMAX 70 mg og 3 av 30 (10 %) pasienter behandlet med placebo.
I en farmakokinetisk studie utviklet 6 av 24 pediatriske osteogenesis imperfecta-pasienter som fikk en enkelt oral dose av FOSAMAX 35 eller 70 mg feber, influensalignende symptomer og/eller mild lymfocytopeni innen 24 til 48 timer etter administrering. Disse hendelsene, som ikke varer mer enn 2 til 3 dager og responderer på paracetamol, samsvarer med en akuttfaserespons som er rapportert hos pasienter som får bisfosfonater, inkludert FOSAMAX. [Se BIVIRKNINGER ]
Geriatrisk bruk
Av pasientene som fikk FOSAMAX i Fracture Intervention Trial (FIT), var 71 % (n=2302) eldre enn eller lik 65 år og 17 % (n=550) var større enn eller lik 75 år. Av pasientene som får FOSAMAX 70 mg i USA og multinasjonale osteoporosebehandlingsstudier hos kvinner, osteoporosestudier hos menn, glukokortikoidinduserte osteoporosestudier og Pagets sykdomsstudier [se Kliniske studier ], henholdsvis 45 %, 54 %, 37 % og 70 % var 65 år eller eldre. Ingen generelle forskjeller i effekt eller sikkerhet ble observert mellom disse pasientene og yngre pasienter, men større sensitivitet hos enkelte eldre individer kan ikke utelukkes.
Nedsatt nyrefunksjon
FOSAMAX 70mg anbefales ikke for pasienter med kreatininclearance mindre enn 35 ml/min. Ingen dosejustering er nødvendig hos pasienter med kreatininclearance-verdier mellom 35-60 ml/min [se KLINISK FARMAKOLOGI ].
Nedsatt leverfunksjon
Siden det er bevis på at alendronat ikke metaboliseres eller skilles ut i gallen, ble det ikke utført studier på pasienter med nedsatt leverfunksjon. Ingen dosejustering er nødvendig [se KLINISK FARMAKOLOGI ].
OVERDOSE
Signifikant dødelighet etter orale enkeltdoser ble sett hos hunnrotter og mus ved henholdsvis 552 mg/kg (3256 mg/m²) og 966 mg/kg (2898 mg/m²). Hos menn var disse verdiene litt høyere, henholdsvis 626 og 1280 mg/kg. Det var ingen dødelighet hos hunder ved orale doser opp til 200 mg/kg (4000 mg/m²).
Ingen spesifikk informasjon er tilgjengelig om behandling av overdosering med FOSAMAX. Hypokalsemi, hypofosfatemi og øvre gastrointestinale bivirkninger, som urolig mage, halsbrann, øsofagitt, gastritt eller sår, kan skyldes oral overdosering. Melk eller syrenøytraliserende midler bør gis for å binde alendronat. På grunn av risikoen for esophageal irritasjon, bør ikke brekninger fremkalles og pasienten skal forbli helt oppreist.
Dialyse ville ikke være gunstig.
KONTRAINDIKASJONER
FOSAMAX 35mg er kontraindisert hos pasienter med følgende tilstander:
- . Unormaliteter i spiserøret som forsinker tømming av spiserøret som striktur eller akalasi [se ADVARSLER OG FORHOLDSREGLER ] . Manglende evne til å stå eller sitte oppreist i minst 30 minutter [se DOSERING OG ADMINISTRASJON ; ADVARSLER OG FORHOLDSREGLER ] . Ikke administrer FOSAMAX 35 mg mikstur til pasienter med økt risiko for aspirasjon. . Hypokalsemi [se ADVARSLER OG FORHOLDSREGLER ] . Overfølsomhet overfor noen komponent i dette produktet. Overfølsomhetsreaksjoner inkludert urticaria og angioødem er rapportert [se BIVIRKNINGER ].
KLINISK FARMAKOLOGI
Virkningsmekanismen
Dyrestudier har indikert følgende virkemåte. På cellulært nivå viser alendronat foretrukket lokalisering til steder for benresorpsjon, spesielt under osteoklaster. Osteoklastene fester seg normalt til benoverflaten, men mangler den rufsete kanten som indikerer aktiv resorpsjon. Alendronat forstyrrer ikke rekruttering eller tilknytning av osteoklaster, men det hemmer osteoklastaktivitet. Studier på mus på lokalisering av radioaktivt [3H]alendronat i bein viste omtrent 10 ganger høyere opptak på osteoklastoverflater enn på osteoblastoverflater. Bein undersøkt 6 og 49 dager etter administrering av [3H]alendronat i henholdsvis rotter og mus, viste at normalt bein ble dannet på toppen av alendronatet, som var inkorporert inne i matrisen. Mens det er inkorporert i benmatrise, er ikke alendronat farmakologisk aktivt. Derfor må alendronat administreres kontinuerlig for å undertrykke osteoklaster på nydannede resorpsjonsoverflater. Histomorfometri hos bavianer og rotter viste at alendronatbehandling reduserer beinomsetning (dvs. antall steder hvor bein omdannes). I tillegg overstiger bendannelsen benresorpsjonen ved disse ombyggingsstedene, noe som fører til progressiv økning i benmasse.

Farmakodynamikk
Alendronat er et bisfosfonat som binder seg til benhydroksyapatitt og spesifikt hemmer aktiviteten til osteoklaster, de benresorberende cellene. Alendronat reduserer benresorpsjon uten direkte effekt på bendannelse, selv om sistnevnte prosess til slutt reduseres fordi benresorpsjon og bendannelse kobles sammen under beinomsetning.
Osteoporose hos postmenopausale kvinner
Osteoporose er preget av lav benmasse som fører til økt risiko for brudd. Diagnosen kan bekreftes ved funn av lav benmasse, tegn på brudd på røntgen, en historie med osteoporotisk fraktur, eller høydetap eller kyfose, noe som tyder på vertebralt (spinal) brudd. Osteoporose forekommer hos både menn og kvinner, men er mest vanlig blant kvinner etter overgangsalderen, når beinomsetningen øker og benresorpsjonshastigheten overstiger bendannelsen. Disse endringene resulterer i progressivt bentap og fører til osteoporose hos en betydelig andel kvinner over 50 år. Brudd, vanligvis i ryggraden, hoften og håndleddet, er de vanlige konsekvensene. Fra 50 år til 90 år øker risikoen for hoftebrudd hos hvite kvinner 50 ganger og risikoen for vertebrale frakturer 15 til 30 ganger. Det er anslått at omtrent 40 % av 50 år gamle kvinner vil pådra seg ett eller flere osteoporose-relaterte brudd i ryggraden, hoften eller håndleddet i løpet av resten av livet. Spesielt hoftebrudd er assosiert med betydelig sykelighet, funksjonshemming og dødelighet.
Daglige orale doser av alendronat (5, 20 og 40 mg i seks uker) hos postmenopausale kvinner ga biokjemiske endringer som indikerte doseavhengig hemming av benresorpsjon, inkludert reduksjoner i urinkalsium og urinmarkører for benkollagennedbrytning (som deoksypyridinolin og kryss- koblede N-telopeptider av type I kollagen). Disse biokjemiske endringene hadde en tendens til å gå tilbake til baseline-verdier så tidlig som 3 uker etter seponering av alendronatbehandling og skilte seg ikke fra placebo etter 7 måneder.
Langtidsbehandling av osteoporose med FOSAMAX 10 mg/dag (i inntil fem år) reduserte urinutskillelse av markører for benresorpsjon, deoksypyridinolin og tverrbundne N-telopeptider av type l kollagen med henholdsvis ca. 50 % og 70 %. , for å nå nivåer som ligner på de man ser hos friske premenopausale kvinner. Lignende reduksjoner ble sett hos pasienter i osteoporoseforebyggende studier som fikk FOSAMAX 5 mg/dag. Nedgangen i benresorpsjonshastigheten indikert av disse markørene var tydelig så tidlig som en måned og nådde etter tre til seks måneder et platå som ble opprettholdt under hele behandlingen med FOSAMAX. I osteoporosebehandlingsstudier reduserte FOSAMAX 10 mg/dag markørene for bendannelse, osteokalsin og benspesifikk alkalisk fosfatase med ca. 50 %, og total serum alkalisk fosfatase med ca. 25 til 30 % for å nå et platå etter 6 til 12 måneder. I osteoporoseforebyggende studier reduserte FOSAMAX 5 mg/dag osteokalsin og total serum alkalisk fosfatase med henholdsvis ca. 40 % og 15 %. Lignende reduksjoner i beinomsetningshastigheten ble observert hos postmenopausale kvinner i løpet av ett års studier med FOSAMAX 70 mg én gang i uken for behandling av osteoporose og én gang ukentlig FOSAMAX 35 mg for forebygging av osteoporose. Disse dataene indikerer at beinomsetningshastigheten nådde en ny steady-state, til tross for den progressive økningen i den totale mengden alendronat avsatt i beinet.
Som et resultat av hemming av benresorpsjon ble det også observert asymptomatiske reduksjoner i serumkalsium- og fosfatkonsentrasjoner etter behandling med FOSAMAX. I langtidsstudiene var reduksjoner fra baseline i serumkalsium (omtrent 2 %) og fosfat (omtrent 4 til 6 %) tydelig den første måneden etter oppstart av FOSAMAX 10 mg. Ingen ytterligere reduksjoner i serumkalsium ble observert i løpet av den femårige behandlingen; serumfosfat gikk imidlertid tilbake til forstudienivåer i løpet av årene tre til fem. Lignende reduksjoner ble observert med FOSAMAX 5 mg/dag. I ettårsstudier med FOSAMAX 35 og 70 mg én gang i uken ble lignende reduksjoner observert etter 6 og 12 måneder. Reduksjonen i serumfosfat kan reflektere ikke bare den positive benmineralbalansen på grunn av FOSAMAX 70mg, men også en reduksjon i nyreabsorpsjon av fosfat.
Osteoporose hos menn
Behandling av menn med osteoporose med FOSAMAX 10 mg/dag i to år reduserte urinutskillelsen av kryssbundne N-telopeptider av type I kollagen med ca. 60 % og benspesifikk alkalisk fosfatase med ca. 40 %. Lignende reduksjoner ble observert i en ettårig studie hos menn med osteoporose som fikk FOSAMAX 70 mg en gang i uken.
Glukokortikoid-indusert osteoporose
Vedvarende bruk av glukokortikoider er ofte assosiert med utvikling av osteoporose og resulterende frakturer (spesielt vertebral, hofte og ribben). Det forekommer både hos menn og kvinner i alle aldre. Osteoporose oppstår som et resultat av hemmet bendannelse og økt benresorpsjon som resulterer i netto bentap. Alendronat reduserer benresorpsjon uten å direkte hemme beindannelse.
kliniske studier på opptil to år' varighet, FOSAMAX 5 og 10 mg/dag reduserte tverrbundne N-telopeptider av type I kollagen (en markør for benresorpsjon) med ca. 60 % og reduserte benspesifikk alkalisk fosfatase og total serum alkalisk fosfatase (markører for bendannelse) ved henholdsvis ca. 15 til 30 % og 8 til 18 %. Som et resultat av hemming av benresorpsjon, induserte FOSAMAX 5 og 10 mg/dag asymptomatiske reduksjoner i serumkalsium (ca. 1 til 2 %) og serumfosfat (ca. 1 til 8 %).
Pagets beinsykdom
Pagets bensykdom er en kronisk fokal skjelettlidelse preget av sterkt økt og uordnet beinremodellering. Overdreven osteoklastisk benresorpsjon etterfølges av osteoblastisk ny beindannelse, noe som fører til erstatning av normal benarkitektur med uorganisert, forstørret og svekket benstruktur.
Kliniske manifestasjoner av Pagets sykdom varierer fra ingen symptomer til alvorlig sykelighet på grunn av beinsmerter, bendeformitet, patologiske frakturer og nevrologiske og andre komplikasjoner. Alkalisk fosfatase i serum, den mest brukte biokjemiske indeksen for sykdomsaktivitet, gir et objektivt mål på sykdommens alvorlighetsgrad og respons på terapi.
FOSAMAX 70mg reduserer beinresorpsjonshastigheten direkte, noe som fører til en indirekte reduksjon i beindannelse. I kliniske studier ga FOSAMAX 40 mg én gang daglig i seks måneder signifikante reduksjoner i serum alkalisk fosfatase så vel som i urinmarkører for nedbrytning av benkollagen. Som et resultat av hemming av benresorpsjon, induserte FOSAMAX generelt milde, forbigående og asymptomatiske reduksjoner i serumkalsium og -fosfat.
Farmakokinetikk
Absorpsjon
forhold til en intravenøs referansedose var gjennomsnittlig oral biotilgjengelighet av alendronat hos kvinner 0,64 % for doser fra 5 til 70 mg når det ble administrert etter en faste over natten og to timer før en standardisert frokost. Oral biotilgjengelighet av 10 mg tabletten hos menn (0,59 %) var lik den hos kvinner når den ble administrert etter faste over natten og 2 timer før frokost.
FOSAMAX 70 mg mikstur og FOSAMAX 70 mg tablett er like biotilgjengelige.
En studie som undersøkte effekten av timing av et måltid på biotilgjengeligheten av alendronat ble utført hos 49 postmenopausale kvinner. Biotilgjengelighet ble redusert (med omtrent 40 %) når 10 mg alendronat ble administrert enten 0,5 eller 1 time før en standardisert frokost, sammenlignet med dosering 2 timer før spising. I studier av behandling og forebygging av osteoporose var alendronat effektivt når det ble administrert minst 30 minutter før frokost.
Biotilgjengelighet var ubetydelig enten alendronat ble administrert sammen med eller opptil to timer etter en standardisert frokost. Samtidig administrering av alendronat og kaffe eller appelsinjuice reduserte biotilgjengeligheten med ca. 60 %.
Fordeling
Prekliniske studier (på hannrotter) viser at alendronat forbigående distribueres til bløtvev etter 1 mg/kg intravenøs administrering, men deretter raskt omfordeles til bein eller utskilles i urinen. Gjennomsnittlig steady-state distribusjonsvolum, eksklusive bein, er minst 28 L hos mennesker. Konsentrasjoner av legemiddel i plasma etter terapeutiske orale doser er for lave (mindre enn 5 ng/ml) for analytisk påvisning. Proteinbinding i humant plasma er omtrent 78 %.
Metabolisme
Det er ingen bevis for at alendronat metaboliseres hos dyr eller mennesker.
Utskillelse
Etter en enkelt intravenøs dose av [14C]alendronat ble omtrent 50 % av radioaktiviteten skilt ut i urinen innen 72 timer, og lite eller ingen radioaktivitet ble gjenfunnet i avføringen. Etter en enkelt 10 mg intravenøs dose var renal clearance av alendronat 71 ml/min (64, 78; 90 % konfidensintervall [CI]), og systemisk clearance oversteg ikke 200 ml/min. Plasmakonsentrasjoner falt med mer enn 95 % innen 6 timer etter intravenøs administrering. Den terminale halveringstiden hos mennesker er estimert til å overstige 10 år, noe som sannsynligvis gjenspeiler frigjøring av alendronat fra skjelettet. Basert på ovenstående anslås det at etter 10 års oral behandling med FOSAMAX (10 mg daglig) er mengden alendronat som frigjøres daglig fra skjelettet ca. 25 % av den som absorberes fra mage-tarmkanalen.
Spesifikke populasjoner
Kjønn
Biotilgjengeligheten og andelen av en intravenøs dose som skilles ut i urinen var lik hos menn og kvinner.
Geriatrisk
Biotilgjengelighet og disposisjon (utskillelse i urin) var lik hos eldre og yngre pasienter. Ingen dosejustering er nødvendig hos eldre pasienter.
Løp
Farmakokinetiske forskjeller på grunn av rase er ikke studert.
Nedsatt nyrefunksjon
Prekliniske studier viser at hos rotter med nyresvikt er økende mengder medikament tilstede i plasma, nyre, milt og tibia. Hos friske kontroller skilles legemidler som ikke er avsatt i bein raskt ut i urinen. Ingen tegn på metning av beinopptak ble funnet etter 3 ukers dosering med kumulative intravenøse doser på 35 mg/kg hos unge hannrotter. Selv om det ikke er utført noen formell farmakokinetisk studie med nedsatt nyrefunksjon hos pasienter, er det sannsynlig at, som hos dyr, vil eliminering av alendronat via nyrene bli redusert hos pasienter med nedsatt nyrefunksjon. Derfor kan det forventes noe større akkumulering av alendronat i bein hos pasienter med nedsatt nyrefunksjon.
Ingen dosejustering er nødvendig for pasienter med kreatininclearance 35 til 60 ml/min. FOSAMAX 35 mg anbefales ikke til pasienter med kreatininclearance mindre enn 35 ml/min på grunn av manglende erfaring med alendronat ved nyresvikt.
Nedsatt leverfunksjon
Siden det er bevis på at alendronat ikke metaboliseres eller skilles ut i gallen, ble det ikke utført studier på pasienter med nedsatt leverfunksjon. Ingen dosejustering er nødvendig.
Narkotikahandel
Intravenøs ranitidin ble vist å doble biotilgjengeligheten av oralt alendronat. Den kliniske betydningen av denne økte biotilgjengeligheten og om lignende økninger vil forekomme hos pasienter som får orale H2-antagonister er ukjent.
Hos friske forsøkspersoner ga oral prednison (20 mg tre ganger daglig i fem dager) ingen klinisk betydningsfull endring i den orale biotilgjengeligheten av alendronat (en gjennomsnittlig økning fra 20 til 44 %).
Produkter som inneholder kalsium og andre multivalente kationer vil sannsynligvis forstyrre absorpsjonen av alendronat.
Dyretoksikologi og/eller farmakologi
De relative hemmende aktivitetene på benresorpsjon og mineralisering av alendronat og etidronat ble sammenlignet i Schenk-analysen, som er basert på histologisk undersøkelse av epifysene til voksende rotter. I denne analysen var den laveste dosen av alendronat som interfererte med benmineralisering (som førte til osteomalaci) 6000 ganger den antiresorptive dosen. Det tilsvarende forholdet for etidronat var én til én. Disse dataene tyder på at alendronat administrert i terapeutiske doser er svært usannsynlig å indusere osteomalaci.
Kliniske studier
Behandling av osteoporose hos postmenopausale kvinner
Daglig dosering
Effekten av FOSAMAX 10 mg daglig ble vurdert i fire kliniske studier. Studie 1, en treårig, multisenter, dobbeltblind, placebokontrollert, amerikansk klinisk studie inkluderte 478 pasienter med en BMD T-score på eller under minus 2,5 med eller uten tidligere vertebralfraktur; Studie 2, en treårig, multisenter, dobbeltblind, placebokontrollert multinasjonal klinisk studie inkluderte 516 pasienter med en BMD T-score på eller under minus 2,5 med eller uten tidligere vertebralfraktur; Studie 3, Three-Year Study of the Fracture Intervention Trial (FIT), en studie som inkluderte 2027 postmenopausale pasienter med minst ett vertebralt brudd ved baseline; og Studie 4, Four-Year Study of FIT: en studie som inkluderte 4432 postmenopausale pasienter med lav benmasse, men uten baseline vertebral fraktur.
Effekt på bruddforekomst
For å vurdere effekten av FOSAMAX på forekomsten av vertebrale frakturer (oppdaget ved digitalisert radiografi; omtrent en tredjedel av disse var klinisk symptomatiske), ble de amerikanske og multinasjonale studiene kombinert i en analyse som sammenlignet placebo med de sammenslåtte doseringsgruppene av FOSAMAX (5 eller 10 mg i tre år eller 20 mg i to år etterfulgt av 5 mg i ett år). Det var en statistisk signifikant reduksjon i andelen pasienter behandlet med FOSAMAX 70 mg som fikk ett eller flere nye vertebrale frakturer sammenlignet med de som ble behandlet med placebo (3,2 % vs. 6,2 %; en relativ risikoreduksjon på 48 %). En reduksjon i det totale antallet nye vertebrale frakturer (4,2 vs. 11,3 per 100 pasienter) ble også observert. I den samlede analysen hadde pasienter som fikk FOSAMAX et tap i statur som var statistisk signifikant mindre enn det som ble observert hos de som fikk placebo (-3,0 mm vs. -4,6 mm).
Fracture Intervention Trial (FIT) besto av to studier på postmenopausale kvinner: treårsstudien av pasienter som hadde minst ett radiografisk vertebralt fraktur ved baseline og fireårsstudien av pasienter med lav benmasse, men uten baseline vertebral fraktur. I begge studiene av FIT fullførte 96 % av randomiserte pasienter studiene (dvs. hadde et avslutningsbesøk ved den planlagte slutten av studien); ca. 80 % av pasientene tok fortsatt studiemedisin etter fullføring.
Frakturintervensjonsforsøk: treårig studie (pasienter med minst ett radiografisk vertebralt brudd ved baseline)
Denne randomiserte, dobbeltblinde, placebokontrollerte, 2027-pasientstudien (FOSAMAX 70mg, n=1022; placebo, n=1005) viste at behandling med FOSAMAX resulterte i statistisk signifikant reduksjon i bruddforekomst etter tre år som vist i tabell 6 .
Videre, i denne populasjonen av pasienter med baseline vertebral fraktur, reduserte behandling med FOSAMAX signifikant forekomsten av sykehusinnleggelser (25,0 % vs. 30,7 %).
I den treårige studien av FIT oppsto brudd i hoften hos 22 (2,2 %) av 1005 pasienter på placebo og 11 (1,1 %) av 1022 pasienter på FOSAMAX, p=0,047. Figur 1 viser den kumulative forekomsten av hoftebrudd i denne studien.
Figur 1: Kumulativ forekomst av hoftebrudd i den treårige studien av FIT (pasienter med radiografisk vertebral fraktur ved baseline)
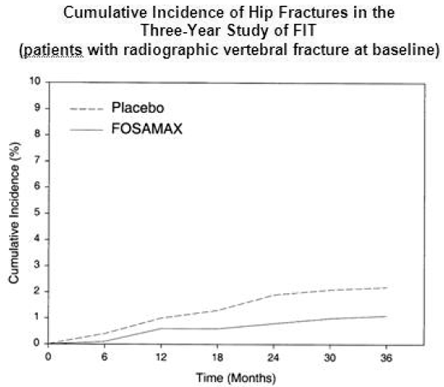
Frakturintervensjonsforsøk: Fireårig studie (pasienter med lav benmasse, men uten baseline radiografisk vertebral fraktur)
Denne randomiserte, dobbeltblinde, placebokontrollerte studien med 4432 pasienter (FOSAMAX 70mg, n=2214; placebo, n=2218) undersøkte ytterligere reduksjonen i bruddforekomst på grunn av FOSAMAX. Hensikten med studien var å rekruttere kvinner med osteoporose, definert som en baseline lårhals-BMD minst to standardavvik under gjennomsnittet for unge voksne kvinner. På grunn av påfølgende revisjoner av de normative verdiene for lårhals-BMD, ble det funnet at 31 % av pasientene ikke oppfyller dette inngangskriteriet, og derfor inkluderte denne studien både osteoporotiske og ikke-nosteoporotiske kvinner. Resultatene er vist i tabell 7 for pasientene med osteoporose.
Bruddresultater på tvers av studier
den treårige studien av FIT reduserte FOSAMAX 35 mg prosentandelen kvinner som opplevde minst ett nytt radiografisk vertebralt brudd fra 15,0 % til 7,9 % (47 % relativ risikoreduksjon, p
FOSAMAX reduserte prosentandelen kvinner som opplevde flere (to eller flere) nye vertebrale frakturer fra 4,2 % til 0,6 % (87 % relativ risikoreduksjon, p
Dermed reduserte FOSAMAX 35 mg forekomsten av radiografiske vertebrale frakturer hos osteoporotiske kvinner enten de hadde et tidligere radiografisk vertebralt fraktur eller ikke.
Effekt på beinmineraltetthet
Benmineraltetthetens effekt av FOSAMAX 10 mg én gang daglig hos postmenopausale kvinner, 44 til 84 år, med osteoporose (benmineraltetthet i lumbal ryggrad [BMD] på minst 2 standardavvik under premenopausalt gjennomsnitt) ble påvist i fire dobbelt- blinde, placebokontrollerte kliniske studier på to eller tre år' varighet.
Figur 2 viser gjennomsnittlig økning i BMD i korsryggen, lårhalsen og trochanter hos pasienter som får FOSAMAX 10 mg/dag i forhold til placebobehandlede pasienter etter tre år for hver av disse studiene.
Figur 2: Osteoporosebehandlingsstudier hos postmenopausale kvinner Økning i BMD FOSAMAX 10 mg/dag etter tre år
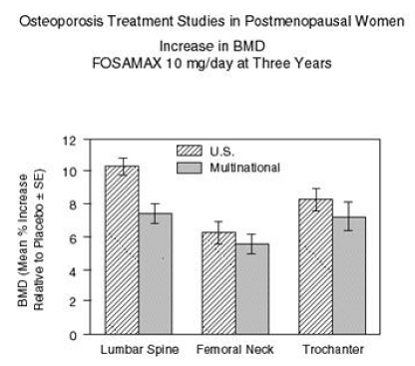
Etter tre år ble signifikant økning i BMD, i forhold til både baseline og placebo, sett på hvert målested i hver studie hos pasienter som fikk FOSAMAX 10 mg/dag. BMD i hele kroppen økte også betydelig i hver studie, noe som tyder på at økningen i beinmasse i ryggraden og hoften ikke skjedde på bekostning av andre skjelettsteder. Økning i BMD var tydelig allerede i tre måneder og fortsatte gjennom de tre årene med behandling. (Se figur 3 for lumbale ryggradsresultater.) I den toårige forlengelsen av disse studiene, resulterte behandling av 147 pasienter med FOSAMAX 10 mg/dag i fortsatt økning i BMD ved lumbalcolumna og trochanter (absolutt ytterligere økning mellom år 3 og 5: korsryggen, 0,94 %; trochanter, 0,88 %). BMD ved lårhalsen, underarmen og hele kroppen ble opprettholdt. FOSAMAX var like effektivt uavhengig av alder, rase, baseline rate av beinomsetning og baseline BMD i området som ble studert (minst 2 standardavvik under premenopausalt gjennomsnitt).
Figur 3: Studier av osteoporosebehandling hos postmenopausale kvinner Tidsforløp for effekt av FOSAMAX 10 mg/dag versus placebo: Lumbal ryggrad BMD prosentvis endring fra baseline
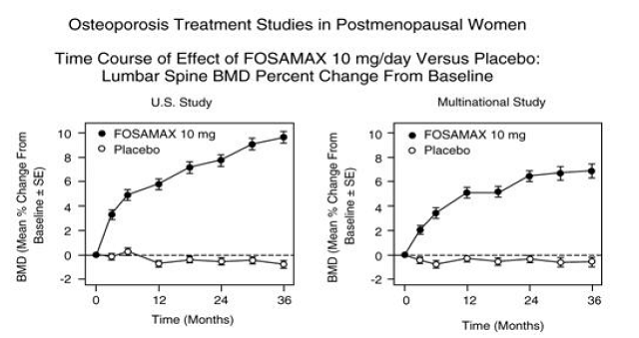
Hos pasienter med postmenopausal osteoporose behandlet med FOSAMAX 10 mg/dag i ett eller to år, ble effekten av behandlingsavbrudd vurdert. Etter seponering var det ingen ytterligere økning i benmasse, og bentapsratene var lik de for placebogruppene.
Beinhistologi
Beinhistologi hos 270 postmenopausale pasienter med osteoporose behandlet med FOSAMAX i doser fra 1 til 20 mg/dag i ett, to eller tre år avslørte normal mineralisering og struktur, samt forventet reduksjon i beinomsetning i forhold til placebo. Disse dataene, sammen med normal beinhistologi og økt benstyrke observert hos rotter og bavianer utsatt for langtidsbehandling med alendronat, støtter konklusjonen om at bein dannet under behandling med FOSAMAX 35 mg er av normal kvalitet.
Effekt på høyde
FOSAMAX, over en tre- eller fireårsperiode, var assosiert med statistisk signifikante reduksjoner i høydetap vs. placebo hos pasienter med og uten baseline radiografiske vertebrale frakturer. Ved slutten av FIT-studiene var forskjellene mellom behandlingsgruppene 3,2 mm i treårsstudien og 1,3 mm i fireårsstudien.
Ukentlig dosering
Den terapeutiske ekvivalensen av FOSAMAX 70 mg en gang i uken (n=519) og FOSAMAX 10 mg daglig (n=370) ble vist i en ettårig, dobbeltblind multisenterstudie av postmenopausale kvinner med osteoporose. I den primære analysen av fullførere var gjennomsnittlig økning fra baseline i lumbalcolumna BMD etter ett år 5,1 % (4,8, 5,4 %; 95 % KI) i 70 mg én gang ukentlig-gruppen (n=440) og 5,4 % ( 5,0, 5,8 %; 95 % KI) i 10 mg daglig gruppe (n=330). De to behandlingsgruppene var også like med hensyn til BMD-økninger på andre skjelettsteder. Resultatene av intensjon-å-behandle-analysen stemte overens med den primære analysen av fullførere.
Samtidig bruk med østrogen/hormonerstatningsterapi (HRT)
Effekten på BMD av behandling med FOSAMAX 10 mg én gang daglig og konjugert østrogen (0,625 mg/dag) enten alene eller i kombinasjon ble vurdert i en to-årig, dobbeltblind, placebokontrollert studie av hysterektomierte postmenopausale osteoporotiske kvinner (n= 425). Etter to år var økningen i lumbalcolumna BMD fra baseline signifikant større med kombinasjonen (8,3 %) enn med enten østrogen eller FOSAMAX alene (begge 6,0 %).
Effekten på BMD når FOSAMAX 35 mg ble lagt til stabile doser (i minst ett år) HRT (østrogen ± gestagen) ble vurdert i en ettårig, dobbeltblind, placebokontrollert studie hos postmenopausale osteoporotiske kvinner (n=428). Tillegg av FOSAMAX 10 mg én gang daglig til HRT ga, etter ett år, signifikant større økning i BMD i lumbal ryggrad (3,7 %) sammenlignet med HRT alene (1,1 %).
disse studiene ble det sett signifikante økninger eller gunstige trender i BMD for kombinert terapi sammenlignet med HRT alene ved total hofte, lårhals og trochanter. Ingen signifikant effekt ble sett for total kropps BMD.
Histomorfometriske studier av transiliacale biopsier hos 92 personer viste normal beinarkitektur. Sammenlignet med placebo var det en 98 % undertrykkelse av beinomsetning (vurdert ved mineraliserende overflate) etter 18 måneders kombinert behandling med FOSAMAX 35 mg og HRT, 94 % på FOSAMAX 35 mg alene, og 78 % på HRT alene. Langtidseffektene av kombinert FOSAMAX 35 mg og HRT på bruddforekomst og bruddtilheling er ikke studert.
Forebygging av osteoporose hos postmenopausale kvinner
Daglig dosering
Forebygging av bentap ble vist i to dobbeltblindede, placebokontrollerte studier av postmenopausale kvinner i alderen 40-60 år. Ett tusen seks hundre ni pasienter (FOSAMAX 5 mg/dag; n=498) som var minst seks måneder postmenopausale ble deltatt i en toårig studie uten hensyn til deres baseline BMD. I den andre studien ble 447 pasienter (FOSAMAX 5 mg/dag; n=88), som var mellom seks måneder og tre år etter overgangsalderen, behandlet i opptil tre år. Hos placebobehandlede pasienter ble det sett BMD-tap på omtrent 1 % per år i ryggraden, hoften (lårhals og trochanter) og hele kroppen. Derimot forhindret FOSAMAX 5 mg/dag bentap hos de fleste pasienter og induserte signifikant økning i gjennomsnittlig benmasse på hvert av disse stedene (se figur 4). I tillegg reduserte FOSAMAX 5 mg/dag frekvensen av bentap ved underarmen med omtrent halvparten i forhold til placebo. FOSAMAX 5 mg/dag var like effektivt i denne populasjonen uavhengig av alder, tid siden menopause, rase og baseline rate av beinomsetning.
Figur 4: Osteoporoseforebyggingsstudier hos postmenopausale kvinner

Beinhistologi
Beinhistologi var normal hos de 28 pasientene som ble biopsiert etter tre år som fikk FOSAMAX i doser på opptil 10 mg/dag.
Ukentlig dosering
Den terapeutiske ekvivalensen av FOSAMAX 35 mg en gang i uken (n=362) og FOSAMAX 5 mg daglig (n=361) ble vist i en ettårig, dobbeltblind multisenterstudie av postmenopausale kvinner uten osteoporose. I den primære analysen av fullfører var gjennomsnittlig økning fra baseline i lumbalcolumna BMD etter ett år 2,9 % (2,6, 3,2 %; 95 % KI) i 35 mg en gang ukentlig-gruppen (n=307) og 3,2 % ( 2,9, 3,5 %; 95 % KI) i gruppen 5 mg daglig (n=298). De to behandlingsgruppene var også like med hensyn til BMD-økninger på andre skjelettsteder. Resultatene av intensjon-å-behandle-analysen stemte overens med den primære analysen av fullførere.
Behandling for å øke beinmassen hos menn med osteoporose
Effekten av FOSAMAX 35 mg hos menn med hypogonadal eller idiopatisk osteoporose ble vist i to kliniske studier.
Daglig dosering
En to-årig, dobbeltblind, placebokontrollert, multisenterstudie av FOSAMAX 10 mg én gang daglig inkluderte totalt 241 menn mellom 31 og 87 år (gjennomsnittlig 63). Alle pasientene i studien hadde enten en BMD T-score mindre enn eller lik -2 ved lårhalsen og mindre enn eller lik -1 ved lumbalcolumna, eller en baseline osteoporotisk fraktur og en BMD T-score mindre enn eller lik -1 ved lårhalsen. Etter to år var gjennomsnittlig økning i BMD i forhold til placebo hos menn som fikk FOSAMAX 10 mg/dag signifikant på følgende steder: korsryggen, 5,3 %; lårhals, 2,6 %; trochanter, 3,1%; og total kropp, 1,6 %. Behandling med FOSAMAX 70mg reduserte også høydetap (FOSAMAX, -0,6 mm vs. placebo, -2,4 mm).
Ukentlig dosering
En ettårig, dobbeltblind, placebokontrollert, multisenterstudie med FOSAMAX 70 mg én gang i uken inkluderte totalt 167 menn mellom 38 og 91 år (gjennomsnittlig 66). Pasientene i studien hadde enten en BMD T-score mindre enn eller lik -2 ved lårhalsen og mindre enn eller lik -1 ved korsryggen, eller en BMD T-score mindre enn eller lik -2 ved korsryggen og mindre enn eller lik -1 ved lårhalsen, eller en baseline osteoporotisk fraktur og en BMD T-score mindre enn eller lik -1 ved lårhalsen. Etter ett år var gjennomsnittlig økning i BMD i forhold til placebo hos menn som fikk FOSAMAX 70 mg én gang ukentlig signifikant på følgende steder: lumbalcolumna, 2,8 %; lårhals, 1,9 %; trochanter, 2,0%; og total kropp, 1,2 %. Disse økningene i BMD var lik de som ble sett etter ett år i studien på 10 mg én gang daglig.
begge studiene var BMD-responsen lik uavhengig av alder (større enn eller lik 65 år vs. mindre enn 65 år), gonadal funksjon (baseline testosteron mindre enn 9 ng/dL vs. større enn eller lik 9 ng/dL) , eller baseline BMD (lårhals og lumbalcolumna T-score mindre enn eller lik -2,5 vs. større enn -2,5).
Behandling av glukokortikoid-indusert osteoporose
Effekten av FOSAMAX 5 og 10 mg én gang daglig hos menn og kvinner som får glukokortikoider (minst 7,5 mg/dag med prednison eller tilsvarende) ble vist i to, ettårige, dobbeltblinde, randomiserte, placebokontrollerte, multisenterstudier av praktisk talt identisk design, den ene utført i USA og den andre i 15 forskjellige land (Multinational [som også inkluderte FOSAMAX 2,5 mg/dag]). Disse studiene inkluderte henholdsvis 232 og 328 pasienter mellom 17 og 83 år med en rekke glukokortikoidkrevende sykdommer. Pasienter fikk tilskudd av kalsium og vitamin D. Figur 5 viser gjennomsnittlig økning i BMD i lumbalcolumna, lårhals og trochanter i forhold til placebo hos pasienter som fikk FOSAMAX 5 mg/dag for hver studie.
Figur 5: Studier i glukokortikoidbehandlede pasienter Økning i BMD FOSAMAX 5 mg/dag etter ett år
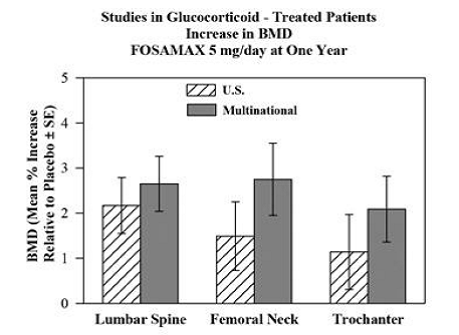
Etter ett år ble det sett signifikant økning i BMD i forhold til placebo i de kombinerte studiene på hvert av disse stedene hos pasienter som fikk FOSAMAX 5 mg/dag. Hos placebobehandlede pasienter forekom en signifikant reduksjon i BMD ved lårhalsen (-1,2 %), og mindre reduksjoner ble sett ved korsryggen og trochanter. BMD i hele kroppen ble opprettholdt med FOSAMAX 5 mg/dag. Økningen i BMD med FOSAMAX 10 mg/dag var lik de med FOSAMAX 5 mg/dag hos alle pasienter bortsett fra postmenopausale kvinner som ikke fikk østrogenbehandling. Hos disse kvinnene var økningen (i forhold til placebo) med FOSAMAX 10 mg/dag større enn de med FOSAMAX 5 mg/dag ved korsryggen (4,1 % vs. 1,6 %) og trochanter (2,8 % vs. 1,7 %). men ikke på andre nettsteder. FOSAMAX 35 mg var effektivt uavhengig av dose eller varighet av glukokortikoidbruk. I tillegg var FOSAMAX like effektivt uavhengig av alder (mindre enn 65 vs. større enn eller lik 65 år), rase (kaukasisk vs. andre raser), kjønn, underliggende sykdom, baseline BMD, baseline beinomsetning og bruk med en en rekke vanlige medisiner.
Benhistologi var normal hos de 49 pasientene som ble biopsiert ved slutten av ett år som fikk FOSAMAX i doser på opptil 10 mg/dag.
Av de opprinnelige 560 pasientene i disse studiene, fortsatte 208 pasienter som forble på minst 7,5 mg/dag med prednison eller tilsvarende inn i en ettårig dobbeltblind forlengelse. Etter to års behandling økte BMD i ryggraden med 3,7 % og 5,0 % i forhold til placebo med henholdsvis FOSAMAX 5 og 10 mg/dag. Signifikante økninger i BMD (i forhold til placebo) ble også observert ved lårhalsen, trochanter og hele kroppen.
Etter ett år opplevde 2,3 % av pasientene behandlet med FOSAMAX 5 eller 10 mg/dag (sammenslått) vs. 3,7 % av de behandlet med placebo et nytt vertebralt brudd (ikke signifikant). I populasjonen som ble studert i to år, reduserte imidlertid behandling med FOSAMAX (sammenslåtte doseringsgrupper: 5 eller 10 mg i to år eller 2,5 mg i ett år etterfulgt av 10 mg i ett år) signifikant forekomsten av pasienter med ny vertebralfraktur (FOSAMAX 0,7 % vs. placebo 6,8 %).
Behandling av Pagets beinsykdom
Effekten av FOSAMAX 40 mg én gang daglig i seks måneder ble vist i to dobbeltblindede kliniske studier av mannlige og kvinnelige pasienter med moderat til alvorlig Pagets sykdom (alkalisk fosfatase minst to ganger øvre normalgrense): en placebo -kontrollert, multinasjonal studie og en amerikansk sammenlignende studie med dinatriumetidronat 400 mg/dag. Figur 6 viser gjennomsnittlig prosentvise endringer fra baseline i serum alkalisk fosfatase i opptil seks måneder med randomisert behandling.
Figur 6: Studier av Pagets sykdom av beineffekt på serum alkalisk fosfatase av FOSAMAX 40 mg/dag versus placebo eller etidronat 400 mg/dag
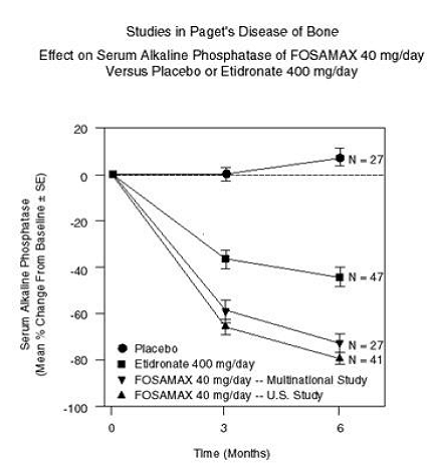
Etter seks måneder var undertrykkelsen av alkalisk fosfatase hos pasienter behandlet med FOSAMAX signifikant større enn det som ble oppnådd med etidronat og i kontrast til fullstendig mangel på respons hos placebobehandlede pasienter. Respons (definert som enten normalisering av serum alkalisk fosfatase eller reduksjon fra baseline større enn eller lik 60%) forekom hos ca. 85 % av pasientene behandlet med FOSAMAX i de kombinerte studiene vs. 30 % i etidronatgruppen og 0 % i placebogruppen. gruppe. FOSAMAX 70 mg var like effektivt uavhengig av alder, kjønn, rase, tidligere bruk av andre bisfosfonater eller baseline alkalisk fosfatase innenfor det undersøkte området (minst to ganger øvre normalgrense).
Benhistologi ble evaluert hos 33 pasienter med Pagets sykdom behandlet med FOSAMAX 40 mg/dag i 6 måneder. Som hos pasienter behandlet for osteoporose [se Kliniske studier ], FOSAMAX svekket ikke mineraliseringen, og den forventede nedgangen i beinomsetningshastigheten ble observert. Normalt lamellært bein ble produsert under behandling med FOSAMAX, selv der eksisterende ben var vevd og uorganisert. Samlet sett støtter benhistologidata konklusjonen om at bein som dannes under behandling med FOSAMAX 35mg er av normal kvalitet.
PASIENTINFORMASJON
FOSAMAX® (FOSS-ah-max)(alendronatnatrium) Tabletter
Les medisinveiledningen som følger med FOSAMAX 70mg før du begynner å ta den og hver gang du får påfyll. Det kan komme ny informasjon. Denne medisinguiden erstatter ikke å snakke med legen din om din medisinske tilstand eller behandling. Snakk med legen din hvis du har spørsmål om FOSAMAX.
Hva er den viktigste informasjonen jeg bør vite om FOSAMAX 70mg?
FOSAMAX 70mg kan forårsake alvorlige bivirkninger, inkludert:
. Problemer med spiserøret . Lavt kalsiumnivå i blodet ditt (hypokalsemi) . Bein-, ledd- eller muskelsmerter . Alvorlige kjevebeinproblemer (osteonekrose) . Uvanlige lårbensbrudd1. Problemer med spiserøret.
Noen mennesker som tar FOSAMAX 35mg kan utvikle problemer i spiserøret (røret som forbinder munnen og magen).
Disse problemene inkluderer irritasjon, betennelse eller sår i spiserøret som noen ganger kan blø.
- . Det er viktig at du tar FOSAMAX 70mg nøyaktig som foreskrevet for å redusere sjansen for å få spiserørsproblemer. (Se avsnittet "Hvordan bør jeg ta FOSAMAX?") . Slutt å ta FOSAMAX og ring legen din umiddelbart hvis du får brystsmerter, ny eller forverret halsbrann, eller har problemer eller smerter når du svelger.
2. Lavt kalsiumnivå i blodet ditt (hypokalsemi).
FOSAMAX kan senke kalsiumnivået i blodet ditt. Hvis du har lavt kalsium i blodet før du begynner å ta FOSAMAX, kan det bli verre under behandlingen. Ditt lave kalsium i blodet må behandles før du tar FOSAMAX. De fleste med lavt kalsiumnivå i blodet har ikke symptomer, men noen kan ha symptomer. Ring legen din med en gang hvis du har symptomer på lavt kalsium i blodet som:
- . Spasmer, rykninger eller kramper i musklene . Nummenhet eller prikking i fingrene, tærne eller rundt munnen
Legen din kan foreskrive kalsium og vitamin D for å forhindre lave kalsiumnivåer i blodet mens du tar FOSAMAX. Ta kalsium og vitamin D slik legen din forteller deg.
3. Bein-, ledd- eller muskelsmerter.
Noen mennesker som tar FOSAMAX utvikler alvorlige bein-, ledd- eller muskelsmerter.
4. Alvorlige kjevebeinproblemer (osteonekrose).
Alvorlige kjevebeinproblemer kan oppstå når du tar FOSAMAX. Legen din bør undersøke munnen din før du starter FOSAMAX. Legen din kan fortelle deg at du skal se tannlegen din før du starter FOSAMAX. Det er viktig for deg å praktisere god munnpleie under behandling med FOSAMAX.
5. Uvanlige lårbensbrudd.
Noen mennesker har utviklet uvanlige brudd i lårbenet. Symptomer på et brudd kan omfatte nye eller uvanlige smerter i hoften, lysken eller låret.
Ring legen din med en gang hvis du har noen av disse bivirkningene.
Hva er FOSAMAX 70mg?
- . FOSAMAX 70mg er et reseptbelagt legemiddel som brukes til å: . Behandle eller forebygge osteoporose hos kvinner etter overgangsalderen. Det bidrar til å redusere sjansen for å få hofte- eller ryggbrudd (brudd). . Øke beinmassen hos menn med osteoporose. . Behandle osteoporose hos enten menn eller kvinner som tar kortikosteroidmedisiner.
Behandle visse menn og kvinner som har Pagets sykdom i beinet.
Det er ikke kjent hvor lenge FOSAMAX 70 mg virker for behandling og forebygging av osteoporose. Du bør oppsøke legen din regelmessig for å finne ut om FOSAMAX 70mg fortsatt er riktig for deg.
FOSAMAX skal ikke brukes til barn.
Hvem bør ikke ta FOSAMAX 70mg?
Ikke ta FOSAMAX hvis du:
- . Har visse problemer med spiserøret, røret som forbinder munnen din med magen . Kan ikke stå eller sitte oppreist i minst 30 minutter . Har lave nivåer av kalsium i blodet . Er allergisk mot FOSAMAX 70mg eller noen av ingrediensene i det. En liste over ingredienser er på slutten av dette pakningsvedlegget.
Hva bør jeg fortelle legen min før jeg tar FOSAMAX 35mg?
Før du starter FOSAMAX, sørg for å snakke med legen din dersom du:
- . Har problemer med å svelge . Har mage- eller fordøyelsesproblemer . Har lavt kalsium i blodet . Planlegg å få tannkirurgi eller fjerne tenner . Har nyreproblemer . Har blitt fortalt at du har problemer med å absorbere mineraler i magen eller tarmene (malabsorpsjonssyndrom) . Er gravid, prøver å bli gravid eller mistenker at du er gravid. Hvis du blir gravid mens du tar FOSAMAX, må du slutte å ta det og kontakte legen din. Det er ikke kjent om FOSAMAX kan skade det ufødte barnet ditt. . Ammer eller planlegger å amme. Det er ikke kjent om FOSAMAX går over i melken din og kan skade babyen din.
Fortell legen din spesielt hvis du tar:
- . antacida . aspirin . Ikke-steroide antiinflammatoriske (NSAID) medisiner
Fortell legen din om alle medisinene du tar, inkludert reseptbelagte og reseptfrie medisiner, vitaminer og urtetilskudd. Visse medisiner kan påvirke hvordan FOSAMAX 70mg virker.
Kjenn til medisinene du tar. Hold en liste over dem og vis den til legen din og apoteket hver gang du får en ny medisin.
Hvordan bør jeg ta FOSAMAX 35mg?
- . Ta FOSAMAX 35 mg nøyaktig slik legen din har fortalt deg. . FOSAMAX virker bare hvis det tas på tom mage. . Ta FOSAMAX 35 mg, etter at du står opp for dagen og før du tar din første mat, drikke eller annen medisin. . Ta FOSAMAX mens du sitter eller står. . Ikke tygg eller sug på en tablett med FOSAMAX. . Svelg FOSAMAX-tablett kun med et fullt glass (6-8 oz) rent vann. . Ikke ta FOSAMAX med mineralvann, kaffe, te, brus eller juice.
- . Hvis du tar Alendronate daglig:
- . Ta 1 alendronattablett én gang om dagen, hver dag etter at du står opp for dagen og før du tar din første mat, drikke eller annen medisin.
- . Velg den ukedagen som passer best til timeplanen din. . Ta 1 dose FOSAMAX hver uke på den valgte dagen etter at du står opp for dagen og før du tar din første mat, drikke eller annen medisin.
Etter å ha svelget FOSAMAX 35 mg tablett, vent minst 30 minutter:
- . Før du legger deg. Du kan sitte, stå eller gå og gjøre vanlige aktiviteter som å lese. . Før du tar din første mat eller drikke, bortsett fra vanlig vann. . Før du tar andre medisiner, inkludert antacida, kalsium og andre kosttilskudd og vitaminer.
Ikke legg deg ned i minst 30 minutter etter at du har tatt FOSAMAX og etter at du har spist dagens første mat.
Hvis du glemmer en dose FOSAMAX 70 mg, ikke ta den senere på dagen. Ta den glemte dosen neste morgen etter at du husker det, og gå deretter tilbake til normal tidsplan. Ikke ta 2 doser på samme dag.
Hvis du tar for mye FOSAMAX 70 mg, ring legen din. Ikke prøv å kaste opp. Ikke legg deg ned.
Hva er de mulige bivirkningene av FOSAMAX 70mg?
FOSAMAX kan forårsake alvorlige bivirkninger.
- . Se "Hva er den viktigste informasjonen jeg bør vite om FOSAMAX?"
De vanligste bivirkningene av FOSAMAX 70mg er:
- . Smerter i mageområdet (mage). . Halsbrann . Forstoppelse . Diaré . Urolig mage . Smerter i bein, ledd eller muskler . Kvalme
Du kan få allergiske reaksjoner, som elveblest eller hevelse i ansiktet, leppene, tungen eller halsen.
Forverring av astma er rapportert.
Fortell legen din dersom du har noen bivirkninger som plager deg eller som ikke går over.
Dette er ikke alle mulige bivirkninger av FOSAMAX. Spør legen din eller apoteket for mer informasjon.
Ring legen din for medisinsk råd om bivirkninger. Du kan rapportere bivirkninger til FDA på 1-800-FDA-1088.
Hvordan oppbevarer jeg FOSAMAX?
- . Oppbevar FOSAMAX 35 mg ved romtemperatur, 59 °F til 86 °F (15 °C til 30 °C). . Oppbevar FOSAMAX i en tett lukket beholder.
Oppbevar FOSAMAX og alle legemidler utilgjengelig for barn.
Generell informasjon om sikker og effektiv bruk av FOSAMAX.
Medisiner er noen ganger foreskrevet for andre formål enn de som er oppført i en medisinveiledning. Ikke bruk FOSAMAX 35mg for en tilstand det ikke er foreskrevet for. Ikke gi FOSAMAX 35 mg til andre mennesker, selv om de har de samme symptomene som du har. Det kan skade dem.
Denne medisinveiledningen oppsummerer den viktigste informasjonen om FOSAMAX. Hvis du vil ha mer informasjon, snakk med legen din. Du kan spørre legen din eller apoteket om informasjon om FOSAMAX som er skrevet for helsepersonell. For mer informasjon, gå til: www.FOSAMAX.com eller ring 1-800-622-4477 (gratis).
Hva er ingrediensene i FOSAMAX?
Aktiv ingrediens: alendronatnatrium
Inaktive ingredienser: mikrokrystallinsk cellulose, vannfri laktose, kroskarmellosenatrium, magnesiumstearat.
Denne medisinveiledningen er godkjent av US Food and Drug Administration.
