Imdur 40mg, 20mg, 30mg, 60mg Isosorbide Bruk, bivirkninger og dosering. Pris i nettapotek. Generisk medisin uten resept.
Hva er Imdur 30mg og hvordan brukes det?
Imdur 30mg er et reseptbelagt legemiddel som brukes til å behandle symptomene på brystsmerter (Angina Pectoris). Imdur 30mg kan brukes alene eller sammen med andre medisiner.
Imdur 20mg tilhører en klasse legemidler som heter nitrater, angina.
Det er ikke kjent om Imdur 60mg er trygt og effektivt hos barn.
Hva er mulige bivirkninger av Imdur?
Bivirkninger av Imdur inkluderer:
- . besvimelse, . raske, uregelmessige eller bankende hjerteslag, . utslett, . kløe, . hevelse i ansikt, tunge og svelg, . alvorlig svimmelhet, og . problemer med å puste
Få medisinsk hjelp med en gang hvis du har noen av symptomene nevnt ovenfor.
De vanligste bivirkningene av Imdur 30mg inkluderer:
- . hodepine, . svimmelhet, . svimmelhet, og . kvalme
Fortell legen dersom du har noen bivirkninger som plager deg eller som ikke går over.
Dette er ikke alle mulige bivirkninger av Imdur. Spør legen din eller apoteket for mer informasjon.
Ring legen din for medisinsk råd om bivirkninger. Du kan rapportere bivirkninger til FDA på 1-800-FDA-1088.
BESKRIVELSE
Isosorbidmononitrat (ISMN), et organisk nitrat og den viktigste biologisk aktive metabolitten av isosorbiddinitrat (ISDN), er en vasodilator med effekter på både arterier og vener.
IMDUR® tabletter, for oral administrering, inneholder enten 30 mg, 60 mg eller 120 mg isosorbidmononitrat i en formulering med forlenget frigivelse. I tillegg inneholder hver tablett følgende inaktive ingredienser: kolloidalt silisiumdioksid, hydrogenert ricinusolje, hypromellose, laktosemonohydrat, magnesiumstearat, mikrokrystallinsk cellulose og talkum.
Molekylformelen til ISMN er C6H9NO6 og molekylvekten er 191,14. Det kjemiske navnet for ISMN er 1,4:3,6-dianhydro-,D-glucitol-5-nitrat; forbindelsen har følgende strukturformel:
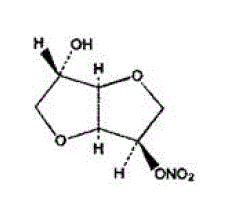
ISMN er en hvit, krystallinsk, luktfri forbindelse som er stabil i luft og i løsning, har et smeltepunkt på ca. 90°C, og en optisk rotasjon på +144° (2% i vann, 20°C).
Isosorbidmononitrat er fritt løselig i vann, etanol, metanol, kloroform, etylacetat og diklormetan.
INDIKASJONER
IMDUR-tabletter er indisert for forebygging av angina pectoris på grunn av koronararteriesykdom. Virkningen av oralt isosorbidmononitrat er ikke tilstrekkelig raskt til at dette produktet kan være nyttig for å avbryte en akutt angina episode.
DOSERING OG ADMINISTRASJON
Den anbefalte startdosen av IMDUR tabletter er 30 mg (gitt som en enkelt 30 mg tablett eller som 1/2 av en 60 mg tablett) eller 60 mg (gitt som en enkelt tablett) én gang daglig. Etter flere dager kan dosen økes til 120 mg (gitt som en enkelt 120 mg tablett eller som to 60 mg tabletter) én gang daglig. I sjeldne tilfeller kan 240 mg være nødvendig. Den daglige dosen av IMDUR tabletter bør tas om morgenen når de står opp. IMDUR Extended Release-tabletter skal ikke tygges eller knuses og skal svelges sammen med et halvt glass væske. Ikke knekk 30 mg tabletten.
HVORDAN LEVERES
IMDUR tabletter med forlenget utgivelse 30 mg er hvite, kapselformede tabletter med delestrek på den ene siden og merket "IMDUR" på siden uten delestrek. De leveres som følger:
100 flasker NDC 0085-1374-01
IMDUR tabletter med forlenget utgivelse 60 mg er hvite, kapselformede tabletter med delestrek på den ene siden med quot;60-60" og inngravert "IMDUR" på siden uten delestrek. De leveres som følger:
100 flasker NDC 0085-2028-01
IMDUR 30 mg tabletter med forlenget utgivelse 120 mg er hvite, kapselformede tabletter merket "IMDUR" på den ene siden og "120" på den andre siden. De leveres som følger:
100 flasker NDC 0085-0091-01
Oppbevares ved kontrollert romtemperatur 20°-25°C (68°-77°F) [Se USP].
Produsert av: Kremers urban pharmaceuticals inc, seymour,IN47274,USA. Revidert: desember 2010
BIVIRKNINGER
Tabellen nedenfor viser frekvensen av bivirkningene som oppstod hos >5 % av forsøkspersonene i tre placebokontrollerte nordamerikanske studier der pasienter i den aktive behandlingsarmen fikk 30 mg, 60 mg, 120 mg eller 240 mg isosorbid mononitrat som IMDUR 60 mg tabletter én gang daglig. I parentes viser samme tabell med hvilke frekvenser disse bivirkningene var assosiert med seponering av behandlingen. Totalt sett avbrøt 8 % av pasientene som fikk 30 mg, 60 mg, 120 mg eller 240 mg isosorbidmononitrat i de tre placebokontrollerte nordamerikanske studiene behandlingen på grunn av bivirkninger. De fleste av disse avbrøt på grunn av hodepine. Svimmelhet var sjelden forbundet med uttak fra disse studiene. Siden hodepine ser ut til å være en doserelatert bivirkning og har en tendens til å forsvinne ved fortsatt behandling, anbefales det at IMDUR-behandling startes med lave doser i flere dager før den økes til ønsket nivå.
FREKVENS OG Uønskede HENDELSER (AVSLUTTET) *
I tillegg ble de tre nordamerikanske studiene slått sammen med 11 kontrollerte studier utført i Europa. Blant de 14 kontrollerte studiene ble totalt 711 pasienter randomisert til IMDUR-tabletter. Når de samlede dataene ble gjennomgått, var hodepine og svimmelhet de eneste bivirkningene som ble rapportert av >5 % av pasientene. Andre bivirkninger, hver rapportert av ≤5 % av eksponerte pasienter, og i mange tilfeller med usikkert forhold til medikamentell behandling, var:
Autonome nervesystemforstyrrelser : Munntørrhet, hetetokter.
Kroppen som en helhet : Asteni, ryggsmerter, brystsmerter, ødem, tretthet, feber, influensalignende symptomer, ubehag, stivhet.
Kardiovaskulære lidelser, generelt : Hjertesvikt, hypertensjon, hypotensjon.
Forstyrrelser i det sentrale og perifere nervesystemet : Svimmelhet, hodepine, hypoestesi, migrene, nevritt, pareser, parestesi, ptose, skjelving, svimmelhet.
Forstyrrelser i mage-tarmsystemet Magesmerter, forstoppelse, diaré, dyspepsi, flatulens, magesår, gastritt, glossitt, hemorragisk magesår, hemoroider, løs avføring, melena, kvalme, oppkast.
Hørsel og vestibulære lidelser : Ørepine, tinnitus, perforering av trommehinnen.
Hjertefrekvens og rytmeforstyrrelser : Arytmi, arytmi atrie, atrieflimmer, bradykardi, grenblokk, ekstrasystole, hjertebank, takykardi, ventrikkeltakykardi.
Lever- og gallesystemlidelser : SGOT-økning, SGPT-økning.
Metabolske og ernæringsforstyrrelser : Hyperurikemi, hypokalemi.
Sykdommer i muskel- og skjelettsystemet : Artralgi, frossen skulder, muskelsvakhet, muskel- og skjelettsmerter, myalgi, myositt, senelidelse, torticollis.
Myo-, endo-, perikardiale og klaffelidelser : Angina pectoris forverret, bilyd i hjertet, unormal hjertelyd, hjerteinfarkt, unormal Q-bølge.
Blodplate-, blødnings- og koagulasjonsforstyrrelser : Purpura, trombocytopeni.
Psykiatriske lidelser Angst, nedsatt konsentrasjon, forvirring, nedsatt libido, depresjon, impotens, søvnløshet, nervøsitet, paroniria, somnolens.
Røde blodlegemer lidelse : Hypokrom anemi.
Reproduksjonsforstyrrelser, kvinner : Atrofisk vaginitt, brystsmerter.
Forstyrrelser i motstandsmekanismen : Bakteriell infeksjon, moniliasis, virusinfeksjon.
Sykdommer i luftveiene : Bronkitt, bronkospasme, hoste, dyspné, økt sputum, tett nese, faryngitt, lungebetennelse, lungeinfiltrasjon, raser, rhinitt, bihulebetennelse.
Hud- og vedhengslidelser : Akne, unormal hårtekstur, økt svetting, kløe, utslett, hudknuter.
Forstyrrelser i urinsystemet : Polyuri, nyresten, urinveisinfeksjon.
Vaskulære (ekstrakardiale) lidelser : Rødming, claudicatio intermittens, leggsår, åreknuter.
Synsforstyrrelser : Konjunktivitt, fotofobi, unormalt syn.
tillegg har følgende spontane bivirkning blitt rapportert under markedsføringen av isosorbidmononitrat: synkope.
NARKOTIKAHANDEL
De vasodilaterende effektene av isosorbidmononitrat kan være additive med effekten av andre vasodilatatorer. Spesielt alkohol har vist seg å ha additive effekter av denne varianten.
Markert symptomatisk ortostatisk hypotensjon er rapportert når kalsiumkanalblokkere og organiske nitrater ble brukt i kombinasjon. Dosejusteringer av begge legemidler kan være nødvendig.
Interaksjoner med legemiddel/laboratorietest
Nitrater og nitritter kan forstyrre Zlatkis-Zak-fargereaksjonen, og forårsake falskt lave målinger i serumkolesterolbestemmelser.
ADVARSLER
Amplifisering av de vasodilaterende effektene av IMDUR med sildenafil kan resultere i alvorlig hypotensjon. Tidsforløpet og doseavhengigheten av denne interaksjonen er ikke studert. Hensiktsmessig støttebehandling er ikke studert, men det virker rimelig å behandle dette som en nitratoverdose, med forhøyning av ekstremitetene og med sentral volumutvidelse.
Fordelene med ISMN hos pasienter med akutt hjerteinfarkt eller kongestiv hjertesvikt er ikke fastslått; fordi effekten av isosorbidmononitrat er vanskelig å avslutte raskt, anbefales ikke dette stoffet i disse innstillingene.
Hvis isosorbidmononitrat brukes under disse forholdene, må nøye klinisk eller hemodynamisk overvåking brukes for å unngå farene med hypotensjon og takykardi.
FORHOLDSREGLER
Generell
Alvorlig hypotensjon, spesielt med oppreist stilling, kan forekomme med selv små doser isosorbidmononitrat. Dette legemidlet bør derfor brukes med forsiktighet hos pasienter som kan være volummangel eller som, uansett årsak, allerede er hypotensive. Hypotensjon indusert av isosorbidmononitrat kan være ledsaget av paradoksal bradykardi og økt angina pectoris.
Nitratbehandling kan forverre angina forårsaket av hypertrofisk kardiomyopati.
Hos industriarbeidere som har hatt langvarig eksponering for ukjente (antagelig høye) doser av organiske nitrater, forekommer toleranse tydelig. Brystsmerter, akutt hjerteinfarkt og til og med plutselig død har skjedd under midlertidig uttak av nitrater fra disse arbeiderne, noe som viser eksistensen av ekte fysisk avhengighet. Betydningen av disse observasjonene for rutinemessig klinisk bruk av oralt isosorbidmononitrat er ikke kjent.
Karsinogenese, mutagenese, svekkelse av fruktbarhet
Ingen bevis for kreftfremkallende egenskaper ble observert hos rotter som ble eksponert for isosorbidmononitrat i diettene ved doser på opptil 900 mg/kg/dag de første 6 månedene og 500 mg/kg/dag i den gjenværende varigheten av en studie der hanner ble doseret. i opptil 121 uker og kvinner ble doseret i opptil 137 uker. Ingen tegn på karsinogenitet ble observert hos mus som ble eksponert for isosorbidmononitrat i diettene deres i opptil 104 uker ved doser på opptil 900 mg/kg/dag.
Isosorbidmononitrat produserte ikke genmutasjoner (Ames-test, muselymfomtest) eller kromosomavvik (humane lymfocytt- og musemikronukleustester) ved biologisk relevante konsentrasjoner.
Ingen effekter på fertilitet ble observert i en studie der hann- og hunnrotter ble administrert doser på opptil 750 mg/kg/dag fra begynnelsen, hos hanner, 9 uker før paring, og hos hunner, 2 uker før paring.
Svangerskap
Teratogene effekter
Graviditetskategori B
studier designet for å oppdage effekter av isosorbidmononitrat på embryo-føtal utvikling, var doser på opptil 240 eller 248 mg/kg/dag, administrert til drektige rotter og kaniner, ikke assosiert med tegn på slike effekter. Disse dyredosene er omtrent 100 ganger den maksimale anbefalte humane dosen (120 mg hos en kvinne på 50 kg) når sammenligning er basert på kroppsvekt; når sammenligning er basert på kroppsoverflate, er rottedosen omtrent 17 ganger humandosen og kanindosen er omtrent 38 ganger humandosen. Det finnes imidlertid ingen tilstrekkelige og godt kontrollerte studier på gravide kvinner. Fordi reproduksjonsstudier på dyr ikke alltid er prediktive for human respons, bør IMDUR tabletter kun brukes under graviditet hvis det er klart nødvendig.
Ikke-ratatogene effekter
Neonatal overlevelse og utvikling og forekomst av dødfødsler ble negativt påvirket når drektige rotter ble administrert orale doser på 750 (men ikke 300) mg isosorbidmononitrat/kg/dag under sen svangerskap og diegivning. Denne dosen (omtrent 312 ganger den humane dosen når sammenligningen er basert på kroppsvekt og 54 ganger den humane dosen når sammenligningen er basert på kroppsoverflaten) var assosiert med reduksjon i mors vektøkning og motorisk aktivitet og tegn på svekket amming.
Ammende mødre
Det er ikke kjent om dette legemidlet skilles ut i morsmelk. Fordi mange legemidler skilles ut i morsmelk, bør det utvises forsiktighet når ISMN administreres til en ammende mor.
Pediatrisk bruk
Sikkerheten og effektiviteten til ISMN hos pediatriske pasienter er ikke fastslått.
Geriatrisk bruk
Kliniske studier av IMDUR 60 mg tabletter inkluderte ikke tilstrekkelig informasjon om pasienter 65 år og eldre for å avgjøre om de responderer annerledes enn yngre pasienter. Annen rapportert klinisk erfaring for IMDUR 20 mg har ikke identifisert forskjeller i respons mellom eldre og yngre pasienter. Klinisk erfaring for organiske nitrater rapportert i litteraturen identifiserte et potensial for alvorlig hypotensjon og økt følsomhet for nitrater hos eldre. Generelt bør dosevalg for en eldre pasient være forsiktig, vanligvis fra den lave enden av doseringsområdet, noe som gjenspeiler den høyere frekvensen av nedsatt lever-, nyre- eller hjertefunksjon, og samtidig sykdom eller annen medikamentell behandling.
Eldre pasienter kan ha redusert baroreseptorfunksjon og kan utvikle alvorlig ortostatisk hypotensjon når vasodilatorer brukes. IMDUR 60mg bør derfor brukes med forsiktighet hos eldre pasienter som kan ha volummangel, på flere medisiner eller som, uansett årsak, allerede er hypotensive. Hypotensjon indusert av isosorbidmononitrat kan være ledsaget av paradoksal bradykardi og økt angina pectoris.
Eldre pasienter kan være mer utsatt for hypotensjon og kan ha større risiko for å falle ved terapeutiske doser av nitroglyserin.
Nitratbehandling kan forverre angina forårsaket av hypertrofisk kardiomyopati, spesielt hos eldre.
OVERDOSE
Hemodynamiske effekter
De dårlige effektene av overdosering av isosorbidmononitrat er generelt et resultat av isosorbidmononitrats evne til å indusere vasodilatasjon, venøs sammenslåing, redusert hjertevolum og hypotensjon. Disse hemodynamiske endringene kan ha protean manifestasjoner, inkludert økt intrakranielt trykk, med noen eller alle av vedvarende bankende hodepine, forvirring og moderat feber; svimmelhet, hjertebank; visuelle forstyrrelser; kvalme og oppkast (muligens med kolikk og til og med blodig diaré); synkope (spesielt i oppreist stilling); luftsult og dyspné, senere etterfulgt av redusert ventilasjonsanstrengelse; diaforese, med huden enten rød eller kald og klam; hjerteblokk og bradykardi; lammelse; koma; anfall og død.
Laboratoriebestemmelser av serumnivåer av isosorbidmononitrat og dets metabolitter er ikke allment tilgjengelige, og slike bestemmelser har i alle fall ingen etablert rolle i behandlingen av isosorbidmononitratoverdose.
Det er ingen data som tyder på hvilken dose isosorbidmononitrat som sannsynligvis er livstruende hos mennesker. Hos rotter og mus er det betydelig dødelighet ved doser på henholdsvis 2000 mg/kg og 3000 mg/kg.
Ingen data er tilgjengelige som tyder på fysiologiske manøvrer (f.eks. manøvrer for å endre pH i urinen) som kan akselerere eliminering av isosorbidmononitrat. Spesielt er dialyse kjent for å være ineffektiv for å fjerne isosorbidmononitrat fra kroppen.
Ingen spesifikk antagonist til de vasodilatatoriske effektene av isosorbidmononitrat er kjent, og ingen intervensjon Ingen spesifikke antagonister til de vasodilatatoriske effektene av isosorbidmononitrat er kjent, og ingen intervensjon har vært gjenstand for kontrollerte studier som terapi for overdosering av isosorbidmononitrat. Fordi hypotensjonen forbundet med overdosering av isosorbidmononitrat er et resultat av venodilatasjon og arteriell hypovolemi, bør forsiktig behandling i denne situasjonen rettes mot en økning i sentralt væskevolum. Passiv heving av pasientens ben kan være tilstrekkelig, men intravenøs infusjon av vanlig saltvann eller lignende væske kan også være nødvendig.
Bruk av epinefrin eller andre arterielle vasokonstriktorer i denne innstillingen vil sannsynligvis gjøre mer skade enn nytte.
Hos pasienter med nyresykdom eller kongestiv hjertesvikt er behandling som resulterer i sentral volumutvidelse ikke uten fare. Behandling av overdosering av isosorbidmononitrat hos disse pasientene kan være subtil og vanskelig, og invasiv overvåking kan være nødvendig.
Methemoglobinemi
Methemoglobinemi er rapportert hos pasienter som får andre organiske nitrater, og det kan sannsynligvis også forekomme som en bivirkning av isosorbidmononitrat. Naturligvis kan nitrationer som frigjøres under metabolismen av isosorbidmononitrat oksidere hemoglobin til methemoglobin. Selv hos pasienter helt uten cytokrom b-reduktaseaktivitet, og selv forutsatt at nitratdelen av isosorbidmononitrat brukes kvantitativt på oksidasjon av hemoglobin, bør det kreves ca. 2 mg/kg isosorbidmononitrat før noen av disse pasientene viser seg klinisk signifikant ( ≥10 %) methemoglobinemi. Hos pasienter med normal reduktasefunksjon bør betydelig produksjon av methemoglobin kreve enda større doser isosorbidmononitrat. I en studie der 36 pasienter mottok 2-4 ukers kontinuerlig nitroglyserinbehandling med 3,1 til 4,4 mg/time (tilsvarer, i total administrert dose av nitrationer, 7,8-11,1 mg isosorbidmononitrat per time), gjennomsnittlig methemoglobinnivå. målt var 0,2 %; dette var sammenlignbart med det som ble observert hos parallelle pasienter som fikk placebo.
Til tross for disse observasjonene er det kasusrapporter om betydelig methemoglobinemi i forbindelse med moderate overdoser av organiske nitrater. Ingen av de berørte pasientene ble antatt å være uvanlig mottakelige.
Methemoglobinnivåer er tilgjengelige fra de fleste kliniske laboratorier. Diagnosen bør mistenkes hos pasienter som viser tegn på nedsatt oksygentilførsel til tross for tilstrekkelig hjertevolum og tilstrekkelig arteriell pO2. Klassisk er methemoglobinemisk blod beskrevet som sjokoladebrunt uten fargeendring ved eksponering for luft. Når methemoglobinemi er diagnostisert, er den foretrukne behandlingen metylenblått, 1-2 mg/kg intravenøst.
KONTRAINDIKASJONER
IMDUR 20 mg tabletter er kontraindisert hos pasienter som har vist overfølsomhet eller idiosynkratiske reaksjoner på andre nitrater eller nitritter.
KLINISK FARMAKOLOGI
Virkningsmekanismen
IMDUR-produktet er en oral formulering med forlenget frigivelse av ISMN, den viktigste aktive metabolitten av isosorbiddinitrat; mesteparten av den kliniske aktiviteten til dinitratet kan tilskrives mononitratet.
Den viktigste farmakologiske virkningen av ISMN og alle organiske nitrater generelt er avslapning av vaskulær glatt muskulatur, noe som gir utvidelse av perifere arterier og vener, spesielt sistnevnte. Utvidelse av venene fremmer perifer samling av blod, reduserer venøs retur til hjertet, og reduserer derved venstre ventrikkel-enddiastolisk trykk og pulmonært kapillærkiletrykk (preload). Arteriolær avslapning reduserer systemisk vaskulær motstand, systolisk arterielt trykk og gjennomsnittlig arterielt trykk (afterload). Utvidelse av koronararteriene forekommer også. Den relative betydningen av forbelastningsreduksjon, etterbelastningsreduksjon og koronar dilatasjon forblir udefinert.
Farmakodynamikk
Doseringsregimer for de fleste kronisk brukte legemidler er utformet for å gi plasmakonsentrasjoner som kontinuerlig er høyere enn en minimalt effektiv konsentrasjon. Denne strategien er upassende for organiske nitrater. Flere godt kontrollerte kliniske studier har brukt treningstesting for å vurdere antianginal effekt av kontinuerlig tilførte nitrater. I det store flertallet av disse studiene kunne aktive stoffer ikke skilles fra placebo etter 24 timer (eller mindre) med kontinuerlig behandling. Forsøk på å overvinne toleranse ved doseøkning, selv til doser langt over de som brukes akutt, har konsekvent mislyktes. Først etter at nitrater har vært borte fra kroppen i flere timer, har deres antianginal effekt blitt gjenopprettet. IMDUR-tabletter, under langtidsbruk over 42 dager dosert med 120 mg én gang daglig, fortsatte å forbedre treningsytelsen 4 timer og 12 timer etter dosering, men effektene (selv om de er bedre enn placebo) er mindre enn eller i beste fall lik effekter av den første dosen på 60 mg.
Farmakokinetikk og metabolisme
Etter oral administrering av ISMN som oppløsning eller tabletter med øyeblikkelig frigjøring, oppnås maksimale plasmakonsentrasjoner av ISMN i løpet av 30 til 60 minutter, med en absolutt biotilgjengelighet på omtrent 100 %. Etter intravenøs administrering fordeles ISMN i hele kroppsvannet på ca. 9 minutter med et distribusjonsvolum på ca. 0,6-0,7 l/kg. Isosorbidmononitrat er omtrent 5 % bundet til humane plasmaproteiner og distribueres til blodceller og spytt. Isosorbidmononitrat metaboliseres primært av leveren, men i motsetning til oralt isosorbiddinitrat, er det ikke gjenstand for first-pass metabolisme. Isosorbidmononitrat elimineres ved denitrering til isosorbid og glukuronidering som mononitrat, med 96 % av den administrerte dosen utskilt i urinen innen 5 dager og bare ca. 1 % eliminert i feces. Minst seks forskjellige forbindelser er påvist i urin, med ca. 2 % av dosen utskilt som uendret medikament og minst fem metabolitter. Metabolittene er ikke farmakologisk aktive. Renal clearance utgjør bare ca. 4 % av total kroppsclearance. Gjennomsnittlig plasmaeliminasjonshalveringstid for ISMN er ca. 5 timer.
Disponeringen av ISMN hos pasienter med ulike grader av nyresvikt, levercirrhose eller hjertedysfunksjon ble evaluert og funnet å være lik den som ble observert hos friske personer. Eliminasjonshalveringstiden for ISMN ble ikke forlenget, og det var ingen legemiddelakkumulering hos pasienter med kronisk nyresvikt etter gjentatt oral dosering.
Farmakokinetikken og/eller biotilgjengeligheten til IMDUR 40 mg tabletter har blitt studert hos både normale frivillige og pasienter etter administrering av enkelt- og flerdoser. Data fra disse studiene tyder på at farmakokinetikken til ISMN administrert som IMDUR-tabletter er lik mellom normale friske frivillige og pasienter med angina pectoris. I enkelt- og flerdosestudier var farmakokinetikken til ISMN doseproporsjonal mellom 30 mg og 240 mg.
en flerdosestudie ble effekten av alder på den farmakokinetiske profilen til IMDUR 60 mg og 120 mg (2 × 60 mg) evaluert hos personer ≥45 år. Resultatene fra denne studien indikerer at det ikke er noen signifikante forskjeller i noen av de farmakokinetiske variablene til ISMN mellom eldre (≥65 år) og yngre individer (45–64 år) for IMDUR 60 mg-dosen. Administrering av IMDUR tabletter 120 mg (2 × 60 mg tabletter hver 24. time i 7 dager) ga en doseproporsjonal økning i Cmax og AUC, uten endringer i Tmax eller terminal halveringstid. Den eldre gruppen (65-74 år) viste 30 % lavere tilsynelatende oral clearance (Cl/F) etter den høyere dosen, dvs. 120 mg, sammenlignet med den yngre gruppen (45-64 år); Cl/F var ikke forskjellig mellom de to gruppene etter 60 mg-kuren. Mens Cl/F var uavhengig av dose i den yngre gruppen, viste den eldre gruppen litt lavere Cl/F etter 120 mg-kuren sammenlignet med 60 mg-kuren. Forskjellene mellom de to aldersgruppene var imidlertid ikke statistisk signifikante. I den samme studien viste kvinner en liten (15 %) reduksjon i clearance når dosen ble økt. Kvinner viste høyere AUC og Cmax sammenlignet med menn, men disse forskjellene ble tilskrevet av forskjeller i kroppsvekt mellom de to gruppene. Når dataene ble analysert med alder som variabel, indikerte resultatene at det ikke var noen signifikante forskjeller i noen av de farmakokinetiske variablene til ISMN mellom eldre (≥65 år) og yngre individer (45-64 år). Resultatene av denne studien bør imidlertid sees med forsiktighet på grunn av det lille antallet forsøkspersoner i hver aldersundergruppe og følgelig mangelen på tilstrekkelig statistisk kraft.
Følgende tabell oppsummerer viktige farmakokinetiske parametere for ISMN etter enkelt- og flerdoseadministrasjon av ISMN som mikstur eller IMDUR-tabletter:
Mateffekter
Matens innflytelse på biotilgjengeligheten til ISMN etter enkeltdoseadministrasjon av IMDUR tabletter 60 mg ble evaluert i tre forskjellige studier som involverte enten en "lett" frokost eller en frokost med høyt kaloriinnhold og høyt fettinnhold. Resultatene av disse studiene indikerer at samtidig matinntak kan redusere hastigheten (økning i Tmax), men ikke graden (AUC) av absorpsjon av ISMN.
Kliniske studier
Kontrollerte studier med IMDUR-tabletter har vist antianginal aktivitet etter akutt og kronisk dosering. Administrering av IMDUR 40 mg tabletter én gang daglig, tatt tidlig om morgenen ved oppreisning, gitt minst 12 timers antianginal aktivitet.
en placebokontrollert parallell studie ble 30, 60, 120 og 240 mg IMDUR 60 mg tabletter administrert én gang daglig i opptil 6 uker. Før randomisering fullførte alle pasienter en 1- til 3-ukers enkeltblind placebofase for å demonstrere nitratrespons og total reproduserbarhet for tredemølle. Treningstoleransetester ved bruk av Bruce-protokollen ble utført før og 4 og 12 timer etter morgendosen på dag 1, 7, 14, 28 og 42 i den dobbeltblinde perioden. IMDUR 60 mg tabletter 30 og 60 mg (kun doser evaluert akutt) viste en signifikant økning fra baseline i total tredemølletid i forhold til placebo 4 og 12 timer etter administrering av den første dosen. På dag 42 viste 120 og 240 mg doser av IMDUR 40 mg tabletter en signifikant økning i total tredemølletid 4 og 12 timer etter dosering, men på dag 42 var 30 og 60 mg dosene ikke lenger differensierbare fra placebo. Gjennom kronisk dosering ble det ikke observert rebound i noen IMDUR-behandlingsgruppe.
Samlet data fra to andre studier, som sammenlignet IMDUR 40 mg tabletter 60 mg én gang daglig, ISDN 30 mg QID og placebo QID hos pasienter med kronisk stabil angina ved bruk av en randomisert, dobbeltblind, treveis crossover-design, fant statistisk signifikant økning i treningstoleranse ganger for IMDUR 20 mg tabletter sammenlignet med placebo ved time 4, 8 og 12 og med ISDN ved time 4. Økningen i treningstoleranse på dag 14, selv om det er statistisk signifikant sammenlignet med placebo, var omtrent halvparten av det som ble sett på dag 1 av studien. .
PASIENTINFORMASJON
Pasienter bør informeres om at den antianginale effekten av IMDUR 60 mg tabletter kan opprettholdes ved å følge den foreskrevne doseringsplanen nøye. For de fleste pasienter kan dette oppnås ved å ta dosen når den oppstår.
Som med andre nitrater, følger daglig hodepine noen ganger behandling med isosorbidmononitrat. Hos pasienter som får denne hodepinen er hodepinen en markør for stoffets aktivitet. Pasienter bør motstå fristelsen til å unngå hodepine ved å endre behandlingsplanen med isosorbidmononitrat, siden tap av hodepine kan være assosiert med samtidig tap av antianginal effekt. Aspirin eller acetaminophen lindrer ofte vellykket isosorbidmononitrat-indusert hodepine uten skadelig effekt på isosorbidmononitrats antianginale effekt.
Behandling med isosorbidmononitrat kan være assosiert med ørhet når du står, spesielt like etter å ha reist seg fra liggende eller sittende stilling. Denne effekten kan være hyppigere hos pasienter som også har konsumert alkohol.
