Seroquel 25mg, 50mg, 100mg, 200mg, 300mg Quetiapine Bruk, bivirkninger og dosering. Pris i nettapotek. Generisk medisin uten resept.
Hva er Seroquel 100mg og hvordan brukes det?
Seroquel 50mg er en reseptbelagt medisin som brukes til å behandle symptomene på schizofreni, bipolar I-lidelse, mani; Bipolar lidelse, depressive episoder; Bipolar I lidelse, vedlikehold; og alvorlig depressiv lidelse. Seroquel 50mg kan brukes alene eller sammen med andre medisiner.
Seroquel tilhører en klasse med legemidler kalt antipsykotika, 2. generasjon; Antimaniske midler.
Det er ikke kjent om Seroquel 200mg er trygt og effektivt hos barn under 12 år.
Hva er de mulige bivirkningene av Seroquel 50mg?
Seroquel kan forårsake alvorlige bivirkninger, inkludert:
- . ukontrollerte muskelbevegelser i ansiktet (tygging, leppesmekking, rynking, tungebevegelse, blunking eller øyebevegelser), . maskelignende utseende av ansiktet, . problemer med å svelge, . problemer med tale, . svimmelhet, . alvorlig forstoppelse, . smertefull eller vanskelig vannlating, . tåkesyn, . tunnelsyn, . øyesmerter, . ser glorier rundt lys, . veldig stive (stive) muskler, . høy feber, . svette, . forvirring, . raske eller ujevne hjerteslag, . skjelvinger, . besvimelse, . økt tørst, . økt vannlating, . tørr i munnen, . lukt av fruktig pust, . feber, . frysninger, . munnsår, . hudsår, . sår hals, . hoste, og . problemer med å puste
Få medisinsk hjelp med en gang hvis du har noen av symptomene nevnt ovenfor.
De vanligste bivirkningene av Seroquel inkluderer:
- . taleproblemer, . svimmelhet, . døsighet, . tretthet, . lite energi, . raske hjerteslag, . tett nese, . økt appetitt, . vektøkning, . urolig mage, . oppkast, . forstoppelse, . tørr munn, og . unormal leverfunksjonstest
Fortell legen dersom du har noen bivirkninger som plager deg eller som ikke går over.
Dette er ikke alle mulige bivirkninger av Seroquel. Spør legen din eller apoteket for mer informasjon.
Ring legen din for medisinsk råd om bivirkninger. Du kan rapportere bivirkninger til FDA på 1-800-FDA-1088.
ADVARSEL
ØKT DØDELIGHET HOS ELDRE PASIENTER MED DEMENSRELATERT PSYKOSE; og SELVmordstanker og adferd
Økt dødelighet hos eldre pasienter med demensrelatert psykose
Eldre pasienter med demensrelatert psykose behandlet med antipsykotiske legemidler har økt risiko for død [se ADVARSLER OG FORHOLDSREGLER]. SEROQUEL er ikke godkjent for behandling av pasienter med demensrelatert psykose [se ADVARSLER OG FORHOLDSREGLER].
Selvmordstanker og -adferd
Antidepressiva økte risikoen for selvmordstanker og -adferd hos barn, ungdom og unge voksne i korttidsstudier. Disse studiene viste ikke en økning i risikoen for selvmordstanker og -adferd ved bruk av antidepressiva hos pasienter over 24 år; det var en reduksjon i risiko ved bruk av antidepressiva hos pasienter i alderen 65 år og eldre [se ADVARSLER OG FORHOLDSREGLER].
Hos pasienter i alle aldre som starter på antidepressiv behandling, overvåk nøye for forverring og for fremvekst av selvmordstanker og selvmordsatferd. Informer familier og omsorgspersoner om behovet for tett observasjon og kommunikasjon med forskriveren [se ADVARSLER OG FORHOLDSREGLER].
SEROQUEL 50mg er ikke godkjent for bruk hos pediatriske pasienter under ti år [se Bruk i spesifikke populasjoner].
BESKRIVELSE
SEROQUEL® (quetiapinfumarat) er et psykotropt middel som tilhører en kjemisk klasse, dibenzotiazepinderivatene. Den kjemiske betegnelsen er 2-[2-(4-dibenzo[b,f][1,4]tiazepin-11-yl-1-piperazinyl)etoksy]-etanolfumarat (2:1) (salt). Det er tilstede i tabletter som fumaratsaltet. Alle doser og tablettstyrker er uttrykt som milligram base, ikke som fumaratsalt. Dens molekylformel er C42H50N6O4S2•C4H4O4 og den har en molekylvekt på 883,11 (fumaratsalt). Strukturformelen er:
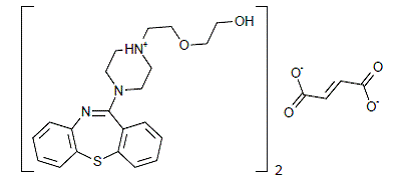
Quetiapinfumarat er et hvitt til off-white krystallinsk pulver som er moderat løselig i vann.
SEROQUEL leveres for oral administrering som 25 mg (rund, fersken), 50 mg (rund, hvit), 100 mg (rund, gul), 200 mg (rund, hvit), 300 mg (kapselformet, hvit) og 400 mg (kapselformede, gule) tabletter.
Inaktive ingredienser er povidon, dibasisk dikalsiumfosfatdihydrat, mikrokrystallinsk cellulose, natriumstivelsesglykolat, laktosemonohydrat, magnesiumstearat, hypromellose, polyetylenglykol og titandioksid.
25 mg tablettene inneholder rødt jernoksid og gult jernoksid og 100 mg og 400 mg tablettene inneholder kun gult jernoksid.
INDIKASJONER
Schizofreni
SEROQUEL XR er indisert for behandling av schizofreni. Effekten av SEROQUEL XR ved schizofreni ble fastslått i en 6-ukers og en vedlikeholdsstudie hos voksne med schizofreni. Effekten ble støttet av tre 6-ukers studier med voksne med schizofreni og en 6-ukers studie hos ungdommer med schizofreni (13-17 år) behandlet med SEROQUEL [se Kliniske studier ].
Bipolar lidelse
SEROQUEL 25mg XR er indisert for akutt behandling av maniske eller blandede episoder assosiert med bipolar lidelse I, både som monoterapi og som et tillegg til litium eller divalproex. Effekten av SEROQUEL XR ved maniske eller blandede episoder av bipolar I-lidelse ble fastslått i en 3-ukers studie hos voksne med maniske eller blandede episoder assosiert med bipolar I-lidelse. Effekten ble støttet av to 12-ukers monoterapistudier og en 3-ukers tilleggsstudie hos voksne med maniske episoder assosiert med bipolar I lidelse, samt en 3-ukers monoterapistudie hos barn og ungdom (10 - 17 år) med maniske episoder assosiert med bipolar lidelse I behandlet med SEROQUEL [se Kliniske studier ].
SEROQUEL 100mg XR er indisert for akutt behandling av depressive episoder assosiert med bipolar lidelse. Effekten av SEROQUEL XR ble fastslått i en 8-ukers studie hos voksne med bipolar I eller II lidelse og støttet av to 8-ukers studier hos voksne med bipolar I eller II lidelse behandlet med SEROQUEL [se Kliniske studier ].
SEROQUEL 100mg XR er indisert for vedlikeholdsbehandling av bipolar lidelse I, som et tillegg til litium eller divalproex. Effekten ble ekstrapolert fra to vedlikeholdsstudier hos voksne med bipolar I lidelse behandlet med SEROQUEL. Effektiviteten av monoterapi for vedlikeholdsbehandling av bipolar lidelse I har ikke blitt systematisk evaluert i kontrollerte kliniske studier [se Kliniske studier ].
Tilleggsbehandling av alvorlig depressiv lidelse (MDD)
SEROQUEL 100mg XR er indisert for bruk som tilleggsbehandling til antidepressiva for behandling av MDD. Effekten av SEROQUEL XR som tilleggsbehandling til antidepressiva ved MDD ble fastslått i to 6-ukers studier hos voksne med MDD som hadde utilstrekkelig respons på antidepressiv behandling [se Kliniske studier ].
Spesielle hensyn ved behandling av pediatrisk schizofreni og bipolar I-lidelse
Pediatrisk schizofreni og bipolar lidelse I er alvorlige psykiske lidelser, men diagnosen kan være utfordrende. For pediatrisk schizofreni kan symptomprofilene variere, og for bipolar lidelse I kan pasienter ha varierende periodisitetsmønstre av maniske eller blandede symptomer. Det anbefales at medikamentell behandling for pediatrisk schizofreni og bipolar lidelse I startes først etter at en grundig diagnostisk evaluering er utført og nøye overveielse av risikoene forbundet med medikamentell behandling. Medisineringsbehandling for både pediatrisk schizofreni og bipolar lidelse I er indisert som en del av et totalbehandlingsprogram som ofte inkluderer psykologiske, pedagogiske og sosiale intervensjoner.
DOSERING OG ADMINISTRASJON
Viktige administrasjonsinstruksjoner
SEROQUEL XR tabletter skal svelges hele og ikke deles, tygges eller knuses.
Det anbefales at SEROQUEL 50 mg XR tas uten mat eller sammen med et lett måltid (omtrent 300 kalorier) [se KLINISK FARMAKOLOGI ].
SEROQUEL 25mg XR bør administreres én gang daglig, helst om kvelden.
Anbefalt dosering
Anbefalt startdose, titrering, doseområde og maksimal SEROQUEL 50 mg XR-dose for hver godkjent indikasjon er vist i tabell 1 nedenfor. Etter initial dosering kan justeringer gjøres oppover eller nedover, om nødvendig, avhengig av den kliniske responsen og toleransen til pasienten [se Kliniske studier ].
Vedlikeholdsbehandling for schizofreni og bipolar lidelse I
Vedlikeholdsbehandling
Pasienter bør periodisk revurderes for å fastslå behovet for vedlikeholdsbehandling og passende dose for slik behandling [se Kliniske studier ].
Doseendringer hos eldre pasienter
Det bør vurderes en langsommere dosetitreringshastighet og en lavere måldose hos eldre og hos pasienter som er svekkede eller som har en disposisjon for hypotensive reaksjoner [se Bruk i spesifikke populasjoner , og KLINISK FARMAKOLOGI ]. Når det er indisert, bør doseøkning utføres med forsiktighet hos disse pasientene.
Eldre pasienter bør startes med SEROQUEL XR 50 mg/dag og dosen kan økes i trinn på 50 mg/dag avhengig av den kliniske responsen og toleransen til den enkelte pasient.
Doseendringer hos pasienter med nedsatt leverfunksjon
Pasienter med nedsatt leverfunksjon bør startes med SEROQUEL XR 50 mg/dag. Dosen kan økes daglig i trinn på 50 mg/dag til en effektiv dose, avhengig av pasientens kliniske respons og toleranse.
Doseendringer når det brukes sammen med CYP3A4-hemmere
SEROQUEL XR-dosen bør reduseres til en sjettedel av den opprinnelige dosen når det tas samtidig med en potent CYP3A4-hemmer (f.eks. ketokonazol, itrakonazol, indinavir, ritonavir, nefazodon, etc.). Når CYP3A4-hemmeren seponeres, bør dosen av SEROQUEL XR økes med 6 ganger [se KLINISK FARMAKOLOGI og NARKOTIKAHANDEL ].
Doseendringer når det brukes sammen med CYP3A4-induktorer
SEROQUEL XR-dosen bør økes opp til 5 ganger den opprinnelige dosen når den brukes i kombinasjon med en kronisk behandling (f.eks. mer enn 7-14 dager) av en potent CYP3A4-induktor (f.eks. fenytoin, karbamazepin, rifampin, avasimibe, St. John's wort etc.). Dosen bør titreres basert på den kliniske responsen og toleransen til den enkelte pasient. Når CYP3A4-induktoren seponeres, bør dosen av SEROQUEL 100 mg XR reduseres til det opprinnelige nivået innen 7-14 dager [se KLINISK FARMAKOLOGI og NARKOTIKAHANDEL ].
Re-initiering av behandling hos pasienter som tidligere er avbrutt
Selv om det ikke finnes data som spesifikt tar for seg gjenoppstart av behandling, anbefales det at den initiale doseringsplanen følges ved gjenoppstart av behandling av pasienter som har vært av Seroquel 50 mg XR i mer enn én uke. Ved restart av pasienter som har vært av Seroquel 300 mg XR i mindre enn én uke, kan det hende at gradvis doseøkning ikke er nødvendig, og vedlikeholdsdosen kan startes på nytt.
Bytte pasienter fra SEROQUEL 50mg tabletter til SEROQUEL 100mg XR tabletter
Pasienter som for tiden behandles med SEROQUEL (formulering med umiddelbar frigjøring) kan byttes til SEROQUEL XR med tilsvarende total daglig dose tatt én gang daglig. Individuelle dosejusteringer kan være nødvendig.
Bytte fra antipsykotika
Det er ingen systematisk innsamlet data for å spesifikt adressere overganger fra andre antipsykotika til SEROQUEL 200mg XR, eller angående samtidig administrering med andre antipsykotika. Mens umiddelbar seponering av den tidligere antipsykotiske behandlingen kan være akseptabel for noen pasienter, kan mer gradvis seponering være mest hensiktsmessig for andre. I alle tilfeller bør perioden med overlappende antipsykotisk administrering minimeres. Ved bytte av pasienter fra depotantipsykotika, hvis det er medisinsk hensiktsmessig, initier SEROQUEL XR-behandling i stedet for neste planlagte injeksjon. Behovet for å fortsette eksisterende ekstrapyramidalt syndrom-medisinering bør revurderes med jevne mellomrom.
HVORDAN LEVERES
Doseringsformer og styrker
- . 50 mg tabletter med forlenget frigivelse er ferskenfargede, filmdrasjerte, kapselformet, bikonvekse, oppskjærte tabletter med "XR 50" på den ene siden og vanlig på den andre siden . 150 mg tabletter med forlenget frigivelse er hvite, filmdrasjerte, kapselformede, bikonvekse, oppskjærte tabletter med "XR 150" på den ene siden og vanlig på den andre siden . 200 mg tabletter med forlenget frigivelse er gule, filmdrasjerte, kapselformede, bikonvekse, intagliterte tabletter med "XR 200" på den ene siden og vanlig på den andre siden . 300 mg tabletter med forlenget frigivelse er blekgule, filmdrasjerte, kapselformede, bikonvekse, intagliterte tabletter med "XR 300" på den ene siden og vanlig på den andre siden . 400 mg tabletter med forlenget frigivelse er hvite, filmdrasjerte, kapselformede, bikonvekse, innskårne tabletter med "XR 400" på den ene siden og vanlig på den andre siden
Oppbevaring og håndtering
50 mg tabletter ( NDC 0310-0280-60) fersken, filmdrasjert, kapselformet, bikonveks, stivnet tablett med "XR 50" på den ene siden og vanlig på den andre, leveres i flasker med 60 tabletter.
150 mg tabletter ( NDC 0310-0281-60) hvit, filmdrasjert, kapselformet, bikonveks, stivnet tablett med "XR 150" på den ene siden og vanlig på den andre, leveres i flasker med 60 tabletter.
200 mg tabletter ( NDC 0310-0282-60) gul, filmdrasjert, kapselformet, bikonveks, stivnet tablett med "XR 200" på den ene siden og vanlig på den andre, leveres i flasker med 60 tabletter.
300 mg tabletter ( NDC 0310-0283-60) blekgul, filmdrasjert, kapselformet, bikonveks, intaglitated tablett med "XR 300" på den ene siden og vanlig på den andre, leveres i flasker med 60 tabletter.
400 mg tabletter ( NDC 0310-0284-60) hvit, filmdrasjert, kapselformet, bikonveks, intaglitated tablett med "XR 400" på den ene siden og vanlig på den andre, leveres i flasker med 60 tabletter.
Oppbevar SEROQUEL XR ved 25°C (77°F); utflukter tillatt til 15-30°C (59-86°F) [Se USP ].
Distribuert av: AstraZeneca Pharmaceuticals LP, Wilmington, DE 19850. Revidert: Mar 2020
BIVIRKNINGER
Følgende bivirkninger er omtalt mer detaljert i andre deler av merkingen:
- . Økt dødelighet hos eldre pasienter med demensrelatert psykose [se ADVARSLER OG FORHOLDSREGLER ] . Selvmordstanker og -atferd hos ungdom og unge voksne [se ADVARSLER OG FORHOLDSREGLER ] . Cerebrovaskulære bivirkninger, inkludert hjerneslag hos eldre pasienter med demensrelatert psykose [se ADVARSLER OG FORHOLDSREGLER ] . Malignt nevroleptikasyndrom (NMS) [se ADVARSLER OG FORHOLDSREGLER ] . Metabolske endringer (hyperglykemi, dyslipidemi, vektøkning) [se ADVARSLER OG FORHOLDSREGLER ] . Tardiv dyskinesi [se ADVARSLER OG FORHOLDSREGLER ] . Hypotensjon [se ADVARSLER OG FORHOLDSREGLER ] . Falls [se ADVARSLER OG FORHOLDSREGLER ] . Økning i blodtrykk (barn og ungdom) [se ADVARSLER OG FORHOLDSREGLER ] . Leukopeni, nøytropeni og agranulocytose [se ADVARSLER OG FORHOLDSREGLER ] . Grå stær [se ADVARSLER OG FORHOLDSREGLER ] . QT-forlengelse [se ADVARSLER OG FORHOLDSREGLER ] . Anfall [se ADVARSLER OG FORHOLDSREGLER ] . Hypotyreose [se ADVARSLER OG FORHOLDSREGLER ] . Hyperprolaktinemi [se ADVARSLER OG FORHOLDSREGLER ] . Potensial for kognitiv og motorisk svekkelse [se ADVARSLER OG FORHOLDSREGLER ] . Kroppstemperaturregulering [se ADVARSLER OG FORHOLDSREGLER ] . Dysfagi [se ADVARSLER OG FORHOLDSREGLER ] . Seponeringssyndrom [se ADVARSLER OG FORHOLDSREGLER ] . Antikolinerge (antimuskarine) effekter [se ADVARSLER OG FORHOLDSREGLER ]
Erfaring fra kliniske studier
Fordi kliniske studier utføres under vidt forskjellige forhold, kan bivirkningsrater observert i kliniske studier av et legemiddel ikke sammenlignes direkte med rater i kliniske studier av et annet medikament og gjenspeiler kanskje ikke ratene observert i praksis.
Voksne
Informasjonen nedenfor er hentet fra en database med kliniske studier for SEROQUEL 200 mg bestående av over 4300 pasienter. Denne databasen inkluderer 698 pasienter eksponert for SEROQUEL for behandling av bipolar depresjon, 405 pasienter eksponert for SEROQUEL 200 mg for behandling av akutt bipolar mani (monoterapi og tilleggsbehandling), 646 pasienter eksponert for SEROQUEL for vedlikeholdsbehandling av bipolar I lidelse som tillegg. behandling, og ca. 2600 pasienter og/eller normale forsøkspersoner eksponert for 1 eller flere doser av SEROQUEL 200 mg for behandling av schizofreni.
Av disse ca. 4 300 forsøkspersonene var ca. 4000 (2300 ved schizofreni, 405 ved akutt bipolar mani, 698 ved bipolar depresjon og 646 for vedlikeholdsbehandling av bipolar I-lidelse) pasienter som deltok i effektivitetsstudier med flere doser, og deres erfaring tilsvarte ca 2400 pasientår. Betingelsene og varigheten av behandlingen med SEROQUEL 200 mg varierte sterkt og inkluderte (i overlappende kategorier) åpne og dobbeltblindede faser av studier, innlagte og polikliniske pasienter, fastdose- og dosetitreringsstudier og kortsiktige eller lengre sikt eksponering. Bivirkninger ble vurdert ved å samle inn bivirkninger, resultater av fysiske undersøkelser, vitale tegn, vekter, laboratorieanalyser, EKG og resultater fra oftalmologiske undersøkelser.
De oppgitte bivirkningsfrekvensene representerer andelen individer som minst én gang opplevde en bivirkning av den oppførte typen.
Bivirkninger forbundet med seponering av behandling i kortsiktige, placebokontrollerte studier
Schizofreni
Totalt sett var det liten forskjell i forekomsten av seponering på grunn av bivirkninger (4 % for SEROQUEL vs. 3 % for placebo) i en pool av kontrollerte studier. Seponering på grunn av søvnighet (0,8 % SEROQUEL 100 mg vs. 0 % placebo) og hypotensjon (0,4 % SEROQUEL 200 mg vs. 0 % placebo) ble imidlertid ansett for å være medikamentrelatert [se ADVARSLER OG FORHOLDSREGLER ].
Bipolar lidelse
Mani
Samlet sett var seponeringer på grunn av bivirkninger 5,7 % for SEROQUEL 25 mg vs. 5,1 % for placebo i monoterapi og 3,6 % for SEROQUEL vs. 5,9 % for placebo i tilleggsbehandling.
Depresjon
Samlet sett var seponeringer på grunn av bivirkninger 12,3 % for SEROQUEL 300 mg vs. 19,0 % for SEROQUEL 600 mg og 5,2 % for placebo.
Vanlige observerte bivirkninger i kortsiktige, placebokontrollerte forsøk
studier med akutt behandling av schizofreni (opptil 6 uker) og bipolar mani (opptil 12 uker), var de vanligst observerte bivirkningene assosiert med bruk av SEROQUEL monoterapi (insidens på 5 % eller mer) og observert med en hastighet på Seroquel minst dobbelt så stor som for placebo var søvnighet (18 %), svimmelhet (11 %), munntørrhet (9 %), forstoppelse (8 %), økt ALAT (5 %), vektøkning (5 %) og dyspepsi ( 5 %).
Bivirkninger som oppstår med en forekomst på 2 % eller mer blant SEROQUEL-behandlede pasienter i kortsiktige, placebokontrollerte studier
Forskriveren bør være oppmerksom på at tallene i tabeller og tabeller ikke kan brukes til å forutsi forekomst av bivirkninger i løpet av vanlig medisinsk praksis der pasientkarakteristikker og andre faktorer avviker fra de som var fremherskende i de kliniske forsøkene. Tilsvarende kan de siterte frekvensene ikke sammenlignes med tall hentet fra andre kliniske undersøkelser som involverer ulike behandlinger, bruksområder og etterforskere. De siterte tallene gir imidlertid den forskrivende legen et visst grunnlag for å estimere det relative bidraget til medikamentelle og ikke-medikamentelle faktorer til bivirkningsforekomsten i befolkningen som ble studert.
Tabell 9 oppregner forekomsten, avrundet til nærmeste prosent, av bivirkninger som oppsto under akuttbehandling av schizofreni (opptil 6 uker) og bipolar mani (opptil 12 uker) hos 2 % eller flere av pasientene behandlet med SEROQUEL (doser som varierer fra 75 til 800 mg/dag) der insidensen hos pasienter behandlet med SEROQUEL var høyere enn forekomsten hos placebobehandlede pasienter.
I studier med akutt tilleggsbehandling av bipolar mani (opptil 3 uker), var de vanligst observerte bivirkningene assosiert med bruk av SEROQUEL (insidens på 5 % eller mer) og observert med en hastighet på SEROQUEL minst to ganger den for placebo. somnolens (34%), munntørrhet (19%), asteni (10%), forstoppelse (10%), magesmerter (7%), postural hypotensjon (7%), faryngitt (6%) og vektøkning (6%) %).
Tabell 10 oppregner forekomsten, avrundet til nærmeste prosent, av bivirkninger som oppsto under behandling (opptil 3 uker) av akutt mani hos 2 % eller flere av pasientene behandlet med SEROQUEL (doser fra 100 til 800 mg/dag) brukt. som tilleggsbehandling til litium og divalproex hvor forekomsten hos pasienter behandlet med SEROQUEL var høyere enn forekomsten hos placebobehandlede pasienter.
I bipolare depresjonsstudier (opptil 8 uker) var de vanligst observerte bivirkningene assosiert med bruk av SEROQUEL (forekomst på 5 % eller mer) og observert med en hastighet på SEROQUEL 200 mg minst dobbelt så høy som for placebo somnolens (57 % ), munntørrhet (44 %), svimmelhet (18 %), forstoppelse (10 %) og sløvhet (5 %).
Tabell 11 oppregner forekomsten, avrundet til nærmeste prosent, av bivirkninger som oppsto under behandling (opptil 8 uker) av bipolar depresjon hos 2 % eller flere av pasientene behandlet med SEROQUEL (doser på 300 og 600 mg/dag) der insidensen hos pasienter behandlet med SEROQUEL var høyere enn forekomsten hos placebobehandlede pasienter.
Undersøkelser etter interaksjoner på grunnlag av kjønn, alder og rase avslørte ingen klinisk betydningsfulle forskjeller i bivirkningsforekomsten på grunnlag av disse demografiske faktorene.
Doseavhengighet av uønskede reaksjoner i kortsiktige, placebokontrollerte forsøk
Doserelaterte bivirkninger
Spontant utløste bivirkningsdata fra en studie av schizofreni som sammenlignet fem faste doser av SEROQUEL (75 mg, 150 mg, 300 mg, 600 mg og 750 mg/dag) med placebo ble undersøkt for doserelaterte bivirkninger. Logistiske regresjonsanalyser avslørte en positiv doserespons (p
Bivirkninger i kliniske studier med quetiapin og ikke oppført andre steder på etiketten:
Følgende bivirkninger er også rapportert med kvetiapin: mareritt, overfølsomhet og forhøyede serumkreatinfosfokinase (ikke assosiert med NMS), galaktoré, bradykardi (som kan oppstå ved eller nær behandlingsstart og være assosiert med hypotensjon og/eller synkope ) reduserte blodplater, somnambulisme (og andre relaterte hendelser), forhøyede gamma-GT-nivåer, hypotermi, dyspné, eosinofili, urinretensjon, intestinal obstruksjon og priapisme.
Ekstrapyramidale symptomer (EPS)
Dystoni
Klasseeffekt
Symptomer på dystoni, langvarige unormale sammentrekninger av muskelgrupper, kan forekomme hos følsomme individer i løpet av de første dagene av behandlingen. Dystoniske symptomer inkluderer: spasmer i nakkemusklene, noen ganger utvikler seg til tetthet i halsen, svelgevansker, pustevansker og/eller tungefremspring. Selv om disse symptomene kan oppstå ved lave doser, forekommer de hyppigere og med større alvorlighetsgrad med høy styrke og ved høyere doser av førstegenerasjons antipsykotiske legemidler. En forhøyet risiko for akutt dystoni er observert hos menn og yngre aldersgrupper.
Fire metoder ble brukt for å måle EPS: (1) Simpson-Angus totalscore (gjennomsnittlig endring fra baseline) som evaluerer Parkinsonisme og akatisi, (2) Barnes Akathisia Rating Scale (BARS) Global Assessment Score, (3) forekomst av spontane klager av EPS (akatisi, akinesi, tannhjulstivhet, ekstrapyramidalt syndrom, hypertoni, hypokinesi, nakkestivhet og tremor), og (4) bruk av antikolinerge medisiner for å behandle EPS.
Voksne
Data fra en 6-ukers klinisk studie av schizofreni som sammenlignet fem faste doser av SEROQUEL (75, 150, 300, 600, 750 mg/dag) ga bevis for mangel på ekstrapyramidale symptomer (EPS) og doserelatert for EPS assosiert med SEROQUEL 100mg behandling. Tre metoder ble brukt for å måle EPS: (1) Simpson-Angus totalscore (gjennomsnittlig endring fra baseline) som evaluerer Parkinsonisme og akatisi, (2) forekomst av spontane plager av EPS (akatisi, akinesi, tannhjulstivhet, ekstrapyramidalt syndrom, hypertoni, hypokinesi, nakkestivhet og skjelving), og (3) bruk av antikolinerge medisiner mot EPS.
tabell 12 inkluderte dystoniske hendelser nakkestivhet, hypertoni, dystoni, muskelstivhet, okulogirasjon; parkinsonisme inkluderte tannhjulstivhet, skjelving, sikling, hypokinesi; akatisi inkluderte akatisi, psykomotorisk agitasjon; dyskinetisk hendelse inkluderte tardiv dyskinesi, dyskinesi, koreoatetose; og andre ekstrapyramidale hendelser inkluderte rastløshet, ekstrapyramidale lidelser, bevegelsesforstyrrelser.
Insidensrater for parkinsonisme målt ved Simpson-Angus totalscore for placebo og de fem faste dosene (75, 150, 300, 600, 750 mg/dag) var: -0,6; -1,0, -1,2; -1,6; -1,8 og -1,8. Hyppigheten av antikolinerge medisiner som ble brukt for å behandle EPS for placebo og de fem faste dosene var: 14 %; 11%; 10 %; 8 %; 12 % og 11 %.
ytterligere seks placebokontrollerte kliniske studier (3 ved akutt mani og 3 ved schizofreni) med variable doser av SEROQUEL, var det ingen forskjeller mellom SEROQUEL- og placebobehandlingsgruppene i forekomsten av EPS, vurdert av Simpson-Angus totalskåre, spontane klager på EPS og bruk av samtidig antikolinerge medisiner for å behandle EPS.
I to placebokontrollerte kliniske studier for behandling av bipolar depresjon ved bruk av 300 mg og 600 mg SEROQUEL 100 mg, var forekomsten av bivirkninger potensielt relatert til EPS 12 % i begge dosegruppene og 6 % i placebogruppen. I disse studiene var forekomsten av de individuelle bivirkningene (akatisi, ekstrapyramidal lidelse, tremor, dyskinesi, dystoni, rastløshet, ufrivillige muskelkontraksjoner, psykomotorisk hyperaktivitet og muskelstivhet) generelt lav og oversteg ikke 4 % i noen behandlingsgruppe.
De 3 behandlingsgruppene var like i gjennomsnittlig endring i SAS total score og BARS Global Assessment score ved slutten av behandlingen. Bruk av samtidig antikolinerge medisiner var sjelden og lik på tvers av de tre behandlingsgruppene.
Barn Og Ungdom
Informasjonen nedenfor er hentet fra en database med kliniske studier for SEROQUEL 200 mg bestående av over 1000 pediatriske pasienter. Denne databasen inkluderer 677 pasienter eksponert for SEROQUEL 200 mg for behandling av schizofreni og 393 barn og ungdom (10-17 år) eksponert for SEROQUEL for behandling av akutt bipolar mani.
Bivirkninger forbundet med seponering av behandling i kortsiktige, placebokontrollerte forsøk
Schizofreni
Forekomsten av seponering på grunn av bivirkninger for quetiapin-behandlede og placebo-behandlede pasienter var henholdsvis 8,2 % og 2,7 %. Bivirkningen som førte til seponering hos 1 % eller flere av pasientene på SEROQUEL og med en høyere forekomst enn placebo, var somnolens (2,7 % og 0 % for placebo).
Bipolar I Mania
Forekomsten av seponering på grunn av bivirkninger for quetiapin-behandlede og placebo-behandlede pasienter var henholdsvis 11,4 % og 4,4 %. Bivirkningene som førte til seponering hos 2 % eller flere av pasientene på SEROQUEL og med en høyere forekomst enn placebo, var søvnighet (4,1 % vs. 1,1 %) og tretthet (2,1 % vs. 0).
Vanlige observerte bivirkninger i kortsiktige, placebokontrollerte forsøk
I behandling for schizofreni (opptil 6 uker) var de vanligst observerte bivirkningene assosiert med bruk av kvetiapin hos ungdom (forekomst på 5 % eller høyere og kvetiapinforekomst minst dobbelt så høy som for placebo) somnolens (34%), svimmelhet (12 %), munntørrhet (7 %), takykardi (7 %).
Ved bipolar manibehandling (opptil 3 uker) var de vanligst observerte bivirkningene assosiert med bruk av kvetiapin hos barn og ungdom (forekomst på 5 % eller mer og kvetiapinforekomst minst dobbelt så høy som for placebo) somnolens (53 %). svimmelhet (18 %), tretthet (11 %), økt appetitt (9 %), kvalme (8 %), oppkast (8 %), takykardi (7 %), munntørrhet (7 %) og vektøkning (6 % ).
I en akutt (8-ukers) SEROQUEL 100 mg XR-studie hos barn og ungdom (10-17 år) med bipolar depresjon, hvor effekt ikke ble fastslått, var de vanligst observerte bivirkningene forbundet med bruk av SEROQUEL XR (forekomst på 5 % eller mer og minst det dobbelte av placebo) var svimmelhet 7 %, diaré 5 %, tretthet 5 % og kvalme 5 %.
Bivirkninger som oppstår med en forekomst på ≥ 2 % blant SEROQUEL 300 mg-behandlede pasienter i kortsiktige, placebokontrollerte studier
Schizofreni (ungdom, 13–17 år)
Følgende funn var basert på en 6-ukers placebokontrollert studie der quetiapin ble administrert i enten doser på 400 eller 800 mg/dag.
Tabell 13 oppregner forekomsten, avrundet til nærmeste prosent, av bivirkninger som oppsto under behandling (opptil 6 uker) av schizofreni hos 2 % eller flere av pasientene behandlet med SEROQUEL (doser på 400 eller 800 mg/dag) hvor forekomsten hos pasienter behandlet med SEROQUEL var minst to ganger insidensen hos placebobehandlede pasienter.
Bivirkninger som potensielt var doserelaterte med høyere frekvens i 800 mg-gruppen sammenlignet med 400 mg-gruppen inkluderte svimmelhet (8 % vs. 15 %), munntørrhet (4 % vs. 10 %) og takykardi (6 % vs. 11 %).
Bipolar I-mani (barn og ungdom 10-17 år)
Følgende funn var basert på en 3-ukers placebokontrollert studie der quetiapin ble administrert i enten doser på 400 eller 600 mg/dag.
Vanlige observerte bivirkninger
Ved bipolar manibehandling (opptil 3 uker) var de vanligst observerte bivirkningene assosiert med bruk av kvetiapin hos barn og ungdom (forekomst på 5 % eller mer og kvetiapinforekomst minst dobbelt så høy som for placebo) somnolens (53 %). svimmelhet (18 %), tretthet (11 %), økt appetitt (9 %), kvalme (8 %), oppkast (8 %), takykardi (7 %), munntørrhet (7 %) og vektøkning (6 % ).
Tabell 14 oppregner forekomsten, avrundet til nærmeste prosent, av bivirkninger som oppsto under behandling (opptil 3 uker) av bipolar mani hos 2 % eller flere av pasientene behandlet med SEROQUEL (doser på 400 eller 600 mg/dag) der insidensen hos pasienter behandlet med SEROQUEL var høyere enn forekomsten hos placebobehandlede pasienter.
Bivirkninger som potensielt var doserelaterte med høyere frekvens i 600 mg-gruppen sammenlignet med 400 mg-gruppen inkluderte somnolens (50 % vs. 57 %), kvalme (6 % vs. 10 %) og takykardi (6 % vs. 9 %).
Ekstrapyramidale symptomer
en kortvarig placebokontrollert monoterapistudie hos ungdomspasienter med schizofreni (6 ukers varighet), var den samlede forekomsten av ekstrapyramidale symptomer 12,9 % (19/147) for SEROQUEL 100 mg og 5,3 % (4/75) for placebo, Selv om forekomsten av de individuelle bivirkningene (akatisi, skjelving, ekstrapyramidal lidelse, hypokinesi, rastløshet, psykomotorisk hyperaktivitet, muskelstivhet, dyskinesi) ikke oversteg 4,1 % i noen behandlingsgruppe. I en korttids placebokontrollert monoterapistudie hos barn og ungdomspasienter med bipolar mani (3 ukers varighet), var den samlede forekomsten av ekstrapyramidale symptomer 3,6 % (7/193) eller SEROQUEL og 1,1 % (1/90) for placebo.
Tabell 15 viser en liste over pasienter med bivirkninger potensielt assosiert med ekstrapyramidale symptomer i den kortsiktige placebokontrollerte monoterapistudien hos ungdomspasienter med schizofreni (6 ukers varighet).
tabell 15–16 inkluderte dystoniske hendelser nakkestivhet, hypertoni og muskelstivhet; parkinsonisme inkluderte tannhjulstivhet og skjelving; akatisi inkluderte bare akatisi; dyskinetisk hendelse inkluderte tardiv dyskinesi, dyskinesi og koreoatetose; og andre ekstrapyramidale hendelser inkluderte rastløshet og ekstrapyramidal lidelse.
Tabell 16 viser en liste over pasienter med bivirkninger assosiert med ekstrapyramidale symptomer i en korttids placebokontrollert monoterapistudie hos barn og ungdomspasienter med bipolar mani (3 ukers varighet).
Laboratorie-, EKG- og vitale tegnendringer observert i kliniske studier
Laboratorieendringer
Antall nøytrofiler
Voksne
placebokontrollerte kliniske monoterapistudier som involverte 3368 pasienter på quetiapinfumarat og 1515 på placebo, var forekomsten av minst én forekomst av nøytrofiltall ADVARSLER OG FORHOLDSREGLER ].
Transaminaseforhøyelser
Voksne
Asymptomatiske, forbigående og reversible økninger i serumtransaminaser (primært ALAT) er rapportert. I schizofrenistudier hos voksne var andelen pasienter med transaminaseforhøyelser på >3 ganger øvre grense for det normale referanseområdet i en samling av 3 til 6 ukers placebokontrollerte studier omtrent 6 % (29/483) for SEROQUEL sammenlignet med 1 % (3/194) for placebo. I forsøk med akutt bipolar mani hos voksne var andelen pasienter med transaminaseøkninger på >3 ganger øvre grense for det normale referanseområdet i en samling av 3-12 ukers placebokontrollerte studier ca. 1 % for både SEROQUEL (3 /560) og placebo (3/294). Disse hepatiske enzymforhøyelsene skjedde vanligvis i løpet av de første 3 ukene av medikamentell behandling og returnerte umiddelbart til nivåer før studien med pågående behandling med SEROQUEL. I bipolare depresjonsstudier var andelen pasienter med transaminaseøkninger på >3 ganger øvre grense for det normale referanseområdet i to 8-ukers placebokontrollerte studier 1 % (5/698) for SEROQUEL 50 mg og 2 % (6/ 347) for placebo.
Redusert hemoglobin
Voksne
I korttids placebokontrollerte studier forekom reduksjoner i hemoglobin til ≤13 g/dL menn, ≤12 g/dL kvinner ved minst én anledning hos 8,3 % (594/7155) av quetiapin-behandlede pasienter sammenlignet med 6,2 % ( 219/3536) av pasienter behandlet med placebo. I en database med kontrollerte og ukontrollerte kliniske studier forekom reduksjoner i hemoglobin til ≤13 g/dL menn, ≤12 g/dL kvinner ved minst én anledning hos 11 % (2277/20729) av quetiapin-behandlede pasienter.
Interferens med skjermer for urinmedisin
Det har vært litteraturrapporter som tyder på falske positive resultater i urinenzymimmunanalyser for metadon og trisykliske antidepressiva hos pasienter som har tatt quetiapin. Forsiktighet bør utvises ved tolkningen av positive urinmedisinske screeningsresultater for disse legemidlene, og bekreftelse ved hjelp av alternativ analyseteknikk (f.eks. kromatografiske metoder) bør vurderes.
EKG-endringer
Voksne
Sammenligninger mellom grupper for sammenslåtte placebokontrollerte studier viste ingen statistisk signifikante SEROQUEL/placebo-forskjeller i andelen pasienter som opplever potensielt viktige endringer i EKG-parametere, inkludert QT, QTc og PR-intervaller. Imidlertid ble andelen pasienter som oppfyller kriteriene for takykardi sammenlignet i fire 3- til 6-ukers placebokontrollerte kliniske studier for behandling av schizofreni, som avslørte en forekomst på 1 % (4/399) for SEROQUEL 100 mg sammenlignet med 0,6 % (1) /156) forekomst for placebo. I forsøk med akutt (monoterapi) bipolar mani var andelen pasienter som oppfyller kriteriene for takykardi 0,5 % (1/192) for SEROQUEL 200 mg sammenlignet med 0 % (0/178) forekomst for placebo. I akutt bipolar mani (tilleggsstudier) var andelen pasienter som oppfyller de samme kriteriene 0,6 % (1/166) for SEROQUEL 100 mg sammenlignet med 0 % (0/171) forekomst for placebo. I bipolare depresjonsstudier hadde ingen pasienter hjertefrekvensøkninger til >120 slag per minutt. Bruk av SEROQUEL 50 mg var assosiert med en gjennomsnittlig økning i hjertefrekvensen, vurdert ved EKG, på 7 slag per minutt sammenlignet med en gjennomsnittlig økning på 1 slag per minutt blant placebopasienter. Denne svake tendensen til takykardi hos voksne kan være relatert til SEROQUELs potensial for å indusere ortostatiske endringer [se ADVARSLER OG FORHOLDSREGLER ].
Barn og ungdom
I den akutte (6-ukers) schizofrenistudien hos ungdom, forekom økning i hjertefrekvens (>110 slag/min) hos 5,2 % (3/73) av pasientene som fikk SEROQUEL 400 mg og 8,5 % (5/74) av pasientene som fikk SEROQUEL 800 mg sammenlignet med 0 % (0/75) av pasientene som fikk placebo. Gjennomsnittlig økning i hjertefrekvens var 3,8 bpm og 11,2 bpm for henholdsvis SEROQUEL 400 mg og 800 mg gruppene, sammenlignet med en reduksjon på 3,3 bpm i placebogruppen [se ADVARSLER OG FORHOLDSREGLER ].
I den akutte (3-ukers) bipolar mani-studien hos barn og ungdom, forekom økning i hjertefrekvens (>110 slag/min) hos 1,1 % (1/89) av pasientene som fikk SEROQUEL 400 mg og 4,7 % (4/85) av pasientene som fikk SEROQUEL 600 mg sammenlignet med 0 % (0/98) av pasientene som fikk placebo. Gjennomsnittlig økning i hjertefrekvens var 12,8 bpm og 13,4 bpm for henholdsvis SEROQUEL 400 mg og 600 mg gruppene, sammenlignet med en reduksjon på 1,7 bpm i placebogruppen [se ADVARSLER OG FORHOLDSREGLER ].
en akutt (8-ukers) SEROQUEL XR-studie hos barn og ungdom (10-17 år) med bipolar depresjon, hvor effekt ikke ble etablert, økte hjertefrekvensen (>110 slag/min 10-12 år og 13-17 år) år) forekom hos 0 % av pasientene som fikk SEROQUEL XR og 1,2 % av pasientene som fikk placebo. Gjennomsnittlig økning i hjertefrekvens var 3,4 bpm for SEROQUEL XR, sammenlignet med 0,3 bpm i placebogruppen [se ADVARSLER OG FORHOLDSREGLER ].
Postmarketing-erfaring
Følgende bivirkninger ble identifisert etter godkjenning av SEROQUEL. Fordi disse reaksjonene rapporteres frivillig fra en populasjon av usikker størrelse, er det ikke alltid mulig å pålitelig estimere frekvensen deres eller etablere en årsakssammenheng med legemiddeleksponering.
Bivirkninger rapportert siden markedsintroduksjonen som var tidsmessig relatert til behandling med quetiapin inkluderer anafylaktisk reaksjon, kardiomyopati, medikamentreaksjon med eosinofili og systemiske symptomer (DRESS), hyponatremi, myokarditt, nattlig enurese, pankreatitt, retrograd amnesi, rabdomediolysesyndrom, rabdomediolyse, rabdomediolyse. (SIADH), Stevens-Johnsons syndrom (SJS), toksisk epidermal nekrolyse (TEN), redusert antall blodplater, alvorlige leverreaksjoner (inkludert hepatitt, levernekrose og leversvikt), agranulocytose, intestinal obstruksjon, ileus, koloniskemi, urinretensjon , søvnapné og akutt generalisert eksantematøs pustulose (AGEP).
NARKOTIKAHANDEL
Effekten av andre legemidler på Quetiapin
Risikoen ved bruk av SEROQUEL i kombinasjon med andre legemidler har ikke blitt grundig evaluert i systematiske studier. Gitt de primære CNS-effektene av SEROQUEL, bør det utvises forsiktighet når det tas i kombinasjon med andre sentralt virkende legemidler. SEROQUEL 300 mg forsterket de kognitive og motoriske effektene av alkohol i en klinisk studie hos personer med utvalgte psykotiske lidelser, og alkoholholdige drikker bør begrenses mens de tar quetiapin.
Eksponering for quetiapin økes av prototypen CYP3A4-hemmere (f.eks. ketokonazol, itrakonazol, indinavir, ritonavir, nefazodon, etc.) og reduseres av prototypen CYP3A4-induktorer (f.eks. fenytoin, karbamazepin, rifampin, avasimibe etc.) . Dosejustering av quetiapin vil være nødvendig hvis det gis samtidig med potente CYP3A4-induktorer eller -hemmere.
CYP3A4-hemmere
Samtidig administrering av ketokonazol, en potent hemmer av cytokrom CYP3A4, resulterte i signifikant økning i kvetiapineksponering. Dosen av SEROQUEL 200 mg bør reduseres til en sjettedel av den opprinnelige dosen hvis den administreres samtidig med en sterk CYP3A4-hemmer [se DOSERING OG ADMINISTRASJON og KLINISK FARMAKOLOGI ].
CYP3A4-indusere
Samtidig administrering av kvetiapin og fenytoin, en CYP3A4-induktor, økte gjennomsnittlig oral clearance av kvetiapin med 5 ganger. Økte doser av SEROQUEL 50 mg opptil 5 ganger kan være nødvendig for å opprettholde kontroll over symptomer på schizofreni hos pasienter som får quetiapin og fenytoin, eller andre kjente potente CYP3A4-indusere [se DOSERING OG ADMINISTRASJON og KLINISK FARMAKOLOGI ]. Når CYP3A4-induktoren seponeres, bør dosen av SEROQUEL 25 mg reduseres til det opprinnelige nivået innen 7-14 dager [se DOSERING OG ADMINISTRASJON ].
Den potensielle effekten av flere samtidige medisiner på quetiapins farmakokinetikk ble studert [se KLINISK FARMAKOLOGI ].
Effekt av quetiapin på andre legemidler
På grunn av potensialet for å indusere hypotensjon, kan SEROQUEL 50 mg forsterke effekten av visse antihypertensiva.
SEROQUEL 25 mg kan motvirke effekten av levodopa og dopaminagonister.
Det er ingen klinisk relevante farmakokinetiske interaksjoner av Seroquel på andre legemidler basert på CYP-veien. Seroquel 50 mg og dets metabolitter er ikke-hemmere av hovedmetaboliserende CYP (1A2, 2C9, 2C19, 2D6 og 3A4).
Narkotikamisbruk og avhengighet
Kontrollert stoff
SEROQUEL er ikke et kontrollert stoff.
Misbruke
SEROQUEL har ikke blitt systematisk studert, hos dyr eller mennesker, for potensialet for misbruk, toleranse eller fysisk avhengighet. Selv om de kliniske studiene ikke avdekket noen tendens til narkotikasøkende atferd, var disse observasjonene ikke systematiske, og det er ikke mulig å forutsi på grunnlag av denne begrensede erfaringen i hvilken grad et CNS-aktivt legemiddel vil bli misbrukt, avledet, og/eller misbrukt en gang markedsført. Følgelig bør pasienter evalueres nøye for en historie med narkotikamisbruk, og slike pasienter bør observeres nøye for tegn på misbruk eller misbruk av SEROQUEL, f.eks. utvikling av toleranse, økning i dose, legemiddelsøkende atferd.
ADVARSLER
Inkludert som en del av "FORHOLDSREGLER" Seksjon
FORHOLDSREGLER
Økt dødelighet hos eldre pasienter med demensrelatert psykose
Eldre pasienter med demensrelatert psykose behandlet med antipsykotiske legemidler har økt risiko for død. Analyse av 17 placebokontrollerte studier (modal varighet på 10 uker), hovedsakelig hos pasienter som tok atypiske antipsykotiske legemidler, viste en risiko for død hos legemiddelbehandlede pasienter på mellom 1,6 til 1,7 ganger risikoen for død hos placebobehandlede pasienter. I løpet av en typisk 10-ukers kontrollert studie var dødsraten hos medikamentbehandlede pasienter ca. 4,5 %, sammenlignet med en rate på ca. 2,6 % i placebogruppen. Selv om dødsårsakene var forskjellige, så de fleste dødsfallene ut til å være enten kardiovaskulære (f.eks. hjertesvikt, plutselig død) eller smittsomme (f.eks. lungebetennelse) av natur. Observasjonsstudier tyder på at behandling med konvensjonelle antipsykotiske legemidler, i likhet med atypiske antipsykotiske legemidler, kan øke dødeligheten. Det er ikke klart i hvilken grad funnene av økt dødelighet i observasjonsstudier kan tilskrives det antipsykotiske legemidlet i motsetning til enkelte kjennetegn(er). SEROQUEL er ikke godkjent for behandling av pasienter med demensrelatert psykose [se ADVARSEL i boks ].
Selvmordstanker og -adferd hos ungdom og unge voksne
Pasienter med alvorlig depressiv lidelse (MDD), både voksne og barn, kan oppleve forverring av depresjonen og/eller fremveksten av selvmordstanker og -adferd (suicidalitet) eller uvanlige endringer i atferd, enten de tar antidepressive medisiner eller ikke, og dette risikoen kan vedvare inntil betydelig remisjon oppstår. Selvmord er en kjent risiko for depresjon og visse andre psykiatriske lidelser, og disse lidelsene er i seg selv de sterkeste prediktorene for selvmord. Det har imidlertid vært en langvarig bekymring for at antidepressiva kan ha en rolle i å indusere forverring av depresjon og fremveksten av suicidalitet hos visse pasienter i de tidlige faser av behandlingen. Samlede analyser av kortsiktige placebokontrollerte studier av antidepressiva (SSRI og andre) viste at disse medikamentene øker risikoen for selvmordstenkning og selvmordsatferd (suicidalitet) hos barn, ungdom og unge voksne (18-24 år) med alvorlig depressiv sykdom. lidelse (MDD) og andre psykiatriske lidelser. Korttidsstudier viste ikke en økning i risikoen for suicidalitet med antidepressiva sammenlignet med placebo hos voksne over 24 år; det var en reduksjon med antidepressiva sammenlignet med placebo hos voksne i alderen 65 år og eldre.
De samlede analysene av placebokontrollerte studier hos barn og ungdom med MDD, tvangslidelse (OCD) eller andre psykiatriske lidelser inkluderte totalt 24 korttidsstudier av 9 antidepressiva med over 4400 pasienter. De samlede analysene av placebokontrollerte studier hos voksne med MDD eller andre psykiatriske lidelser inkluderte totalt 295 korttidsstudier (median varighet på 2 måneder) med 11 antidepressiva med over 77 000 pasienter. Det var betydelig variasjon i risiko for suicidalitet blant legemidler, men en tendens til en økning i yngre pasienter for nesten alle legemidler som ble studert. Det var forskjeller i absolutt risiko for suicidalitet på tvers av de forskjellige indikasjonene, med høyest forekomst av MDD. Risikoforskjellene (legemiddel vs. placebo) var imidlertid relativt stabile innenfor aldersstrata og på tvers av indikasjoner. Disse risikoforskjellene (medikament-placebo-forskjell i antall tilfeller av suicidalitet per 1000 behandlede pasienter) er gitt i tabell 2.
Ingen selvmord skjedde i noen av de pediatriske studiene. Det var selvmord i voksenforsøkene, men antallet var ikke tilstrekkelig til å komme til noen konklusjon om legemiddeleffekt på selvmord.
Det er ukjent om suicidalitetsrisikoen strekker seg til langvarig bruk, dvs. utover flere måneder. Det er imidlertid betydelig bevis fra placebokontrollerte vedlikeholdsforsøk hos voksne med depresjon på at bruk av antidepressiva kan forsinke tilbakefall av depresjon.
Alle pasienter som behandles med antidepressiva for enhver indikasjon bør overvåkes hensiktsmessig og observeres nøye for klinisk forverring, suicidalitet og uvanlige endringer i atferd, spesielt i løpet av de første månedene av en medikamentell behandlingskur, eller ved doseendringer, enten økninger eller synker.
Følgende symptomer, angst, agitasjon, panikkanfall, søvnløshet, irritabilitet, fiendtlighet, aggressivitet, impulsivitet, akatisi (psykomotorisk rastløshet), hypomani og mani, er rapportert hos voksne og pediatriske pasienter som også behandles med antidepressiva for alvorlig depressiv lidelse som for andre indikasjoner, både psykiatriske og ikke-psykiatriske. Selv om det ikke er etablert en årsakssammenheng mellom fremveksten av slike symptomer og enten forverring av depresjon og/eller fremveksten av selvmordsimpulser, er det bekymring for at slike symptomer kan representere forløpere til fremvoksende suicidalitet.
Det bør vurderes å endre det terapeutiske regimet, inkludert eventuelt seponering av medisinen, hos pasienter hvis depresjon er vedvarende verre, eller som opplever ny suicidalitet eller symptomer som kan være forløpere til forverring av depresjon eller suicidalitet, spesielt hvis disse symptomene er alvorlige, brå i debut, eller var ikke en del av pasientens symptomer.
Familier og omsorgspersoner til pasienter som behandles med antidepressiva for alvorlig depressiv lidelse eller andre indikasjoner, både psykiatriske og ikke-psykiatriske, bør varsles om behovet for å overvåke pasienter for fremveksten av agitasjon, irritabilitet, uvanlige endringer i atferd og de andre symptomene. beskrevet ovenfor, samt fremveksten av suicidalitet, og å rapportere slike symptomer umiddelbart til helsepersonell. Slik overvåking bør inkludere daglig observasjon av familier og omsorgspersoner. Resepter for SEROQUEL bør skrives ut for den minste mengde tabletter i samsvar med god pasientbehandling, for å redusere risikoen for overdosering.
Screening av pasienter for bipolar lidelse
En alvorlig depressiv episode kan være den første presentasjonen av bipolar lidelse. Det er generelt antatt (men ikke etablert i kontrollerte studier) at behandling av en slik episode med et antidepressivum alene kan øke sannsynligheten for utfelling av en blandet/manisk episode hos pasienter med risiko for bipolar lidelse. Hvorvidt noen av symptomene beskrevet ovenfor representerer en slik konvertering er ukjent. Før behandling med et antidepressivt middel, inkludert SEROQUEL, startes, bør imidlertid pasienter med depressive symptomer screenes tilstrekkelig for å avgjøre om de har risiko for bipolar lidelse; slik screening bør inkludere en detaljert psykiatrisk historie, inkludert en familiehistorie med selvmord, bipolar lidelse og depresjon.
Cerebrovaskulære bivirkninger, inkludert hjerneslag, hos eldre pasienter med demensrelatert psykose
I placebokontrollerte studier med risperidon, aripiprazol og olanzapin hos eldre personer med demens, var det en høyere forekomst av cerebrovaskulære bivirkninger (cerebrovaskulære ulykker og forbigående iskemiske angrep) inkludert dødsfall sammenlignet med placebobehandlede personer. SEROQUEL er ikke godkjent for behandling av pasienter med demensrelatert psykose [se også ADVARSEL i boks og Økt dødelighet hos eldre pasienter med demensrelatert psykose ].
Malignt nevroleptikasyndrom (NMS)
Et potensielt dødelig symptomkompleks noen ganger referert til som malignt nevroleptisk syndrom (NMS) er rapportert i forbindelse med administrering av antipsykotiske legemidler, inkludert SEROQUEL. Sjeldne tilfeller av NMS er rapportert med SEROQUEL. Kliniske manifestasjoner av NMS er hyperpyreksi, muskelstivhet, endret mental status og bevis på autonom ustabilitet (uregelmessig puls eller blodtrykk, takykardi, diaforese og hjerterytmeforstyrrelser). Ytterligere tegn kan inkludere forhøyet kreatininfosfokinase, myoglobinuri (rabdomyolyse) og akutt nyresvikt.
Den diagnostiske evalueringen av pasienter med dette syndromet er komplisert. For å komme frem til en diagnose er det viktig å utelukke tilfeller der den kliniske presentasjonen inkluderer både alvorlig medisinsk sykdom (f.eks. lungebetennelse, systemisk infeksjon, etc.) og ubehandlede eller utilstrekkelig behandlede ekstrapyramidale tegn og symptomer (EPS). Andre viktige hensyn i differensialdiagnosen inkluderer sentral antikolinergisk toksisitet, heteslag, medikamentfeber og primær sentralnervesystem (CNS) patologi.
Behandlingen av NMS bør omfatte: 1) umiddelbar seponering av antipsykotiske legemidler og andre legemidler som ikke er avgjørende for samtidig behandling; 2) intensiv symptomatisk behandling og medisinsk overvåking; og 3) behandling av eventuelle samtidige alvorlige medisinske problemer som spesifikke behandlinger er tilgjengelige for. Det er ingen generell enighet om spesifikke farmakologiske behandlingsregimer for NMS.
Dersom en pasient trenger antipsykotisk medikamentbehandling etter bedring fra NMS, bør mulig gjeninnføring av medikamentell behandling vurderes nøye. Pasienten bør overvåkes nøye siden tilbakefall av NMS er rapportert.
Metabolske endringer
Atypiske antipsykotiske legemidler har vært assosiert med metabolske endringer som inkluderer hyperglykemi/diabetes mellitus, dyslipidemi og kroppsvektøkning. Mens alle medikamentene i klassen har vist seg å produsere noen metabolske endringer, har hvert legemiddel sin egen spesifikke risikoprofil. Hos noen pasienter ble det observert en forverring av mer enn én av de metabolske parametrene vekt, blodsukker og lipider i kliniske studier. Endringer i disse metabolske profiler bør håndteres som klinisk hensiktsmessig.
Hyperglykemi og diabetes mellitus
Hyperglykemi, i noen tilfeller ekstrem og assosiert med ketoacidose eller hyperosmolar koma eller død, er rapportert hos pasienter behandlet med atypiske antipsykotika, inkludert quetiapin. Vurdering av sammenhengen mellom atypisk antipsykotisk bruk og glukoseavvik kompliseres av muligheten for økt bakgrunnsrisiko for diabetes mellitus hos pasienter med schizofreni og den økende forekomsten av diabetes mellitus i befolkningen generelt. Gitt disse konfounderne, er forholdet mellom atypisk antipsykotisk bruk og hyperglykemi-relaterte bivirkninger ikke fullstendig forstått. Epidemiologiske studier tyder imidlertid på økt risiko for hyperglykemi-relaterte bivirkninger hos pasienter behandlet med de atypiske antipsykotika. Nøyaktige risikoestimater for hyperglykemi-relaterte bivirkninger hos pasienter behandlet med atypiske antipsykotika er ikke tilgjengelig.
Pasienter med etablert diagnose diabetes mellitus som starter på atypiske antipsykotika bør overvåkes regelmessig for forverring av glukosekontrollen. Pasienter med risikofaktorer for diabetes mellitus (f.eks. fedme, familiehistorie med diabetes) som starter behandling med atypiske antipsykotika, bør gjennomgå fastende blodsukkertesting i begynnelsen av behandlingen og med jevne mellomrom under behandlingen. Alle pasienter som behandles med atypiske antipsykotika bør overvåkes for symptomer på hyperglykemi, inkludert polydipsi, polyuri, polyfagi og svakhet. Pasienter som utvikler symptomer på hyperglykemi under behandling med atypiske antipsykotika bør gjennomgå fastende blodsukkertesting. I noen tilfeller har hyperglykemi gått over når det atypiske antipsykotikaet ble seponert; noen pasienter trengte imidlertid fortsettelse av antidiabetisk behandling til tross for seponering av det mistenkte legemidlet.
Voksne
en 24-ukers studie (aktiv-kontrollert, 115 pasienter behandlet med SEROQUEL) designet for å evaluere glykemisk status med oral glukosetoleransetesting av alle pasienter, ved uke 24 var forekomsten av et glukosenivå etter glukoseutfordring ≥200 mg/dL 1,7 % og forekomsten av et fastende blodsukkernivå ≥126 mg/dL var 2,6 %. Gjennomsnittlig endring i fastende glukose fra baseline var 3,2 mg/dL og gjennomsnittlig endring i 2-timers glukose fra baseline var -1,8 mg/dL for quetiapin.
2 langtids placebokontrollerte, randomiserte kliniske seponeringsstudier for vedlikehold av bipolar I lidelse, gjennomsnittlig eksponering på 213 dager for SEROQUEL (646 pasienter) og 152 dager for placebo (680 pasienter), var gjennomsnittlig endring i glukose fra baseline +5,0 mg /dL for SEROQUEL 100 mg og –0,05 mg/dL for placebo. Den eksponeringsjusterte frekvensen av økt blodsukkernivå (≥126 mg/dL) for pasienter mer enn 8 timer siden et måltid (men noen pasienter kan ikke ha vært utelukket fra kaloriinntak fra væske under fasteperioden) var 18,0 per 100 pasientår for SEROQUEL (10,7 % av pasientene; n=556) og 9,5 for placebo per 100 pasientår (4,6 % av pasientene; n=581).
Barn og ungdom
en placebokontrollert SEROQUEL 25 mg monoterapistudie av ungdomspasienter (13-17 år) med schizofreni (6 ukers varighet), gjennomsnittlig endring i fastende glukosenivåer for SEROQUEL (n=138) sammenlignet med placebo (n=67) var – 0,75 mg/dL versus –1,70 mg/dL. I en placebokontrollert SEROQUEL 300 mg monoterapistudie av barn og ungdomspasienter (10-17 år) med bipolar mani (3 ukers varighet), gjennomsnittlig endring i fastende glukosenivå for SEROQUEL (n=170) sammenlignet med placebo (n) =81) var 3,62 mg/dL mot –1,17 mg/dL. Ingen pasienter i verken studien med et baseline normalt fastende glukosenivå (
en placebokontrollert SEROQUEL XR monoterapistudie (8 ukers varighet) av barn og ungdomspasienter (1017 år) med bipolar depresjon, hvor effekt ikke ble fastslått, var gjennomsnittlig endring i fastende glukosenivåer for SEROQUEL 300mg XR (n= 60) sammenlignet med placebo (n=62) var 1,8 mg/dL mot 1,6 mg/dL. I denne studien var det ingen pasienter i gruppene som ble behandlet med SEROQUEL XR eller placebo med et normalt fastende glukosenivå ved baseline (126 mg/dL. Det var én pasient i SEROQUEL 25 mg XR-gruppen med et baseline-grensenivå for fastende glukose (>100 mg/dL og 126 mg/dL sammenlignet med null pasienter i placebo gruppe.
Dyslipidemi
Voksne
Tabell 4 viser prosentandelen av voksne pasienter med endringer i totalkolesterol, triglyserider, LDL-kolesterol og HDL-kolesterol fra baseline etter indikasjon i kliniske studier med SEROQUEL.
Barn og ungdom
Tabell 5 viser prosentandelen av barn og ungdom med endringer i totalkolesterol, triglyserider, LDL-kolesterol og HDL-kolesterol fra baseline i kliniske studier med SEROQUEL.
I en placebokontrollert SEROQUEL XR monoterapistudie (8 ukers varighet) av barn og ungdomspasienter (1017 år) med bipolar depresjon, hvor effekt ikke ble fastslått, var prosentandelen av barn og ungdom med endringer i totalt kolesterol (≥200) mg/dL), triglyserider (≥150 mg/dL), LDL-kolesterol (≥ 130 mg/dL) og HDL-kolesterol (≤40 mg/dL) fra baseline til klinisk signifikante nivåer var: totalkolesterol 8 % (7 /83) for SEROQUEL 50 mg XR vs. 6 % (5/84) for placebo; triglyserider 28 % (22/80) for SEROQUEL 100 mg XR vs. 9 % (7/82) for placebo; LDL-kolesterol 2 % (2/86) for SEROQUEL XR vs. 4 % (3/85) for placebo og HDL-kolesterol 20 % (13/65) for SEROQUEL XR vs. 15 % (11/74) for placebo.
Vektøkning
Økning i vekt er observert i kliniske studier. Pasienter som får kvetiapin bør overvåkes regelmessig.
Voksne
I kliniske studier med SEROQUEL 50 mg har følgende vektøkninger blitt rapportert.
Barn og ungdom
I to kliniske studier med SEROQUEL 25 mg, en ved bipolar mani og en ved schizofreni, er rapporterte vektøkninger inkludert i tabell 7.
Gjennomsnittlig endring i kroppsvekt i schizofrenistudien var 2,0 kg i SEROQUEL 25 mg-gruppen og -0,4 kg i placebogruppen og i bipolar manistudien var den 1,7 kg i SEROQUEL 200 mg-gruppen og 0,4 kg i placebogruppen.
en åpen studie som inkluderte pasienter fra de to ovennevnte pediatriske studiene, fullførte 63 % av pasientene (241/380) 26 ukers behandling med SEROQUEL. Etter 26 ukers behandling var gjennomsnittlig økning i kroppsvekt 4,4 kg. 45 prosent av pasientene gikk opp ≥7 % av kroppsvekten, ikke justert for normal vekst. For å justere for normal vekst over 26 uker ble en økning på minst 0,5 standardavvik fra baseline i BMI brukt som et mål på en klinisk signifikant endring; 18,3 % av pasientene på SEROQUEL oppfylte dette kriteriet etter 26 ukers behandling.
I en klinisk studie for SEROQUEL XR hos barn og ungdom (10-17 år) med bipolar depresjon, hvor effekt ikke ble fastslått, var prosentandelen av pasienter med vektøkning ≥7 % av kroppsvekten til enhver tid 15 % ( 14/92) for SEROQUEL 25 mg XR vs. 10 % (10/100) for placebo. Gjennomsnittlig endring i kroppsvekt var 1,4 kg i SEROQUEL 50 mg XR-gruppen vs. 0,6 kg i placebogruppen.
Ved behandling av pediatriske pasienter med SEROQUEL 50 mg for enhver indikasjon, bør vektøkning vurderes mot det som forventes for normal vekst.
Tardiv dyskinesi
Et syndrom med potensielt irreversible, ufrivillige, dyskinetiske bevegelser kan utvikles hos pasienter som behandles med antipsykotiske legemidler, inkludert quetiapin. Selv om prevalensen av syndromet ser ut til å være høyest blant eldre, spesielt eldre kvinner, er det umulig å stole på prevalensestimater for å forutsi, ved starten av antipsykotisk behandling, hvilke pasienter som sannsynligvis vil utvikle syndromet. Hvorvidt antipsykotiske legemidler er forskjellige i deres potensial til å forårsake tardiv dyskinesi er ukjent.
Risikoen for å utvikle tardiv dyskinesi og sannsynligheten for at den blir irreversibel antas å øke etter hvert som behandlingens varighet og den totale kumulative dosen av antipsykotiske legemidler som gis til pasienten øker. Imidlertid kan syndromet utvikle seg, selv om det er mye mindre vanlig, etter relativt korte behandlingsperioder ved lave doser eller kan til og med oppstå etter seponering av behandlingen.
Tardiv dyskinesi kan gi seg, delvis eller fullstendig, hvis antipsykotisk behandling seponeres. Antipsykotisk behandling kan imidlertid i seg selv undertrykke (eller delvis undertrykke) tegn og symptomer på syndromet og kan derved muligens maskere den underliggende prosessen. Effekten som symptomatisk undertrykkelse har på det langsiktige forløpet av syndromet er ukjent.
Gitt disse hensynene bør SEROQUEL 50 mg forskrives på en måte som mest sannsynlig minimerer forekomsten av tardiv dyskinesi. Kronisk antipsykotisk behandling bør generelt være forbeholdt pasienter som ser ut til å lide av en kronisk sykdom som (1) er kjent for å reagere på antipsykotiske legemidler, og (2) for hvem alternative, like effektive, men potensielt mindre skadelige behandlinger ikke er tilgjengelige eller hensiktsmessige. . Hos pasienter som trenger kronisk behandling, bør den minste dosen og den korteste behandlingsvarigheten som gir en tilfredsstillende klinisk respons søkes. Behovet for fortsatt behandling bør revurderes med jevne mellomrom.

Hvis tegn og symptomer på tardiv dyskinesi vises hos en pasient på SEROQUEL 200 mg, bør seponering av medikamentet vurderes. Noen pasienter kan imidlertid trenge behandling med SEROQUEL 200 mg til tross for tilstedeværelsen av syndromet.
Hypotensjon
Quetiapin kan indusere ortostatisk hypotensjon assosiert med svimmelhet, takykardi og, hos noen pasienter, synkope, spesielt under den initiale dosetitreringsperioden, sannsynligvis noe som gjenspeiler dets α1-adrenerge antagonistegenskaper. Synkope ble rapportert hos 1 % (28/3265) av pasientene behandlet med SEROQUEL, sammenlignet med 0,2 % (2/954) på placebo og ca. 0,4 % (2/527) på aktive kontrollmedisiner. Ortostatisk hypotensjon, svimmelhet og synkope kan føre til fall.
SEROQUEL 25mg bør brukes med spesiell forsiktighet hos pasienter med kjent kardiovaskulær sykdom (historie med hjerteinfarkt eller iskemisk hjertesykdom, hjertesvikt eller ledningsforstyrrelser), cerebrovaskulær sykdom eller tilstander som kan disponere pasienter for hypotensjon (dehydrering, hypovolemi og behandling med antihypertensive medisiner). Risikoen for ortostatisk hypotensjon og synkope kan reduseres ved å begrense startdosen til 25 mg to ganger daglig [se DOSERING OG ADMINISTRASJON ]. Hvis hypotensjon oppstår under titrering til måldosen, er en retur til forrige dose i titreringsskjemaet hensiktsmessig.
Falls
Atypiske antipsykotiske legemidler, inkludert SEROQUEL, kan forårsake somnolens, postural hypotensjon, motorisk og sensorisk ustabilitet, noe som kan føre til fall og følgelig brudd eller andre skader. For pasienter med sykdommer, tilstander eller medisiner som kan forverre disse effektene, fullfør fallrisikovurderinger ved oppstart av antipsykotisk behandling og gjentatte ganger for pasienter på langvarig antipsykotisk behandling.
Økning i blodtrykk (barn og ungdom)
placebokontrollerte studier hos barn og ungdom med schizofreni (6 ukers varighet) eller bipolar mani (3 ukers varighet), var forekomsten av økninger til enhver tid i systolisk blodtrykk (≥20 mmHg) 15,2 % (51/335) ) for SEROQUEL 50 mg og 5,5 % (9/163) for placebo; forekomsten av økninger til enhver tid i diastolisk blodtrykk (≥10 mmHg) var 40,6 % (136/335) for SEROQUEL og 24,5 % (40/163) for placebo. I den 26-ukers åpne kliniske studien opplevde ett barn med en rapportert historie med hypertensjon en hypertensiv krise. Blodtrykket hos barn og ungdom bør måles i begynnelsen av og med jevne mellomrom under behandlingen.
en placebokontrollert SEROQUEL XR klinisk studie (8 ukers varighet) hos barn og ungdom (10-17 år) med bipolar depresjon, hvor effekt ikke ble fastslått, var forekomsten av økninger i systolisk blodtrykk til enhver tid (≥ 20 mmHg) var 6,5 % (6/92) for SEROQUEL XR og 6,0 % (6/100) for placebo; forekomsten av økninger til enhver tid i diastolisk blodtrykk (≥10 mmHg) var 46,7 % (43/92) for SEROQUEL 25 mg XR og 36,0 % (36/100) for placebo.
Leukopeni, nøytropeni og agranulocytose
I kliniske studier og erfaring etter markedsføring har hendelser med leukopeni/nøytropeni blitt rapportert tidsmessig relatert til atypiske antipsykotiske midler, inkludert SEROQUEL. Agranulocytose er rapportert.
Agranulocytose (definert som absolutt nøytrofiltall
Mulige risikofaktorer for leukopeni/nøytropeni inkluderer allerede eksisterende lavt antall hvite blodlegemer (WBC) og historie med legemiddelindusert leukopeni/nøytropeni. Pasienter med en eksisterende lav WBC eller en historie med medikamentindusert leukopeni/nøytropeni bør få fullstendig blodtelling (CBC) overvåket ofte i løpet av de første månedene av behandlingen og bør seponere SEROQUEL 50 mg ved første tegn på en nedgang i WBC i fravær av andre årsaksfaktorer.
Pasienter med nøytropeni bør overvåkes nøye for feber eller andre symptomer eller tegn på infeksjon og behandles umiddelbart dersom slike symptomer eller tegn oppstår. Pasienter med alvorlig nøytropeni (absolutt nøytrofiltall
Grå stær
Utviklingen av grå stær ble observert i forbindelse med behandling med quetiapin i kroniske hundestudier [se Ikke-klinisk toksikologi ]. Linseforandringer har også blitt observert hos voksne, barn og ungdom under langvarig behandling med SEROQUEL 100 mg, men en årsakssammenheng med bruk av SEROQUEL 200 mg er ikke fastslått. Likevel kan muligheten for lentikulære endringer ikke utelukkes på dette tidspunktet. Derfor anbefales undersøkelse av linsen med metoder som er tilstrekkelige til å oppdage kataraktdannelse, slik som spaltelampeundersøkelse eller andre passende sensitive metoder, ved oppstart av behandling eller kort tid etterpå, og med 6-måneders intervaller under kronisk behandling.
QT-forlengelse
kliniske studier var quetiapin ikke assosiert med en vedvarende økning i QT-intervaller. QT-effekten ble imidlertid ikke systematisk evaluert i en grundig QT-studie. Etter markedsføring ble det rapportert tilfeller av QT-forlengelse hos pasienter som overdoserte quetiapin [se OVERDOSE ], hos pasienter med samtidig sykdom, og hos pasienter som tar medisiner kjent for å forårsake elektrolyttforstyrrelser eller øke QT-intervallet [se NARKOTIKAHANDEL ].
Bruk av quetiapin bør unngås i kombinasjon med andre legemidler som er kjent for å forlenge QTc, inkludert klasse 1A antiarytmika (f.eks. kinidin, prokainamid) eller klasse III antiarytmika (f.eks. amiodaron, sotalol), antipsykotiske medisiner (f.eks. ziprasidon, klorpromazin, tioridazin), antibiotika (f.eks. gatifloxacin, moxifloxacin) eller en hvilken som helst annen klasse medikamenter som er kjent for å forlenge QTc-intervallet (f.eks. pentamidin, levometadylacetat, metadon).
Quetiapin bør også unngås under omstendigheter som kan øke risikoen for forekomst av torsade de pointes og/eller plutselig død, inkludert (1) en historie med hjertearytmier som bradykardi; (2) hypokalemi eller hypomagnesemi; (3) samtidig bruk av andre legemidler som forlenger QTc-intervallet; og (4) tilstedeværelse av medfødt forlengelse av QT-intervallet.
Forsiktighet bør også utvises når quetiapin foreskrives til pasienter med økt risiko for QT-forlengelse (f.eks. kardiovaskulær sykdom, familiehistorie med QT-forlengelse, eldre, kongestiv hjertesvikt og hjertehypertrofi).
Anfall
Under kliniske studier forekom anfall hos 0,5 % (20/3490) av pasientene behandlet med SEROQUEL sammenlignet med 0,2 % (2/954) på placebo og 0,7 % (4/527) på aktive kontrollmedisiner. Som med andre antipsykotika, bør SEROQUEL 25 mg brukes med forsiktighet hos pasienter med anfall i anamnesen eller med tilstander som potensielt senker krampeterskelen, f.eks. Alzheimers demens. Tilstander som senker anfallsterskelen kan være mer utbredt i en befolkning på 65 år eller eldre.
Hypotyreose
Voksne
Kliniske studier med quetiapin viste doserelaterte reduksjoner i thyreoideahormonnivåer. Reduksjonen i totalt og fritt tyroksin (T4) på ca. 20 % i den øvre enden av det terapeutiske doseområdet var maksimal i de første seks ukene av behandlingen og opprettholdt uten tilpasning eller progresjon under mer kronisk behandling. I nesten alle tilfeller var seponering av quetiapin-behandling assosiert med en reversering av effektene på total og fri T4, uavhengig av behandlingens varighet. Mekanismen som quetiapin påvirker skjoldbruskkjertelaksen med er uklar. Hvis det er en effekt på hypothalamus-hypofyse-aksen, kan det hende at måling av TSH alene ikke gjenspeiler en pasients skjoldbruskkjertelstatus nøyaktig. Derfor bør både TSH og fritt T4, i tillegg til klinisk vurdering, måles ved baseline og ved oppfølging.
tilleggsstudiene for mani, der SEROQUEL 50 mg ble lagt til litium eller divalproex, hadde 12 % (24/196) av SEROQUEL 200 mg-behandlede pasienter sammenlignet med 7 % (15/203) av placebobehandlede pasienter forhøyede TSH-nivåer. Av de SEROQUEL 300 mg-behandlede pasientene med forhøyede TSH-nivåer, hadde 3 samtidig lave frie T4-nivåer (fritt T4
Omtrent 0,7 % (26/3489) av SEROQUEL-pasientene opplevde TSH-økninger i monoterapistudier. Noen pasienter med TSH-økninger trengte erstatning for skjoldbruskkjertelen.
I alle quetiapin-studier var forekomsten av endringer i skjoldbruskhormoner og TSH 1: reduksjon i fritt T4 (5 mIU/L), 4,9 % (956/19412). Hos åtte pasienter, der TBG ble målt, var nivåene av TBG uendret.
Tabell 8 viser forekomsten av disse endringene i korttids placebokontrollerte kliniske studier.
I kortsiktige placebokontrollerte monoterapistudier var forekomsten av gjensidige endringer i T3 og TSH 0,0 % for både quetiapin (1/4800) og placebo (0/2190), og for T4 og TSH var endringene 0,1 % (7) /6154) for quetiapin versus 0,0 % (1/3007) for placebo.
Barn Og Ungdom
I akutte placebokontrollerte studier hos barn og unge pasienter med schizofreni (6 ukers varighet) eller bipolar mani (3 ukers varighet), forekomsten av endringer i skjoldbruskkjertelfunksjonsverdier til enhver tid for SEROQUEL 100 mg-behandlede pasienter og placebo-behandlede pasienter for forhøyet TSH var henholdsvis 2,9 % (8/280) vs. 0,7 % (1/138), og for redusert total tyroksin var henholdsvis 2,8 % (8/289) vs. 0 % (0/145). Av de SEROQUEL-behandlede pasientene med forhøyede TSH-nivåer, hadde 1 samtidig lavt fritt T4-nivå ved slutten av behandlingen.
Hyperprolaktinemi
Voksne
Under kliniske studier med kvetiapin forekom forekomsten av endringer i prolaktinnivåer til en klinisk signifikant verdi hos 3,6 % (158/4416) av pasientene behandlet med kvetiapin sammenlignet med 2,6 % (51/1968) på placebo.
Barn Og Ungdom
I akutte placebokontrollerte studier hos barn og ungdomspasienter med bipolar mani (3 ukers varighet) eller schizofreni (6 ukers varighet), var forekomsten av endringer i prolaktinnivåer til en verdi (>20 μg/L menn; >26 μg /L kvinner til enhver tid) var 13,4 % (18/134) for SEROQUEL sammenlignet med 4 % (3/75) for placebo hos menn og 8,7 % (9/104) for SEROQUEL 25 mg sammenlignet med 0 % (0/39) for placebo hos kvinner.
Som andre legemidler som antagoniserer dopamin D2-reseptorer, øker SEROQUEL 300mg prolaktinnivået hos noen pasienter, og økningen kan vedvare under kronisk administrering. Hyperprolaktinemi, uavhengig av etiologi, kan undertrykke hypotalamisk GnRH, noe som resulterer i redusert hypofysegonadotropinsekresjon. Dette kan i sin tur hemme reproduksjonsfunksjonen ved å svekke gonadal steroidogenese hos både kvinnelige og mannlige pasienter. Galaktoré, amenoré, gynekomasti og impotens er rapportert hos pasienter som får prolaktinøkende forbindelser. Langvarig hyperprolaktinemi når assosiert med hypogonadisme kan føre til redusert bentetthet hos både kvinnelige og mannlige forsøkspersoner.
Vevskultureksperimenter indikerer at omtrent en tredjedel av brystkreft hos mennesker er prolaktinavhengig in vitro, en faktor av potensiell betydning dersom forskrivning av disse legemidlene vurderes hos en pasient med tidligere påvist brystkreft. Som vanlig med forbindelser som øker frigjøring av prolaktin, ble brystkjertel- og bukspyttkjertel-celle-neoplasi (mammære adenokarsinomer, hypofyse- og bukspyttkjerteladenomer) observert i karsinogenitetsstudier utført på mus og rotter. Verken kliniske studier eller epidemiologiske studier utført til dags dato har vist en sammenheng mellom kronisk administrering av denne klassen av legemidler og tumorgenese hos mennesker, men tilgjengelig bevis er for begrenset til å være avgjørende [se Ikke-klinisk toksikologi ].
Potensial for kognitiv og motorisk svikt
Somnolens var en vanlig rapportert bivirkning rapportert hos pasienter behandlet med SEROQUEL, spesielt i løpet av 3-5 dagers perioden med initial dosetitrering. I schizofrenistudier ble det rapportert somnolens hos 18 % (89/510) av pasientene på SEROQUEL 200 mg sammenlignet med 11 % (22/206) av placebopasientene. I forsøk med akutt bipolar mani med SEROQUEL 200 mg som monoterapi, ble det rapportert somnolens hos 16 % (34/209) av pasientene på SEROQUEL 300 mg sammenlignet med 4 % av placebopasientene. I forsøk med akutt bipolar mani med SEROQUEL som tilleggsbehandling ble det rapportert somnolens hos 34 % (66/196) av pasientene på SEROQUEL sammenlignet med 9 % (19/203) av placebopasientene. I bipolare depresjonsstudier ble det rapportert somnolens hos 57 % (398/698) av pasientene på SEROQUEL 50 mg sammenlignet med 15 % (51/347) av placebopasientene. Siden SEROQUEL 25mg har potensial til å svekke dømmekraft, tenkning eller motoriske ferdigheter, bør pasienter advares mot å utføre aktiviteter som krever mental årvåkenhet, som å betjene et motorkjøretøy (inkludert biler) eller bruke farlige maskiner til de er rimelig sikre på at SEROQUEL-terapi gjør det. ikke påvirke dem negativt. Somnolens kan føre til fall.
Kroppstemperaturregulering
Selv om det ikke er rapportert med SEROQUEL 100mg, har forstyrrelse av kroppens evne til å redusere kjernekroppstemperaturen blitt tilskrevet antipsykotiske midler. Passende forsiktighet anbefales ved forskrivning av SEROQUEL 300 mg til pasienter som vil oppleve tilstander som kan bidra til en økning i kjernekroppstemperaturen, f.eks. å trene hardt, eksponering for ekstrem varme, samtidig motta medisiner med antikolinergisk aktivitet, eller være utsatt for dehydrering.
Dysfagi
Esophageal dysmotilitet og aspirasjon har vært assosiert med bruk av antipsykotiske legemidler. Aspirasjonspneumoni er en vanlig årsak til sykelighet og dødelighet hos eldre pasienter, spesielt de med avansert Alzheimers demens. SEROQUEL 100mg og andre antipsykotiske legemidler bør brukes med forsiktighet hos pasienter med risiko for aspirasjonspneumoni.
Seponeringssyndrom
Akutte abstinenssymptomer, som søvnløshet, kvalme og oppkast, er beskrevet etter brå seponering av atypiske antipsykotiske legemidler, inkludert SEROQUEL. I korttids placebokontrollerte, kliniske monoterapistudier med SEROQUEL 25 mg XR som inkluderte en seponeringsfase som evaluerte seponeringssymptomer, var den samlede forekomsten av pasienter som opplevde ett eller flere seponeringssymptomer etter brå seponering 12,1 % (241/1993) for SEROQUEL XR. og 6,7 % (71/1065) for placebo. Forekomsten av de individuelle bivirkningene (dvs. søvnløshet, kvalme, hodepine, diaré, oppkast, svimmelhet og irritabilitet) oversteg ikke 5,3 % i noen behandlingsgruppe og forsvant vanligvis etter 1 uke etter seponering. Gradvis tilbaketrekking anbefales. [se Bruk i spesifikke populasjoner ]
Antikolinerge (antimuskarine) effekter
Norquetiapin, en aktiv metabolitt av quetiapin, har moderat til sterk affinitet for flere muskarine reseptorsubtyper. Dette bidrar til antikolinerge bivirkninger når SEROQUEL 25 mg brukes i terapeutiske doser, tas samtidig med andre antikolinerge medisiner eller tas i overdose. SEROQUEL bør brukes med forsiktighet hos pasienter som får medisiner som har antikolinerge (antimuskarine) effekter [se OVERDOSE og KLINISK FARMAKOLOGI ].
Forstoppelse var en vanlig rapportert bivirkning hos pasienter behandlet med quetiapin og representerer en risikofaktor for intestinal obstruksjon. Intestinal obstruksjon er rapportert med kvetiapin, inkludert dødelige rapporter hos pasienter som fikk flere samtidige medisiner som reduserer tarmmotiliteten.
SEROQUEL 300 mg bør brukes med forsiktighet hos pasienter med en nåværende diagnose eller tidligere urinretensjon, klinisk signifikant prostatahypertrofi, forstoppelse eller økt intraokulært trykk.
Informasjon om pasientveiledning
Råd pasienten til å lese den FDA-godkjente pasientmerkingen (Medikamentveiledning).
Pasienter bør informeres om følgende problemer og bes om å varsle sin forskriver dersom disse oppstår mens de tar SEROQUEL.
Økt dødelighet hos eldre pasienter med demensrelatert psykose Pasienter og omsorgspersoner bør informeres om at eldre pasienter med demensrelatert psykose behandlet med atypiske antipsykotiske legemidler har økt risiko for død sammenlignet med placebo. Quetiapin er ikke godkjent for eldre pasienter med demensrelatert psykose [se ADVARSLER OG FORHOLDSREGLER ].
Selvmordstanker og -adferd
Pasienter, deres familier og deres omsorgspersoner bør oppmuntres til å være oppmerksomme på fremveksten av angst, agitasjon, panikkanfall, søvnløshet, irritabilitet, fiendtlighet, aggressivitet, impulsivitet, akatisi (psykomotorisk rastløshet), hypomani, mani, andre uvanlige endringer i atferd. , forverring av depresjon og selvmordstanker, spesielt tidlig under antidepressiv behandling og når dosen justeres opp eller ned. Familier og omsorgspersoner til pasienter bør rådes til å se etter forekomsten av slike symptomer på daglig basis, siden endringer kan være brå. Slike symptomer bør rapporteres til pasientens forskriver eller helsepersonell, spesielt hvis de er alvorlige, plutselige eller ikke var en del av pasientens symptomer. Symptomer som disse kan være assosiert med økt risiko for suicidal tenkning og atferd og indikerer behov for svært nøye overvåking og muligens endringer i medisinen [se ADVARSLER OG FORHOLDSREGLER ].
Malignt nevroleptikasyndrom (NMS)
Pasienter bør rådes til å rapportere til legen om tegn eller symptomer som kan være relatert til NMS. Disse kan inkludere muskelstivhet og høy feber [se ADVARSLER OG FORHOLDSREGLER ].
Hyperglykemi og diabetes mellitus
Pasienter bør være oppmerksomme på symptomene på hyperglykemi (høyt blodsukker) og diabetes mellitus. Pasienter som er diagnostisert med diabetes, de med risikofaktorer for diabetes, eller de som utvikler disse symptomene under behandlingen, bør få kontrollert blodsukkeret i begynnelsen av og med jevne mellomrom under behandlingen [se ADVARSLER OG FORHOLDSREGLER ].
Høyt kolesterol
Pasienter bør informeres om at økninger i totalkolesterol, LDL-kolesterol og triglyserider og reduksjoner i HDL-kolesterol kan forekomme. Pasienter bør få overvåket lipidprofilen i begynnelsen av og med jevne mellomrom under behandlingen [se ADVARSLER OG FORHOLDSREGLER ].
Vektøkning
Pasienter bør informeres om at de kan oppleve vektøkning. Pasienter bør få overvåket vekten regelmessig [se ADVARSLER OG FORHOLDSREGLER ].
Ortostatisk hypotensjon
Pasienter bør informeres om risikoen for ortostatisk hypotensjon (symptomer inkluderer svimmelhet eller svimmelhet når de står, noe som kan føre til fall), spesielt i perioden med initial dosetitrering, og også ved gjenoppstart av behandling eller økning i dose [ se ADVARSLER OG FORHOLDSREGLER ].
Økt blodtrykk hos barn og ungdom
Barn og ungdomspasienter bør få målt blodtrykket i begynnelsen av og med jevne mellomrom under behandlingen [se ADVARSLER OG FORHOLDSREGLER ].
Leukopeni/Neutropeni
Pasienter med en eksisterende lav WBC eller en historie med legemiddelindusert leukopeni/nøytropeni bør informeres om at de bør få CBC overvåket mens de tar SEROQUEL. Pasienter bør rådes til å snakke med legen så snart som mulig hvis de har feber, influensalignende symptomer, sår hals eller annen infeksjon, da dette kan være et resultat av svært lavt hvitt blodlegeme, som kan kreve at Seroquel 100 mg stoppet og/eller behandling som skal gis [se ADVARSLER OG FORHOLDSREGLER ].
Interferens med kognitiv og motorisk ytelse
Pasienter bør informeres om risikoen for somnolens eller sedasjon (som kan føre til fall), spesielt i perioden med initial dosetitrering. Pasienter bør advares mot å utføre enhver aktivitet som krever mental årvåkenhet, som å betjene et motorkjøretøy (inkludert biler) eller å betjene maskiner, inntil de er rimelig sikre på at quetiapinterapi ikke påvirker dem negativt [se ADVARSLER OG FORHOLDSREGLER ].
Varmeeksponering og dehydrering
Pasienter bør informeres om passende omsorg for å unngå overoppheting og dehydrering [se ADVARSLER OG FORHOLDSREGLER ].
Samtidig medisinering
Som med andre medisiner, bør pasienter rådes til å varsle legen dersom de tar, eller planlegger å ta, reseptbelagte eller reseptfrie legemidler [se NARKOTIKAHANDEL ].
Svangerskap
Råd gravide kvinner til å varsle helsepersonell dersom de blir gravide eller har tenkt å bli gravide under behandling med SEROQUEL. Informer pasienter om at SEROQUEL kan forårsake ekstrapyramidale og/eller abstinenssymptomer (agitasjon, hypertoni, hypotoni, skjelving, somnolens, pustebesvær og matforstyrrelser) hos en nyfødt. Gi pasienter beskjed om at det finnes et graviditetsregister som overvåker graviditetsutfall hos kvinner eksponert for SEROQUEL 25 mg under graviditet [se Bruk i spesifikke populasjoner ].
Infertilitet
Informer kvinner med reproduksjonsevne at SEROQUEL kan svekke fertiliteten på grunn av en økning i serumprolaktinnivået. Effektene på fertilitet er reversible [se Bruk i spesifikke populasjoner ].
Behov for omfattende behandlingsprogram
SEROQUEL er indisert som en integrert del av et totalt behandlingsprogram for ungdom med schizofreni og pediatrisk bipolar lidelse som kan inkludere andre tiltak (psykologiske, pedagogiske og sosiale). Effektivitet og sikkerhet av SEROQUEL 100 mg er ikke fastslått hos pediatriske pasienter under 13 år for schizofreni eller under 10 år for bipolar mani. Riktig pedagogisk plassering er avgjørende og psykososial intervensjon er ofte nyttig. Beslutningen om å foreskrive atypisk antipsykotisk medisin vil avhenge av legens vurdering av kroniske og alvorlighetsgrad av pasientens symptomer [se INDIKASJONER ].
Ikke-klinisk toksikologi
Karsinogenese, mutagenese, svekkelse av fruktbarhet
Karsinogenese
Karsinogenitetsstudier ble utført på C57BL-mus og Wistar-rotter. Quetiapin ble administrert i dietten til mus i doser på 20, 75, 250 og 750 mg/kg og til rotter ved sondemating i doser på 25, 75 og 250 mg/kg i to år. Disse dosene tilsvarer 0,1, 0,5, 1,5 og 4,5 ganger MRHD på 800 mg/dag basert på mg/m2 kroppsoverflateareal (mus) eller 0,3, 1 og 3 ganger MRHD basert på mg/m2 kroppsoverflateareal (rotter). Det var statistisk signifikante økninger i follikulære adenomer i skjoldbruskkjertelen hos hannmus ved doser 1,5 og 4,5 ganger MRHD basert på mg/m2 kroppsoverflateareal og hos hannrotter ved en dose på 3 ganger MRHD på mg/m2 kroppsoverflate. Melkekjerteladenokarsinomer ble statistisk signifikant økt hos hunnrotter ved alle testede doser (0,3, 1 og 3 ganger MRHD basert på mg/m2 kroppsoverflate).
Skjoldbruskkjertelfollikulære celleadenomer kan være et resultat av kronisk stimulering av skjoldbruskkjertelen med skjoldbruskkjertelstimulerende hormon (TSH) som følge av økt metabolisme og clearance av tyroksin fra gnagerlever. Endringer i TSH, tyroksin og tyroksinclearance i samsvar med denne mekanismen ble observert i subkroniske toksisitetsstudier på rotter og mus og i en 1-årig toksisitetsstudie på rotter; resultatene av disse studiene var imidlertid ikke definitive. Relevansen av økningen i follikulære celleadenomer i skjoldbruskkjertelen for menneskelig risiko, uansett mekanisme, er ukjent.
Antipsykotiske legemidler har vist seg å kronisk øke prolaktinnivået hos gnagere. Serummålinger i en 1-årig toksisitetsstudie viste at quetiapin økte median prolaktinnivå i serum maksimalt 32- og 13-dobling hos henholdsvis hann- og hunnrotter. Økning i brystneoplasmer er funnet hos gnagere etter kronisk administrering av andre antipsykotiske legemidler og anses å være prolaktin-mediert. Relevansen av denne økte forekomsten av prolaktin-mediert brystkjerteltumor hos rotter for menneskelig risiko er ukjent [se ADVARSLER OG FORHOLDSREGLER ].
Mutagenese
Quetiapin var ikke mutagent eller klastogent i standard genotoksisitetstester. Det mutagene potensialet til quetiapin ble testet i in vitro Ames bakteriell genmutasjonsanalyse og i in vitro pattedyrgenmutasjonsanalyse i kinesisk hamster eggstokkceller. Det klastogene potensialet til quetiapin ble testet i in vitro kromosomavviksanalyse i dyrkede humane lymfocytter og i in vivo benmargsmikronukleusanalyse hos rotter opp til 500 mg/kg, som er 6 ganger den maksimale anbefalte humane dosen basert på mg/m2 kroppsoverflate.
Nedsatt fruktbarhet
Quetiapin reduserte paring og fertilitet hos Sprague-Dawley hannrotter ved orale doser på 50 og 150 mg/kg eller omtrent 1 og 3 ganger MRHD på 800 mg/dag basert på mg/m2 kroppsoverflate. Legemiddelrelaterte effekter inkluderte økninger i paringsintervall og i antall parringer som kreves for vellykket impregnering. Disse effektene fortsatte å bli observert ved 3 ganger MRHD selv etter en to ukers periode uten behandling. Ingen-effektdosen for svekket parring og fertilitet hos hannrotter var 25 mg/kg, eller 0,3 ganger MRHD-dosen basert på mg/m2 kroppsoverflate. Quetiapin påvirket paring og fertilitet negativt hos Sprague-Dawley hunnrotter ved en oral dose omtrent 1 ganger MRHD på 800 mg/dag basert på mg/m2 kroppsoverflate. Legemiddelrelaterte effekter inkluderte reduksjoner i paringer og i paringer som resulterte i graviditet, og en økning i paringsintervallet. En økning i uregelmessige brunstsykluser ble observert ved doser på 10 og 50 mg/kg, eller omtrent 0,1 og 1 ganger MRHD på 800 mg/dag basert på mg/m2 kroppsoverflate. Ingen-effektdosen hos hunnrotter var 1 mg/kg, eller 0,01 ganger MRHD på 800 mg/dag basert på mg/m2 kroppsoverflate.
Bruk i spesifikke populasjoner
Svangerskap
Eksponeringsregister for graviditet
Det finnes et graviditetseksponeringsregister som overvåker graviditetsutfall hos kvinner som eksponeres for atypiske antipsykotika, inkludert SEROQUEL 50 mg, under graviditet. Helsepersonell oppfordres til å registrere pasienter ved å kontakte National Pregnancy Registry for Atypical Antipsychotics på 1-866-961-2388 eller online på http://womensmentalhealth.org/clinical-and-research-programs/pregnancyregistry/
Risikosammendrag
Nyfødte eksponert for antipsykotiske legemidler (inkludert SEROQUEL) i tredje trimester har risiko for ekstrapyramidale og/eller abstinenssymptomer etter fødsel (se Kliniske betraktninger ). Samlet tilgjengelige data fra publiserte epidemiologiske studier av gravide kvinner eksponert for quetiapin har ikke etablert en medikamentassosiert risiko for alvorlige fødselsskader, spontanabort eller ugunstige utfall hos mor eller foster (se Data ). Det er risiko for moren forbundet med ubehandlet schizofreni, bipolar I eller alvorlig depressiv lidelse, og med eksponering for antipsykotika, inkludert SEROQUEL 200 mg, under graviditet (se Kliniske betraktninger ).
I dyrestudier forekom embryo-føtal toksisitet inkludert forsinkelser i skjelettforbening ved omtrent 1 og 2 ganger den maksimale anbefalte humane dosen (MRHD) på 800 mg/dag hos både rotter og kaniner, og en økt forekomst av karpal/tarsal bøyning (mindre) bløtvevsanomali) hos kaninfostre ved omtrent 2 ganger MRHD. I tillegg ble fostervekten redusert hos begge artene. Maternell toksisitet (observert som redusert kroppsvekt og/eller død) forekom ved 2 ganger MRHD hos rotter og omtrent 1-2 ganger MRHD hos kaniner.
Estimert bakgrunnsrisiko for alvorlige fødselsskader og spontanabort for de angitte populasjonene er ukjent. Alle graviditeter har en bakgrunnsrisiko for fødselsskader, tap eller andre uheldige utfall. I den generelle befolkningen i USA er den estimerte bakgrunnsrisikoen for alvorlige fødselsskader og spontanabort i klinisk anerkjente svangerskap henholdsvis 2 til 4 % og 15 til 20 %.
Kliniske betraktninger
Sykdomsrelatert mors- og/eller fosterrisiko
Det er en risiko for mor fra ubehandlet schizofreni, eller bipolar lidelse I, inkludert økt risiko for tilbakefall, sykehusinnleggelse og selvmord. Schizofreni og bipolar lidelse I er assosiert med økte uønskede perinatale utfall, inkludert prematur fødsel. Det er ikke kjent om dette er et direkte resultat av sykdommen eller andre komorbide faktorer.
En prospektiv, longitudinell studie fulgte 201 gravide kvinner med en historie med alvorlig depressiv lidelse som var euthymic og tok antidepressiva i begynnelsen av svangerskapet. Kvinnene som sluttet med antidepressiva under svangerskapet hadde større sannsynlighet for å få tilbakefall av alvorlig depresjon enn kvinner som fortsatte med antidepressiva. Vurder risikoen for ubehandlet depresjon når du avbryter eller endrer behandling med antidepressiva under graviditet og etter fødsel.
Fetale/neonatale bivirkninger
Ekstrapyramidale og/eller abstinenssymptomer, inkludert agitasjon, hypertoni, hypotoni, skjelving, somnolens, pustebesvær og matforstyrrelser er rapportert hos nyfødte som ble eksponert for antipsykotiske legemidler, inkludert SEROQUEL 50 mg, i løpet av tredje trimester av svangerskapet. Disse symptomene varierte i alvorlighetsgrad. Overvåk nyfødte for ekstrapyramidale og/eller abstinenssymptomer og håndter symptomene på riktig måte. Noen nyfødte kom seg i løpet av timer eller dager uten spesifikk behandling; andre krevde langvarig sykehusinnleggelse.
Data
Menneskelige data
Publiserte data fra observasjonsstudier, fødselsregistre og kasusrapporter om bruk av atypiske antipsykotika under graviditet rapporterer ikke en klar sammenheng med antipsykotika og store fødselsskader. En retrospektiv kohortstudie fra en Medicaid-database med 9258 kvinner eksponert for antipsykotika under graviditet indikerte ikke en samlet økt risiko for alvorlige fødselsskader.
Dyredata
Når drektige rotter og kaniner ble eksponert for quetiapin under organogenese, var det ingen teratogene effekt hos fostre. Doser var 25, 50 og 200 mg/kg hos rotter og 25, 50 og 100 mg/kg hos kaniner som er omtrent 0,3, 0,6 og 2 ganger (rotter) og 0,6, 1 og 2 ganger (kaniner) MRHD for schizofreni på 800 mg/dag basert på mg/m2 kroppsoverflate. Det var imidlertid tegn på embryo-føtal toksisitet inkludert forsinkelser i skjelettforbening ved omtrent 1 og 2 ganger MRHD på 800 mg/dag hos både rotter og kaniner, og en økt forekomst av karpal/tarsal bøyning (mindre bløtvevsanomali) hos kaninfostre ved omtrent 2 ganger MRHD. I tillegg ble fostervekten redusert hos begge artene. Maternell toksisitet (observert som redusert kroppsvekt og/eller død) forekom ved 2 ganger MRHD hos rotter og ca. 1-2 ganger MRHD (alle testede doser) hos kaniner.
en peri/postnatal reproduksjonsstudie på rotter ble det ikke observert legemiddelrelaterte effekter når gravide kvinner ble behandlet med quetiapin i doser 0,01, 0,1 og 0,2 ganger MRHD på 800 mg/dag basert på mg/m2 kroppsoverflate. I en foreløpig peri/postnatal studie var det imidlertid økning i foster- og valpedød, og reduksjon i gjennomsnittlig kullvekt ved 3 ganger MRHD.
Amming
Risikosammendrag
Begrensede data fra publisert litteratur rapporterer tilstedeværelse av kvetiapin i morsmelk ved en relativ spedbarnsdose på
Kvinner og menn med reproduktivt potensial
Infertilitet
Kvinner
Basert på den farmakologiske virkningen av quetiapin (D2-antagonisme), kan behandling med SEROQUEL resultere i en økning i serumprolaktinnivåer, noe som kan føre til en reversibel reduksjon i fertilitet hos kvinner med reproduksjonspotensial [se ADVARSLER OG FORHOLDSREGLER ].
Pediatrisk bruk
Generelt var bivirkningene observert hos barn og ungdom under de kliniske studiene lik de i den voksne befolkningen med få unntak. Økning i systolisk og diastolisk blodtrykk forekom hos barn og ungdom og forekom ikke hos voksne. Ortostatisk hypotensjon forekom hyppigere hos voksne (4-7 %) sammenlignet med barn og ungdom ( ADVARSLER OG FORHOLDSREGLER og BIVIRKNINGER ].
Schizofreni
Effekten og sikkerheten til SEROQUEL 50 mg i behandling av schizofreni hos ungdom i alderen 13-17 år ble vist i en 6-ukers, dobbeltblind, placebokontrollert studie [se INDIKASJONER , DOSERING OG ADMINISTRASJON , BIVIRKNINGER , og Kliniske studier ].
Sikkerhet og effektivitet av SEROQUEL 300 mg hos pediatriske pasienter under 13 år med schizofreni er ikke fastslått.
Vedlikehold
Sikkerheten og effektiviteten til SEROQUEL i vedlikeholdsbehandling av bipolar lidelse er ikke fastslått hos pediatriske pasienter under 18 år. Sikkerheten og effektiviteten til SEROQUEL i vedlikeholdsbehandling av schizofreni er ikke fastslått hos noen pasientpopulasjon, inkludert pediatriske pasienter.
Bipolar mani
Effekten og sikkerheten til SEROQUEL ved behandling av mani hos barn og ungdom i alderen 10-17 år med bipolar lidelse I ble demonstrert i en 3-ukers, dobbeltblind, placebokontrollert, multisenterstudie [se INDIKASJONER , DOSERING OG ADMINISTRASJON , BIVIRKNINGER , og Kliniske studier ]. Sikkerhet og effektivitet av SEROQUEL hos pediatriske pasienter under 10 år med bipolar mani er ikke fastslått.
Bipolar depresjon
Sikkerhet og effektivitet av SEROQUEL 300 mg hos pediatriske pasienter under 18 år med bipolar depresjon er ikke fastslått. En klinisk studie med SEROQUEL XR ble utført hos barn og ungdom (10-17 år) med bipolar depresjon, effekt ble ikke fastslått.
Noen forskjeller i farmakokinetikken til quetiapin ble observert mellom barn/ungdom (10-17 år) og voksne. Når det ble justert for vekt, var AUC og Cmax for quetiapin henholdsvis 41 % og 39 % lavere hos barn og ungdom sammenlignet med voksne. Farmakokinetikken til den aktive metabolitten, norquetiapin, var lik for barn/ungdom og voksne etter justering for vekt [se KLINISK FARMAKOLOGI ].
Geriatrisk bruk
Av de ca. 3700 pasientene i kliniske studier med SEROQUEL 300 mg, var 7 % (232) 65 år eller eldre. Generelt var det ingen indikasjon på forskjellig tolerabilitet av SEROQUEL hos eldre sammenlignet med yngre voksne. Likevel bør tilstedeværelsen av faktorer som kan redusere farmakokinetisk clearance, øke den farmakodynamiske responsen på SEROQUEL 200 mg eller forårsake dårligere toleranse eller ortostase, føre til vurdering av en lavere startdose, langsommere titrering og nøye overvåking under den innledende doseringsperioden i eldre. Gjennomsnittlig plasmaclearance av SEROQUEL 25 mg ble redusert med 30 % til 50 % hos eldre pasienter sammenlignet med yngre pasienter [se KLINISK FARMAKOLOGI og DOSERING OG ADMINISTRASJON ].
Nedsatt nyrefunksjon
Klinisk erfaring med SEROQUEL hos pasienter med nedsatt nyrefunksjon er begrenset [se KLINISK FARMAKOLOGI ].
Nedsatt leverfunksjon
Siden quetiapin metaboliseres i stor grad av leveren, forventes høyere plasmanivåer hos pasienter med nedsatt leverfunksjon. I denne populasjonen anbefales en lav startdose på 25 mg/dag og dosen kan økes i trinn på 25 mg/dag-50 mg/dag [se DOSERING OG ADMINISTRASJON og KLINISK FARMAKOLOGI ].
OVERDOSE
Menneskelig erfaring
I kliniske studier er overlevelse rapportert ved akutte overdoser på opptil 30 gram quetiapin. De fleste pasienter som overdoserte opplevde ingen bivirkninger eller kom seg helt etter de rapporterte hendelsene. Død er rapportert i en klinisk studie etter en overdose på 13,6 gram quetiapin alene. Generelt var rapporterte tegn og symptomer de som var et resultat av en overdrivelse av legemidlets kjente farmakologiske effekter, dvs. døsighet, sedasjon, takykardi, hypotensjon og antikolinerg toksisitet inkludert koma og delirium. Pasienter med allerede eksisterende alvorlig kardiovaskulær sykdom kan ha økt risiko for effekter av overdose [se ADVARSLER OG FORHOLDSREGLER ]. Ett tilfelle, som involverte en estimert overdose på 9600 mg, var assosiert med hypokalemi og førstegrads hjerteblokk. Etter markedsføring er det rapportert tilfeller av QT-forlengelse med overdose.
Håndtering av overdosering
Etabler og vedlikehold en luftvei og sørg for tilstrekkelig oksygenering og ventilasjon. Kardiovaskulær overvåking bør starte umiddelbart og bør inkludere kontinuerlig elektrokardiografisk overvåking for å oppdage mulige arytmier.
Hensiktsmessige støttetiltak er bærebjelken i ledelsen. For den mest oppdaterte informasjonen om håndtering av Seroquel XR-overdosering, kontakt et sertifisert regionalt giftkontrollsenter (1-800-222-1222).
KONTRAINDIKASJONER
Overfølsomhet overfor quetiapin eller noen hjelpestoffer i SEROQUEL XR-formuleringen. Anafylaktiske reaksjoner er rapportert hos pasienter behandlet med SEROQUEL XR.
KLINISK FARMAKOLOGI
Virkningsmekanismen
Virkningsmekanismen til quetiapin i de listede indikasjonene er uklar. Effekten av quetiapin ved disse indikasjonene kan imidlertid medieres gjennom en kombinasjon av dopamin type 2 (D2) og serotonin type 2 (5HT2) antagonisme. Den aktive metabolitten, N-desalkylquetiapin (norquetiapin), har lignende aktivitet ved D2, men større aktivitet ved 5HT2A-reseptorer, enn moderstoffet (quetiapin).
Farmakodynamikk
Quetiapin og dets metabolitt, norquetiapin, har affinitet for flere nevrotransmitterreseptorer med norquetiapin-binding med høyere affinitet enn quetiapin generelt. Ki-verdiene for quetiapin og norquetiapin ved dopamin D1 er 428/99,8 nM, ved D2 626/489 nM, ved serotonin 5HT1A 1040/191 nM ved 5HT2A 38/2,9 nM, ved histamin H1 ,14 M1,14 M1,14 M1, 14 M1, 14 M1. 38,3 nM, og ved adrenerg alb 14,6/46,4 nM og ved a2-reseptorer 617/1290 nM, henholdsvis. Quetiapin og norquetiapin mangler merkbar affinitet til benzodiazepinreseptorene.
Effekt på QT-intervall
kliniske studier var quetiapin ikke assosiert med en vedvarende økning i QT-intervaller. QT-effekten ble imidlertid ikke systematisk evaluert i en grundig QT-studie. Etter markedsføring ble det rapportert tilfeller av QT-forlengelse hos pasienter som overdoserte quetiapin [se OVERDOSE ], hos pasienter med samtidig sykdom, og hos pasienter som tar medisiner som er kjent for å forårsake elektrolyttforstyrrelser eller øke QT-intervallet.
Farmakokinetikk
Voksne
Quetiapinfumarataktivitet skyldes primært det opprinnelige legemidlet. Multippeldose-farmakokinetikken til quetiapin er doseproporsjonal innenfor det foreslåtte kliniske doseområdet, og quetiapinakkumulering er forutsigbar ved gjentatt dosering. Eliminering av quetiapin skjer hovedsakelig via levermetabolisme med en gjennomsnittlig terminal halveringstid på ca. 6 timer innenfor det foreslåtte kliniske doseområdet. Steady-state konsentrasjoner forventes å oppnås innen to dager etter dosering. Det er usannsynlig at quetiapin vil forstyrre metabolismen av legemidler som metaboliseres av cytokrom P450-enzymer.
Barn Og Ungdom
Ved steady state var farmakokinetikken til moderstoffet, hos barn og ungdom (10-17 år), lik hos voksne. Når det ble justert for dose og vekt, var imidlertid AUC og Cmax for moderstoffet henholdsvis 41 % og 39 % lavere hos barn og ungdom enn hos voksne. For den aktive metabolitten, norquetiapin, var AUC og Cmax henholdsvis 45 % og 31 % høyere hos barn og ungdom enn hos voksne. Når justert for dose og vekt, var farmakokinetikken til metabolitten, norquetiapin, lik for barn og ungdom og voksne [se Bruk i spesifikke populasjoner ].
Absorpsjon
Quetiapinfumarat absorberes raskt etter oral administrering og når maksimal plasmakonsentrasjon etter 1,5 timer. Tablettformuleringen er 100 % biotilgjengelig i forhold til oppløsning. Biotilgjengeligheten av quetiapin påvirkes marginalt av administrering med mat, med Cmax og AUC-verdier økt med henholdsvis 25 % og 15 %.
Fordeling
Quetiapin er vidt distribuert i hele kroppen med et tilsynelatende distribusjonsvolum på 10±4 l/kg. Det er 83 % bundet til plasmaproteiner ved terapeutiske konsentrasjoner. In vitro påvirket ikke quetiapin bindingen av warfarin eller diazepam til humant serumalbumin. I sin tur endret verken warfarin eller diazepam bindingen av quetiapin.
Metabolisme og eliminering
Etter en enkelt oral dose av 14C-quetiapin ble mindre enn 1 % av den administrerte dosen skilt ut som uendret legemiddel, noe som indikerer at kvetiapin er høyt metabolisert. Omtrent 73 % og 20 % av dosen ble gjenfunnet i henholdsvis urin og avføring.
Quetiapin metaboliseres i stor grad i leveren. De viktigste metabolske veiene er sulfoksidasjon til sulfoksidmetabolitten og oksidasjon til modersyremetabolitten; begge metabolittene er farmakologisk inaktive. In vitro-studier med humane levermikrosomer viste at cytokrom P450 3A4 isoenzymet er involvert i metabolismen av quetiapin til dens viktigste, men inaktive, sulfoksidmetabolitt og i metabolismen av dens aktive metabolitt N-desalkyl quetiapin.
Alder
Oral clearance av quetiapin ble redusert med 40 % hos eldre pasienter (≥ 65 år, n=9) sammenlignet med unge pasienter (n=12), og dosejustering kan være nødvendig [se DOSERING OG ADMINISTRASJON ].
Kjønn
Det er ingen kjønnseffekt på farmakokinetikken til quetiapin.
Løp
Det er ingen raseeffekt på farmakokinetikken til quetiapin.
Røyking
Røyking har ingen effekt på oral clearance av quetiapin.
Nyreinsuffisiens
Pasienter med alvorlig nedsatt nyrefunksjon (Clcr=10-30 mL/min/1,73 m2, n=8) hadde en 25 % lavere gjennomsnittlig oral clearance enn normale forsøkspersoner (Clcr > 80 mL/min/1,73 m2, n=8), men plasmakonsentrasjoner av kvetiapin hos pasienter med nyreinsuffisiens var innenfor konsentrasjonsområdet som ble sett hos normale personer som fikk samme dose. Dosejustering er derfor ikke nødvendig hos disse pasientene [se Bruk i spesifikke populasjoner ].
Leverinsuffisiens
Pasienter med nedsatt leverfunksjon (n=8) hadde en 30 % lavere gjennomsnittlig oral clearance av quetiapin enn normale forsøkspersoner. Hos to av de 8 pasientene med nedsatt leverfunksjon var AUC og Cmax 3 ganger høyere enn de som vanligvis observeres hos friske personer. Siden quetiapin metaboliseres i stor grad i leveren, forventes høyere plasmanivåer hos personer med nedsatt leverfunksjon, og dosejustering kan være nødvendig [se DOSERING OG ADMINISTRASJON og BRUK I SPESIFIKKE BEFOLKNINGER ].
Studier av legemiddel-medikamentinteraksjoner
In vivo vurderingene av effekt av andre legemidler på farmakokinetikken til quetiapin er oppsummert i tabell 17 [se DOSERING OG ADMINISTRASJON og NARKOTIKAHANDEL ].
In vitro enzymhemmingsdata tyder på at quetiapin og 9 av dets metabolitter vil ha liten hemmende effekt på in vivo metabolisme mediert av cytokromer CYP 1A2, 2C9, 2C19, 2D6 og 3A4. Quetiapin i doser på 750 mg/dag påvirket ikke enkeltdose-farmakokinetikken til antipyrin, litium eller lorazepam (tabell 18) [se NARKOTIKAHANDEL ].
Dyretoksikologi og/eller farmakologi
Quetiapin forårsaket en doserelatert økning i pigmentavsetning i skjoldbruskkjertelen i toksisitetsstudier på rotter som varte 4 uker eller lenger, og i en 2-årig karsinogenitetsstudie på mus. Doser var 10, 25, 50, 75, 150 og 250 mg/kg i rottestudier som er omtrent 0,1, 0,3, 0,6, 1, 2 og 3 ganger MRHD på 800 mg/dag basert på mg/m2 kroppsoverflate. , henholdsvis. Doser i musekarsinogenitetsstudien var 20, 75, 250 og 750 mg/kg som er omtrent 0,1, 0,5, 1,5 og 4,5 ganger MRHD på 800 mg/dag basert på mg/m2 kroppsoverflate. Pigmentavsetning ble vist å være irreversibel hos rotter. Identiteten til pigmentet kunne ikke bestemmes, men ble funnet å være samlokalisert med quetiapin i follikulære epitelceller i skjoldbruskkjertelen. De funksjonelle effektene og relevansen av dette funnet for menneskelig risiko er ukjent.
Hos hunder som fikk quetiapin i 6 eller 12 måneder, men ikke i 1 måned, oppsto fokal trekantet grå stær ved krysset mellom bakre suturer i den ytre cortex av linsen med en dose på 100 mg/kg, eller 4 ganger MRHD på 800 mg/dag basert på mg/m2 kroppsoverflate. Dette funnet kan skyldes hemming av kolesterolbiosyntesen av quetiapin. Quetiapin forårsaket en doserelatert reduksjon i plasmakolesterolnivåer i studier med gjentatte doser på hunder og aper; Det var imidlertid ingen sammenheng mellom plasmakolesterol og tilstedeværelsen av grå stær hos individuelle hunder. Utseendet til delta-8kolestanol i plasma er i samsvar med hemming av et sent stadium i kolesterolbiosyntesen hos disse artene. Det var også en 25 % reduksjon i kolesterolinnholdet i den ytre cortex av linsen observert i en spesiell studie på quetiapinbehandlede hunnhunder. Narkotikarelatert grå stær har ikke blitt sett hos noen andre arter; I en 1-årig studie på aper ble det imidlertid påvist et tverrstripet utseende av den fremre linseoverflaten hos 2/7 kvinner ved en dose på 225 mg/kg eller 5,5 ganger MRHD på 800 mg/dag basert på mg/m2 kropp flateareal.
Kliniske studier
Schizofreni
Korttidsprøver-Voksne
Effekten av SEROQUEL 50 mg i behandling av schizofreni ble fastslått i 3 korttids (6 ukers) kontrollerte studier med inneliggende pasienter med schizofreni som oppfylte DSM III-R-kriteriene for schizofreni. Selv om en enkelt fast dose haloperidolarm ble inkludert som en sammenlignende behandling i en av de tre studiene, var denne enkelt haloperidoldosegruppen utilstrekkelig til å gi en pålitelig og gyldig sammenligning av SEROQUEL 200mg og haloperidol.
Flere instrumenter ble brukt for å vurdere psykiatriske tegn og symptomer i disse studiene, blant dem Brief Psychiatric Rating Scale (BPRS), en multi-element inventar av generell psykopatologi som tradisjonelt brukes til å evaluere effekten av medikamentell behandling ved schizofreni. BPRS-psykoseklyngen (konseptuell desorganisering, hallusinatorisk atferd, mistenksomhet og uvanlig tankeinnhold) anses som en spesielt nyttig undergruppe for vurdering av aktivt psykotiske schizofrene pasienter. En annen tradisjonell vurdering, Clinical Global Impression (CGI), gjenspeiler inntrykket av en dyktig observatør, fullt kjent med manifestasjonene av schizofreni, om den generelle kliniske tilstanden til pasienten.
Resultatene av forsøkene følger:
. en 6-ukers, placebokontrollert studie (n=361) (studie 1) som involverte 5 faste doser av SEROQUEL (75 mg/dag, 150 mg/dag, 300 mg/dag, 600 mg/dag og 750 mg/dag dag gitt i delte doser tre ganger per dag), var de 4 høyeste dosene av SEROQUEL generelt overlegne placebo på BPRS-totalskåren, BPRS-psykoseklusteret og CGI-alvorlighetsskåren, med maksimal effekt sett ved 300 mg/dag, og effekten av doser på 150 mg/dag til 750 mg/dag var generelt umulig å skille. . I en 6-ukers, placebokontrollert studie (n=286) (studie 2) som involverte titrering av SEROQUEL 300 mg i høy (opptil 750 mg/dag gitt i delte doser tre ganger daglig) og lav (opptil 250 mg/dag) dag gitt i delte doser tre ganger per dag), var bare høydose SEROQUEL 200 mg-gruppen (gjennomsnittlig dose, 500 mg/dag) overlegen placebo på BPRS-totalskåren, BPRS-psykoseklusteret og CGI-alvorlighetsskåren. . en 6-ukers dose- og doseregime-sammenligningsstudie (n=618) (studie 3) som involverte to faste doser av SEROQUEL (450 mg/dag gitt i delte doser både to ganger daglig og tre ganger daglig og 50 mg/dag fordelt på doser to ganger daglig), var bare dosegruppen 450 mg/dag (225 mg gitt to ganger daglig) overlegen i forhold til 50 mg/dag (25 mg gitt to ganger daglig) SEROQUEL-dosegruppen på BPRS-totalskåren, BPRS-psykoseklyngen, og CGI alvorlighetsgraden.De primære effektresultatene av disse tre studiene i behandling av schizofreni hos voksne er presentert i tabell 19.
Undersøkelse av populasjonsundergrupper (rase, kjønn og alder) avdekket ingen differensiell respons på grunnlag av rase eller kjønn, med en tilsynelatende større effekt hos pasienter under 40 år sammenlignet med de eldre enn 40. Den kliniske betydningen av dette funnet er ukjent.
Ungdom (13–17 år)
Effekten av SEROQUEL 300 mg ved behandling av schizofreni hos ungdom (13-17 år) ble vist i en 6-ukers, dobbeltblind, placebokontrollert studie (studie 4). Pasienter som oppfylte DSM-IV diagnostiske kriterier for schizofreni ble randomisert i en av tre behandlingsgrupper: SEROQUEL 400 mg/dag (n=73), SEROQUEL 800 mg/dag (n=74) eller placebo (n=75). Studiemedisin ble startet med 50 mg/dag og på dag 2 økt til 100 mg/dag (delt og gitt to eller tre ganger daglig). Deretter ble dosen titrert til måldosen på 400 mg/dag eller 800 mg/dag ved bruk av trinn på 100 mg/dag, delt og gitt to eller tre ganger daglig. Den primære effektvariabelen var gjennomsnittlig endring fra baseline i total positiv og negativ syndromskala (PANSS).
SEROQUEL ved 400 mg/dag og 800 mg/dag var overlegen placebo i reduksjonen av PANSS totalskåre. De primære effektresultatene av denne studien i behandling av schizofreni hos ungdom er presentert i tabell 19.
Bipolar lidelse
Bipolar I-lidelse, maniske eller blandede episoder
Voksne
Effekten av SEROQUEL ved akutt behandling av maniske episoder ble fastslått i 3 placebokontrollerte studier hos pasienter som oppfylte DSM-IV-kriteriene for bipolar I lidelse med maniske episoder. Disse studiene inkluderte pasienter med eller uten psykotiske trekk og ekskluderte pasienter med rask sykling og blandede episoder. Av disse studiene var 2 monoterapi (12 uker) og 1 var tilleggsbehandling (3 uker) til enten litium eller divalproex. Nøkkelresultatene i disse studiene var endring fra baseline i Young Mania Rating Scale (YMRS)-score ved 3 og 12 uker for monoterapi og etter 3 uker for tilleggsbehandling. Tilleggsbehandling er definert som samtidig initiering eller påfølgende administrering av SEROQUEL 100 mg med litium eller divalproex.
Det primære vurderingsinstrumentet som ble brukt for å vurdere maniske symptomer i disse forsøkene var YMRS, en 11-punkts klinikervurdert skala som tradisjonelt ble brukt til å vurdere graden av manisk symptomatologi (irritabilitet, forstyrrende/aggressiv atferd, søvn, forhøyet humør, tale, økt aktivitet, seksuell interesse, språk-/tankeforstyrrelse, tankeinnhold, utseende og innsikt) i området fra 0 (ingen maniske trekk) til 60 (maksimal poengsum).
Resultatene av forsøkene følger:
Monoterapi
Effekten av SEROQUEL ved akutt behandling av bipolar mani ble fastslått i 2 placebokontrollerte studier. I to 12-ukers studier (n=300, n=299) som sammenlignet SEROQUEL med placebo, var SEROQUEL 300 mg overlegen placebo når det gjelder reduksjon av YMRS totalscore ved uke 3 og 12. Flertallet av pasientene i disse studiene tok SEROQUEL 100 mg ble dosert i et område mellom 400 mg/dag og 800 mg per dag (studie 1 og 2 i tabell 20).
Tilleggsterapi
denne 3-ukers placebokontrollerte studien ble 170 pasienter med bipolar mani (YMRS ≥20) randomisert til å motta SEROQUEL 100 mg eller placebo som tilleggsbehandling til litium eller divalproex. Pasienter kan ha mottatt et adekvat behandlingsforløp med litium eller divalproex før randomisering. SEROQUEL 50 mg var overlegen placebo når det ble lagt til litium eller divalproex alene i reduksjonen av YMRS totalscore (studie 3 i tabell 20).
Flertallet av pasientene i denne studien som tok SEROQUEL 25 mg ble doseret i et område mellom 400 mg/dag og 800 mg/dag. I en lignende utformet studie (n=200), var SEROQUEL assosiert med en forbedring i YMRS-skåre, men viste ikke overlegenhet i forhold til placebo, muligens på grunn av en høyere placeboeffekt.
De primære effektresultatene av disse studiene i behandling av mani hos voksne er presentert i tabell 20.
Barn og ungdom (10-17 år)
Effekten av SEROQUEL ved akutt behandling av maniske episoder assosiert med bipolar lidelse I hos barn og ungdom (10-17 år) ble vist i en 3-ukers, dobbeltblind, placebokontrollert, multisenterstudie (studie 4 i Tabell 20). Pasienter som oppfylte DSM-IV diagnostiske kriterier for en manisk episode ble randomisert i en av tre behandlingsgrupper: SEROQUEL 400 mg/dag (n=95), SEROQUEL 600 mg/dag (n=98) eller placebo (n=91) . Studiemedisin ble startet med 50 mg/dag og på dag 2 økt til 100 mg/dag (delte doser gitt to eller tre ganger daglig). Deretter ble dosen titrert til en måldose på 400 mg/dag eller 600 mg/dag ved bruk av trinn på 100 mg/dag, gitt i delte doser to eller tre ganger daglig. Den primære effektvariabelen var gjennomsnittlig endring fra baseline i total YMRS-skåre.
SEROQUEL 400 mg/dag og 600 mg/dag var overlegen placebo i reduksjonen av YMRS totalscore (tabell 20).
Bipolar lidelse, depressive episoder
Voksne
Effekten av SEROQUEL 25 mg for akutt behandling av depressive episoder assosiert med bipolar lidelse ble fastslått i 2 identisk utformede 8-ukers, randomiserte, dobbeltblinde, placebokontrollerte studier (N=1045) (studier 5 og 6 i tabell 21) . Disse studiene inkluderte pasienter med enten bipolar I- eller II-lidelse og de med eller uten et raskt sykkelforløp. Pasienter randomisert til SEROQUEL 200 mg ble administrert faste doser på enten 300 mg eller 600 mg én gang daglig.
Det primære vurderingsinstrumentet som ble brukt til å vurdere depressive symptomer i disse studiene var Montgomery-Asberg Depression Rating Scale (MADRS), en 10-elements klinikervurdert skala med skårer fra 0 til 60. Det primære endepunktet i begge studiene var endringen fra baseline i MADRS-score ved uke 8. I begge studiene var SEROQUEL 50 mg bedre enn placebo med hensyn til reduksjon av MADRS-score. Forbedring av symptomer, målt ved endring i MADRS-skåre i forhold til placebo, ble sett i begge studiene på dag 8 (uke 1) og utover. I disse studiene ble det ikke sett ytterligere fordeler med dosen på 600 mg. For 300 mg-dosegruppen ble det sett statistisk signifikante forbedringer i forhold til placebo i generell livskvalitet og tilfredshet relatert til ulike funksjonsområder, målt ved bruk av Q-LES-Q(SF).
De primære effektresultatene fra disse studiene i akutt behandling av depressive episoder assosiert med bipolar lidelse hos voksne er presentert i tabell 21.
Vedlikeholdsbehandling som et tillegg til litium eller divalproex
Effekten av SEROQUEL 100 mg i vedlikeholdsbehandling av bipolar I-lidelse ble fastslått i 2 placebokontrollerte studier på pasienter (n=1326) som oppfylte DSM-IV-kriteriene for bipolar I-lidelse (studiene 7 og 8 i figur 1 og 2). Forsøkene inkluderte pasienter hvis siste episode var manisk, deprimert eller blandet, med eller uten psykotiske trekk. I den åpne fasen måtte pasientene være stabile på SEROQUEL pluss litium eller divalproex i minst 12 uker for å bli randomisert. I gjennomsnitt ble pasientene stabilisert i 15 uker. I randomiseringsfasen fortsatte pasientene behandlingen med litium eller divalproex og ble randomisert til å motta enten SEROQUEL (administrert to ganger daglig med totalt 400 mg/dag til 800 mg/dag) eller placebo. Omtrent 50 % av pasientene hadde avbrutt behandlingen fra SEROQUEL-gruppen på dag 280 og 50 % av placebogruppen hadde avbrutt på dag 117 med dobbeltblind behandling. Det primære endepunktet i disse studiene var tid til gjentakelse av en stemningsbegivenhet (manisk, blandet eller deprimert episode). En stemningsbegivenhet ble definert som medisinering eller sykehusinnleggelse for en stemningsepisode; YMRS-score≥20 eller MADRS-score≥20 ved 2 påfølgende vurderinger; eller studieavbrudd på grunn av en stemningsbegivenhet (Figur 1 og Figur 2).
begge studiene var SEROQUEL overlegen placebo når det gjaldt å øke tiden til gjentakelse av enhver stemningsbegivenhet. Behandlingseffekten var til stede for økende tid til tilbakefall av både maniske og deprimerte episoder. Effekten av SEROQUEL var uavhengig av en hvilken som helst spesifikk undergruppe (tildelt humørstabilisator, kjønn, alder, rase, siste bipolar episode eller rask sykling).
Figur 1: Kaplan-Meier-kurver over tid til gjentakelse av en stemningsbegivenhet (studie 7)
Figur 2: Kaplan-Meier-kurver over tid til gjentakelse av en stemningsbegivenhet (Studie 8)
PASIENTINFORMASJON
SEROQUEL (SER-oh-kwell)(quetiapinfumarat) Tabletter
Les denne medisinveiledningen før du begynner å ta SEROQUEL og hver gang du får påfyll. Det kan komme ny informasjon. Denne informasjonen erstatter ikke å snakke med helsepersonell om din medisinske tilstand eller din behandling.
Hva er den viktigste informasjonen jeg bør vite om SEROQUEL?
SEROQUEL 100mg kan forårsake alvorlige bivirkninger, inkludert:
. risiko for død hos eldre med demens. Medisiner som SEROQUEL kan øke risikoen for død hos eldre mennesker som har hukommelsestap (demens). SEROQUEL 100mg er ikke for behandling av psykose hos eldre med demens. . risiko for selvmordstanker eller -handlinger (antidepressive medisiner, depresjon og andre alvorlige psykiske lidelser, og selvmordstanker eller -handlinger).- . Snakk med helsepersonellet ditt eller ditt familiemedlem om:
- . alle risikoer og fordeler ved behandling med antidepressiva. . alle behandlingsvalg for depresjon eller annen alvorlig psykisk lidelse
- . Vær nøye med eventuelle endringer, spesielt plutselige endringer, i humør, atferd, tanker eller følelser. Dette er svært viktig når en antidepressiv medisin startes eller når dosen endres. . Ring helsepersonell med en gang for å rapportere nye eller plutselige endringer i humør, atferd, tanker eller følelser. . Hold alle oppfølgingsbesøk hos helsepersonell som planlagt. Ring helsepersonell mellom besøkene etter behov, spesielt hvis du har bekymringer om symptomer.
Ring en helsepersonell med en gang hvis du eller familiemedlemmet ditt har noen av følgende symptomer, spesielt hvis de er nye, verre eller bekymrer deg:
- . tanker om selvmord eller å dø . forsøk på å begå selvmord . ny eller verre depresjon . ny eller verre angst . føler meg veldig urolig eller rastløs . panikk anfall . problemer med å sove (søvnløshet) . ny eller verre irritabilitet . opptrer aggressivt, er sint eller voldelig . handler på farlige impulser . en ekstrem økning i aktivitet og prat (mani) . andre uvanlige endringer i atferd eller humør
Hva annet trenger jeg å vite om antidepressiva?
- . Slutt aldri en antidepressiv medisin uten først å snakke med helsepersonell. Å stoppe en antidepressiv medisin plutselig kan forårsake andre symptomer. . Antidepressiva er medisiner som brukes til å behandle depresjon og andre sykdommer. Det er viktig å diskutere alle risikoene ved å behandle depresjon, og også risikoen ved å ikke behandle den. Pasienter og deres familier eller andre omsorgspersoner bør diskutere alle behandlingsvalg med helsepersonell, ikke bare bruken av antidepressiva. . Antidepressiva har andre bivirkninger. Snakk med helsepersonell om bivirkningene av medisinen som er foreskrevet for deg eller ditt familiemedlem. . Antidepressiva kan samhandle med andre medisiner. Kjenn til alle medisinene du eller ditt familiemedlem tar. Hold en liste over alle medisiner for å vise helsepersonell. Ikke start nye medisiner uten først å sjekke med helsepersonell. . Ikke alle antidepressive medisiner foreskrevet for barn er FDA-godkjent for bruk hos barn. Snakk med barnets helsepersonell for mer informasjon.
Hva er SEROQUEL 300mg?
SEROQUEL 100mg er et reseptbelagt legemiddel som brukes til å behandle:
- . schizofreni hos personer 13 år eller eldre . bipolar lidelse hos voksne, inkludert:
- . depressive episoder assosiert med bipolar lidelse . maniske episoder assosiert med bipolar lidelse I alene eller med litium eller divalproex . langtidsbehandling av bipolar lidelse I med litium eller divalproex
Det er ikke kjent om SEROQUEL 100mg er trygt og effektivt hos barn under 10 år.
Hva bør jeg fortelle helsepersonell før jeg tar SEROQUEL 100mg?
Før du tar SEROQUEL 200mg, fortell helsepersonell dersom du har eller har hatt:
- . diabetes eller høyt blodsukker hos deg eller din familie. Helsepersonell bør sjekke blodsukkeret ditt før du starter med SEROQUEL 300mg, og også under behandlingen . høye nivåer av totalkolesterol, triglyserider eller LDL-kolesterol, eller lave nivåer av HDL-kolesterol . lavt eller høyt blodtrykk . lavt antall hvite blodlegemer . grå stær . anfall . unormale skjoldbruskprøver . høye prolaktinnivåer . hjerteproblemer . leverproblemer . enhver annen medisinsk tilstand . graviditet eller planlegger å bli gravid. Det er ikke kjent om SEROQUEL 100 mg vil skade det ufødte barnet ditt. . Hvis du blir gravid mens du får SEROQUEL, snakk med helsepersonell om registrering hos National Pregnancy Registry for Atypical Antipsychotics. Du kan registrere deg ved å ringe 1-866-961-2388 eller gå til http://womensmentalhealth.org/clinical-and-research-programs/pregnancyregistry/ . amming eller planlegger å amme. SEROQUEL kan gå over i morsmelk. Snakk med helsepersonell om den beste måten å mate babyen din på hvis du får SEROQUEL. . hvis du har eller har hatt en tilstand hvor du ikke kan tømme blæren helt (urinretensjon), har forstørret prostata eller forstoppelse eller økt trykk inne i øynene.
Fortell helsepersonell om alle medisinene du tar eller nylig har tatt inkludert reseptbelagte medisiner, reseptfrie medisiner, urtetilskudd og vitaminer.
SEROQUEL 300mg og andre legemidler kan påvirke hverandre og forårsake alvorlige bivirkninger. SEROQUEL 200mg kan påvirke måten andre medisiner virker på, og andre medisiner kan påvirke hvordan SEROQUEL 200mg virker.
Fortell helsepersonell dersom du har en urinmedisinskelse fordi SEROQUEL kan påvirke testresultatene dine. Fortell de som tar testen at du tar SEROQUEL.
Hvordan skal jeg ta SEROQUEL?
- . Ta SEROQUEL nøyaktig slik helsepersonell ber deg ta det. Ikke endre dosen selv. . Ta SEROQUEL 25 mg gjennom munnen, med eller uten mat. . Hvis du føler at du må slutte med SEROQUEL 25mg, snakk med helsepersonell først. Hvis du plutselig slutter å ta SEROQUEL, kan du få bivirkninger som søvnproblemer eller problemer med å holde deg i søvn (søvnløshet), kvalme og oppkast. . Hvis du glemmer en dose av SEROQUEL 25 mg, ta den så snart du husker det. Hvis du er nær neste dose, hopp over den glemte dosen. Bare ta neste dose til vanlig tid. Ikke ta 2 doser samtidig med mindre helsepersonell ber deg om det. Hvis du ikke er sikker på doseringen, ring legen din.
Hva bør jeg unngå mens jeg tar SEROQUEL 100mg?
- . Ikke kjør bil, bruk maskiner eller gjør andre farlige aktiviteter før du vet hvordan SEROQUEL påvirker deg. SEROQUEL kan gjøre deg døsig. . Unngå å bli overopphetet eller dehydrert.
- . Ikke overtren. . I varmt vær, hold deg inne på et kjølig sted hvis mulig. . Hold deg unna solen. Ikke bruk for mye eller tunge klær. . Drikk mye vann.
Hva er mulige bivirkninger av SEROQUEL 300mg?
SEROQUEL 200mg kan forårsake alvorlige bivirkninger, inkludert:
- . Se "Hva er den viktigste informasjonen jeg bør vite om SEROQUEL 200mg?" . hjerneslag som kan føre til døden kan skje hos eldre personer med demens som tar medisiner som SEROQUEL . malignt neuroleptisk syndrom (NMS). NMS er en sjelden, men svært alvorlig tilstand som kan oppstå hos personer som tar antipsykotiske legemidler, inkludert SEROQUEL. NMS kan forårsake død og må behandles på sykehus. Ring helsepersonell med en gang hvis du blir alvorlig syk og har noen eller alle disse symptomene:
- . høy feber . overdreven svetting . stive muskler . forvirring . endringer i pusten, hjerterytmen og blodtrykket
- . opphopning av syre i blodet ditt på grunn av ketoner (ketoacidose) . koma . død
Økning i blodsukkeret kan forekomme hos noen personer som tar SEROQUEL. Ekstremt høyt blodsukker kan føre til koma eller død. Hvis du har diabetes eller risikofaktorer for diabetes (som overvekt eller en familiehistorie med diabetes) bør helsepersonell sjekke blodsukkeret ditt før du starter med SEROQUEL 50 mg og under behandlingen. Ring helsepersonell dersom du har noen av disse symptomene på høyt blodsukker (hyperglykemi) mens du tar SEROQUEL:
- . føler meg veldig tørst . trenger å tisse mer enn vanlig . føler meg veldig sulten . føler seg svak eller sliten . får vondt i magen . føler deg forvirret, eller pusten din lukter fruktig
De vanligste bivirkningene av SEROQUEL 50mg inkluderer:
Hos voksne:
- . døsighet . plutselig blodtrykksfall når du står opp . vektøkning . treghet . unormale leverprøver . urolig mage . tørr i munnen . svimmelhet . svakhet . magesmerter . forstoppelse . sår hals
Hos barn og ungdom:
- . døsighet . svimmelhet . utmattelse . kvalme . tørr i munnen . vektøkning . økt appetitt . oppkast . rask hjerterytme
Dette er ikke alle mulige bivirkninger av SEROQUEL. For mer informasjon, spør helsepersonell eller apotek.
Ring legen din for medisinsk råd om bivirkninger. Du kan rapportere bivirkninger til FDA på 1-800-FDA-1088.
Hvordan bør jeg oppbevare SEROQUEL 100mg?
- . Oppbevar SEROQUEL 100 mg ved romtemperatur, mellom 20 °C til 25 °C (68 °F til 77 °F). . Oppbevar SEROQUEL og alle legemidler utilgjengelig for barn.
Generell informasjon om sikker og effektiv bruk av SEROQUEL
Medisiner er noen ganger foreskrevet for andre formål enn de som er oppført i en medisinveiledning. Ikke bruk SEROQUEL for en tilstand det ikke er foreskrevet for. Ikke gi SEROQUEL til andre mennesker, selv om de har de samme symptomene som du har. Det kan skade dem.
Denne medisinguiden oppsummerer den viktigste informasjonen om SEROQUEL. Hvis du vil ha mer informasjon, snakk med helsepersonell. Du kan spørre apoteket eller helsepersonell om informasjon om SEROQUEL 100mg som er skrevet for helsepersonell.
For mer informasjon, gå til www.SEROQUEL.com , eller ring 1-800-236-9933.
Hva er ingrediensene i SEROQUEL 200mg?
Aktiv ingrediens: quetiapinfumarat
Inaktive ingredienser: povidon, dibasisk dikalsiumfosfatdihydrat, mikrokrystallinsk cellulose, natriumstivelsesglykolat, laktosemonohydrat, magnesiumstearat, hypromellose, polyetylenglykol og titandioksid. 25 mg tablettene inneholder rødt og gult jernoksid. 100 mg og 400 mg tablettene inneholder kun gult jernoksid.
Denne medisinveiledningen er godkjent av US Food and Drug Administration.
