Zyprexa 2.5mg, 5mg, 7.5mg, 10mg, 15mg, 20mg Olanzapine Bruk, bivirkninger og dosering. Pris i nettapotek. Generisk medisin uten resept.
Hva er Zyprexa 10mg og hvordan brukes det?
Zyprexa er et reseptbelagt legemiddel som brukes til å behandle symptomene på schizofreni og bipolar lidelse (manisk depresjon). Zyprexa kan brukes alene eller sammen med andre medisiner.
- . Zyprexa tilhører en klasse legemidler som kalles antipsykotika, 2. generasjons antimaniske midler. . Det er ikke kjent om Zyprexa er trygt og effektivt hos barn under 13 år.
Hva er de mulige bivirkningene av Zyprexa 15mg?
Zyprexa kan forårsake alvorlige bivirkninger, inkludert:
- . ukontrollerte muskelbevegelser i ansiktet ditt (tygging, leppesmaling, rynking, tungebevegelse, blunking eller øyebevegelser), . problemer med å snakke eller svelge, . hevelse i hender eller føtter, . forvirring, . uvanlige tanker eller oppførsel, . hallusinasjoner, . tanker om å skade deg selv, . plutselig svakhet eller dårlig følelse, . feber, . frysninger, . sår hals, . hovent tannkjøtt, . smertefulle munnsår, . smerte ved svelging, . hudsår, . forkjølelses- eller influensasymptomer, . hoste, . føler meg veldig tørst eller varm, . manglende evne til å urinere, . kraftig svette, . varm eller tørr hud, . smerter i øvre mage, . kløe, . tap av Appetit, . mørk urin, . leirefarget avføring, . gulfarging av hud eller øyne (gulsott), . økt tørst, . økt vannlating, . sult, . tørr i munnen, . lukt av fruktig pust, . døsighet, . tåkesyn, . vekttap, . veldig stive muskler, . høy feber, . forvirring, . raske eller ujevne hjerteslag, . skjelvinger, og . svimmelhet
Få medisinsk hjelp med en gang hvis du har noen av symptomene nevnt ovenfor.
De vanligste bivirkningene av Zyprexa inkluderer:
- . vektøkning (mer vanlig hos tenåringer), . økt appetitt, . hodepine, . svimmelhet, . døsighet, . føler seg trøtt eller rastløs, . problemer med tale eller hukommelse, . skjelvinger eller skjelvinger, . nummenhet eller prikkende følelse, . personlighetsendringer, . tørr i munnen, . økt spyttutskillelse, . magesmerter, . forstoppelse, og . smerter i armer eller ben
Fortell legen dersom du har noen bivirkninger som plager deg eller som ikke går over.
Dette er ikke alle mulige bivirkninger av Zyprexa. Spør legen din eller apoteket for mer informasjon.
Ring legen din for medisinsk råd om bivirkninger. Du kan rapportere bivirkninger til FDA på 1-800-FDA-1088.
ADVARSEL
ØKT DØDELIGHET HOS ELDRE PASIENTER MED DEMENSRELATTER PSYKOSE
Eldre pasienter med demensrelatert psykose behandlet med antipsykotiske legemidler har økt risiko for død. Analyser av sytten placebokontrollerte studier (modal varighet på 10 uker), hovedsakelig hos pasienter som tok atypiske antipsykotiske legemidler, viste en risiko for død hos legemiddelbehandlede pasienter på mellom 1,6 og 1,7 ganger risikoen for død hos placebobehandlede pasienter. I løpet av en typisk 10-ukers kontrollert studie var dødsraten hos medikamentbehandlede pasienter ca. 4,5 %, sammenlignet med en rate på ca. 2,6 % i placebogruppen. Selv om dødsårsakene var forskjellige, så de fleste dødsfallene ut til å være enten kardiovaskulære (f.eks. hjertesvikt, plutselig død) eller smittsomme (f.eks. lungebetennelse) av natur. Observasjonsstudier tyder på at i likhet med atypiske antipsykotiske legemidler, kan behandling med konvensjonelle antipsykotiske legemidler øke dødeligheten. Det er ikke klart i hvilken grad funnene av økt dødelighet i observasjonsstudier kan tilskrives det antipsykotiske legemidlet i motsetning til enkelte kjennetegn(er). ZYPREXA (olanzapin) er ikke godkjent for behandling av pasienter med demensrelatert psykose [se ADVARSLER OG FORHOLDSREGLER og PASIENTINFORMASJON ].
Når du bruker ZYPREXA 15mg og fluoksetin i kombinasjon, se også avsnittet Advarsel i eske i pakningsvedlegget til Symbyax.
BESKRIVELSE
ZYPREXA (olanzapin) er et atypisk antipsykotikum som tilhører tienobenzodiazepinklassen. Den kjemiske betegnelsen er 2-metyl-4-(4-metyl-1-piperazinyl)-10H-tieno[2,3-b] [1,5]benzodiazepin. Molekylformelen er C17H20N4S, som tilsvarer en molekylvekt på 312,44. Den kjemiske strukturen er:
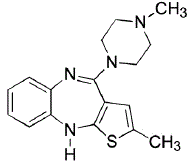
Olanzapin er et gult krystallinsk fast stoff, som er praktisk talt uløselig i vann.
ZYPREXA 7,5 mg tabletter er kun beregnet for oral administrering.
Hver tablett inneholder olanzapin tilsvarende 2,5 mg (8 μmol), 5 mg (16 μmol), 7,5 mg (24 μmol), 10 mg (32 μmol), 15 mg (48 μmol) eller 20 mg (64 μmol). Inaktive ingredienser er karnaubavoks, krospovidon, hydroksypropylcellulose, hypromellose, laktose, magnesiumstearat, mikrokrystallinsk cellulose og andre inaktive ingredienser. Fargebelegget inneholder titandioksid (alle styrker), FD&C Blue No. 2 Aluminium Lake (15 mg), eller Syntetisk rødt jernoksid (20 mg). Tablettene på 2,5, 5, 7,5 og 10 mg er merket med spiselig blekk som inneholder FD&C Blue No. 2 Aluminium Lake.
ZYPREXA 2,5 mg ZYDIS (olanzapin oralt desintegrerende tabletter) er kun beregnet for oral administrering.
Hver oralt desintegrerende tablett inneholder olanzapin tilsvarende 5 mg (16 μmol), 10 mg (32 μmol), 15 mg (48 μmol) eller 20 mg (64 μmol). Det begynner å gå i oppløsning i munnen i løpet av sekunder, slik at innholdet deretter kan svelges med eller uten væske. ZYPREXA 15mg ZYDIS (olanzapin oralt desintegrerende tabletter) inneholder også følgende inaktive ingredienser: gelatin, mannitol, aspartam, natriummetylparaben og natriumpropylparaben.
ZYPREXA 2,5 mg intramuskulært (olanzapin til injeksjon) er kun beregnet for intramuskulær bruk.
Hvert hetteglass sørger for administrering av 10 mg (32 μmol) olanzapin med inaktive ingredienser 50 mg laktosemonohydrat og 3,5 mg vinsyre. Saltsyre og/eller natriumhydroksid kan ha blitt tilsatt under produksjonen for å justere pH.
INDIKASJONER
Schizofreni
Oral ZYPREXA er indisert for behandling av schizofreni. Effekten ble etablert i tre kliniske studier med voksne pasienter med schizofreni: to 6-ukers studier og en vedlikeholdsstudie. Hos ungdomspasienter med schizofreni (alder 13-17) ble effekt etablert i en 6-ukers studie [se Kliniske studier ].
Når de skal velge blant de alternative behandlingene som er tilgjengelige for ungdom, bør klinikere vurdere det økte potensialet (hos ungdom sammenlignet med voksne) for vektøkning og dyslipidemi. Klinikere bør vurdere den potensielle langsiktige risikoen når de forskriver til ungdom, og i mange tilfeller kan dette føre til at de vurderer å foreskrive andre legemidler først hos ungdom [se ADVARSLER OG FORHOLDSREGLER ].
Bipolar I-lidelse (maniske eller blandede episoder)
Monoterapi
Oral ZYPREXA er indisert for akutt behandling av maniske eller blandede episoder assosiert med bipolar I lidelse og vedlikeholdsbehandling av bipolar I lidelse. Effekten ble etablert i tre kliniske studier på voksne pasienter med maniske eller blandede episoder av bipolar I lidelse: to 3- til 4-ukers studier og en monoterapi vedlikeholdsstudie. Hos ungdomspasienter med maniske eller blandede episoder assosiert med bipolar lidelse I (alder 13-17), ble effekt etablert i en 3-ukers studie [se Kliniske studier ].
Når de skal velge blant de alternative behandlingene som er tilgjengelige for ungdom, bør klinikere vurdere det økte potensialet (hos ungdom sammenlignet med voksne) for vektøkning og dyslipidemi. Klinikere bør vurdere den potensielle langsiktige risikoen når de forskriver til ungdom, og i mange tilfeller kan dette føre til at de vurderer å foreskrive andre legemidler først hos ungdom [se ADVARSLER OG FORHOLDSREGLER ].
Tilleggsterapi til litium eller valproat
Oral ZYPREXA 5mg er indisert for behandling av maniske eller blandede episoder assosiert med bipolar lidelse I som et tillegg til litium eller valproat. Effekten ble etablert i to 6-ukers kliniske studier hos voksne. Effektiviteten av tilleggsbehandling for langvarig bruk har ikke blitt systematisk evaluert i kontrollerte studier [se Kliniske studier ].
Spesielle hensyn ved behandling av pediatrisk schizofreni og bipolar I-lidelse
Pediatrisk schizofreni og bipolar lidelse I er alvorlige psykiske lidelser; diagnose kan imidlertid være utfordrende. For pediatrisk schizofreni kan symptomprofilene variere, og for bipolar I-lidelse kan pediatriske pasienter ha varierende periodisitetsmønstre av maniske eller blandede symptomer. Det anbefales at medikamentell behandling for pediatrisk schizofreni og bipolar lidelse I startes først etter at en grundig diagnostisk evaluering er utført og nøye overveielse av risikoene forbundet med medikamentell behandling. Medisinbehandling for både pediatrisk schizofreni og bipolar lidelse I bør være en del av et totalbehandlingsprogram som ofte inkluderer psykologiske, pedagogiske og sosiale intervensjoner.
ZYPREXA 15mg intramuskulær: agitasjon assosiert med schizofreni og bipolar I-mani
ZYPREXA 15mg IntraMuscular er indisert for behandling av akutt agitasjon assosiert med schizofreni og bipolar I-mani.
Effekt ble demonstrert i 3 korttids (24 timers IM-behandling) placebokontrollerte studier hos opprørte voksne inneliggende pasienter med: schizofreni eller bipolar lidelse I (maniske eller blandede episoder) [se Kliniske studier ].
"Psykomotorisk agitasjon" er definert i DSM-IV som "overdreven motorisk aktivitet assosiert med en følelse av indre spenning." Pasienter som opplever agitasjon viser ofte atferd som forstyrrer deres diagnose og omsorg, f.eks. truende atferd, eskalerende eller akutt plagsom atferd, eller selvutmattende atferd, noe som fører til at klinikere bruker intramuskulære antipsykotiske medisiner for å oppnå umiddelbar kontroll over agitasjonen.
ZYPREXA og fluoksetin i kombinasjon: Depressive episoder assosiert med bipolar I-lidelse
Oral ZYPREXA og fluoksetin i kombinasjon er indisert for behandling av depressive episoder assosiert med bipolar lidelse I, basert på kliniske studier. Når du bruker ZYPREXA 10 mg og fluoksetin i kombinasjon, se avsnittet om kliniske studier i pakningsvedlegget til Symbyax.
ZYPREXA monoterapi er ikke indisert for behandling av depressive episoder assosiert med bipolar I lidelse.
ZYPREXA og fluoksetin i kombinasjon: behandlingsresistent depresjon
Oral ZYPREXA og fluoksetin i kombinasjon er indisert for behandling av behandlingsresistent depresjon (alvorlig depressiv lidelse hos pasienter som ikke responderer på 2 separate studier av forskjellige antidepressiva med tilstrekkelig dose og varighet i den aktuelle episoden), basert på kliniske studier hos voksne pasienter . Når du bruker ZYPREXA og fluoksetin i kombinasjon, se avsnittet om kliniske studier i pakningsvedlegget til Symbyax.
ZYPREXA 5 mg monoterapi er ikke indisert for behandling av behandlingsresistent depresjon.
DOSERING OG ADMINISTRASJON
Schizofreni
Voksne
Dosevalg
Oralt olanzapin bør administreres en gang om dagen uten hensyn til måltider, vanligvis begynnende med 5 til 10 mg initialt, med en måldose på 10 mg/dag innen flere dager. Ytterligere dosejusteringer, hvis indisert, bør vanligvis skje med intervaller på ikke mindre enn 1 uke, siden steady state for olanzapin ikke vil oppnås før ca. 1 uke hos den typiske pasienten. Når dosejustering er nødvendig, anbefales doseøkninger/reduksjoner på 5 mg én gang daglig.
Effekt ved schizofreni ble vist i et doseområde på 10 til 15 mg/dag i kliniske studier. Doser over 10 mg/dag ble imidlertid ikke vist å være mer effektive enn dosen på 10 mg/dag. En økning til en dose høyere enn måldosen på 10 mg/dag (dvs. til en dose på 15 mg/dag eller mer) anbefales kun etter klinisk vurdering. Olanzapin er ikke indisert for bruk i doser over 20 mg/dag.
Dosering i spesielle populasjoner
Anbefalt startdose er 5 mg hos pasienter som er svekkede, som har en disposisjon for hypotensive reaksjoner, som ellers viser en kombinasjon av faktorer som kan resultere i langsommere metabolisme av olanzapin (f.eks. ikke-røykende kvinnelige pasienter ≥65 år), eller som kan være mer farmakodynamisk følsomme for olanzapin [se ADVARSLER OG FORHOLDSREGLER , NARKOTIKAHANDEL , og KLINISK FARMAKOLOGI ]. Når det er indisert, bør doseøkning utføres med forsiktighet hos disse pasientene.
Vedlikeholdsbehandling
Effektiviteten av oral olanzapin, 10 mg/dag til 20 mg/dag, for å opprettholde behandlingsrespons hos schizofrene pasienter som hadde vært stabile på ZYPREXA i ca. 8 uker og deretter ble fulgt for tilbakefall, er vist i en placebokontrollert studie [se Kliniske studier ]. Helsepersonell som velger å bruke ZYPREXA i lengre perioder bør med jevne mellomrom revurdere den langsiktige nytten av legemidlet for den enkelte pasient.
Ungdom
Dosevalg
Oralt olanzapin bør administreres på en gang-daglig plan uten hensyn til måltider med en anbefalt startdose på 2,5 eller 5 mg, med en måldose på 10 mg/dag. Effekt hos ungdom med schizofreni ble demonstrert basert på et fleksibelt doseområde på 2,5 til 20 mg/dag i kliniske studier, med en gjennomsnittlig modal dose på 12,5 mg/dag (gjennomsnittlig dose på 11,1 mg/dag). Når dosejustering er nødvendig, anbefales doseøkninger/reduksjoner på 2,5 eller 5 mg.
Sikkerheten og effektiviteten til doser over 20 mg/dag har ikke blitt evaluert i kliniske studier [se Kliniske studier ].
Vedlikeholdsbehandling
Effekten av ZYPREXA for vedlikeholdsbehandling av schizofreni i ungdomspopulasjonen har ikke blitt systematisk evaluert; vedlikeholdseffekt kan imidlertid ekstrapoleres fra voksne data sammen med sammenligninger av olanzapin farmakokinetiske parametere hos voksne og ungdom. Det anbefales derfor generelt at pasienter med respons fortsetter utover den akutte responsen, men med den laveste dosen som er nødvendig for å opprettholde remisjon. Pasienter bør med jevne mellomrom revurderes for å fastslå behovet for vedlikeholdsbehandling.
Bipolar I-lidelse (maniske eller blandede episoder)
Voksne
Dosevalg for monoterapi
Oralt olanzapin bør administreres en gang om dagen uten hensyn til måltider, vanligvis med 10 eller 15 mg. Dosejusteringer, hvis indisert, bør vanligvis skje med intervaller på ikke mindre enn 24 timer, noe som gjenspeiler prosedyrene i de placebokontrollerte studiene. Når dosejustering er nødvendig, anbefales doseøkninger/reduksjoner på 5 mg én gang daglig.
Kortsiktig (3-4 uker) antimanisk effekt ble vist i et doseområde på 5 mg til 20 mg/dag i kliniske studier. Sikkerheten til doser over 20 mg/dag har ikke blitt evaluert i kliniske studier [se Kliniske studier ].
Vedlikehold monoterapi
Fordelen med å opprettholde bipolare I-pasienter på monoterapi med oral ZYPREXA 10 mg i en dose på 5 til 20 mg/dag, etter å ha oppnådd en responderstatus i en gjennomsnittlig varighet på 2 uker, ble vist i en kontrollert studie [se Kliniske studier ]. Helsepersonell som velger å bruke ZYPREXA i lengre perioder bør med jevne mellomrom revurdere den langsiktige nytten av legemidlet for den enkelte pasient.
Dosevalg for tilleggsbehandling
Når det administreres som tilleggsbehandling til litium eller valproat, bør oral olanzapindosering vanligvis begynne med 10 mg én gang daglig uten hensyn til måltider.
Antimanisk effekt ble vist i et doseområde på 5 mg til 20 mg/dag i kliniske studier [se Kliniske studier ]. Sikkerheten til doser over 20 mg/dag har ikke blitt evaluert i kliniske studier.
Ungdom
Dosevalg
Oralt olanzapin bør administreres på en gang-daglig plan uten hensyn til måltider med en anbefalt startdose på 2,5 eller 5 mg, med en måldose på 10 mg/dag. Effekt hos ungdom med bipolar lidelse I (maniske eller blandede episoder) ble vist basert på et fleksibelt doseområde på 2,5 til 20 mg/dag i kliniske studier, med en gjennomsnittlig modal dose på 10,7 mg/dag (gjennomsnittlig dose på 8,9 mg/dag). ). Når dosejustering er nødvendig, anbefales doseøkninger/reduksjoner på 2,5 eller 5 mg.
Sikkerheten og effektiviteten til doser over 20 mg/dag har ikke blitt evaluert i kliniske studier [se Kliniske studier ].
Vedlikeholdsbehandling
Effekten av ZYPREXA 7,5 mg for vedlikeholdsbehandling av bipolar lidelse I hos ungdom er ikke evaluert; vedlikeholdseffekt kan imidlertid ekstrapoleres fra voksne data sammen med sammenligninger av olanzapin farmakokinetiske parametere hos voksne og ungdom. Det anbefales derfor generelt at pasienter med respons fortsetter utover den akutte responsen, men med den laveste dosen som er nødvendig for å opprettholde remisjon. Pasienter bør med jevne mellomrom revurderes for å fastslå behovet for vedlikeholdsbehandling.
Administrering av ZYPREXA ZYDIS (olanzapin oralt desintegrerende tabletter)
Etter å ha åpnet posen, fjern folien på blisterpakningen. Ikke skyv tabletten gjennom folien. Umiddelbart etter åpning av blisterpakningen, bruk tørre hender, fjern tabletten og legg hele ZYPREXA 15 mg ZYDIS i munnen. Tablettdesintegrasjon skjer raskt i spytt, slik at det lett kan svelges med eller uten væske.
ZYPREXA Intramuskulær: Agitasjon assosiert med schizofreni og bipolar I-mani
Dosevalg for agiterte voksne pasienter med schizofreni og bipolar I-mani
Effekten av intramuskulært olanzapin til injeksjon for å kontrollere agitasjon ved disse lidelsene ble vist i et doseområde på 2,5 mg til 10 mg. Anbefalt dose hos disse pasientene er 10 mg. En lavere dose på 5 eller 7,5 mg kan vurderes når kliniske faktorer tilsier det [se Kliniske studier ]. Hvis agitasjon som tilsier ytterligere intramuskulære doser vedvarer etter startdosen, kan påfølgende doser opp til 10 mg gis. Effekten av gjentatte doser av intramuskulært olanzapin til injeksjon hos opprørte pasienter har imidlertid ikke blitt systematisk evaluert i kontrollerte kliniske studier. Sikkerheten til totale daglige doser større enn 30 mg, eller 10 mg injeksjoner gitt oftere enn 2 timer etter den første dosen og 4 timer etter den andre dosen er heller ikke evaluert i kliniske studier. Maksimal dosering av intramuskulært olanzapin (f.eks. 3 doser på 10 mg administrert med 2-4 timers mellomrom) kan være assosiert med en betydelig forekomst av signifikant ortostatisk hypotensjon [se ADVARSLER OG FORHOLDSREGLER ]. Det anbefales derfor at pasienter som trenger påfølgende intramuskulære injeksjoner vurderes for ortostatisk hypotensjon før administrering av eventuelle påfølgende doser av intramuskulært olanzapin til injeksjon. Administrering av en tilleggsdose til en pasient med en klinisk signifikant postural endring i systolisk blodtrykk anbefales ikke.
Hvis pågående olanzapinbehandling er klinisk indisert, kan oral olanzapin initieres i et område på 5-20 mg/dag så snart det er klinisk hensiktsmessig [se Schizofreni og Bipolar I-lidelse (maniske eller blandede episoder) ].
Intramuskulær dosering i spesielle populasjoner
En dose på 5 mg/injeksjon bør vurderes for geriatriske pasienter eller når andre kliniske faktorer tilsier det. En lavere dose på 2,5 mg/injeksjon bør vurderes for pasienter som ellers kan være svekket, være disponert for hypotensive reaksjoner eller være mer farmakodynamisk følsomme overfor olanzapin [se ADVARSLER OG FORHOLDSREGLER , NARKOTIKAHANDEL , og KLINISK FARMAKOLOGI ].
Administrering av ZYPREXA intramuskulært
ZYPREXA Intra Muscular er kun beregnet for intramuskulær bruk. Ikke administrer intravenøst eller subkutant. Injiser sakte, dypt inn i muskelmassen. Parenterale legemidler bør inspiseres visuelt for partikler og misfarging før administrering, når oppløsning og beholder tillater det.
Instruksjoner for tilberedning av ZYPREXA 2,5 mg intramuskulært med sterilt vann til injeksjon
Løs opp innholdet i hetteglasset med 2,1 ml sterilt vann til injeksjon for å få en oppløsning som inneholder ca. 5 mg/ml olanzapin. Den resulterende løsningen skal virke klar og gul. ZYPREXA 7,5 mg intramuskulært rekonstituert med sterilt vann til injeksjon skal brukes umiddelbart (innen 1 time) etter rekonstituering. Kast ubrukt del.
Følgende tabell viser injeksjonsvolumer for tilførsel av ulike doser av intramuskulært olanzapin til injeksjon rekonstituert med sterilt vann til injeksjon.
Informasjon om fysisk inkompatibilitet
ZYPREXA 15mg IntraMuscular skal kun rekonstitueres med sterilt vann til injeksjonsvæsker. ZYPREXA 20mg IntraMuscular bør ikke kombineres i en sprøyte med diazepam-injeksjon fordi det oppstår utfelling når disse produktene blandes. Lorazepam-injeksjon skal ikke brukes til å rekonstituere ZYPREXA IntraMuscular da denne kombinasjonen resulterer i en forsinket rekonstitusjonstid. ZYPREXA IntraMuscular bør ikke kombineres i en sprøyte med haloperidolinjeksjon fordi den resulterende lave pH har vist seg å bryte ned olanzapin over tid.
ZYPREXA 20mg og fluoksetin i kombinasjon: depressive episoder assosiert med bipolar I-lidelse
Når du bruker ZYPREXA 7,5 mg og fluoksetin i kombinasjon, se også avsnittet om kliniske studier i pakningsvedlegget til Symbyax.
Voksne
Oralt olanzapin bør administreres i kombinasjon med fluoksetin én gang daglig om kvelden, uten hensyn til måltider, vanligvis med 5 mg oralt olanzapin og 20 mg fluoksetin. Dosejusteringer, hvis indisert, kan gjøres i henhold til effekt og tolerabilitet innenfor doseområder for oralt olanzapin 5 til 12,5 mg og fluoksetin 20 til 50 mg. Antidepressiv effekt ble vist med ZYPREXA 10 mg og fluoksetin i kombinasjon hos voksne pasienter med et doseområde på olanzapin 6 til 12 mg og fluoksetin 25 til 50 mg. Sikkerhet ved samtidig administrering av doser over 18 mg olanzapin med 75 mg fluoksetin har ikke blitt evaluert i kliniske studier.
Barn og ungdom (10-17 år)
Oralt olanzapin bør administreres i kombinasjon med fluoksetin én gang daglig om kvelden, uten hensyn til måltider, vanligvis med 2,5 mg oralt olanzapin og 20 mg fluoksetin. Dosejusteringer, hvis indisert, kan gjøres i henhold til effekt og tolerabilitet. Sikkerhet ved samtidig administrering av doser over 12 mg olanzapin med 50 mg fluoksetin har ikke blitt evaluert i pediatriske kliniske studier.
Sikkerhet og effekt av ZYPREXA og fluoksetin i kombinasjon ble bestemt i kliniske studier som støttet godkjenning av Symbyax (fastdosekombinasjon av ZYPREXA og fluoksetin). Symbyax doseres mellom 3 mg/25 mg (olanzapin/fluoksetin) per dag og 12 mg/50 mg (olanzapin/fluoksetin) per dag. Følgende tabell viser passende individuelle komponentdoser av ZYPREXA 10 mg og fluoksetin versus Symbyax. Dosejusteringer, hvis indisert, bør gjøres med de individuelle komponentene i henhold til effekt og toleranse.
Selv om det ikke finnes noen bevis for å svare på spørsmålet om hvor lenge en pasient behandlet med ZYPREXA og fluoksetin i kombinasjon bør forbli på det, er det generelt akseptert at bipolar I lidelse, inkludert depressive episoder assosiert med bipolar I lidelse, er en kronisk lidelse. sykdom som krever kronisk behandling. Helsepersonell bør med jevne mellomrom revurdere behovet for fortsatt farmakoterapi.
ZYPREXA 5 mg monoterapi er ikke indisert for behandling av depressive episoder assosiert med bipolar I lidelse.
ZYPREXA 7,5 mg og fluoksetin i kombinasjon: behandlingsresistent depresjon
Når du bruker ZYPREXA og fluoksetin i kombinasjon, se også avsnittet om kliniske studier i pakningsvedlegget til Symbyax.
Oralt olanzapin bør administreres i kombinasjon med fluoksetin én gang daglig om kvelden, uten hensyn til måltider, vanligvis med 5 mg oralt olanzapin og 20 mg fluoksetin. Dosejusteringer, hvis indisert, kan gjøres i henhold til effekt og tolerabilitet innenfor doseområder for oralt olanzapin 5 til 20 mg og fluoksetin 20 til 50 mg. Antidepressiv effekt ble vist med olanzapin og fluoksetin i kombinasjon hos voksne pasienter med et doseområde på olanzapin 6 til 18 mg og fluoksetin 25 til 50 mg.
Sikkerhet og effekt av olanzapin i kombinasjon med fluoksetin ble bestemt i kliniske studier som støttet godkjenning av Symbyax (kombinasjon med fast dose av olanzapin og fluoksetin). Symbyax doseres mellom 3 mg/25 mg (olanzapin/fluoksetin) per dag og 12 mg/50 mg (olanzapin/fluoksetin) per dag. Tabell 1 ovenfor viser passende individuelle komponentdoser av ZYPREXA og fluoksetin versus Symbyax. Dosejusteringer, hvis indisert, bør gjøres med de individuelle komponentene i henhold til effekt og toleranse.
Selv om det ikke finnes noen bevis for å svare på spørsmålet om hvor lenge en pasient behandlet med ZYPREXA og fluoksetin i kombinasjon bør forbli på det, er det generelt akseptert at behandlingsresistent depresjon (større depressiv lidelse hos voksne pasienter som ikke reagerer på 2 separate forsøk med forskjellige antidepressiva med tilstrekkelig dose og varighet i den aktuelle episoden) er en kronisk sykdom som krever kronisk behandling. Helsepersonell bør med jevne mellomrom revurdere behovet for fortsatt farmakoterapi.
Sikkerhet ved samtidig administrering av doser over 18 mg olanzapin med 75 mg fluoksetin har ikke blitt evaluert i kliniske studier.
ZYPREXA 7,5 mg monoterapi er ikke indisert for behandling av behandlingsresistent depresjon (alvorlig depressiv lidelse hos pasienter som ikke responderer på 2 antidepressiva med tilstrekkelig dose og varighet i den aktuelle episoden).
ZYPREXA 10mg og fluoksetin i kombinasjon: Dosering i spesielle populasjoner
Startdosen av oral olanzapin 2,5-5 mg med fluoksetin 20 mg bør brukes til pasienter med disposisjon for hypotensive reaksjoner, pasienter med nedsatt leverfunksjon, eller pasienter som viser en kombinasjon av faktorer som kan bremse metabolismen av olanzapin eller fluoksetin i kombinasjon (kvinnelig kjønn, geriatrisk alder, ikke-røykerstatus), eller de pasientene som kan være farmakodynamisk følsomme for olanzapin. Dosejustering kan være nødvendig hos pasienter som viser en kombinasjon av faktorer som kan redusere metabolismen. Når det er indisert, bør doseøkning utføres med forsiktighet hos disse pasientene. ZYPREXA og fluoksetin i kombinasjon har ikke blitt systematisk studert hos pasienter over 65 år eller hos pasienter under 10 år [se ADVARSLER OG FORHOLDSREGLER , NARKOTIKAHANDEL , og KLINISK FARMAKOLOGI ].
HVORDAN LEVERES
Doseringsformer og styrker
ZYPREXA 2,5 mg, 5 mg, 7,5 mg og 10 mg tabletter er hvite, runde og merket med blått blekk med LILLY og tablettnummer. 15 mg tablettene er elliptiske, blå og preget med LILLY og tablettnummer. 20 mg tablettene er elliptiske, rosa og preget med LILLY og tablettnummer. Tabletter blir ikke skåret. Nettbrettene er tilgjengelige som følger:
ZYPREXA 10mg ZYDIS (olanzapin oralt desintegrerende tabletter) er gule, runde og preget med tablettstyrken. Tabletter blir ikke skåret. Nettbrettene er tilgjengelige som følger:
ZYPREXA 15 mg intramuskulært er tilgjengelig i 10 mg hetteglass (1s).
ZYPREXA 2,5 mg, 5 mg, 7,5 mg og 10 mg tabletter er hvite, runde og merket med blått blekk med LILLY og tablettnummer. 15 mg tablettene er elliptiske, blå og preget med LILLY og tablettnummer. 20 mg tablettene er elliptiske, rosa og preget med LILLY og tablettnummer. Nettbrettene er tilgjengelige som følger:
ZYPREXA 2,5 mg ZYDIS (olanzapin oralt desintegrerende tabletter) er gule, runde og preget med tablettstyrken. Nettbrettene er tilgjengelige som følger:
ZYPREXA Intramuskulær er tilgjengelig i:
NDC 0002-7597-01 (nr. VL7597) – 10 mg hetteglass (1s)
Oppbevaring og håndtering
Oppbevar ZYPREXA tabletter, ZYPREXA ZYDIS og ZYPREXA intramuskulære hetteglass (før rekonstituering) ved kontrollert romtemperatur, 20° til 25°C (68° til 77°F) [se USP ]. Rekonstituert ZYPREXA 20mg IntraMuscular kan oppbevares ved kontrollert romtemperatur, 20° til 25°C (68° til 77°F) [se USP i opptil 1 time om nødvendig. Kast ubrukt del av rekonstituert ZYPREXA IntraMuscular. USP definerer kontrollert romtemperatur som en temperatur som opprettholdes termostatisk og som omfatter det vanlige og vanlige arbeidsmiljøet på 20° til 25°C (68° til 77°F); som resulterer i en gjennomsnittlig kinetisk temperatur beregnet til ikke å være mer enn 25°C; og som gir mulighet for utflukter mellom 15° og 30°C (59° og 86°F) som oppleves på apotek, sykehus og varehus.
Beskytt ZYPREXA-tabletter og ZYPREXA ZYDIS mot lys og fuktighet. Beskytt ZYPREXA IntraMuscular mot lys, ikke frys.
Markedsført av: Lilly USA, LLC, Indianapolis, IN 46285, USA. Revidert: oktober 2019
BIVIRKNINGER
Når du bruker ZYPREXA 2,5 mg og fluoksetin i kombinasjon, se også avsnittet Bivirkninger i pakningsvedlegget til Symbyax.
Erfaring fra kliniske forsøk
Fordi kliniske studier utføres under vidt forskjellige forhold, kan bivirkningsrater observert i kliniske studier av et medikament ikke sammenlignes direkte med rater i kliniske studier av et annet legemiddel, og kan ikke gjenspeile eller forutsi hyppighetene observert i praksis.
Kliniske studier hos voksne
Informasjonen nedenfor for olanzapin er hentet fra en klinisk studiedatabase for olanzapin bestående av 10 504 voksne pasienter med ca. 4765 pasientår med eksponering for olanzapin pluss 722 pasienter med eksponering for intramuskulært olanzapin til injeksjon. Denne databasen inkluderer: (1) 2500 pasienter som deltok i multidose orale olanzapin førmarkedsføringsstudier i schizofreni og Alzheimers sykdom, som representerer omtrent 1122 pasientår med eksponering per 14. februar 1995; (2) 182 pasienter som deltok i oral olanzapin premarketing bipolar I-lidelse (maniske eller blandede episoder) studier som representerte omtrent 66 pasientår med eksponering; (3) 191 pasienter som deltok i en oral olanzapin-studie av pasienter med ulike psykiatriske symptomer i forbindelse med Alzheimers sykdom, som representerte omtrent 29 pasientår med eksponering; (4) 5788 ekstra pasienter fra 88 orale olanzapin kliniske studier per 31. desember 2001; (5) 1843 ytterligere pasienter fra 41 olanzapin kliniske studier per 31. oktober 2011; og (6) 722 pasienter som deltok i intramuskulære olanzapin til injeksjonsstudier før markedsføring hos opprørte pasienter med schizofreni, bipolar I-lidelse (maniske eller blandede episoder) eller demens. Også inkludert nedenfor er informasjon fra den 6-ukers kliniske studiedatabasen for olanzapin i kombinasjon med litium eller valproat før markedsføring, bestående av 224 pasienter som deltok i studier med bipolar I lidelse (maniske eller blandede episoder) med ca. 22 pasientårs eksponering.
Betingelsene og varigheten av behandlingen med olanzapin varierte sterkt og inkluderte (i overlappende kategorier) åpne og dobbeltblinde faser av studier, innlagte og polikliniske pasienter, fastdose- og dosetitreringsstudier, og korttids- eller langtidseksponering . Bivirkninger ble vurdert ved å samle inn bivirkninger, resultater av fysiske undersøkelser, vitale tegn, vekter, laboratorieanalytter, EKG, røntgen av thorax og resultater fra oftalmologiske undersøkelser.
Enkelte deler av diskusjonen nedenfor knyttet til objektive eller numeriske sikkerhetsparametere, nemlig doseavhengige bivirkninger, endringer i vitale tegn, vektøkning, laboratorieendringer og EKG-endringer er avledet fra studier på pasienter med schizofreni og har ikke blitt duplisert for bipolar I-lidelse (maniske eller blandede episoder) eller agitasjon. Imidlertid gjelder denne informasjonen også generelt for bipolar lidelse I (maniske eller blandede episoder) og agitasjon.
Bivirkninger under eksponering ble oppnådd ved spontanrapport og registrert av kliniske etterforskere ved bruk av terminologi etter eget valg. Det er følgelig ikke mulig å gi et meningsfullt estimat av andelen individer som opplever bivirkninger uten først å gruppere lignende typer reaksjoner i et mindre antall standardiserte reaksjonskategorier. I tabellene og tabellene som følger, har MedDRA og COSTART Dictionary terminologi blitt brukt for å klassifisere rapporterte bivirkninger.
De oppgitte bivirkningsfrekvensene representerer andelen individer som minst én gang opplevde en behandlingsutløst bivirkning av den oppførte typen. En reaksjon ble ansett som behandlingsoppstått hvis den oppstod for første gang eller forverret seg under behandling etter baseline-evaluering. De rapporterte reaksjonene inkluderer ikke de reaksjonsbegrepene som var så generelle at de var uinformative. Reaksjoner oppført andre steder i merkingen kan ikke gjentas nedenfor. Det er viktig å understreke at selv om reaksjonene oppsto under behandling med olanzapin, var de ikke nødvendigvis forårsaket av det. Hele etiketten bør leses for å få en fullstendig forståelse av sikkerhetsprofilen til olanzapin.
Forskriveren bør være oppmerksom på at tallene i tabeller og tabeller ikke kan brukes til å forutsi forekomst av bivirkninger i løpet av vanlig medisinsk praksis der pasientkarakteristikker og andre faktorer avviker fra de som var fremherskende i de kliniske forsøkene. Tilsvarende kan de siterte frekvensene ikke sammenlignes med tall hentet fra andre kliniske undersøkelser som involverer ulike behandlinger, bruksområder og etterforskere. De siterte tallene gir imidlertid den forskrivende helsepersonell et visst grunnlag for å estimere det relative bidraget til medikamentelle og ikke-medikamentelle faktorer til forekomsten av bivirkninger i den populasjonen som ble studert.
Forekomst av uønskede reaksjoner i kortsiktige, placebokontrollerte og kombinasjonsforsøk
Følgende funn er basert på forhåndsmarkedsføringsstudier av (1) oral olanzapin for schizofreni, bipolar lidelse I (maniske eller blandede episoder), en påfølgende studie med pasienter som har ulike psykiatriske symptomer i forbindelse med Alzheimers sykdom, og kombinasjonsstudier før markedsføring, og (2 ) intramuskulært olanzapin til injeksjon hos agiterte pasienter med schizofreni eller bipolar I-mani.
Bivirkninger forbundet med seponering av behandling i kortsiktige, placebokontrollerte studier
Schizofreni
Totalt sett var det ingen forskjell i forekomsten av seponering på grunn av bivirkninger (5 % for oralt olanzapin vs 6 % for placebo). Seponering på grunn av økning i ALAT ble imidlertid ansett for å være medikamentrelatert (2 % for oralt olanzapin vs 0 % for placebo).
Bipolar I-lidelse (maniske eller blandede episoder) Monoterapi
Totalt sett var det ingen forskjell i forekomsten av seponering på grunn av bivirkninger (2 % for oralt olanzapin vs 2 % for placebo).
Opphisselse
Totalt sett var det ingen forskjell i forekomsten av seponering på grunn av bivirkninger (0,4 % for intramuskulært olanzapin til injeksjon vs 0 % for placebo).
Bivirkninger forbundet med seponering av behandling i kortsiktige kombinasjonsforsøk
Bipolar I-lidelse (maniske eller blandede episoder), olanzapin som tillegg til litium eller valproat
I en studie av pasienter som allerede tolererte enten litium eller valproat som monoterapi, var seponeringsfrekvensen på grunn av bivirkninger 11 % for kombinasjonen av oral olanzapin med litium eller valproat sammenlignet med 2 % for pasienter som fortsatt fikk litium- eller valproat monoterapi. Seponeringer med kombinasjonen av oral olanzapin og litium eller valproat som forekom hos mer enn 1 pasient var: somnolens (3 %), vektøkning (1 %) og perifert ødem (1 %).
Vanlige observerte bivirkninger i kortsiktige, placebokontrollerte forsøk
De vanligst observerte bivirkningene assosiert med bruk av oral olanzapin (forekomst på 5 % eller mer) og som ikke ble observert ved en tilsvarende forekomst blant placebo-behandlede pasienter (olanzapin forekomst minst dobbelt så stor som for placebo) var:
Olanzapin intramuskulært
Det ble observert 1 bivirkning (somnolens) med en forekomst på 5 % eller mer blant intramuskulært olanzapin for injeksjonsbehandlede pasienter og ikke observert ved en tilsvarende forekomst blant placebo-behandlede pasienter (olanzapin forekomst minst dobbelt så stor som for placebo) under placebo -kontrollerte studier før markedsføring. Forekomsten av somnolens i løpet av den 24 timers IM-behandlingsperioden i kliniske studier hos agiterte pasienter med schizofreni eller bipolar I-mani var 6 % for intramuskulært olanzapin til injeksjon og 3 % for placebo.
Bivirkninger som oppstår med en forekomst på 2 % eller mer blant orale olanzapin-behandlede pasienter i kortsiktige, placebokontrollerte studier
Tabell 11 oppregner forekomsten, avrundet til nærmeste prosent, av behandlingsutløste bivirkninger som oppsto hos 2 % eller flere av pasientene behandlet med oral olanzapin (doser ≥2,5 mg/dag) og med høyere forekomst enn placebo som deltok i den akutte fase av placebokontrollerte studier.
Doseavhengighet av bivirkninger
En dosegruppeforskjell er observert for tretthet, svimmelhet, vektøkning og prolaktinøkning. I en enkelt 8-ukers randomisert, dobbeltblind, fastdosestudie som sammenlignet 10 (N=199), 20 (N=200) og 40 (N=200) mg/dag oral olanzapin hos voksne pasienter med schizofreni eller schizoaffektiv lidelse, forekomst av tretthet (10 mg/dag: 1,5 %; 20 mg/dag: 2,1 %; 40 mg/dag: 6,6 %) ble observert med signifikante forskjeller mellom 10 vs 40 og 20 vs 40 mg/dag. Forekomsten av svimmelhet (10 mg/dag: 2,6 %; 20 mg/dag: 1,6 %; 40 mg/dag: 6,6 %) ble observert med signifikante forskjeller mellom 20 og 40 mg. Dosegruppeforskjeller ble også notert for vektøkning og prolaktinøkning [se ADVARSLER OG FORHOLDSREGLER ].
Følgende tabell tar for seg doserelaterthet for andre bivirkninger ved bruk av data fra en schizofrenistudie som involverer faste doseområder for oralt olanzapin. Den teller prosentandelen av pasienter med behandlingsutløste bivirkninger for de tre fastdosegruppene og placebo. Dataene ble analysert ved hjelp av Cochran-Armitage-testen, ekskludert placebogruppen, og tabellen inkluderer bare de bivirkningene det var en trend for.
Vanlige observerte bivirkninger i korttidsforsøk med oralt olanzapin som tillegg til litium eller valproat
I bipolar I lidelse (maniske eller blandede episoder) tilleggs placebokontrollerte studier, var de vanligst observerte bivirkningene assosiert med kombinasjonen av olanzapin og litium eller valproat (insidens på ≥5 % og minst to ganger placebo):
Bivirkninger som oppstår med en forekomst på 2 % eller mer blant orale olanzapin-behandlede pasienter i korttidsforsøk med olanzapin som tillegg til litium eller valproat
Tabell 14 oppregner forekomsten, avrundet til nærmeste prosent, av behandlingsutløste bivirkninger som oppsto hos 2 % eller flere av pasientene behandlet med kombinasjonen av olanzapin (doser ≥5 mg/dag) og litium eller valproat og med forekomst større enn litium eller valproat alene som deltok i den akutte fasen av placebokontrollerte kombinasjonsforsøk.
For spesifikk informasjon om bivirkningene observert med litium eller valproat, se avsnittet Bivirkninger i pakningsvedlegget for disse andre produktene.
Bivirkninger som oppstår med en forekomst på 1 % eller mer blant intramuskulært olanzapin for injeksjonsbehandlede pasienter i kortsiktige, placebokontrollerte studier
Tabell 15 oppregner forekomsten, avrundet til nærmeste prosent, av behandlingsutløste bivirkninger som oppsto hos 1 % eller flere av pasientene behandlet med intramuskulært olanzapin til injeksjon (doseområde på 2,5-10 mg/injeksjon) og med høyere forekomst enn placebo som deltok i de kortsiktige, placebokontrollerte studiene med agiterte pasienter med schizofreni eller bipolar I-mani.
Ekstrapyramidale symptomer
Følgende tabell oppregner prosentandelen av pasienter med behandlingsfremkomne ekstrapyramidale symptomer vurdert ved kategoriske analyser av formelle vurderingsskalaer under akuttbehandling i en kontrollert klinisk studie som sammenligner oral olanzapin ved 3 faste doser med placebo i behandling av schizofreni i løpet av en 6-ukers prøve.
Følgende tabell oppregner prosentandelen av pasienter med behandlingsfremkomne ekstrapyramidale symptomer vurdert ved spontant rapporterte bivirkninger under akuttbehandling i den samme kontrollerte kliniske studien som sammenlignet olanzapin ved 3 faste doser med placebo i behandlingen av schizofreni i en 6-ukers studie.
Følgende tabell oppregner prosentandelen av ungdomspasienter med behandlingsfremkommende ekstrapyramidale symptomer, vurdert av spontant rapporterte bivirkninger under akuttbehandling (doseområde: 2,5 til 20 mg/dag).
Følgende tabell oppregner prosentandelen av pasienter med behandlingsfremkommende ekstrapyramidale symptomer, vurdert ved kategoriske analyser av formelle vurderingsskalaer under kontrollerte kliniske studier som sammenligner faste doser av intramuskulært olanzapin til injeksjon med placebo i agitasjon. Pasienter i hver dosegruppe kunne få opptil 3 injeksjoner under forsøkene [se Kliniske studier ]. Pasientvurderinger ble utført i løpet av 24 timer etter den initiale dosen av intramuskulært olanzapin til injeksjon.
Følgende tabell oppregner prosentandelen av pasienter med ekstrapyramidale symptomer som oppstår ved behandling, vurdert av spontant rapporterte bivirkninger i den samme kontrollerte kliniske studien som sammenligner faste doser av intramuskulært olanzapin til injeksjon med placebo hos opprørte pasienter med schizofreni.
Dystoni, klasseeffekt
Symptomer på dystoni, langvarige unormale sammentrekninger av muskelgrupper, kan forekomme hos følsomme individer i løpet av de første dagene av behandlingen. Dystoniske symptomer inkluderer: spasmer i nakkemusklene, noen ganger utvikler seg til tetthet i halsen, svelgevansker, pustevansker og/eller tungefremspring. Selv om disse symptomene kan oppstå ved lave doser, er frekvensen og alvorlighetsgraden større med høy styrke og ved høyere doser av førstegenerasjons antipsykotiske legemidler. Generelt kan en økt risiko for akutt dystoni observeres hos menn og yngre aldersgrupper som får antipsykotika; Imidlertid har hendelser med dystoni blitt rapportert sjelden (
Andre uønskede reaksjoner
Andre uønskede reaksjoner observert under den kliniske studieevalueringen av oralt olanzapin
Følgende er en liste over behandlingsutløste bivirkninger rapportert av pasienter behandlet med oralt olanzapin (ved flere doser ≥1 mg/dag) i kliniske studier. Denne oppføringen er ikke ment å inkludere reaksjoner (1) som allerede er oppført i tidligere tabeller eller andre steder i merking, (2) der en medikamentårsak var fjern, (3) som var så generelle at de var uinformative, (4) som ikke var anses å ha signifikante kliniske implikasjoner, eller (5) som skjedde med en hastighet lik eller mindre enn placebo. Reaksjoner er klassifisert etter kroppssystem ved å bruke følgende definisjoner: hyppige bivirkninger er de som forekommer hos minst 1/100 pasienter; sjeldne bivirkninger er de som forekommer hos 1/100 til 1/1000 pasienter; sjeldne reaksjoner er de som forekommer hos færre enn 1/1000 pasienter.
Kroppen som en helhet - Sjeldne: frysninger, ansiktsødem, lysfølsomhetsreaksjon, selvmordsforsøk1; Sjeldne: frysninger og feber, bakruseffekt, plutselig død1.
Sirkulasjonssystem - Sjelden: cerebrovaskulær ulykke, vasodilatasjon.
Fordøyelsessystemet - Sjeldne: abdominal distensjon, kvalme og oppkast, tungeødem; Sjeldne: ileus, intestinal obstruksjon, fettavleiring i leveren.
Hemisk og lymfesystem - Sjelden: trombocytopeni.
Metabolske og ernæringsforstyrrelser - Hyppig: øket alkalisk fosfatase; Sjeldne: bilirubinemi, hypoproteinemi.
Muskel- og skjelettsystemet - Sjelden: osteoporose.
nervesystemet - Sjeldne: ataksi, dysartri, redusert libido, stupor; Sjelden: koma.
Luftveiene - Sjelden: neseblødning; Sjelden: lungeødem.
Hud og vedheng - Sjelden: alopecia.
Spesielle sanser - Sjeldne: unormal akkommodasjon, tørre øyne; Sjelden: mydriasis.
Urogenital system - Sjeldne: amenoré2, brystsmerter, redusert menstruasjon, impotens2, økt menstruasjon2, menorragi2, metrorragi2, polyuri2, urinfrekvens, urinretensjon, urintrang, nedsatt vannlating.
1 Disse begrepene representerer alvorlige bivirkninger, men oppfyller ikke definisjonen for bivirkninger. De er inkludert her på grunn av deres seriøsitet. 2 Justert for kjønn.
Andre bivirkninger observert under den kliniske studieevalueringen av intramuskulært olanzapin til injeksjon
Følgende er en liste over behandlingsutløste bivirkninger rapportert av pasienter behandlet med intramuskulært olanzapin til injeksjon (ved 1 eller flere doser ≥2,5 mg/injeksjon) i kliniske studier. Denne oppføringen er ikke ment å inkludere reaksjoner (1) som allerede er oppført i tidligere tabeller eller andre steder i merking, (2) der en medikamentårsak var fjern, (3) som var så generelle at de var uinformative, (4) som ikke var anses å ha signifikante kliniske implikasjoner, eller (5) som skjedde med en hastighet lik eller mindre enn placebo. Reaksjoner er klassifisert etter kroppssystem ved å bruke følgende definisjoner: hyppige bivirkninger er de som forekommer hos minst 1/100 pasienter; sjeldne bivirkninger er de som forekommer hos 1/100 til 1/1000 pasienter.
Kroppen som en helhet - Hyppig: smerte på injeksjonsstedet.
Sirkulasjonssystem - Sjelden: synkope.
Fordøyelsessystemet - Sjelden: kvalme.
Metabolske og ernæringsforstyrrelser - Sjelden: økt kreatinfosfokinase.
Kliniske studier hos ungdomspasienter (alder 13 til 17 år)
Vanlige observerte bivirkninger i orale olanzapin kortsiktige, placebokontrollerte studier
Bivirkninger hos ungdomspasienter behandlet med oral olanzapin (doser ≥2,5 mg) rapportert med en insidens på 5 % eller mer og rapportert minst dobbelt så hyppig som placebo-behandlede pasienter er oppført i tabell 21.
Bivirkninger som oppstår med en forekomst på 2 % eller mer blant orale olanzapin-behandlede pasienter i korttids (3-6 uker), placebokontrollerte studier
Bivirkninger hos ungdomspasienter behandlet med oral olanzapin (doser ≥2,5 mg) rapportert med en forekomst på 2 % eller mer og høyere enn placebo er oppført i tabell 22.
Vitale tegn og laboratoriestudier
Endringer av vitale tegn
Oral olanzapin var assosiert med ortostatisk hypotensjon og takykardi i kliniske studier. Intramuskulært olanzapin til injeksjon var assosiert med bradykardi, hypotensjon og takykardi i kliniske studier [se ADVARSLER OG FORHOLDSREGLER ].
Laboratorieendringer
Olanzapin monoterapi hos voksne
En vurdering av erfaringen før markedsføring av olanzapin viste en sammenheng med asymptomatiske økninger i ALAT, ASAT og GGT. Innenfor den opprinnelige premarketingdatabasen med ca. 2400 voksne pasienter med baseline ALAT ≤90 IE/l, var forekomsten av ALAT-økninger til >200 IE/l 2 % (50/2381). Ingen av disse pasientene opplevde gulsott eller andre symptomer som kan tilskrives nedsatt leverfunksjon, og de fleste hadde forbigående forandringer som hadde en tendens til å normalisere seg mens behandlingen med olanzapin fortsatte.
placebokontrollerte monoterapistudier med olanzapin hos voksne ble det observert klinisk signifikante ALAT-økninger (endring fra
Fra en analyse av laboratoriedata i en integrert database med 41 fullførte kliniske studier på voksne pasienter behandlet med oralt olanzapin, ble høye GGT-nivåer registrert hos ≥1 % (88/5245) av pasientene.
Forsiktighet bør utvises hos pasienter med tegn og symptomer på nedsatt leverfunksjon, hos pasienter med eksisterende tilstander assosiert med begrenset leverfunksjonsreserve, og hos pasienter som behandles med potensielt hepatotoksiske legemidler.
Administrering av olanzapin var også assosiert med økninger i serumprolaktin [se ADVARSLER OG FORHOLDSREGLER ], med en asymptomatisk økning av eosinofiltallet hos 0,3 % av pasientene, og med en økning i CPK.
Fra en analyse av laboratoriedata i en integrert database med 41 fullførte kliniske studier på voksne pasienter behandlet med oral olanzapin, ble forhøyet urinsyre registrert hos ≥3 % (171/4641) av pasientene.
Olanzapin monoterapi hos ungdom
placebokontrollerte kliniske studier av ungdomspasienter med schizofreni eller bipolar lidelse I (maniske eller blandede episoder), ble det observert høyere frekvenser for følgende behandlingsoppståtte funn, når som helst, i laboratorieanalytter sammenlignet med placebo: forhøyet ALAT (≥3X ULN) hos pasienter med ALAT ved baseline
placebokontrollerte monoterapistudier med olanzapin hos ungdom, ble klinisk signifikante ALAT-økninger (endring fra
EKG-endringer
sammenslåtte studier av voksne så vel som sammenslåtte studier av ungdom, var det ingen signifikante forskjeller mellom olanzapin og placebo i andelen pasienter som opplever potensielt viktige endringer i EKG-parametre, inkludert QT, QTc (Fridericia korrigert) og PR-intervaller. Olanzapinbruk var assosiert med en gjennomsnittlig økning i hjertefrekvens sammenlignet med placebo (voksne: +2,4 slag per minutt vs ingen endring med placebo; ungdom: +6,3 slag per minutt vs -5,1 slag per minutt med placebo). Denne økningen i hjertefrekvens kan være relatert til olanzapins potensial for å indusere ortostatiske endringer [se ADVARSLER OG FORHOLDSREGLER ].
Postmarketing-erfaring
Følgende bivirkninger er identifisert under bruk av ZYPREXA etter godkjenning. Fordi disse reaksjonene rapporteres frivillig fra en populasjon av usikker størrelse, er det vanskelig å pålitelig estimere frekvensen eller vurdere en årsakssammenheng med legemiddeleksponering.
Bivirkninger rapportert siden markedsintroduksjonen som var tidsmessig (men ikke nødvendigvis kausalt) relatert til ZYPREXA-behandling inkluderer følgende: allergisk reaksjon (f.eks. anafylaktoid reaksjon, angioødem, kløe eller urticaria), kolestatisk eller blandet leverskade, diabetisk koma, diabetisk ketoacidose, seponeringsreaksjon (diaforese, kvalme eller oppkast), legemiddelreaksjon med eosinofili og systemiske symptomer (DRESS), hepatitt, gulsott, nøytropeni, pankreatitt, priapisme, utslett, rastløse ben-syndrom, rabdomyolyse, stamming1 og venøse tromboemboliske hendelser (lungeemboliske hendelser) dyp venøs trombose). Tilfeldige kolesterolnivåer på ≥240 mg/dL og tilfeldige triglyseridnivåer på ≥1000 mg/dL er rapportert.
1 Stamming ble kun studert i orale og langtidsvirkende injeksjonsformuleringer (LAI).
NARKOTIKAHANDEL
Risikoen ved bruk av olanzapin i kombinasjon med andre legemidler har ikke blitt grundig evaluert i systematiske studier.
Potensial for andre legemidler å påvirke olanzapin
Diazepam
Samtidig administrering av diazepam og olanzapin forsterket den ortostatiske hypotensjonen observert med olanzapin.
Cimetidin og antacida
Enkeltdoser av cimetidin (800 mg) eller antacida som inneholder aluminium og magnesium påvirket ikke den orale biotilgjengeligheten av olanzapin.
Induktorer av CYP1A2
Karbamazepinbehandling (200 mg to ganger daglig) forårsaker en ca. 50 % økning i clearance av olanzapin. Denne økningen skyldes sannsynligvis det faktum at karbamazepin er en potent induser av CYP1A2-aktivitet. Høyere daglige doser av karbamazepin kan føre til en enda større økning i olanzapinclearance.
Alkohol
Etanol (45 mg/70 kg enkeltdose) hadde ingen effekt på olanzapins farmakokinetikk. Samtidig administrering av alkohol (dvs. etanol) med olanzapin forsterket den ortostatiske hypotensjonen observert med olanzapin [se NARKOTIKAHANDEL ].
Hemmere av CYP1A2
Fluvoxamin
Fluvoxamin, en CYP1A2-hemmer, reduserer clearance av olanzapin. Dette resulterer i en gjennomsnittlig økning i olanzapin Cmax etter fluvoksamin på 54 % hos kvinnelige ikke-røykere og 77 % hos mannlige røykere. Gjennomsnittlig økning i olanzapin AUC er henholdsvis 52 % og 108 %. Lavere doser av olanzapin bør vurderes hos pasienter som får samtidig behandling med fluvoksamin.
Hemmere av CYP2D6
Fluoksetin
Fluoksetin (60 mg enkeltdose eller 60 mg daglig dose i 8 dager) forårsaker en liten (gjennomsnittlig 16 %) økning i maksimal konsentrasjon av olanzapin og en liten (gjennomsnittlig 16 %) reduksjon i olanzapinclearance. Størrelsen på virkningen av denne faktoren er liten sammenlignet med den generelle variasjonen mellom individer, og doseendring anbefales derfor ikke rutinemessig. Når du bruker ZYPREXA og fluoksetin i kombinasjon, se også avsnittet om legemiddelinteraksjoner i pakningsvedlegget til Symbyax.
Warfarin
Warfarin (20 mg enkeltdose) påvirket ikke olanzapins farmakokinetikk.
Induktorer av CYP1A2 eller glukuronyltransferase
Omeprazol og rifampin kan forårsake en økning i olanzapinclearance.
Kull
Administrering av aktivt kull (1 g) reduserte Cmax og AUC for oralt olanzapin med ca. 60 %. Siden toppnivåer av olanzapin vanligvis ikke oppnås før ca. 6 timer etter dosering, kan kull være en nyttig behandling for overdosering av olanzapin.
Potensial for Olanzapin til å påvirke andre legemidler
CNS-virkende legemidler
Gitt de primære CNS-effektene av olanzapin, bør det utvises forsiktighet når olanzapin tas i kombinasjon med andre sentralt virkende legemidler og alkohol.
Antihypertensive midler
På grunn av potensialet for å indusere hypotensjon, kan olanzapin forsterke effekten av visse antihypertensiva.
Levodopa og dopaminagonister
Olanzapin kan motvirke effekten av levodopa og dopaminagonister.
Lorazepam (IM)
Administrering av intramuskulært lorazepam (2 mg) 1 time etter intramuskulært olanzapin til injeksjon (5 mg) påvirket ikke farmakokinetikken til olanzapin, ukonjugert lorazepam eller total lorazepam signifikant. Denne samtidige administreringen av intramuskulært lorazepam og intramuskulært olanzapin til injeksjon bidro imidlertid til søvnighet observert med begge legemidlene alene [se ADVARSLER OG FORHOLDSREGLER ].
Litium
Flere doser av olanzapin (10 mg i 8 dager) påvirket ikke kinetikken til litium. Derfor krever samtidig administrering av olanzapin ikke dosejustering av litium [se ADVARSLER OG FORHOLDSREGLER ].
Valproat
Olanzapin (10 mg daglig i 2 uker) påvirket ikke steady state plasmakonsentrasjonene av valproat. Derfor krever samtidig administrering av olanzapin ikke dosejustering av valproat [se ADVARSLER OG FORHOLDSREGLER ].
Effekt av olanzapin på legemiddelmetaboliserende enzymer
In vitro-studier med humane levermikrosomer tyder på at olanzapin har lite potensial til å hemme CYP1A2, CYP2C9, CYP2C19, CYP2D6 og CYP3A. Det er derfor lite sannsynlig at olanzapin forårsaker klinisk viktige legemiddelinteraksjoner mediert av disse enzymene.
Imipramin
Enkeltdoser av olanzapin påvirket ikke farmakokinetikken til imipramin eller dets aktive metabolitt desipramin.
Warfarin
Enkeltdoser av olanzapin påvirket ikke farmakokinetikken til warfarin.
Diazepam
Olanzapin påvirket ikke farmakokinetikken til diazepam eller dets aktive metabolitt Ndesmethyldiazepam. Imidlertid økte diazepam administrert sammen med olanzapin den ortostatiske hypotensjonen observert med begge legemidlene gitt alene.
Alkohol
Flere doser olanzapin påvirket ikke kinetikken til etanol.
Biperiden
Flere doser olanzapin påvirket ikke kinetikken til biperiden.
Teofyllin
Flere doser av olanzapin påvirket ikke farmakokinetikken til teofyllin eller dets metabolitter.
Narkotikamisbruk og avhengighet
Avhengighet
studier prospektivt designet for å vurdere misbruk og avhengighetspotensial, ble olanzapin vist å ha akutte depressive CNS-effekter, men lite eller ingen potensiale for misbruk eller fysisk avhengighet hos rotter som fikk orale doser opptil 15 ganger daglig oral MRHD (20 mg) og rhesus-aper administrerte orale doser opptil 8 ganger den daglige orale MRHD basert på mg/m² kroppsoverflate.
Olanzapin har ikke blitt systematisk studert hos mennesker for potensialet for misbruk, toleranse eller fysisk avhengighet. Selv om de kliniske studiene ikke avdekket noen tendens til legemiddelsøkende atferd, var disse observasjonene ikke systematiske, og det er ikke mulig å forutsi på grunnlag av denne begrensede erfaringen i hvilken grad et CNS-aktivt legemiddel vil bli misbrukt, avledet , og/eller misbrukt en gang markedsført. Følgelig bør pasienter evalueres nøye for en historie med narkotikamisbruk, og slike pasienter bør observeres nøye for tegn på misbruk eller misbruk av olanzapin (f.eks. utvikling av toleranse, økning i dose, legemiddelsøkende atferd).
ADVARSLER
Inkludert som en del av FORHOLDSREGLER seksjon.
FORHOLDSREGLER
Når du bruker ZYPREXA 7,5 mg og fluoksetin i kombinasjon, se også avsnittet Advarsler og forsiktighetsregler i pakningsvedlegget til Symbyax.
Eldre pasienter med demensrelatert psykose
Økt dødelighet
Eldre pasienter med demensrelatert psykose behandlet med antipsykotiske legemidler har økt risiko for død. ZYPREXA 20mg er ikke godkjent for behandling av pasienter med demensrelatert psykose [se ADVARSEL i boks, Bruk hos pasienter med samtidig sykdom og PASIENTINFORMASJON].
I placebokontrollerte kliniske studier av eldre pasienter med demensrelatert psykose, var forekomsten av død hos olanzapin-behandlede pasienter signifikant høyere enn placebo-behandlede pasienter (henholdsvis 3,5 % vs 1,5 %).
Cerebrovaskulære bivirkninger (CVAE), inkludert hjerneslag
Cerebrovaskulære bivirkninger (f.eks. slag, forbigående iskemisk angrep), inkludert dødsfall, ble rapportert hos pasienter i studier med olanzapin hos eldre pasienter med demensrelatert psykose. I placebokontrollerte studier var det en signifikant høyere forekomst av cerebrovaskulære bivirkninger hos pasienter behandlet med olanzapin sammenlignet med pasienter behandlet med placebo. Olanzapin er ikke godkjent for behandling av pasienter med demensrelatert psykose [se ADVARSEL i boks og PASIENTINFORMASJON ].
Selvmord
Muligheten for et selvmordsforsøk er iboende ved schizofreni og ved bipolar lidelse I, og tett oppfølging av høyrisikopasienter bør følge medikamentell behandling. Resepter for olanzapin bør skrives ut for den minste mengde tabletter i samsvar med god pasientbehandling, for å redusere risikoen for overdosering.
Malignt nevroleptikasyndrom (NMS)
Et potensielt dødelig symptomkompleks noen ganger referert til som malignt nevroleptisk syndrom (NMS) er rapportert i forbindelse med administrering av antipsykotiske legemidler, inkludert olanzapin. Kliniske manifestasjoner av NMS er hyperpyreksi, muskelstivhet, endret mental status og tegn på autonom ustabilitet (uregelmessig puls eller blodtrykk, takykardi, diaforese og hjerterytmeforstyrrelser). Ytterligere tegn kan inkludere forhøyet kreatininfosfokinase, myoglobinuri (rabdomyolyse) og akutt nyresvikt.
Den diagnostiske evalueringen av pasienter med dette syndromet er komplisert. For å komme frem til en diagnose er det viktig å utelukke tilfeller der den kliniske presentasjonen inkluderer både alvorlig medisinsk sykdom (f.eks. lungebetennelse, systemisk infeksjon, etc.) og ubehandlede eller utilstrekkelig behandlede ekstrapyramidale tegn og symptomer (EPS). Andre viktige hensyn i differensialdiagnosen inkluderer sentral antikolinergisk toksisitet, heteslag, medikamentfeber og primær patologi i sentralnervesystemet.
Behandlingen av NMS bør omfatte: 1) umiddelbar seponering av antipsykotiske legemidler og andre legemidler som ikke er avgjørende for samtidig behandling; 2) intensiv symptomatisk behandling og medisinsk overvåking; og 3) behandling av eventuelle samtidige alvorlige medisinske problemer som spesifikke behandlinger er tilgjengelige for. Det er ingen generell enighet om spesifikke farmakologiske behandlingsregimer for NMS.
Dersom en pasient trenger antipsykotisk medikamentbehandling etter bedring fra NMS, bør mulig gjeninnføring av medikamentell behandling vurderes nøye. Pasienten bør overvåkes nøye, siden tilbakefall av NMS er rapportert [se PASIENTINFORMASJON ].
Legemiddelreaksjon med eosinofili og systemiske symptomer (DRESS)
Legemiddelreaksjon med eosinofili og systemiske symptomer (DRESS) er rapportert ved eksponering for olanzapin. DRESS kan oppstå med en kutan reaksjon (som utslett eller eksfoliativ dermatitt), eosinofili, feber og/eller lymfadenopati med systemiske komplikasjoner som hepatitt, nefritt, pneumonitt, myokarditt og/eller perikarditt. DRESS er noen ganger dødelig. Seponer olanzapin hvis det er mistanke om DRESS [se PASIENTINFORMASJON ].
Metabolske endringer
Atypiske antipsykotiske legemidler har vært assosiert med metabolske endringer inkludert hyperglykemi, dyslipidemi og vektøkning. Metabolske endringer kan være assosiert med økt kardiovaskulær/cerebrovaskulær risiko. Olanzapins spesifikke metabolske profil er presentert nedenfor.
Hyperglykemi og diabetes mellitus
Helsepersonell bør vurdere risikoene og fordelene når de forskriver olanzapin til pasienter med en etablert diagnose av diabetes mellitus, eller som har grenseoverskridende økt blodsukkernivå (fastende 100-126 mg/dL, ikke-fastende 140-200 mg/dL). Pasienter som tar olanzapin bør overvåkes regelmessig for forverret glukosekontroll. Pasienter som starter behandling med olanzapin bør gjennomgå fastende blodsukkertesting i begynnelsen av behandlingen og med jevne mellomrom under behandlingen. Alle pasienter som behandles med atypiske antipsykotika bør overvåkes for symptomer på hyperglykemi, inkludert polydipsi, polyuri, polyfagi og svakhet. Pasienter som utvikler symptomer på hyperglykemi under behandling med atypiske antipsykotika bør gjennomgå fastende blodsukkertesting. I noen tilfeller har hyperglykemi gått over når det atypiske antipsykotikaet ble seponert; noen pasienter trengte imidlertid fortsettelse av antidiabetisk behandling til tross for seponering av det mistenkte legemidlet [se PASIENTINFORMASJON ].
Hyperglykemi, i noen tilfeller ekstrem og assosiert med ketoacidose eller hyperosmolar koma eller død, er rapportert hos pasienter behandlet med atypiske antipsykotika inkludert olanzapin. Vurdering av sammenhengen mellom atypisk antipsykotisk bruk og glukoseavvik kompliseres av muligheten for økt bakgrunnsrisiko for diabetes mellitus hos pasienter med schizofreni og den økende forekomsten av diabetes mellitus i befolkningen generelt. Epidemiologiske studier tyder på økt risiko for behandlingsfremkommede hyperglykemi-relaterte bivirkninger hos pasienter behandlet med atypiske antipsykotika. Mens relative risikoestimater er inkonsekvente, ser sammenhengen mellom atypiske antipsykotika og økninger i glukosenivåer ut til å falle på et kontinuum, og olanzapin ser ut til å ha en større assosiasjon enn noen andre atypiske antipsykotika.
Gjennomsnittlig økning i blodsukker har blitt observert hos pasienter behandlet (median eksponering på 9,2 måneder) med olanzapin i fase 1 av Clinical Antipsychotic Trials of Intervention Effectiveness (CATIE). Gjennomsnittlig økning av serumglukose (fastende og ikke-fastende prøver) fra baseline til gjennomsnittet av de 2 høyeste serumkonsentrasjonene var 15,0 mg/dL.
I en studie av friske frivillige hadde forsøkspersoner som fikk olanzapin (N=22) i 3 uker en gjennomsnittlig økning i fastende blodsukker sammenlignet med baseline på 2,3 mg/dL. Placebo-behandlede personer (N=19) hadde en gjennomsnittlig økning i fastende blodsukker sammenlignet med baseline på 0,34 mg/dL.
Olanzapin monoterapi hos voksne
en analyse av 5 placebokontrollerte voksne olanzapin monoterapistudier med en median behandlingsvarighet på ca. 3 uker, var olanzapin assosiert med en større gjennomsnittlig endring i fastende glukosenivå sammenlignet med placebo (2,76 mg/dL versus 0,17 mg/dL). Forskjellen i gjennomsnittlige endringer mellom olanzapin og placebo var større hos pasienter med tegn på glukosedysregulering ved baseline (pasienter diagnostisert med diabetes mellitus eller relaterte bivirkninger, pasienter behandlet med antidiabetiske midler, pasienter med et tilfeldig glukosenivå ved baseline ≥200 mg/ dL, og/eller et fastende glukosenivå på ≥126 mg/dL. Olanzapin-behandlede pasienter hadde en større gjennomsnittlig HbA1c-økning fra baseline på 0,04 % (median eksponering 21 dager), sammenlignet med en gjennomsnittlig HbA1c-reduksjon på 0,06 % hos placebobehandlede personer (median eksponering 17 dager).
en analyse av 8 placebokontrollerte studier (median behandlingseksponering 4-5 uker), hadde 6,1 % av olanzapin-behandlede forsøkspersoner (N=855) behandlingsutløst glykosuri sammenlignet med 2,8 % av placebo-behandlede individer (N=599) . Tabell 2 viser kortsiktige og langsiktige endringer i fastende glukosenivåer fra monoterapistudier med olanzapin hos voksne.

Gjennomsnittlig endring i fastende glukose for pasienter eksponert i minst 48 uker var 4,2 mg/dL (N=487). I analyser av pasienter som fullførte 9-12 måneder med olanzapinbehandling, fortsatte gjennomsnittlig endring i fastende og ikke-fastende glukosenivåer å øke over tid.
Olanzapin monoterapi hos ungdom
Sikkerhet og effekt av olanzapin er ikke fastslått hos pasienter under 13 år. I en analyse av 3 placebokontrollerte olanzapin monoterapistudier av ungdomspasienter, inkludert de med schizofreni (6 uker) eller bipolar lidelse I (maniske eller blandede episoder) (3 uker), var olanzapin assosiert med en større gjennomsnittlig endring fra baseline i faste. glukosenivåer sammenlignet med placebo (2,68 mg/dL mot -2,59 mg/dL). Gjennomsnittlig endring i fastende glukose for ungdom eksponert i minst 24 uker var 3,1 mg/dL (N=121). Tabell 3 viser kortsiktige og langsiktige endringer i fastende blodsukker fra monoterapistudier med olanzapin i ungdom.
Dyslipidemi
Uønskede endringer i lipider har blitt observert ved bruk av olanzapin. Klinisk overvåking, inkludert baseline og periodiske oppfølgingslipidevalueringer hos pasienter som bruker olanzapin, anbefales [se PASIENTINFORMASJON ].
Klinisk signifikante, og noen ganger svært høye (>500 mg/dL), økninger i triglyseridnivåer er observert ved bruk av olanzapin. Beskjeden gjennomsnittlig økning i totalkolesterol er også sett ved bruk av olanzapin.
Olanzapin monoterapi hos voksne
en analyse av 5 placebokontrollerte olanzapin monoterapistudier med behandlingsvarighet opptil 12 uker, hadde olanzapinbehandlede pasienter økninger fra baseline i gjennomsnittlig fastende totalkolesterol, LDL-kolesterol og triglyserider på 5,3 mg/dL, 3,0 mg/dL og 20,8 mg/dL henholdsvis sammenlignet med reduksjoner fra baseline i gjennomsnittlig fastende totalkolesterol, LDL-kolesterol og triglyserider på 6,1 mg/dL, 4,3 mg/dL og 10,7 mg/dL for placebobehandlede pasienter. For fastende HDL-kolesterol ble det ikke observert noen klinisk betydningsfulle forskjeller mellom olanzapin-behandlede pasienter og placebo-behandlede pasienter. Gjennomsnittlig økning i fastende lipidverdier (totalkolesterol, LDL-kolesterol og triglyserider) var større hos pasienter uten tegn på lipiddysregulering ved baseline, der lipiddysregulering ble definert som pasienter diagnostisert med dyslipidemi eller relaterte bivirkninger, pasienter behandlet med lipidsenkende midler, eller pasienter med høye baseline lipidnivåer.
langtidsstudier (minst 48 uker) hadde pasientene økninger fra baseline i gjennomsnittlig fastende totalkolesterol, LDL-kolesterol og triglyserider på henholdsvis 5,6 mg/dL, 2,5 mg/dL og 18,7 mg/dL, og en gjennomsnittlig reduksjon i fastende HDL-kolesterol på 0,16 mg/dL. I en analyse av pasienter som fullførte 12 måneders behandling, økte ikke gjennomsnittlig ikke-fastende totalkolesterol ytterligere etter ca. 4-6 måneder.
Andelen pasienter som hadde endringer (minst én gang) i totalt kolesterol, LDL-kolesterol eller triglyserider fra normalt eller borderline til høyt, eller endringer i HDL-kolesterol fra normalt eller borderline til lavt, var større i langtidsstudier (minst 48 uker) sammenlignet med korttidsstudier. Tabell 4 viser kategoriske endringer i fastende lipidverdier.
fase 1 av Clinical Antipsychotic Trials of Intervention Effectiveness (CATIE), over en median eksponering på 9,2 måneder, var gjennomsnittlig økning i triglyserider hos pasienter som tok olanzapin 40,5 mg/dL. I fase 1 av CATIE var gjennomsnittlig økning i totalkolesterol 9,4 mg/dL.
Olanzapin monoterapi hos ungdom
Sikkerhet og effekt av olanzapin er ikke fastslått hos pasienter under 13 år. I en analyse av 3 placebokontrollerte olanzapin monoterapistudier av ungdom, inkludert de med schizofreni (6 uker) eller bipolar lidelse I (maniske eller blandede episoder) (3 uker), hadde olanzapinbehandlede ungdommer økning fra baseline i gjennomsnittlig fastende totalkolesterol, LDL kolesterol og triglyserider på henholdsvis 12,9 mg/dL, 6,5 mg/dL og 28,4 mg/dL, sammenlignet med økninger fra baseline i gjennomsnittlig fastende totalkolesterol og LDL-kolesterol på 1,3 mg/dL og 1,0 mg/dL, og en reduksjon i triglyserider på 1,1 mg/dL for placebobehandlede ungdom. For fastende HDL-kolesterol ble det ikke observert noen klinisk betydningsfulle forskjeller mellom olanzapinbehandlede ungdom og placebobehandlede ungdom.
langtidsstudier (minst 24 uker) hadde ungdom økning fra baseline i gjennomsnittlig fastende totalkolesterol, LDL-kolesterol og triglyserider på henholdsvis 5,5 mg/dL, 5,4 mg/dL og 20,5 mg/dL, og en gjennomsnittlig reduksjon i fastende HDL-kolesterol på 4,5 mg/dL. Tabell 5 viser kategoriske endringer i fastende lipidverdier hos ungdom.
Vektøkning
Potensielle konsekvenser av vektøkning bør vurderes før oppstart med olanzapin. Pasienter som får olanzapin bør få regelmessig overvåking av vekten [se Informasjon om pasientveiledning ].
Olanzapin monoterapi hos voksne
en analyse av 13 placebokontrollerte olanzapin monoterapistudier, økte olanzapin-behandlede pasienter i gjennomsnitt 2,6 kg (5,7 lb) sammenlignet med et gjennomsnittlig vekttap på 0,3 kg (0,6 lb) hos placebo-behandlede pasienter med en median eksponering på 6 uker ; 22,2 % av olanzapinbehandlede pasienter gikk opp minst 7 % av baselinevekten, sammenlignet med 3 % av placebobehandlede pasienter, med en median eksponering for hendelsen på 8 uker; 4,2 % av olanzapinbehandlede pasienter gikk opp minst 15 % av baselinevekten, sammenlignet med 0,3 % av placebobehandlede pasienter, med en median eksponering for hendelsen på 12 uker. Klinisk signifikant vektøkning ble observert på tvers av alle baseline Body Mass Index (BMI) kategorier. Seponering på grunn av vektøkning forekom hos 0,2 % av olanzapin-behandlede pasienter og hos 0 % av placebo-behandlede pasienter.
langtidsstudier (minst 48 uker) var gjennomsnittlig vektøkning 5,6 kg (12,3 lb) (median eksponering på 573 dager, N=2021). Prosentandelen av pasienter som gikk opp minst 7 %, 15 % eller 25 % av baseline-kroppsvekten ved langtidseksponering var henholdsvis 64 %, 32 % og 12 %. Seponering på grunn av vektøkning skjedde hos 0,4 % av olanzapinbehandlede pasienter etter minst 48 ukers eksponering.
Tabell 6 inkluderer data om vektøkning hos voksne med olanzapin samlet fra 86 kliniske studier. Dataene i hver kolonne representerer data for de pasientene som fullførte behandlingsperioder av den angitte varigheten.
Dosegruppeforskjeller med hensyn til vektøkning er observert. I en enkelt 8-ukers randomisert, dobbeltblind studie med fast dose som sammenlignet 10 (N=199), 20 (N=200) og 40 (N=200) mg/dag oral olanzapin hos voksne pasienter med schizofreni eller schizoaffektiv lidelse, gjennomsnittlig vektøkning fra baseline til endepunkt (10 mg/dag: 1,9 kg; 20 mg/dag: 2,3 kg; 40 mg/dag: 3 kg) ble observert med signifikante forskjeller mellom 10 og 40 mg/dag.
Olanzapin monoterapi hos ungdom
Sikkerhet og effekt av olanzapin er ikke fastslått hos pasienter under 13 år. Gjennomsnittlig vektøkning hos ungdom var større enn hos voksne. I 4 placebokontrollerte studier forekom seponering på grunn av vektøkning hos 1 % av olanzapin-behandlede pasienter, sammenlignet med 0 % av placebo-behandlede pasienter.
langtidsstudier (minst 24 uker) var gjennomsnittlig vektøkning 11,2 kg (24,6 lb); (median eksponering på 201 dager, N=179). Prosentandelen av ungdommer som gikk opp minst 7 %, 15 % eller 25 % av kroppsvekten sin ved langtidseksponering var henholdsvis 89 %, 55 % og 29 %. Blant ungdomspasienter var gjennomsnittlig vektøkning etter baseline BMI-kategori henholdsvis 11,5 kg (25,3 lb), 12,1 kg (26,6 lb) og 12,7 kg (27,9 lb) for normal (N=106), overvekt (N=26) og overvektige (N=17). Seponering på grunn av vektøkning skjedde hos 2,2 % av olanzapin-behandlede pasienter etter minst 24 ukers eksponering.
Tabell 8 viser data om vektøkning hos ungdom med olanzapin samlet fra 6 kliniske studier. Dataene i hver kolonne representerer data for de pasientene som fullførte behandlingsperioder av den angitte varigheten. Lite data fra kliniske studier er tilgjengelig om vektøkning hos ungdom med olanzapin utover 6 måneders behandling.
Tardiv dyskinesi
Et syndrom med potensielt irreversible, ufrivillige, dyskinetiske bevegelser kan utvikles hos pasienter som behandles med antipsykotiske legemidler. Selv om prevalensen av syndromet ser ut til å være høyest blant eldre, spesielt eldre kvinner, er det umulig å stole på prevalensestimater for å forutsi, ved starten av antipsykotisk behandling, hvilke pasienter som sannsynligvis vil utvikle syndromet. Hvorvidt antipsykotiske legemidler er forskjellige i deres potensial til å forårsake tardiv dyskinesi er ukjent.
Risikoen for å utvikle tardiv dyskinesi og sannsynligheten for at den blir irreversibel antas å øke etter hvert som behandlingens varighet og den totale kumulative dosen av antipsykotiske legemidler som gis til pasienten øker. Imidlertid kan syndromet utvikle seg, selv om det er mye mindre vanlig, etter relativt korte behandlingsperioder ved lave doser eller kan til og med oppstå etter seponering av behandlingen.
Tardiv dyskinesi kan gi seg, delvis eller fullstendig, hvis antipsykotisk behandling seponeres. Antipsykotisk behandling kan imidlertid i seg selv undertrykke (eller delvis undertrykke) tegn og symptomer på syndromet og kan derved muligens maskere den underliggende prosessen. Effekten som symptomatisk undertrykkelse har på det langsiktige forløpet av syndromet er ukjent.
Gitt disse hensynene bør olanzapin forskrives på en måte som mest sannsynlig minimerer forekomsten av tardiv dyskinesi. Kronisk antipsykotisk behandling bør generelt være forbeholdt pasienter (1) som lider av en kronisk sykdom som er kjent for å reagere på antipsykotiske legemidler, og (2) for hvem alternative, like effektive, men potensielt mindre skadelige behandlinger ikke er tilgjengelige eller hensiktsmessige. Hos pasienter som trenger kronisk behandling, bør den minste dosen og den korteste behandlingsvarigheten som gir en tilfredsstillende klinisk respons søkes. Behovet for fortsatt behandling bør revurderes med jevne mellomrom.
Hvis det oppstår tegn og symptomer på tardiv dyskinesi hos en pasient på olanzapin, bør seponering av medikamentet vurderes. Noen pasienter kan imidlertid trenge behandling med olanzapin til tross for tilstedeværelsen av syndromet.
For spesifikk informasjon om advarsler om litium eller valproat, se avsnittet Advarsler i pakningsvedlegget for disse andre produktene.
Ortostatisk hypotensjon
Olanzapin kan indusere ortostatisk hypotensjon assosiert med svimmelhet, takykardi, bradykardi og, hos noen pasienter, synkope, spesielt under den initiale dosetitreringsperioden, sannsynligvis noe som gjenspeiler dets α1-adrenerge antagonistiske egenskaper [se Informasjon om pasientveiledning ].
Fra en analyse av vitale tegndata i en integrert database med 41 fullførte kliniske studier hos voksne pasienter behandlet med oralt olanzapin, ble ortostatisk hypotensjon registrert hos ≥20 % (1277/6030) av pasientene.
For oral olanzapinbehandling kan risikoen for ortostatisk hypotensjon og synkope reduseres ved å starte behandlingen med 5 mg QD [se DOSERING OG ADMINISTRASJON ]. En mer gradvis titrering til måldosen bør vurderes dersom hypotensjon oppstår.
Hypotensjon, bradykardi med eller uten hypotensjon, takykardi og synkope ble også rapportert under de kliniske studiene med intramuskulært olanzapin til injeksjon. I en åpen klinisk farmakologisk studie på ikke-agiterte pasienter med schizofreni der sikkerheten og toleransen til intramuskulært olanzapin ble evaluert under et maksimalt doseringsregime (tre 10 mg doser administrert med 4 timers mellomrom), opplevde omtrent en tredjedel av disse pasientene en signifikant ortostatisk reduksjon i systolisk blodtrykk (dvs. reduksjon ≥30 mmHg) [se DOSERING OG ADMINISTRASJON ]. Synkope ble rapportert hos 0,6 % (15/2500) av olanzapin-behandlede pasienter i fase 2-3 orale olanzapin-studier og hos 0,3 % (2/722) av olanzapin-behandlede pasienter med agitasjon i intramuskulære olanzapin for injeksjonsstudier. Tre normale frivillige i fase 1-studier med intramuskulært olanzapin opplevde hypotensjon, bradykardi og sinuspauser på opptil 6 sekunder som forsvant spontant (i 2 tilfeller oppsto reaksjonene på intramuskulært olanzapin, og i 1 tilfelle på oralt olanzapin). Risikoen for denne sekvensen av hypotensjon, bradykardi og sinuspause kan være større hos ikke-psykiatriske pasienter sammenlignet med psykiatriske pasienter som muligens er mer tilpasset visse effekter av psykofarmaka. For intramuskulær olanzapin til injeksjonsbehandling, bør pasienter forbli liggende hvis de er døsige eller svimle etter injeksjon inntil undersøkelse har indikert at de ikke opplever postural hypotensjon, bradykardi og/eller hypoventilasjon.
Olanzapin bør brukes med spesiell forsiktighet hos pasienter med kjent kardiovaskulær sykdom (historie med hjerteinfarkt eller iskemi, hjertesvikt eller ledningsforstyrrelser), cerebrovaskulær sykdom og tilstander som kan disponere pasienter for hypotensjon (dehydrering, hypovolemi og behandling med antihypertensive medisiner). ) hvor forekomsten av synkope, eller hypotensjon og/eller bradykardi kan sette pasienten i økt medisinsk risiko.
Forsiktighet er nødvendig hos pasienter som får behandling med andre legemidler som har effekter som kan indusere hypotensjon, bradykardi, respirasjons- eller sentralnervesystemdepresjon [se NARKOTIKAHANDEL ]. Samtidig administrering av intramuskulært olanzapin og parenteralt benzodiazepin anbefales ikke på grunn av muligheten for overdreven sedasjon og kardiorespiratorisk depresjon.
Falls
ZYPREXA kan forårsake somnolens, postural hypotensjon, motorisk og sensorisk ustabilitet, som kan føre til fall og følgelig brudd eller andre skader. For pasienter med sykdommer, tilstander eller medisiner som kan forverre disse effektene, fullfør fallrisikovurderinger ved oppstart av antipsykotisk behandling og gjentatte ganger for pasienter på langvarig antipsykotisk behandling.
Leukopeni, nøytropeni og agranulocytose
Klasseeffekt
I kliniske studier og/eller erfaring etter markedsføring har hendelser med leukopeni/nøytropeni blitt rapportert tidsmessig relatert til antipsykotiske midler, inkludert ZYPREXA. Agranulocytose er også rapportert.
Mulige risikofaktorer for leukopeni/nøytropeni inkluderer allerede eksisterende lavt antall hvite blodlegemer (WBC) og historie med legemiddelindusert leukopeni/nøytropeni. Pasienter med en historie med klinisk signifikant lav WBC eller medikamentindusert leukopeni/nøytropeni bør få fullstendig blodtelling (CBC) overvåket ofte i løpet av de første månedene av behandlingen, og seponering av ZYPREXA bør vurderes ved første tegn på en klinisk signifikant nedgang. i WBC i fravær av andre årsaksfaktorer.
Pasienter med klinisk signifikant nøytropeni bør overvåkes nøye for feber eller andre symptomer eller tegn på infeksjon og behandles umiddelbart dersom slike symptomer eller tegn oppstår. Pasienter med alvorlig nøytropeni (absolutt nøytrofiltall
Dysfagi
Esophageal dysmotilitet og aspirasjon har vært assosiert med bruk av antipsykotiske legemidler. Aspirasjonspneumoni er en vanlig årsak til sykelighet og dødelighet hos pasienter med avansert Alzheimers sykdom. Olanzapin er ikke godkjent for behandling av pasienter med Alzheimers sykdom.
Anfall
Under premarketingtesting forekom anfall hos 0,9 % (22/2500) av olanzapinbehandlede pasienter. Det var forvirrende faktorer som kan ha bidratt til forekomsten av anfall i mange av disse tilfellene. Olanzapin bør brukes med forsiktighet hos pasienter med tidligere anfall eller med tilstander som potensielt senker krampeterskelen, f.eks. Alzheimers demens. Olanzapin er ikke godkjent for behandling av pasienter med Alzheimers sykdom. Tilstander som senker anfallsterskelen kan være mer utbredt i en befolkning på 65 år eller eldre.
Potensial for kognitiv og motorisk svikt
Somnolens var en vanlig rapportert bivirkning assosiert med olanzapinbehandling, som oppstod med en forekomst på 26 % hos olanzapinpasienter sammenlignet med 15 % hos placebopasienter. Denne bivirkningen var også doserelatert. Somnolens førte til seponering hos 0,4 % (9/2500) av pasientene i premarketingdatabasen.
Siden olanzapin har potensial til å svekke dømmekraft, tenkning eller motoriske ferdigheter, bør pasienter advares mot bruk av farlige maskiner, inkludert biler, inntil de er rimelig sikre på at olanzapinbehandling ikke påvirker dem negativt [se Informasjon om pasientveiledning ].
Kroppstemperaturregulering
Forstyrrelse av kroppens evne til å redusere kjernekroppstemperaturen er blitt tilskrevet antipsykotiske midler. Passende forsiktighet anbefales ved forskrivning av olanzapin til pasienter som vil oppleve tilstander som kan bidra til en økning i kjernekroppstemperaturen, f.eks. å trene hardt, eksponering for ekstrem varme, samtidig motta medisiner med antikolinerg aktivitet, eller være utsatt for dehydrering [se PASIENTINFORMASJON ].
Bruk hos pasienter med samtidig sykdom
Klinisk erfaring med olanzapin hos pasienter med visse samtidige systemiske sykdommer er begrenset [se KLINISK FARMAKOLOGI ].
Olanzapin viser in vitro muskarin reseptoraffinitet. I kliniske studier før markedsføring med olanzapin var olanzapin assosiert med forstoppelse, munntørrhet og takykardi, alle bivirkninger muligens relatert til kolinerg antagonisme. Slike bivirkninger var ikke ofte grunnlaget for seponering av olanzapin, men olanzapin bør brukes med forsiktighet hos pasienter med klinisk signifikant prostatahypertrofi, trangvinkelglaukom eller en historie med paralytisk ileus eller relaterte tilstander.
5 placebokontrollerte studier av olanzapin hos eldre pasienter med demensrelatert psykose (n=1184), ble følgende behandlingsutløste bivirkninger rapportert hos olanzapinbehandlede pasienter med en insidens på minst 2 % og signifikant høyere enn placebo- behandlede pasienter: fall, somnolens, perifert ødem, unormal gange, urininkontinens, sløvhet, økt vekt, asteni, pyreksi, lungebetennelse, munntørrhet og visuelle hallusinasjoner. Frekvensen av seponering på grunn av bivirkninger var høyere med olanzapin enn placebo (13 % vs. 7 %). Eldre pasienter med demensrelatert psykose behandlet med olanzapin har økt risiko for død sammenlignet med placebo. Olanzapin er ikke godkjent for behandling av pasienter med demensrelatert psykose [se ADVARSEL i boks , Eldre pasienter med demensrelatert psykose , og PASIENTINFORMASJON ].
Olanzapin har ikke blitt evaluert eller brukt i nevneverdig grad hos pasienter med en nylig historie med hjerteinfarkt eller ustabil hjertesykdom. Pasienter med disse diagnosene ble ekskludert fra kliniske studier før markedsføring. På grunn av risikoen for ortostatisk hypotensjon med olanzapin, bør det utvises forsiktighet hos hjertepasienter [se Ortostatisk hypotensjon ].
Hyperprolaktinemi
Som med andre legemidler som antagoniserer dopamin D2-reseptorer, øker olanzapin prolaktinnivået, og økningen vedvarer under kronisk administrering. Hyperprolaktinemi kan undertrykke hypotalamisk GnRH, noe som resulterer i redusert hypofysegonadotropinsekresjon. Dette kan i sin tur hemme reproduksjonsfunksjonen ved å svekke gonadal steroidogenese hos både kvinnelige og mannlige pasienter. Galaktoré, amenoré, gynekomasti og impotens er rapportert hos pasienter som får prolaktinøkende forbindelser. Langvarig hyperprolaktinemi når assosiert med hypogonadisme kan føre til redusert bentetthet hos både kvinnelige og mannlige forsøkspersoner.
Vevskultureksperimenter indikerer at omtrent en tredjedel av brystkreft hos mennesker er prolaktinavhengig in vitro, en faktor av potensiell betydning dersom forskrivning av disse legemidlene vurderes hos en pasient med tidligere påvist brystkreft. Som vanlig med forbindelser som øker frigjøring av prolaktin, ble en økning i brystkjertelneoplasi observert i olanzapin karsinogenitetsstudier utført på mus og rotter [se Ikke-klinisk toksikologi ]. Verken kliniske studier eller epidemiologiske studier utført til dags dato har vist en sammenheng mellom kronisk administrering av denne klassen medikamenter og tumorgenese hos mennesker; tilgjengelig bevis anses for begrenset til å være avgjørende på dette tidspunktet.
placebokontrollerte olanzapin kliniske studier (opptil 12 uker) ble endringer fra normal til høy i prolaktinkonsentrasjon observert hos 30 % av voksne behandlet med olanzapin sammenlignet med 10,5 % av voksne behandlet med placebo. I en samlet analyse fra kliniske studier inkludert 8136 voksne behandlet med olanzapin, inkluderte potensielt assosierte kliniske manifestasjoner menstruasjonsrelaterte hendelser1 (2 % [49/3240] av kvinner), seksuell funksjonsrelaterte hendelser2 (2 % [150/8136] av kvinner). og menn), og brystrelaterte hendelser3 (0,7 % [23/3240] av kvinner, 0,2 % [9/4896] av menn).
placebokontrollerte olanzapin monoterapistudier hos ungdomspasienter (opptil 6 uker) med schizofreni eller bipolar lidelse I (maniske eller blandede episoder), ble endringer fra normal til høy i prolaktinkonsentrasjon observert hos 47 % av olanzapin-behandlede pasienter sammenlignet med 7 % av placebobehandlede pasienter. I en samlet analyse fra kliniske studier inkludert 454 ungdommer behandlet med olanzapin, inkluderte potensielt assosierte kliniske manifestasjoner menstruasjonsrelaterte hendelser1 (1 % [2/168] av kvinner), seksuell funksjonsrelaterte hendelser2 (0,7 % [3/454] av kvinner og menn ), og brystrelaterte hendelser3 (2 % [3/168] av kvinner, 2 % [7/286] av menn) [se Bruk i spesifikke populasjoner ].
1 Basert på et søk etter følgende termer: amenoré, hypomenoré, menstruasjon forsinket og oligomenoré.
2 Basert på et søk etter følgende termer: anorgasmi, forsinket utløsning, erektil dysfunksjon, redusert libido, tap av libido, unormal orgasme og seksuell dysfunksjon.
Basert på et søk etter følgende termer: utflod fra bryster, forstørrelse eller hevelse, galaktoré, gynekomasti og ammingsforstyrrelse.
Dosegruppeforskjeller med hensyn til prolaktinøkning er observert. I en enkelt 8-ukers randomisert, dobbeltblind, fastdosestudie som sammenlignet 10 (N=199), 20 (N=200) og 40 (N=200) mg/dag oral olanzapin hos voksne pasienter med schizofreni eller schizoaffektiv lidelse, forekomst av prolaktinøkning >24,2 ng/ml (kvinnelig) eller >18,77 ng/ml (mann) når som helst under forsøket (10 mg/dag: 31,2 %; 20 mg/dag: 42,7 %; 40 mg/dag : 61,1 %) indikerte signifikante forskjeller mellom 10 vs 40 mg/dag og 20 vs 40 mg/dag.
Bruk i kombinasjon med fluoksetin, litium eller valproat
Ved bruk av ZYPREXA og fluoksetin i kombinasjon, bør forskriveren også se avsnittet Advarsler og forsiktighetsregler i pakningsvedlegget til Symbyax. Ved bruk av ZYPREXA i kombinasjon med litium eller valproat, bør forskriveren se avsnittene Advarsler og forsiktighetsregler i pakningsvedlegget for litium eller valproat [se NARKOTIKAHANDEL ].
Laboratorietester
Fastende blodsukkertesting og lipidprofil i begynnelsen av og med jevne mellomrom under behandlingen anbefales [se Metabolske endringer og PASIENTINFORMASJON ].
Informasjon om pasientveiledning
Råd pasienten til å lese den FDA-godkjente pasientmerkingen ( Medisinveiledning ) for de orale formuleringene.
Pasienter bør informeres om følgende problemer og bes om å varsle sin forskriver dersom disse oppstår mens de tar ZYPREXA 15 mg som monoterapi eller i kombinasjon med fluoksetin. Hvis du ikke tror du blir bedre eller er bekymret for tilstanden din mens du tar ZYPREXA 2,5 mg, ring legen din. Når du bruker ZYPREXA og fluoksetin i kombinasjon, se også avsnittet om pasientrådgivning i pakningsvedlegget til Symbyax.
Eldre pasienter med demensrelatert psykose: økt dødelighet og cerebrovaskulære bivirkninger (CVAE), inkludert hjerneslag
Pasienter og omsorgspersoner bør informeres om at eldre pasienter med demensrelatert psykose behandlet med antipsykotiske legemidler har økt risiko for død. Pasienter og omsorgspersoner bør informeres om at eldre pasienter med demensrelatert psykose behandlet med ZYPREXA hadde en signifikant høyere forekomst av cerebrovaskulære bivirkninger (f.eks. slag, forbigående iskemisk anfall) sammenlignet med placebo.
ZYPREXA er ikke godkjent for eldre pasienter med demensrelatert psykose [se ADVARSEL i boks og ADVARSLER OG FORHOLDSREGLER ].
Malignt nevroleptikasyndrom (NMS)
Pasienter og omsorgspersoner bør informeres om at et potensielt dødelig symptomkompleks noen ganger referert til som NMS er rapportert i forbindelse med administrering av antipsykotiske legemidler, inkludert ZYPREXA. Tegn og symptomer på NMS inkluderer hyperpyreksi, muskelstivhet, endret mental status og tegn på autonom ustabilitet (uregelmessig puls eller blodtrykk, takykardi, diaforese og hjerterytmeforstyrrelser) [se ADVARSLER OG FORHOLDSREGLER ].
Legemiddelreaksjon med eosinofili og systemiske symptomer (DRESS)
Pasienter bør rådes til å rapportere til helsepersonell så tidlig som mulig av tegn og symptomer som kan være assosiert med legemiddelreaksjon med eosinofili og systemiske symptomer (DRESS) [se ADVARSLER OG FORHOLDSREGLER ].
Hyperglykemi og diabetes mellitus
Pasienter bør informeres om den potensielle risikoen for hyperglykemi-relaterte bivirkninger. Pasienter bør overvåkes regelmessig for forverret glukosekontroll. Pasienter som har diabetes bør følge legens instruksjoner om hvor ofte de skal sjekke blodsukkeret mens de tar ZYPREXA [se ADVARSLER OG FORHOLDSREGLER ].
Dyslipidemi
Pasienter bør informeres om at dyslipidemi har oppstått under behandling med ZYPREXA. Pasienter bør få overvåket lipidprofilen regelmessig [se ADVARSLER OG FORHOLDSREGLER ].
Vektøkning
Pasienter bør informeres om at vektøkning har skjedd under behandling med ZYPREXA. Pasienter bør få overvåket vekten regelmessig [se ADVARSLER OG FORHOLDSREGLER ].
Ortostatisk hypotensjon
Pasienter bør informeres om risikoen for ortostatisk hypotensjon, spesielt i perioden med initial dosetitrering og i forbindelse med bruk av samtidige legemidler som kan potensere den ortostatiske effekten av ZYPREXA, f.eks. diazepam eller alkohol [se ADVARSLER OG FORHOLDSREGLER og NARKOTIKAHANDEL ]. Pasienter bør rådes til å endre stilling forsiktig for å forhindre ortostatisk hypotensjon, og legge seg ned hvis de føler seg svimmel eller besvimer, til de føler seg bedre. Pasienter bør rådes til å ringe legen sin dersom de opplever noen av følgende tegn og symptomer assosiert med ortostatisk hypotensjon: svimmelhet, rask eller langsom hjerterytme eller besvimelse.
Potensial for kognitiv og motorisk svikt
Fordi ZYPREXA har potensial til å svekke dømmekraft, tenkning eller motoriske ferdigheter, bør pasienter advares mot bruk av farlige maskiner, inkludert biler, inntil de er rimelig sikre på at ZYPREXA-terapi ikke påvirker dem negativt [se ADVARSLER OG FORHOLDSREGLER ].
Kroppstemperaturregulering
Pasienter bør informeres om passende omsorg for å unngå overoppheting og dehydrering. Pasienter bør rådes til å ringe legen sin umiddelbart hvis de blir alvorlig syke og har noen eller alle disse symptomene på dehydrering: svette for mye eller ikke i det hele tatt, munntørrhet, veldig varm følelse, tørst, ikke i stand til å produsere urin [ se ADVARSLER OG FORHOLDSREGLER ].
Samtidig medisinering
Pasienter bør rådes til å informere helsepersonell dersom de tar, eller planlegger å ta, Symbyax. Pasienter bør også rådes til å informere helsepersonell dersom de tar, planlegger å ta eller har sluttet å ta reseptbelagte eller reseptfrie legemidler, inkludert urtetilskudd, siden det er potensial for interaksjoner [se NARKOTIKAHANDEL ].
Alkohol
Pasienter bør rådes til å unngå alkohol mens de tar ZYPREXA [se NARKOTIKAHANDEL ].
Fenylketonurika
ZYPREXA 10mg ZYDIS (olanzapin oralt desintegrerende tabletter) inneholder fenylalanin (henholdsvis 0,34, 0,45, 0,67 eller 0,90 mg per 5, 10, 15 eller 20 mg tablett) [se BESKRIVELSE ].
Bruk i spesifikke populasjoner
Svangerskap
Råd kvinner til å varsle helsepersonell dersom de blir gravide eller har tenkt å bli gravide under behandling med ZYPREXA. Informer pasienter om at ZYPREXA kan forårsake ekstrapyramidale symptomer og/eller abstinenssymptomer (agitasjon, hypertoni, hypotoni, skjelving, somnolens, pustebesvær og matforstyrrelser) hos en nyfødt. Gi pasienter beskjed om at det finnes et eksponeringsregister for graviditet som overvåker graviditetsutfall hos kvinner eksponert for ZYPREXA 7,5 mg under graviditet [se Bruk i spesifikke populasjoner ].
Amming
Råd ammende kvinner som bruker ZYPREXA 20 mg for å overvåke spedbarn for overdreven sedasjon, irritabilitet, dårlig mating og ekstrapyramidale symptomer (skjelvinger og unormale muskelbevegelser) og å søke medisinsk hjelp hvis de merker disse tegnene. [se Bruk i spesifikke populasjoner ].
Infertilitet
Informer kvinner med reproduksjonsevne at ZYPREXA kan svekke fertiliteten på grunn av en økning i serumprolaktinnivået. Effektene på fertilitet er reversible [se Bruk i spesifikke populasjoner ].
Pediatrisk bruk
ZYPREXA 15 mg er indisert for behandling av schizofreni og maniske eller blandede episoder assosiert med bipolar I lidelse hos ungdom 13 til 17 år. Sammenlignet med pasienter fra kliniske studier for voksne, var det sannsynlig at ungdom gikk opp i vekt, opplevde økt sedasjon og hadde større økninger i totalkolesterol, triglyserider, LDL-kolesterol, prolaktin og hepatiske aminotransferasenivåer. Pasienter bør informeres om potensielle langsiktige risikoer forbundet med ZYPREXA og informeres om at disse risikoene kan føre til at de vurderer andre legemidler først [se INDIKASJONER OG BRUK ]. Sikkerhet og effektivitet av ZYPREXA 5mg hos pasienter under 13 år er ikke fastslått. Sikkerhet og effekt av ZYPREXA 15 mg og fluoksetin i kombinasjon hos pasienter i alderen 10 til 17 år er etablert for akutt behandling av depressive episoder assosiert med bipolar I lidelse. Sikkerhet og effektivitet av ZYPREXA og fluoksetin i kombinasjon hos pasienter ADVARSLER OG FORHOLDSREGLER og Bruk i spesifikke populasjoner ].
Behov for omfattende behandlingsprogram hos pediatriske pasienter
ZYPREXA 20mg er indisert som en integrert del av et totalt behandlingsprogram for pediatriske pasienter med schizofreni og bipolar lidelse som kan inkludere andre tiltak (psykologiske, pedagogiske, sosiale) for pasienter med lidelsen. Effektiviteten og sikkerheten til ZYPREXA 7,5 mg er ikke fastslått hos pediatriske pasienter under 13 år. Atypiske antipsykotika er ikke beregnet på bruk hos pediatriske pasienter som viser symptomer sekundært til miljøfaktorer og/eller andre primære psykiatriske lidelser. Riktig pedagogisk plassering er avgjørende og psykososial intervensjon er ofte nyttig. Beslutningen om å foreskrive atypisk antipsykotisk medisin vil avhenge av helsepersonells vurdering av kroniske og alvorlighetsgrad av pasientens symptomer [se INDIKASJONER OG BRUK ].
Ikke-klinisk toksikologi
Karsinogenese, mutagenese, svekkelse av fruktbarhet
Karsinogenese
Orale karsinogenitetsstudier ble utført på mus og rotter. Olanzapin ble administrert til mus i to 78-ukers studier i doser på 3, 10, 30/20 mg/kg/dag (tilsvarer 0,8-5 ganger daglig oral MRHD basert på mg/m² kroppsoverflate) og 0,25, 2 , 8 mg/kg/dag (tilsvarer 0,06-2 ganger daglig oral MRHD basert på mg/m² kroppsoverflate). Rotter ble dosert i 2 år i doser på 0,25, 1, 2,5, 4 mg/kg/dag (hanner) og 0,25, 1, 4, 8 mg/kg/dag (hunn) (tilsvarer 0,13-2 og 0,13-4) ganger daglig oral MRHD basert på henholdsvis mg/m² kroppsoverflate). Forekomsten av leverhemangiomer og hemangiosarkomer var signifikant økt i 1 musestudie på hunnmus ved 2 ganger daglig oral MRHD basert på mg/m² kroppsoverflate. Disse svulstene ble ikke økt i en annen musestudie på kvinner som ble doseret opptil 2-5 ganger den daglige orale MRHD basert på mg/m² kroppsoverflate; i denne studien var det en høy forekomst av tidlig dødelighet hos menn i 30/20 mg/kg/dag-gruppen. Forekomsten av brystkjerteladenomer og adenokarsinomer var signifikant økt hos hunnmus med doser på ≥2 mg/kg/dag og hos hunnrotter dosert med ≥4 mg/kg/dag (0,5 og 2 ganger daglig oral MRHD basert på mg/m²) henholdsvis kroppsoverflate). Antipsykotiske legemidler har vist seg å kronisk øke prolaktinnivået hos gnagere. Serumprolaktinnivåer ble ikke målt under olanzapin karsinogenitetsstudier; målinger under subkroniske toksisitetsstudier viste imidlertid at olanzapin økte serumprolaktinnivået opptil 4 ganger hos rotter ved de samme dosene som ble brukt i karsinogenitetsstudien. En økning i brystkjertelneoplasmer er funnet hos gnagere etter kronisk administrering av andre antipsykotiske legemidler og anses å være prolaktinmediert. Relevansen for menneskelig risiko for funn av prolaktinmedierte endokrine svulster hos gnagere er ukjent [se ADVARSLER OG FORHOLDSREGLER ].
Mutagenese
Ingen bevis for genotoksisk potensiale for olanzapin ble funnet i Ames revers mutasjonstest, in vivo mikronukleustest i mus, kromosomavvikstest i kinesisk hamster ovarieceller, ikke-planlagt DNA-syntesetest i rottehepatocytter, induksjon av forovermutasjonstest i muselymfomceller , eller in vivo søsterkromatidutvekslingstest i benmarg hos kinesiske hamstere.
Nedsatt fruktbarhet
en oral fertilitets- og reproduksjonsstudie hos rotter ble parringsytelsen hos hanner, men ikke fertiliteten, svekket ved en dose på 22,4 mg/kg/dag, og hunnens fertilitet ble redusert ved en dose på 3 mg/kg/dag (11 og 1,5). ganger daglig oral MRHD basert på henholdsvis mg/m² kroppsoverflate). Seponering av olanzapinbehandling reverserte effektene på mannlig parringsytelse. Hos hunnrotter ble den prekoitale perioden økt og paringsindeksen redusert med 5 mg/kg/dag (2,5 ganger den daglige orale MRHD basert på mg/m² kroppsoverflate). Diestrous ble forlenget og brunst forsinket med 1,1 mg/kg/dag (0,6 ganger daglig oral MRHD basert på mg/m² kroppsoverflateareal); derfor kan olanzapin gi en forsinkelse i eggløsningen.
Bruk i spesifikke populasjoner
Når du bruker ZYPREXA og fluoksetin i kombinasjon, se også avsnittet Bruk i spesifikke populasjoner i pakningsvedlegget til Symbyax.
Svangerskap
Eksponeringsregister for graviditet
Det finnes et graviditetseksponeringsregister som overvåker graviditetsutfall hos kvinner som eksponeres for atypiske antipsykotika, inkludert ZYPREXA, under graviditet. Helsepersonell oppfordres til å registrere pasienter ved å kontakte National Pregnancy Registry for Atypical Antipsychotics på 1-866-961-2388 eller besøk http://womensmentalhealth.org/clinical-and-research-programs/pregnancyregistry/.
Risikosammendrag
Nyfødte eksponert for antipsykotiske legemidler, inkludert ZYPREXA, i løpet av tredje trimester har risiko for ekstrapyramidale og/eller abstinenssymptomer etter fødsel (se Kliniske betraktninger ). Samlet tilgjengelige data fra publiserte epidemiologiske studier av gravide kvinner eksponert for olanzapin har ikke etablert en medikamentassosiert risiko for alvorlige fødselsskader, spontanabort eller uønskede utfall hos mor eller foster (se Data ). Det er risiko for moren forbundet med ubehandlet schizofreni eller bipolar lidelse I og med eksponering for antipsykotika, inkludert ZYPREXA 7,5 mg, under graviditet (se Kliniske betraktninger ).
Olanzapin var ikke teratogent når det ble gitt oralt til drektige rotter og kaniner i doser som er 9- og 30 ganger den daglige orale maksimale anbefalte humane dosen (MRHD), basert på mg/m² kroppsoverflate; noen føtale toksisiteter ble observert ved disse dosene (se Data ).
Estimert bakgrunnsrisiko for alvorlige fødselsskader og spontanabort for de angitte populasjonene er ukjent. Alle graviditeter har en bakgrunnsrisiko for fødselsskader, tap eller andre uheldige utfall. I den generelle befolkningen i USA er den estimerte bakgrunnsrisikoen for alvorlige fødselsskader og spontanabort i klinisk anerkjente svangerskap henholdsvis 2 % til 4 % og 15 % til 20 %.
Kliniske betraktninger
Sykdomsassosiert mors- og embryo-/fosterrisiko
Det er en risiko for mor fra ubehandlet schizofreni eller bipolar lidelse I, inkludert økt risiko for tilbakefall, sykehusinnleggelse og selvmord. Schizofreni og bipolar lidelse I er assosiert med økte uønskede perinatale utfall, inkludert prematur fødsel. Det er ikke kjent om dette er et direkte resultat av sykdommen eller andre komorbide faktorer.
Fetale/neonatale bivirkninger
Ekstrapyramidale og/eller abstinenssymptomer, inkludert agitasjon, hypertoni, hypotoni, skjelving, somnolens, pustebesvær og matforstyrrelser er rapportert hos nyfødte som ble eksponert for antipsykotiske legemidler, inkludert ZYPREXA 2,5 mg, i løpet av tredje trimester av svangerskapet. Disse symptomene har variert i alvorlighetsgrad. Overvåk nyfødte for ekstrapyramidale og/eller abstinenssymptomer og håndter symptomene på riktig måte. Noen nyfødte kom seg i løpet av timer eller dager uten spesifikk behandling; andre krevde langvarig sykehusinnleggelse.
Data
Menneskelige data
Placentapassasje er rapportert i publiserte studierapporter; placentapassasjeraten var imidlertid svært varierende, varierende mellom 7 % og 167 % ved fødselen etter eksponering under graviditet. Den kliniske relevansen av dette funnet er ukjent.
Publiserte data fra observasjonsstudier, fødselsregistre og kasusrapporter som har evaluert bruk av atypiske antipsykotika under graviditet, fastslår ikke økt risiko for store fødselsskader. En retrospektiv kohortstudie fra en Medicaid-database med 9258 kvinner eksponert for antipsykotika under graviditet indikerte ikke en samlet økt risiko for alvorlige fødselsskader.
Dyredata
orale reproduksjonsstudier på rotter med doser opptil 18 mg/kg/dag og kaniner ved doser opptil 30 mg/kg/dag (henholdsvis 9 og 30 ganger daglig oral MRHD basert på mg/m² kroppsoverflateareal). ingen tegn på teratogenitet ble observert. I en oral rotteteratologistudie ble tidlige resorpsjoner og økt antall ikke-levedyktige fostre observert ved en dose på 18 mg/kg/dag (9 ganger den daglige orale MRHD basert på mg/m² kroppsoverflate), og svangerskapet ble forlenget ved 10. mg/kg/dag (5 ganger daglig oral MRHD basert på mg/m² kroppsoverflate). I en oral kanin-teratologistudie oppsto føtal toksisitet som økte resorpsjoner og redusert fostervekt ved en maternal toksisk dose på 30 mg/kg/dag (30 ganger daglig oral MRHD basert på mg/m² kroppsoverflate).
Amming
Risikosammendrag
Olanzapin finnes i morsmelk. Det er rapportert for mye sedasjon, irritabilitet, dårlig mating og ekstrapyramidale symptomer (skjelvinger og unormale muskelbevegelser) hos spedbarn som er eksponert for olanzapin gjennom morsmelk (se Kliniske betraktninger ). Det er ingen informasjon om effekten av olanzapin på melkeproduksjonen.
De utviklingsmessige og helsemessige fordelene ved amming bør vurderes sammen med morens kliniske behov for ZYPREXA og eventuelle bivirkninger på det ammede barnet fra ZYPREXA eller fra morens underliggende tilstand.
Kliniske betraktninger
Spedbarn som eksponeres for ZYPREXA 7,5 mg bør overvåkes for overdreven sedasjon, irritabilitet, dårlig mating og ekstrapyramidale symptomer (skjelvinger og unormale muskelbevegelser).
Kvinner og menn med reproduktivt potensial
Infertilitet
Kvinner
Basert på den farmakologiske virkningen av olanzapin (D2-reseptorantagonisme), kan behandling med ZYPREXA resultere i en økning i serumprolaktinnivåer, noe som kan føre til en reversibel reduksjon i fertilitet hos kvinner med reproduksjonspotensial [se ADVARSLER OG FORHOLDSREGLER ].
Pediatrisk bruk
Sikkerheten og effektiviteten til oral ZYPREXA ved behandling av schizofreni og maniske eller blandede episoder assosiert med bipolar I-lidelse ble fastslått i korttidsstudier hos ungdom (i alderen 13 til 17 år). Bruk av ZYPREXA hos ungdom støttes av bevis fra tilstrekkelige og godt kontrollerte studier av ZYPREXA 5 mg der 268 ungdommer fikk ZYPREXA 20 mg i et område på 2,5 til 20 mg/dag [se Kliniske studier ]. Anbefalt startdose for ungdom er lavere enn for voksne [se DOSERING OG ADMINISTRASJON ]. Sammenlignet med pasienter fra kliniske studier for voksne, var det sannsynlig at ungdom gikk opp i vekt, opplevde økt sedasjon og hadde større økninger i totalkolesterol, triglyserider, LDL-kolesterol, prolaktin og hepatiske aminotransferasenivåer [se ADVARSLER OG FORHOLDSREGLER og BIVIRKNINGER ]. Når de skal velge blant de alternative behandlingene som er tilgjengelige for ungdom, bør klinikere vurdere det økte potensialet (hos ungdom sammenlignet med voksne) for vektøkning og dyslipidemi. Klinikere bør vurdere den potensielle langsiktige risikoen når de forskriver til ungdom, og i mange tilfeller kan dette føre til at de vurderer å foreskrive andre legemidler først hos ungdom [se INDIKASJONER OG BRUK ].
Sikkerhet og effekt av olanzapin hos barn PASIENTINFORMASJON ].
Sikkerhet og effekt av ZYPREXA 7,5 mg og fluoksetin i kombinasjon hos barn og ungdom (10 til 17 år) er etablert for akutt behandling av depressive episoder assosiert med bipolar lidelse I.
Sikkerhet og effektivitet av ZYPREXA og fluoksetin i kombinasjon hos barn
Geriatrisk bruk
Av de 2500 pasientene i premarketing kliniske studier med oral olanzapin, var 11 % (263) 65 år eller eldre. Hos pasienter med schizofreni var det ingen indikasjon på noen annen tolerabilitet av olanzapin hos eldre sammenlignet med yngre pasienter. Studier på eldre pasienter med demensrelatert psykose har antydet at det kan være en annen toleranseprofil i denne populasjonen sammenlignet med yngre pasienter med schizofreni. Eldre pasienter med demensrelatert psykose behandlet med olanzapin har økt risiko for død sammenlignet med placebo. I placebokontrollerte studier av olanzapin hos eldre pasienter med demensrelatert psykose, var det en høyere forekomst av cerebrovaskulære bivirkninger (f.eks. slag, forbigående iskemisk anfall) hos pasienter behandlet med olanzapin sammenlignet med pasienter behandlet med placebo. Olanzapin er ikke godkjent for behandling av pasienter med demensrelatert psykose. Tilstedeværelsen av faktorer som kan redusere farmakokinetisk clearance eller øke den farmakodynamiske responsen på olanzapin bør også føre til vurdering av en lavere startdose for enhver geriatrisk pasient [se ADVARSEL i boks , DOSERING OG ADMINISTRASJON , og ADVARSLER OG FORHOLDSREGLER ].
Kliniske studier av ZYPREXA og fluoksetin i kombinasjon inkluderte ikke tilstrekkelig antall pasienter ≥65 år til å avgjøre om de responderer annerledes enn yngre pasienter.
OVERDOSE
Menneskelig erfaring
I premarketing-studier som involverte mer enn 3100 pasienter og/eller normale forsøkspersoner, ble utilsiktet eller tilsiktet akutt overdosering av olanzapin identifisert hos 67 pasienter. Hos pasienten som tok den største identifiserte mengden, 300 mg, var de eneste symptomene som ble rapportert døsighet og sløret tale. Hos det begrensede antallet pasienter som ble evaluert på sykehus, inkludert pasienten som tok 300 mg, var det ingen observasjoner som indikerte en negativ endring i laboratorieanalytter eller EKG. Vitale tegn var vanligvis innenfor normale grenser etter overdoser.
postmarketingrapporter om overdosering med olanzapin alene, har symptomer blitt rapportert i de fleste tilfellene. Hos symptomatiske pasienter inkluderte symptomer med ≥10 % forekomst agitasjon/aggressivitet, dysartri, takykardi, ulike ekstrapyramidale symptomer og redusert bevissthetsnivå fra sedasjon til koma. Blant mindre vanlige rapporterte symptomer var følgende potensielt medisinsk alvorlige reaksjoner: aspirasjon, hjerte-lungestans, hjertearytmier (som supraventrikulær takykardi og 1 pasient som opplevde sinuspause med spontan gjenopptakelse av normal rytme), delirium, mulig nevroleptisk respiratorisk depresjon/respiratorisk depresjon. , kramper, hypertensjon og hypotensjon. Eli Lilly and Company har mottatt rapporter om dødsfall i forbindelse med overdose av olanzapin alene. I 1 tilfelle av død ble mengden akutt inntatt olanzapin rapportert å være muligens så lav som 450 mg oral olanzapin; I et annet tilfelle ble det imidlertid rapportert at en pasient overlevde et akutt olanzapininntak av ca. 2 g oralt olanzapin.
Håndtering av overdose
For aktuell informasjon om behandling av ZYPREXA (olanzapin) overdose, kontakt et sertifisert giftkontrollsenter (1-800-222-1222 eller www.poison.org). Muligheten for multippel legemiddelinvolvering bør vurderes. Ved akutt overdosering, etablere og vedlikeholde en luftvei og sikre tilstrekkelig oksygenering og ventilasjon, som kan inkludere intubasjon. Mageskylling (etter intubasjon, hvis pasienten er bevisstløs) og administrering av aktivt kull sammen med et avføringsmiddel bør vurderes. Administrering av aktivt kull (1 g) reduserte Cmax og AUC for oralt olanzapin med ca. 60 %. Siden toppnivåer av olanzapin vanligvis ikke oppnås før ca. 6 timer etter dosering, kan kull være en nyttig behandling for overdosering av olanzapin.
Muligheten for obtundation, anfall eller dystoniske reaksjoner i hode og nakke etter overdose kan skape en risiko for aspirasjon med indusert emesis. Kardiovaskulær overvåking bør starte umiddelbart og bør inkludere kontinuerlig elektrokardiografisk overvåking for å oppdage mulige arytmier.
Det finnes ingen spesifikk motgift mot olanzapin. Derfor bør passende støttetiltak settes i gang. Hypotensjon og sirkulasjonskollaps bør behandles med passende tiltak som intravenøse væsker og/eller sympatomimetika. (Ikke bruk epinefrin, dopamin eller andre sympatomimetika med beta-agonistaktivitet, siden betastimulering kan forverre hypotensjon ved olanzapin-indusert alfablokkade.) Nøye medisinsk tilsyn og overvåking bør fortsette til pasienten blir frisk.
For spesifikk informasjon om overdosering med litium eller valproat, se avsnittet Overdosering i pakningsvedlegget for disse produktene. For spesifikk informasjon om overdosering med olanzapin og fluoksetin i kombinasjon, se avsnittet Overdosering i pakningsvedlegget til Symbyax.
KONTRAINDIKASJONER
- . Ingen med ZYPREXA monoterapi. . Når du bruker ZYPREXA og fluoksetin i kombinasjon, se også avsnittet Kontraindikasjoner i pakningsvedlegget for Symbyax. . For spesifikk informasjon om kontraindikasjoner for litium eller valproat, se avsnittet Kontraindikasjoner i pakningsvedlegget for disse andre produktene.
KLINISK FARMAKOLOGI
Virkningsmekanismen
Virkningsmekanismen til olanzapin i de listede indikasjonene er uklar. Effekten av olanzapin ved schizofreni kan imidlertid medieres gjennom en kombinasjon av dopamin og serotonin type 2 (5HT2) antagonisme.
Farmakodynamikk
Olanzapin binder seg med høy affinitet til følgende reseptorer: serotonin 5HT2A/2C, 5HT6 (henholdsvis Ki=4, 11 og 5 nM), dopamin D1-4 (Ki=11-31 nM), histamin H1 (Ki=7 nM). ), og adrenerge al-reseptorer (Ki=19 nM). Olanzapin er en antagonist med moderat affinitetsbinding for henholdsvis serotonin 5HT3 (Ki=57 nM) og muskarin M1-5 (Ki=73, 96, 132, 32 og 48 nM). Olanzapin binder seg med lav affinitet til GABAA, BZD og β-adrenerge reseptorer (Ki>10 μM).
Farmakokinetikk
Oral administrasjon, monoterapi
Olanzapin absorberes godt og når maksimal konsentrasjon i løpet av ca. 6 timer etter en oral dose. Det elimineres i stor grad ved førstegangsmetabolisme, med omtrent 40 % av dosen metabolisert før den når den systemiske sirkulasjonen. Mat påvirker ikke hastigheten eller omfanget av olanzapinabsorpsjon. Farmakokinetiske studier viste at ZYPREXA 5 mg tabletter og ZYPREXA ZYDIS (olanzapin oralt disintegrerende tabletter) doseringsformer av olanzapin er bioekvivalente.
Olanzapin viser lineær kinetikk over det kliniske doseringsområdet. Halveringstiden varierer fra 21 til 54 timer (5. til 95. persentil; gjennomsnittlig 30 timer), og tilsynelatende plasmaclearance varierer fra 12 til 47 l/time (5. til 95. persentil; gjennomsnittlig 25 l/time).
Administrering av olanzapin én gang daglig fører til steady-state konsentrasjoner i løpet av ca. 1 uke som er omtrent det dobbelte av konsentrasjonene etter enkeltdoser. Plasmakonsentrasjoner, halveringstid og clearance av olanzapin kan variere mellom individer på grunnlag av røykestatus, kjønn og alder.
Olanzapin er omfattende distribuert over hele kroppen, med et distribusjonsvolum på ca. 1000 L. Det er 93 % bundet til plasmaproteiner over konsentrasjonsområdet 7 til 1100 ng/ml, og binder primært til albumin og α1-syreglykoprotein.
Metabolisme og eliminering
Etter en enkelt oral dose av 14C-merket olanzapin, ble 7 % av dosen av olanzapin gjenvunnet i urinen som uendret legemiddel, noe som indikerer at olanzapin er høyt metabolisert. Omtrent 57 % og 30 % av dosen ble gjenfunnet i henholdsvis urin og avføring. I plasma utgjorde olanzapin bare 12 % av AUC for total radioaktivitet, noe som indikerer betydelig eksponering for metabolitter. Etter gjentatt dosering var de viktigste sirkulerende metabolittene 10-N-glukuronid, tilstede ved steady state ved 44 % av konsentrasjonen av olanzapin, og 4´-N-desmetylolanzapin, tilstede ved steady state ved 31 % av konsentrasjonen av olanzapin . Begge metabolittene mangler farmakologisk aktivitet ved de observerte konsentrasjonene.
Direkte glukuronidering og cytokrom P450 (CYP)-mediert oksidasjon er de primære metabolske veiene for olanzapin. In vitro-studier tyder på at CYP 1A2 og 2D6, og det flavinholdige monooksygenasesystemet er involvert i olanzapinoksidasjon. CYP2D6-mediert oksidasjon ser ut til å være en mindre metabolsk vei in vivo, fordi clearance av olanzapin ikke er redusert hos personer med mangel på dette enzymet.
Intramuskulær administrasjon
ZYPREXA IntraMuscular resulterer i rask absorpsjon med maksimal plasmakonsentrasjon innen 15 til 45 minutter. Basert på en farmakokinetisk studie hos friske frivillige, gir en dose på 5 mg intramuskulært olanzapin til injeksjon i gjennomsnitt en maksimal plasmakonsentrasjon som er omtrent 5 ganger høyere enn den maksimale plasmakonsentrasjonen produsert av en 5 mg dose oralt olanzapin. Arealet under kurven oppnådd etter en intramuskulær dose er lik det som oppnås etter oral administrering av samme dose. Halveringstiden observert etter intramuskulær administrering er lik den som observeres etter oral dosering. Farmakokinetikken er lineær over det kliniske doseringsområdet. Metabolske profiler etter intramuskulær administrering er kvalitativt lik metabolske profiler etter oral administrering.
Spesifikke populasjoner
Nedsatt nyrefunksjon
Fordi olanzapin er sterkt metabolisert før utskillelse og bare 7 % av legemidlet skilles ut uendret, er det usannsynlig at nyresvikt alene vil ha stor innvirkning på farmakokinetikken til olanzapin. De farmakokinetiske egenskapene til olanzapin var like hos pasienter med alvorlig nedsatt nyrefunksjon og normale personer, noe som indikerer at dosejustering basert på graden av nedsatt nyrefunksjon ikke er nødvendig. I tillegg fjernes ikke olanzapin ved dialyse. Effekten av nedsatt nyrefunksjon på metabolitteliminasjon er ikke studert.
Nedsatt leverfunksjon
Selv om tilstedeværelsen av nedsatt leverfunksjon kan forventes å redusere clearance av olanzapin, viste en studie av effekten av nedsatt leverfunksjon hos personer (n=6) med klinisk signifikant (Childs Pugh Klassifikasjon A og B) cirrhose liten effekt på farmakokinetikken. av olanzapin.
Geriatrisk
en studie med 24 friske forsøkspersoner, var gjennomsnittlig eliminasjonshalveringstid for olanzapin omtrent 1,5 ganger høyere hos eldre (≥65 år) enn hos ikke-eldre forsøkspersoner ( DOSERING OG ADMINISTRASJON ].
Kjønn
Clearance av olanzapin er omtrent 30 % lavere hos kvinner enn hos menn. Det var imidlertid ingen tilsynelatende forskjeller mellom menn og kvinner i effektivitet eller bivirkninger. Doseendringer basert på kjønn bør ikke være nødvendig.
Røykestatus
Olanzapinclearance er omtrent 40 % høyere hos røykere enn hos ikke-røykere, selv om dosejusteringer ikke er rutinemessig anbefalt.
Løp
In vivo-studier har vist at eksponeringen er lik blant japanere, kinesere og kaukasiere, spesielt etter normalisering for kroppsvektsforskjeller. Doseendringer for rase anbefales derfor ikke.
Kombinerte effekter
De kombinerte effektene av alder, røyking og kjønn kan føre til betydelige farmakokinetiske forskjeller i populasjoner. Clearance hos unge røykende menn, for eksempel, kan være 3 ganger høyere enn hos eldre ikke-røykende kvinner. Dosejustering kan være nødvendig hos pasienter som viser en kombinasjon av faktorer som kan resultere i langsommere metabolisme av olanzapin [se DOSERING OG ADMINISTRASJON ].
Ungdom (alder 13 til 17 år)
I kliniske studier var de fleste ungdommene ikke-røykere, og denne populasjonen hadde en lavere gjennomsnittlig kroppsvekt, noe som resulterte i høyere gjennomsnittlig eksponering for olanzapin sammenlignet med voksne.
Dyretoksikologi og/eller farmakologi
dyrestudier med olanzapin var de viktigste hematologiske funnene reversible perifere cytopenier hos individuelle hunder dosert med 10 mg/kg (17 ganger daglig oral MRHD basert på mg/m² kroppsoverflate), doserelaterte reduksjoner i lymfocytter og nøytrofiler hos mus , og lymfopeni hos rotter. Noen få hunder behandlet med 10 mg/kg utviklet reversibel nøytropeni og/eller reversibel hemolytisk anemi mellom 1 og 10 måneders behandling. Doserelaterte reduksjoner i lymfocytter og nøytrofiler ble sett hos mus som fikk doser på 10 mg/kg (lik 2 ganger daglig oral MRHD basert på mg/m² kroppsoverflate) i studier av 3 måneders varighet. Uspesifikk lymfopeni, forenlig med redusert kroppsvektøkning, forekom hos rotter som fikk 22,5 mg/kg (11 ganger daglig oral MRHD basert på mg/m² kroppsoverflate) i 3 måneder eller 16 mg/kg (8 ganger daglig oral MRHD basert på på mg/m² kroppsoverflate) i 6 eller 12 måneder. Ingen tegn på benmargscytotoksisitet ble funnet hos noen av de undersøkte artene. Benmarg var normocellulært eller hypercellulært, noe som indikerer at reduksjonen i sirkulerende blodceller sannsynligvis skyldtes perifere (ikke-marg) faktorer.
Kliniske studier
Når du bruker ZYPREXA 7,5 mg og fluoksetin i kombinasjon, se også avsnittet om kliniske studier i pakningsvedlegget til Symbyax.
Schizofreni
Voksne
Effekten av oral olanzapin i behandlingen av schizofreni ble fastslått i 2 korttids (6 ukers) kontrollerte studier med voksne inneliggende pasienter som oppfylte DSM III-R-kriteriene for schizofreni. En enkelt haloperidolarm ble inkludert som en sammenlignende behandling i 1 av de 2 studiene, men denne studien sammenlignet ikke disse 2 legemidlene på hele spekteret av klinisk relevante doser for begge.
Flere instrumenter ble brukt for å vurdere psykiatriske tegn og symptomer i disse studiene, blant dem Brief Psychiatric Rating Scale (BPRS), en multi-element inventar av generell psykopatologi som tradisjonelt brukes til å evaluere effekten av medikamentell behandling ved schizofreni. BPRS-psykoseklyngen (konseptuell desorganisering, hallusinatorisk atferd, mistenksomhet og uvanlig tankeinnhold) anses som en spesielt nyttig undergruppe for vurdering av aktivt psykotiske schizofrene pasienter. En annen tradisjonell vurdering, Clinical Global Impression (CGI), gjenspeiler inntrykket av en dyktig observatør, fullt kjent med manifestasjonene av schizofreni, om den generelle kliniske tilstanden til pasienten. I tillegg ble det brukt 2 mer nylig utviklede skalaer; disse inkluderte 30-elementers positive og negative skala (PANSS), der de 18 elementene i BPRS er innebygd, og skalaen for vurdering av negative symptomer (SANS). Prøvesammendragene nedenfor fokuserer på følgende resultater: PANSS total og/eller BPRS total; BPRS psykose cluster; PANSS negativ underskala eller SANS; og CGI-alvorlighet. Resultatene av forsøkene følger:
(1) I en 6-ukers, placebokontrollert studie (n=149) som involverte 2 faste olanzapindoser på 1 og 10 mg/dag (en gang daglig), olanzapin med 10 mg/dag (men ikke 1 mg/dag). dag), var overlegen placebo på PANSS-totalskåren (også på den ekstraherte BPRS-totalen), på BPRS-psykoseklyngen, på PANSS Negative-subskalaen og på CGI-alvorlighet.
(2) I en 6-ukers, placebokontrollert studie (n=253) som involverte 3 faste doseområder av olanzapin (5 ± 2,5 mg/dag, 10 ± 2,5 mg/dag og 15 ± 2,5 mg/dag) på en én gang daglig, var de 2 høyeste olanzapindosegruppene (faktiske gjennomsnittlige doser på henholdsvis 12 og 16 mg/dag) overlegne placebo på BPRS totalskåre, BPRS psykosekluster og CGI alvorlighetsgrad; den høyeste olanzapindosegruppen var overlegen placebo på SANS. Det var ingen klar fordel for høydosegruppen fremfor middelsdosegruppen.
(3) I en langtidsstudie ble voksne polikliniske pasienter (n=326) som hovedsakelig oppfylte DSM-IV-kriteriene for schizofreni og som holdt seg stabile på olanzapin under åpen behandling i minst 8 uker, randomisert til å fortsette med sitt nåværende olanzapin doser (fra 10 til 20 mg/dag) eller til placebo. Oppfølgingsperioden for å observere pasienter for tilbakefall, definert i form av økning i BPRS-positive symptomer eller sykehusinnleggelse, var planlagt i 12 måneder, men kriterier ble oppfylt for å stoppe studien tidlig på grunn av et overskudd av placebo-tilbakefall sammenlignet med tilbakefall av olanzapin , og olanzapin var overlegen placebo i tide til tilbakefall, det primære resultatet for denne studien. Således var olanzapin mer effektivt enn placebo til å opprettholde effekt hos pasienter stabilisert i ca. 8 uker og fulgt i en observasjonsperiode på opptil 8 måneder.
Undersøkelse av populasjonsundergrupper (rase og kjønn) avdekket ingen differensiell respons på grunnlag av disse undergruppene.
Ungdom
Effekten av oral olanzapin ved akutt behandling av schizofreni hos ungdom (alder 13 til 17 år) ble fastslått i en 6-ukers dobbeltblind, placebokontrollert, randomisert studie av innlagte og polikliniske pasienter med schizofreni (n=107) som møtte diagnostiske kriterier i henhold til DSM-IV-TR og bekreftet av Kiddie Schedule for Affective Disorders and Schizophrenia for School Aged Children-Present and Lifetime Version (K-SADS-PL).
Det primære vurderingsinstrumentet som ble brukt for å vurdere psykiatriske tegn og symptomer i denne studien var den forankrede versjonen av den totale poengsummen for kort psykiatrisk vurderingsskala for barn (BPRS-C).
denne fleksible dosestudien var olanzapin 2,5 til 20 mg/dag (gjennomsnittlig modal dose 12,5 mg/dag, gjennomsnittlig dose på 11,1 mg/dag) mer effektivt enn placebo i behandlingen av ungdom diagnostisert med schizofreni, som støttet av statistisk signifikant større gjennomsnittlig reduksjon i BPRS-C totalskåre for pasienter i olanzapinbehandlingsgruppen enn i placebogruppen.
Selv om det ikke er noen bevis tilgjengelig for å svare på spørsmålet om hvor lenge ungdomspasienten som behandles med ZYPREXA bør opprettholdes, kan vedlikeholdseffekt ekstrapoleres fra voksne data sammen med sammenligninger av olanzapin farmakokinetiske parametere hos voksne og ungdom. Det anbefales generelt at pasienter med respons fortsetter utover den akutte responsen, men med den laveste dosen som er nødvendig for å opprettholde remisjon. Pasienter bør med jevne mellomrom revurderes for å fastslå behovet for vedlikeholdsbehandling.
Bipolar I-lidelse (maniske eller blandede episoder)
Voksne
Monoterapi
Effekten av oral olanzapin ved behandling av maniske eller blandede episoder ble fastslått i 2 korttids (en 3-ukers og en 4-ukers) placebokontrollerte studier hos voksne pasienter som oppfylte DSM-IV-kriteriene for bipolar I-lidelse med maniske eller blandede episoder. Disse studiene inkluderte pasienter med eller uten psykotiske trekk og med eller uten et hurtigsyklingsforløp.
Det primære vurderingsinstrumentet som ble brukt for å vurdere maniske symptomer i disse forsøkene var Young Mania Rating Scale (Y-MRS), en 11-elements kliniker-vurdert skala som tradisjonelt brukes til å vurdere graden av manisk symptomatologi (irritabilitet, forstyrrende/aggressiv atferd, søvn). , forhøyet humør, tale, økt aktivitet, seksuell interesse, språk-/tankeforstyrrelser, tankeinnhold, utseende og innsikt) i området fra 0 (ingen maniske trekk) til 60 Â (maksimal poengsum). Det primære resultatet i disse studiene var endring fra baseline i Y-MRS totalscore. Resultatene av forsøkene følger:
(1) I en 3-ukers placebokontrollert studie (n=67) som involverte et doseområde av olanzapin (5-20 mg/dag, én gang daglig, med start på 10 mg/dag), var olanzapin overlegen placebo i reduksjon av Y-MRS totalscore. I en identisk designet studie utført samtidig med den første studien, viste olanzapin en lignende behandlingsforskjell, men muligens på grunn av prøvestørrelse og stedvariasjon, ble det ikke vist å være overlegen placebo på dette utfallet.
(2) I en 4-ukers placebokontrollert studie (n=115) som involverte et doseområde av olanzapin (5-20 mg/dag, én gang daglig, med start ved 15 mg/dag), var olanzapin overlegen placebo i reduksjon av Y-MRS totalscore.
(3) I en annen studie, 361 pasienter som oppfyller DSM-IV-kriteriene for en manisk eller blandet episode av bipolar I-lidelse som hadde respondert under en innledende åpen behandlingsfase i ca. 2 uker i gjennomsnitt på olanzapin 5 til 20 mg/ dag ble randomisert til enten fortsettelse av olanzapin med samme dose (n=225) eller til placebo (n=136), for observasjon av tilbakefall. Omtrent 50 % av pasientene hadde avsluttet behandlingen fra olanzapingruppen på dag 59 og 50 % av placebogruppen hadde avbrutt på dag 23 av dobbeltblind behandling. Respons under den åpne fasen ble definert ved å ha en reduksjon av Y-MRS totalscore til ≤12 og HAM-D 21 til ≤8. Tilbakefall under den dobbeltblinde fasen ble definert som en økning av Y-MRS eller HAM-D 21 totalskåre til ≥15, eller å bli innlagt på sykehus for enten mani eller depresjon. I den randomiserte fasen opplevde pasienter som fikk fortsatt olanzapin betydelig lengre tid til tilbakefall.
Tilskudd til litium eller valproat
Effekten av oral olanzapin med samtidig litium eller valproat ved behandling av maniske eller blandede episoder ble fastslått i 2 kontrollerte studier hos pasienter som oppfylte DSM-IV-kriteriene for bipolar I lidelse med maniske eller blandede episoder. Disse studiene inkluderte pasienter med eller uten psykotiske trekk og med eller uten et hurtigsyklingsforløp. Resultatene av forsøkene følger:
(1) I en 6-ukers placebokontrollert kombinasjonsstudie ble 175 polikliniske pasienter på litium- eller valproatbehandling med utilstrekkelig kontrollerte maniske eller blandede symptomer (Y-MRS ≥16) randomisert til å motta enten olanzapin eller placebo, i kombinasjon med sin opprinnelige behandling . Olanzapin (i et doseområde på 5-20 mg/dag, én gang daglig, med start ved 10 mg/dag) kombinert med litium eller valproat (i et terapeutisk område på 0,6 mEq/L til 1,2 mEq/L eller 50 μg/ml til 125 μg/mL, henholdsvis) var overlegen litium eller valproat alene i reduksjonen av Y-MRS totalscore.
(2) I en andre 6-ukers placebokontrollert kombinasjonsstudie ble 169 polikliniske pasienter på litium- eller valproatbehandling med utilstrekkelig kontrollerte maniske eller blandede symptomer (Y-MRS ≥16) randomisert til å motta enten olanzapin eller placebo, i kombinasjon med deres opprinnelige terapi. Olanzapin (i et doseområde på 5-20 mg/dag, én gang daglig, med start ved 10 mg/dag) kombinert med litium eller valproat (i et terapeutisk område på 0,6 mEq/L til 1,2 mEq/L eller 50 μg/ml til 125 μg/mL, henholdsvis) var overlegen litium eller valproat alene i reduksjonen av Y-MRS totalscore.
Ungdom
Akutt monoterapi
Effekten av oralt olanzapin ved behandling av akutte maniske eller blandede episoder hos ungdom (alder 13 til 17 år) ble fastslått i en 3-ukers, dobbeltblind, placebokontrollert, randomisert studie av innlagte og polikliniske ungdommer som møtte diagnosen. kriterier for maniske eller blandede episoder assosiert med bipolar lidelse I (med eller uten psykotiske trekk) i henhold til DSM-IV-TR (n=161). Diagnosen ble bekreftet av K-SADS-PL.
Det primære vurderingsinstrumentet som ble brukt for å vurdere maniske symptomer i denne studien var den totale poengsummen for ungdomsstrukturert Young-Mania Rating Scale (Y-MRS).
denne fleksible dosestudien var olanzapin 2,5 til 20 mg/dag (gjennomsnittlig modal dose 10,7 mg/dag, gjennomsnittlig dose på 8,9 mg/dag) mer effektivt enn placebo i behandlingen av ungdom med maniske eller blandede episoder assosiert med bipolar I lidelse, som støttet av den statistisk signifikant større gjennomsnittlige reduksjonen i Y-MRS totalskåre for pasienter i olanzapinbehandlingsgruppen enn i placebogruppen.
Selv om det ikke er noen bevis tilgjengelig for å svare på spørsmålet om hvor lenge ungdomspasienten som behandles med ZYPREXA bør opprettholdes, kan vedlikeholdseffekt ekstrapoleres fra voksne data sammen med sammenligninger av olanzapin farmakokinetiske parametere hos voksne og ungdom. Det anbefales generelt at pasienter med respons fortsetter utover den akutte responsen, men med den laveste dosen som er nødvendig for å opprettholde remisjon. Pasienter bør med jevne mellomrom revurderes for å fastslå behovet for vedlikeholdsbehandling.
Agitasjon assosiert med schizofreni og bipolar I-mani
Effekten av intramuskulært olanzapin til injeksjon for behandling av agitasjon ble fastslått i 3 kortsiktige (24 timers IM-behandling) placebokontrollerte studier hos urolige voksne innleggende pasienter fra 2 diagnostiske grupper: schizofreni og bipolar lidelse I (maniske eller blandede episoder) . Hver av studiene inkluderte en enkelt aktiv komparatorbehandlingsarm av enten haloperidolinjeksjon (schizofrenistudier) eller lorazepaminjeksjon (bipolar I-manistudie). Pasienter som ble registrert i studiene måtte: (1) bedømmes av de kliniske etterforskerne som klinisk opphisset og klinisk passende kandidater for behandling med intramuskulær medisin, og (2) utvise et nivå av agitasjon som nådde eller oversteg en terskelscore på ≥14 på de 5 elementene som består av positiv og negativ syndromskala (PANSS) Excited Component (dvs. dårlig impulskontroll, spenning, fiendtlighet, manglende samarbeidsevne og spenningselementer) med minst 1 individuell elementscore ≥4 ved bruk av et 1-7 poengsystem (1= fraværende, 4 = moderat, 7 = ekstrem). I studiene var gjennomsnittlig baseline PANSS Excited Component-skåre 18,4, med skårer fra 13 til 32 (av en maksimal score på 35), noe som tyder på overveiende moderate nivåer av agitasjon med noen pasienter som opplever milde eller alvorlige nivåer av agitasjon. Det primære effektmålet som ble brukt for å vurdere agitasjonstegn og -symptomer i disse studiene var endringen fra baseline i PANSS Excited Component 2 timer etter injeksjon. Pasienter kunne få opptil 3 injeksjoner i løpet av 24-timers IM-behandlingsperioder; pasienter kunne imidlertid ikke få den andre injeksjonen før etter den første 2 timers perioden da det primære effektmålet ble vurdert. Resultatene av forsøkene følger:
(1) I en placebokontrollert studie med opprørte inneliggende pasienter som oppfyller DSM-IV-kriteriene for schizofreni (n=270), ble 4 faste intramuskulære olanzapin til injeksjonsdoser på 2,5 mg, 5 mg, 7,5 mg og 10 mg evaluert. Alle doser var statistisk overlegne placebo på PANSS Excited Component 2 timer etter injeksjon. Effekten var imidlertid større og mer konsistent for de 3 høyeste dosene. Det var ingen signifikante parvise forskjeller for 7,5 og 10 mg doser i forhold til 5 mg doser.
(2) I en andre placebokontrollert studie med opprørte inneliggende pasienter som oppfyller DSM-IV-kriteriene for schizofreni (n=311), ble 1 fast intramuskulær olanzapin til injeksjonsdose på 10 mg evaluert. Olanzapin til injeksjon var statistisk overlegen placebo på PANSS Excited Component 2 timer etter injeksjon.
(3) I en placebokontrollert studie med opphissede inneliggende pasienter som oppfyller DSM-IV-kriteriene for bipolar lidelse I (og som for tiden viser en akutt manisk eller blandet episode med eller uten psykotiske trekk) (n=201), 1 fast intramuskulær olanzapin til injeksjonsdose på 10 mg ble evaluert. Olanzapin til injeksjon var statistisk overlegen placebo på PANSS Excited Component 2 timer etter injeksjon.
Undersøkelse av populasjonsundergrupper (alder, rase og kjønn) avslørte ingen differensiell respons på grunnlag av disse undergruppene.
PASIENTINFORMASJON
ZYPREXA® (zy-PREX-a) (olanzapin) Tablett
ZYPREXA® ZYDIS® (zy-PREX-a ZY-dis) (olanzapin) Tablett, oralt desintegrerende
Les medisinveiledningen som følger med ZYPREXA før du begynner å ta den og hver gang du får påfyll. Det kan komme ny informasjon. Denne medisinveiledningen erstatter ikke å snakke med legen din om din medisinske tilstand eller behandling. Snakk med legen din eller apoteket hvis det er noe du ikke forstår eller du ønsker å lære mer om ZYPREXA.
Hva er den viktigste informasjonen jeg bør vite om ZYPREXA?
ZYPREXA 20mg kan forårsake alvorlige bivirkninger, inkludert:
. Økt risiko for død hos eldre som er forvirret, har hukommelsestap og har mistet kontakten med virkeligheten (demensrelatert psykose). . Høyt blodsukker (hyperglykemi). . Høye fettnivåer i blodet (økt kolesterol og triglyserider), spesielt hos tenåringer i alderen 13 til 17 eller når det brukes i kombinasjon med fluoksetin hos barn i alderen 10 til 17. . Vektøkning, spesielt hos tenåringer i alderen 13 til 17 eller når det brukes i kombinasjon med fluoksetin hos barn i alderen 10 til 17.Disse alvorlige bivirkningene er beskrevet nedenfor.
1. Økt risiko for død hos eldre som er forvirret, har hukommelsestap og har mistet kontakten med virkeligheten (demensrelatert psykose). ZYPREXA er ikke godkjent for behandling av psykose hos eldre personer med demens.
2. Høyt blodsukker (hyperglykemi). Høyt blodsukker kan skje hvis du allerede har diabetes eller hvis du aldri har hatt diabetes. Høyt blodsukker kan føre til:
- . en opphopning av syre i blodet ditt på grunn av ketoner (ketoacidose) . koma . død
Legen din bør ta tester for å kontrollere blodsukkeret ditt før du begynner å ta ZYPREXA 7,5 mg og under behandlingen. Hos personer som ikke har diabetes, forsvinner noen ganger høyt blodsukker når ZYPREXA 7,5 mg stoppes. Personer med diabetes og noen personer som ikke hadde diabetes før de tok ZYPREXA, må ta medisiner for høyt blodsukker selv etter at de sluttet å ta ZYPREXA.
Hvis du har diabetes, følg legens instruksjoner om hvor ofte du skal sjekke blodsukkeret mens du tar ZYPREXA.
Ring legen din dersom du har noen av disse symptomene på høyt blodsukker (hyperglykemi) mens du tar ZYPREXA:
- . føler meg veldig tørst . trenger å tisse mer enn vanlig . føler meg veldig sulten . føler seg svak eller sliten . får vondt i magen . føler deg forvirret eller pusten din lukter fruktig
3. Høye fettnivåer i blodet (kolesterol og triglyserider). Høye fettnivåer kan forekomme hos personer som behandles med ZYPREXA 10 mg, spesielt hos tenåringer (13 til 17 år), eller når det brukes i kombinasjon med fluoksetin hos barn (10 til 17 år). Det kan hende du ikke har noen symptomer, så legen din bør ta blodprøver for å sjekke kolesterol- og triglyseridnivåene dine før du begynner å ta ZYPREXA og under behandlingen.
4. Vektøkning. Vektøkning er svært vanlig hos personer som tar ZYPREXA. Tenåringer (13 til 17 år) har større sannsynlighet for å gå opp i vekt og få mer vekt enn voksne. Barn (10 til 17 år) er også mer sannsynlig å gå opp i vekt og gå opp mer enn voksne når ZYPREXA 7,5 mg brukes i kombinasjon med fluoksetin. Noen mennesker kan gå opp mye i vekt mens de tar ZYPREXA, så du og legen din bør sjekke vekten din regelmessig. Snakk med legen din om måter å kontrollere vektøkning på, for eksempel å spise et sunt, balansert kosthold og trene.
Hva er ZYPREXA?
ZYPREXA er et reseptbelagt legemiddel som brukes til å behandle:
- . schizofreni hos personer 13 år eller eldre. . bipolar lidelse, inkludert:
- . maniske eller blandede episoder som skjer med bipolar lidelse I hos personer i alderen 13 år eller eldre. . maniske eller blandede episoder som oppstår med bipolar lidelse I, når det brukes sammen med medisinen litium eller valproat, hos voksne. . langtidsbehandling av bipolar lidelse I hos voksne.
ZYPREXA 7,5 mg er ikke godkjent for bruk hos barn under 13 år. ZYPREXA 10 mg i kombinasjon med fluoksetin er ikke godkjent for bruk hos barn under 10 år.
Symptomene på schizofreni inkluderer å høre stemmer, se ting som ikke er der, ha tro som ikke er sann, og være mistenksom eller tilbaketrukket.
Symptomene på bipolar lidelse I inkluderer vekslende perioder med depresjon og høyt eller irritabelt humør, økt aktivitet og rastløshet, løpende tanker, snakke raskt, impulsiv atferd og redusert behov for søvn.
Symptomene på behandlingsresistent depresjon inkluderer nedsatt humør, redusert interesse, økte skyldfølelser, redusert energi, redusert konsentrasjon, endringer i appetitt og selvmordstanker eller -adferd.
Noen av symptomene dine kan forbedres med behandling. Hvis du ikke tror du blir bedre, ring legen din.
Hva bør jeg fortelle legen min før jeg tar ZYPREXA?
ZYPREXA er kanskje ikke riktig for deg. Før du starter ZYPREXA, fortell legen din dersom du har eller hadde:
- . hjerteproblemer . anfall . diabetes eller høyt blodsukkernivå (hyperglykemi) . høye kolesterol- eller triglyseridnivåer i blodet ditt . leverproblemer . lavt eller høyt blodtrykk . slag eller "minislag" også kalt forbigående iskemiske anfall (TIA) . Alzheimers sykdom . trangvinklet glaukom . forstørret prostata hos menn . tarmobstruksjon . fenylketonuri, fordi ZYPREXA 5mg ZYDIS inneholder fenylalanin . brystkreft . tanker om selvmord eller å skade deg selv . enhver annen medisinsk tilstand . er gravid eller planlegger å bli gravid. Det er ikke kjent om ZYPREXA 2,5 mg vil skade det ufødte barnet ditt.
- . Hvis du blir gravid mens du får ZYPREXA 20 mg, snakk med helsepersonell om registrering hos det nasjonale svangerskapsregisteret for atypiske antipsykotika. Du kan registrere deg ved å ringe 1-866-961-2388 eller gå til http://womensmentalhealth.org/clinical-andresearch-programs/pregnancyregistry/.
Fortell legen din hvis du trener mye eller ofte er på varme steder.
Symptomene på bipolar lidelse I, behandlingsresistent depresjon eller schizofreni kan omfatte tanker om selvmord eller skade deg selv eller andre. Hvis du har disse tankene når som helst, fortell legen din eller gå til legevakten umiddelbart.
Fortell legen din om alle medisinene du tar, inkludert reseptbelagte og reseptfrie medisiner, vitaminer og urtetilskudd. ZYPREXA 20mg og noen medisiner kan interagere med hverandre og virker kanskje ikke like bra, eller forårsake mulige alvorlige bivirkninger. Legen din kan fortelle deg om det er trygt å ta ZYPREXA sammen med andre legemidler. Ikke start eller stopp noen medisin mens du tar ZYPREXA uten å snakke med legen din først.
Hvordan skal jeg ta ZYPREXA 7,5 mg?
- . Ta ZYPREXA nøyaktig som foreskrevet. Legen din må kanskje endre (justere) dosen av ZYPREXA 15 mg til den er riktig for deg. . Hvis du glemmer en dose av ZYPREXA 20 mg, ta den glemte dosen så snart du husker det. Hvis det nesten er tid for neste dose, hopp over den glemte dosen og ta neste dose til vanlig tid. Ikke ta to doser ZYPREXA 10 mg samtidig. . For å forhindre alvorlige bivirkninger, må du ikke slutte å ta ZYPREXA plutselig. Hvis du må slutte å ta ZYPREXA, kan legen din fortelle deg hvordan du trygt kan slutte å ta det. . Hvis du tar for mye ZYPREXA, ring legen din eller giftkontrollsenteret på 1-800-222-1222 med en gang, eller få akuttbehandling. . ZYPREXA 10 mg kan tas med eller uten mat. . ZYPREXA tas vanligvis én gang hver dag. . Ta ZYPREXA 20mg ZYDIS som følger:
- . Pass på at hendene er tørre. . Åpne posen og fjern folien på blisterpakningen. Ikke skyv tabletten gjennom folien. . Så snart du åpner blisterpakningen, fjern tabletten og legg den i munnen. . Tabletten vil raskt desintegreres i spyttet slik at du enkelt kan svelge den med eller uten å drikke væske.
Hva bør jeg unngå mens jeg tar ZYPREXA?
- . ZYPREXA kan forårsake søvnighet og kan påvirke din evne til å ta beslutninger, tenke klart eller reagere raskt. Du bør ikke kjøre bil, bruke tunge maskiner eller gjøre andre farlige aktiviteter før du vet hvordan ZYPREXA 7,5 mg påvirker deg. . Unngå å drikke alkohol mens du tar ZYPREXA. Å drikke alkohol mens du tar ZYPREXA kan gjøre deg søvnigere enn om du tar ZYPREXA 15 mg alene.
Hva er de mulige bivirkningene av ZYPREXA 5mg?
Alvorlige bivirkninger kan oppstå når du tar ZYPREXA 5mg, inkludert:
- . Se «Hva er den viktigste informasjonen jeg bør vite om ZYPREXA?», som beskriver økt risiko for død hos eldre mennesker med demensrelatert psykose og risikoen for høyt blodsukker, høyt kolesterol- og triglyseridnivå, og vektøkning. . Økt forekomst av hjerneslag eller "minislag" kalt forbigående iskemiske anfall (TIA) hos eldre mennesker med demensrelatert psykose (eldre mennesker som har mistet kontakten med virkeligheten på grunn av forvirring og hukommelsestap). ZYPREXA er ikke godkjent for disse pasientene. . Malignt nevroleptikasyndrom (NMS): NMS er en sjelden, men svært alvorlig tilstand som kan forekomme hos personer som tar antipsykotiske legemidler, inkludert ZYPREXA. NMS kan forårsake død og må behandles på sykehus. Ring legen din med en gang hvis du blir alvorlig syk og har noen av disse symptomene:
- . høy feber . overdreven svetting . stive muskler . forvirring . endringer i pusten, hjerterytmen og blodtrykket.
- . svette for mye eller ikke i det hele tatt . tørr i munnen . føler meg veldig varm . føler seg tørst . ikke i stand til å produsere urin.
Vanlige bivirkninger av ZYPREXA inkluderer: mangel på energi, munntørrhet, økt appetitt, søvnighet, skjelvinger, hard eller sjelden avføring, svimmelhet, endringer i atferd eller rastløshet.
Andre vanlige bivirkninger hos tenåringer (13-17 år) inkluderer: hodepine, smerter i mageområdet (mage), smerter i armer eller ben, eller tretthet. Tenåringer opplevde større økninger i prolaktin, leverenzymer og søvnighet sammenlignet med voksne.
Fortell legen din om eventuelle bivirkninger som plager deg eller som ikke forsvinner.
Dette er ikke alle mulige bivirkninger med ZYPREXA. Spør legen din eller apoteket for mer informasjon.
Ring legen din for medisinsk råd om bivirkninger. Du kan rapportere bivirkninger til FDA på 1-800-FDA-1088.
Hvordan bør jeg oppbevare ZYPREXA?
- . Oppbevar ZYPREXA ved romtemperatur, mellom 68 °F til 77 °F (20 °C til 25 °C). . Hold ZYPREXA unna lys. . Hold ZYPREXA 15 mg tørt og vekk fra fuktighet.
Oppbevar ZYPREXA 5mg og alle legemidler utilgjengelig for barn.
Generell informasjon om ZYPREXA
Medisiner er noen ganger foreskrevet for andre formål enn de som er oppført i en medisinveiledning. Ikke bruk ZYPREXA for en tilstand det ikke er foreskrevet for. Ikke gi ZYPREXA 5 mg til andre mennesker, selv om de har samme tilstand. Det kan skade dem.
Denne medisinveiledningen oppsummerer den viktigste informasjonen om ZYPREXA. Hvis du vil ha mer informasjon, snakk med legen din. Du kan spørre legen din eller apoteket om informasjon om ZYPREXA 20mg som er skrevet for helsepersonell. For mer informasjon om ZYPREXA ring 1-800-Lilly-Rx (1-800-545-5979).
Hva er ingrediensene i ZYPREXA?
Aktiv ingrediens: olanzapin
Inaktive ingredienser:
karnaubavoks, krospovidon, hydroksypropylcellulose, hypromellose, laktose, magnesiumstearat, mikrokrystallinsk cellulose og andre inaktive ingredienser. Fargebelegget inneholder: Titanium Dioxide, FD&C Blue No. 2 Aluminium Lake, eller Synthetic Red Iron Oxide.
ZYDIS - gelatin, mannitol, aspartam, natriummetylparaben og natriumpropylparaben.
Denne medisinveiledningen er godkjent av US Food and Drug Administration.
