Wellbutrin 150mg, 300mg Bupropion Bruk, bivirkninger og dosering. Pris i nettapotek. Generisk medisin uten resept.
Hva er Wellbutrin 150mg og hvordan brukes det?
Wellbutrin 150mg er en reseptbelagt medisin som brukes til å behandle symptomene på alvorlig depresjon og sesongmessige affektive lidelser. Wellbutrin 150mg kan brukes alene eller sammen med andre medisiner.
Wellbutrin 150mg tilhører en klasse legemidler som kalles antidepressiva, dopaminreopptakshemmere, antidepressiva, andre hjelpemidler for røykeavvenning.
Hva er de mulige bivirkningene av Wellbutrin 150mg?
Wellbutrin kan forårsake alvorlige bivirkninger, inkludert:
- . anfall (kramper), . forvirring, . uvanlige endringer i humør eller atferd, . tåkesyn, . tunnelsyn, . øyesmerter eller hevelse, . ser glorier rundt lys, . rask eller uregelmessig hjerterytme, . løpende tanker, . økt energi, . hensynsløs oppførsel, . føler meg ekstremt glad eller irritabel, . snakker mer enn vanlig, og . alvorlige søvnproblemer
Få medisinsk hjelp med en gang hvis du har noen av symptomene nevnt ovenfor.
De vanligste bivirkningene av Wellbutrin inkluderer:
- . tørr i munnen, . tett nese, . synsproblemer, . hørselsproblemer, . kvalme, . oppkast, . forstoppelse, . søvnproblemer (søvnløshet), . skjelvinger, . svette, . føler seg engstelig eller nervøs, . raske hjerteslag, . forvirring, . opphisselse, . fiendtlighet, . utslett, . hodepine, . svimmelhet, og . leddsmerter
Fortell legen dersom du har noen bivirkninger som plager deg eller som ikke går over.
Dette er ikke alle mulige bivirkninger av Wellbutrin. Spør legen din eller apoteket for mer informasjon.
Ring legen din for medisinsk råd om bivirkninger. Du kan rapportere bivirkninger til FDA på 1-800-FDA-1088
ADVARSEL
SELVmordstanker og adferd
SUICIDALITET OG ANTIDEPRESSIVA MEDIKA
Antidepressiva økte risikoen for selvmordstanker og selvmordsatferd hos barn, ungdom og unge voksne i korttidsstudier. Disse studiene viste ikke en økning i risikoen for selvmordstanker og -adferd ved bruk av antidepressiva hos personer over 24 år; det var en reduksjon i risiko ved bruk av antidepressiva hos personer i alderen 65 år og eldre [se ADVARSLER OG FORHOLDSREGLER].
Hos pasienter i alle aldre som starter på antidepressiv behandling, overvåk nøye for forverring og for fremvekst av selvmordstanker og selvmordsatferd. Informer familier og omsorgspersoner om behovet for tett observasjon og kommunikasjon med forskriveren [se ADVARSLER OG FORHOLDSREGLER].
BESKRIVELSE
WELLBUTRIN (bupropionhydroklorid), et antidepressivum av aminoketonklassen, er kjemisk ikke relatert til trisykliske, tetrasykliske, selektive serotoninreopptakshemmere eller andre kjente antidepressiva. Dens struktur ligner mye på dietylpropion; det er relatert til fenyletylaminer. Det er betegnet som (±)-1-(3-klorfenyl)-2-[(1,1-dimetyletyl)amino]-1-propanonhydroklorid. Molekylvekten er 276,2. Molekylformelen er C13H18ClNO•HCl. Bupropionhydrokloridpulver er hvitt, krystallinsk og svært løselig i vann. Den har en bitter smak og gir følelsen av lokalbedøvelse på munnslimhinnen. Strukturformelen er:
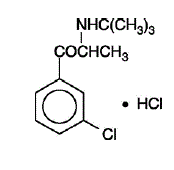
WELLBUTRIN leveres for oral administrering som 75 mg (gult-gull) og 100 mg (rødt) filmdrasjerte tabletter. Hver tablett inneholder den merkede mengden bupropionhydroklorid og de inaktive ingrediensene: 75 mg tablett – D&C Yellow No. 10 Lake, FD&C Yellow No. 6 Lake, hydroksypropylcellulose, hypromellose, mikrokrystallinsk cellulose, polyetylenglykol, talkum og titandioksid; 100 mg tablett – FD&C Red No. 40 Lake, FD&C Yellow No. 6 Lake, hydroksypropylcellulose, hypromellose, mikrokrystallinsk cellulose, polyetylenglykol, talkum og titandioksid.
INDIKASJONER
WELLBUTRIN (bupropionhydroklorid) er indisert for behandling av alvorlig depressiv lidelse (MDD), som definert av Diagnostic and Statistical Manual (DSM).
Effekten av WELLBUTRIN 300 mg i behandlingen av en alvorlig depressiv episode ble fastslått i to 4-ukers kontrollerte polikliniske studier og en 6-ukers kontrollert poliklinisk studie med voksne personer med MDD [se Kliniske studier ].
DOSERING OG ADMINISTRASJON
Generelle bruksanvisninger
For å minimere risikoen for anfall, øk dosen gradvis [se ADVARSLER OG FORHOLDSREGLER ]. Økning i dose bør ikke overstige 100 mg/dag i en 3-dagers periode. WELLBUTRIN tabletter skal svelges hele og ikke knuses, deles eller tygges. WELLBUTRIN 300 mg kan tas med eller uten mat.
Anbefalt startdose er 200 mg/dag, gitt som 100 mg to ganger daglig. Etter 3 dagers dosering kan dosen økes til 300 mg/dag, gitt som 100 mg 3 ganger daglig, med minst 6 timer mellom påfølgende doser. Dosering over 300 mg/dag kan oppnås ved bruk av 75 eller 100 mg tabletter.
Maksimalt 450 mg/dag, gitt i oppdelte doser på ikke mer enn 150 mg hver, kan vurderes for pasienter som ikke viser noen klinisk bedring etter flere ukers behandling med 300 mg/dag. Administrer 100 mg tabletten 4 ganger daglig for ikke å overskride grensen på 150 mg i en enkelt dose.
Det er generelt enighet om at akutte episoder med depresjon krever flere måneder eller lenger med antidepressiv medikamentell behandling utover responsen i den akutte episoden. Det er ukjent om dosen av WELLBUTRIN som er nødvendig for vedlikeholdsbehandling er identisk med dosen som ga en initial respons. Vurder med jevne mellomrom behovet for vedlikeholdsbehandling og passende dose for slik behandling.
Dosejustering hos pasienter med nedsatt leverfunksjon
Hos pasienter med moderat til alvorlig nedsatt leverfunksjon (Child-Pugh-score: 7 til 15), er maksimal dose WELLBUTRIN 150 mg 75 mg/dag. Hos pasienter med lett nedsatt leverfunksjon (Child-Pugh-score: 5 til 6), bør du vurdere å redusere dosen og/eller doseringsfrekvensen [se Bruk i spesifikke populasjoner , KLINISK FARMAKOLOGI ].
Dosejustering hos pasienter med nedsatt nyrefunksjon
Vurder å redusere dosen og/eller frekvensen av WELLBUTRIN 150 mg hos pasienter med nedsatt nyrefunksjon (glomerulær filtreringshastighet mindre enn 90 ml/min) [se Bruk i spesifikke populasjoner , KLINISK FARMAKOLOGI ].
Bytte en pasient til eller fra et monoaminoksidasehemmer (MAOI) antidepressivum
Det bør gå minst 14 dager mellom seponering av en MAO-hemmer beregnet på å behandle depresjon og oppstart av behandling med WELLBUTRIN. Omvendt bør det tillates minst 14 dager etter seponering av WELLBUTRIN før du starter et MAO-antidepressivum [se KONTRAINDIKASJONER , NARKOTIKAHANDEL ].
Bruk av WELLBUTRIN med reversible MAO-hemmere som linezolid eller metylenblått
Ikke start WELLBUTRIN 300 mg hos en pasient som behandles med en reversibel MAO-hemmer som linezolid eller intravenøs metylenblått. Legemiddelinteraksjoner kan øke risikoen for hypertensive reaksjoner. Hos en pasient som trenger mer akutt behandling av en psykiatrisk tilstand, bør ikke-farmakologiske intervensjoner, inkludert sykehusinnleggelse, vurderes [se KONTRAINDIKASJONER , NARKOTIKAHANDEL ].
noen tilfeller kan en pasient som allerede får behandling med WELLBUTRIN trenge akuttbehandling med linezolid eller intravenøs metylenblått. Hvis akseptable alternativer til linezolid eller intravenøs behandling med metylenblått ikke er tilgjengelig og de potensielle fordelene ved behandling med linezolid eller intravenøs metylenblått vurderes å oppveie risikoen for hypertensive reaksjoner hos en bestemt pasient, bør WELLBUTRIN 300 mg stoppes umiddelbart, og linezolid eller intravenøs metylen blått kan administreres. Pasienten bør overvåkes i 2 uker eller inntil 24 timer etter siste dose linezolid eller intravenøs metylenblått, avhengig av hva som kommer først. Behandling med WELLBUTRIN 300 mg kan gjenopptas 24 timer etter siste dose linezolid eller intravenøs metylenblått.
Risikoen for å administrere metylenblått på ikke-intravenøse veier (som orale tabletter eller ved lokal injeksjon) eller i intravenøse doser mye lavere enn 1 mg/kg med WELLBUTRIN 300 mg er uklar. Legen bør likevel være klar over muligheten for en legemiddelinteraksjon ved slik bruk [se KONTRAINDIKASJONER , NARKOTIKAHANDEL ].
HVORDAN LEVERES
Doseringsformer og styrker
- . 75 mg – gul-gull, runde, bikonvekse tabletter merket med “WELLBUTRIN 75”. . 100 mg - røde, runde, bikonvekse tabletter merket med "WELLBUTRIN 100".
Oppbevaring og håndtering
WELLBUTRIN 150 mg tabletter, 75 mg bupropionhydroklorid, er gulgull, runde, bikonvekse tabletter merket med "WELLBUTRIN 75" i flasker med 100 stk. NDC 0173-0177-55).
WELLBUTRIN tabletter, 100 mg bupropionhydroklorid, er røde, runde, bikonvekse tabletter merket med "WELLBUTRIN 100" i flasker med 100 stk. NDC 0173-0178-55).
Oppbevares ved romtemperatur, 20° til 25°C (68° til 77°F); utflukter tillatt mellom 15°C og 30°C (59°F og 86°F) [Se USP kontrollert romtemperatur ]. Beskytt mot lys og fuktighet.
Produsert for: GlaxoSmithKline, Research Triangle Park,. Revidert: november 2019
BIVIRKNINGER
Følgende bivirkninger er omtalt mer detaljert i andre deler av merkingen:
- . Selvmordstanker og -atferd hos ungdom og unge voksne [se ADVARSEL i boks , ADVARSLER OG FORHOLDSREGLER ] . Nevropsykiatriske symptomer og selvmordsrisiko ved røykeavvenningsbehandling [se ADVARSLER OG FORHOLDSREGLER ] . Anfall [se ADVARSLER OG FORHOLDSREGLER ] . Hypertensjon [se ADVARSLER OG FORHOLDSREGLER ] . Aktivering av mani eller hypomani [se ADVARSLER OG FORHOLDSREGLER ] . Psykose og andre nevropsykiatriske reaksjoner [se ADVARSLER OG FORHOLDSREGLER ] . Vinkel-lukkende glaukom [se ADVARSLER OG FORHOLDSREGLER ] . Overfølsomhetsreaksjoner [se ADVARSLER OG FORHOLDSREGLER ]
Erfaring fra kliniske forsøk
Fordi kliniske studier utføres under vidt forskjellige forhold, kan bivirkningsrater observert i kliniske studier av et legemiddel ikke sammenlignes direkte med rater i kliniske studier av et annet legemiddel, og gjenspeiler kanskje ikke ratene observert i klinisk praksis.
Bivirkninger som fører til seponering av behandling
Bivirkningene var tilstrekkelig plagsomme til å forårsake seponering av behandling med WELLBUTRIN hos omtrent 10 % av de 2400 forsøkspersonene og friske frivillige som deltok i kliniske studier under produktets første utvikling. De mer vanlige hendelsene som forårsaker seponering inkluderer nevropsykiatriske forstyrrelser (3,0 %), primært agitasjon og abnormiteter i mental status; gastrointestinale forstyrrelser (2,1 %), primært kvalme og oppkast; nevrologiske forstyrrelser (1,7 %), primært anfall, hodepine og søvnforstyrrelser; og dermatologiske problemer (1,4 %), primært utslett. Det er imidlertid viktig å merke seg at mange av disse hendelsene skjedde ved doser som overstiger den anbefalte daglige dosen.
Vanlige observerte bivirkninger
Bivirkninger som vanligvis oppstår hos personer behandlet med WELLBUTRIN er agitasjon, munntørrhet, søvnløshet, hodepine/migrene, kvalme/oppkast, forstoppelse, skjelving, svimmelhet, overdreven svetting, tåkesyn, takykardi, forvirring, utslett, fiendtlighet, hjertearrytmi og hørsel. forstyrrelse.
Tabell 2 oppsummerer bivirkningene som oppsto i placebokontrollerte studier med en insidens på minst 1 % av pasientene som fikk WELLBUTRIN 150 mg og hyppigere hos disse forsøkspersonene enn i placebogruppen.
Andre bivirkninger observert under den kliniske utviklingen av WELLBUTRIN
Forholdene og varigheten av eksponeringen for WELLBUTRIN varierte sterkt, og en betydelig del av erfaringen ble oppnådd i åpne og ukontrollerte kliniske omgivelser. I løpet av denne erfaringen ble det rapportert om en rekke uønskede hendelser; uten passende kontroller er det imidlertid umulig å fastslå med sikkerhet hvilke hendelser som var eller ikke ble forårsaket av WELLBUTRIN. Følgende oppregning er organisert etter organsystem og beskriver hendelser i form av deres relative rapporteringsfrekvens i databasen.
Følgende definisjoner av frekvens brukes: Hyppige bivirkninger er definert som de som forekommer hos minst 1/100 personer. Sjeldne bivirkninger er de som forekommer hos 1/100 til 1/1 000 personer, mens sjeldne hendelser er de som forekommer hos mindre enn 1/1 000 personer.
Kardiovaskulær Hyppig var ødem; sjeldne var brystsmerter, elektrokardiogram (EKG) abnormiteter (premature slag og uspesifikke ST-T endringer), og kortpustethet/dyspné; sjeldne var rødme og hjerteinfarkt.
Dermatologisk: Sjelden var alopecia.
Endokrine: Sjelden var gynekomasti; sjelden var glykosuri.
Gastrointestinale: Sjeldne var dysfagi, tørsteforstyrrelse og leverskade/gulsott; sjelden var tarmperforering.
Genitourinært: Hyppig var natturi; sjeldne var vaginal irritasjon, testikkelhevelse, urinveisinfeksjon, smertefull ereksjon og forsinket ejakulasjon; sjeldne var enurese og urininkontinens.
Nevrologisk: Hyppige var ataksi/inkoordinasjon, anfall, myoklonus, dyskinesi og dystoni; sjeldne var mydriasis, vertigo og dysartri; sjeldne var elektroencefalogram (EEG) abnormitet og nedsatt oppmerksomhet.
Nevropsykiatrisk: Hyppig var mani/hypomani, økt libido, hallusinasjoner, redusert seksuell funksjon og depresjon; sjeldne var hukommelsessvikt, depersonalisering, psykose, dysfori, humørstabilitet, paranoia og formell tankeforstyrrelse; sjelden var selvmordstanker.
Muntlige klager: Hyppig var stomatitt; sjeldne var tannpine, bruksisme, tannkjøttirritasjon og oral ødem.
Luftveiene: Sjeldne var bronkitt og kortpustethet/dyspné; sjelden var lungeemboli.
Spesielle sanser: Sjelden var synsforstyrrelser; sjelden var diplopi.
Uspesifikk: Hyppige var influensalignende symptomer; sjeldne var uspesifikke smerter; sjelden var overdose.
Endret appetitt og vekt
Et vekttap på mer enn 5 lbs. forekom hos 28 % av pasientene som fikk WELLBUTRIN. Denne forekomsten er omtrent dobbelt så stor som hos sammenlignbare personer behandlet med trisykliske eller placebo. Videre, mens 35 % av pasientene som fikk trisykliske antidepressiva gikk opp i vekt, var det bare 9,4 % av pasientene behandlet med WELLBUTRIN som gjorde det. Følgelig, hvis vekttap er et stort synlig tegn på en pasients depressive sykdom, bør det anorektiske og/eller vektreduserende potensialet til WELLBUTRIN vurderes.
Postmarketing-erfaring
Følgende bivirkninger er identifisert under bruk av WELLBUTRIN etter godkjenning og er ikke beskrevet andre steder i etiketten. Fordi disse reaksjonene rapporteres frivillig fra en populasjon av usikker størrelse, er det ikke alltid mulig å pålitelig estimere frekvensen deres eller etablere en årsakssammenheng med legemiddeleksponering.
Kropp (generelt)
Artralgi, myalgi og feber med utslett og andre symptomer som tyder på forsinket overfølsomhet. Disse symptomene kan ligne på serumsyke [se ADVARSLER OG FORHOLDSREGLER ].
Kardiovaskulær
Hypertensjon (i noen tilfeller alvorlig), ortostatisk hypotensjon, tredjegrads hjerteblokk.
Endokrine
Hyponatremi, syndrom med upassende antidiuretisk hormonsekresjon, hyperglykemi, hypoglykemi.
Gastrointestinale
Esofagitt, hepatitt.
Hemisk og lymfatisk
Ekkymose, leukocytose, leukopeni, trombocytopeni. Endret PT og/eller INR, sjelden assosiert med hemorragiske eller trombotiske komplikasjoner, ble observert når bupropion ble administrert samtidig med warfarin.
Muskuloskeletal
Muskelstivhet/feber/rabdomyolyse, muskelsvakhet.
Nervesystemet
Aggresjon, koma, fullført selvmord, delirium, drømmeavvik, paranoide tanker, parestesi, parkinsonisme, rastløshet, selvmordsforsøk, avsløring av tardiv dyskinesi.
Hud og vedheng
Stevens-Johnsons syndrom, angioødem, eksfoliativ dermatitt, urticaria.
Spesielle sanser
Tinnitus, økt intraokulært trykk.
NARKOTIKAHANDEL
Potensial for andre legemidler å påvirke WELLBUTRIN
Bupropion metaboliseres primært til hydroksybupropion av CYP2B6. Derfor eksisterer potensialet for legemiddelinteraksjoner mellom WELLBUTRIN og legemidler som hemmer eller induserer CYP2B6.
Hemmere av CYP2B6
Tiklopidin og klopidogrel
Samtidig behandling med disse legemidlene kan øke eksponeringen for bupropion, men redusere eksponeringen for hydroksybupropion. Basert på klinisk respons, kan dosejustering av WELLBUTRIN være nødvendig når det administreres sammen med CYP2B6-hemmere (f.eks. tiklopidin eller klopidogrel) [se KLINISK FARMAKOLOGI ].
Induktorer av CYP2B6
Ritonavir, Lopinavir og Efavirenz
Samtidig behandling med disse legemidlene kan redusere eksponeringen for bupropion og hydroksybupropion. Doseøkning av WELLBUTRIN kan være nødvendig når det administreres sammen med ritonavir, lopinavir eller efavirenz [se KLINISK FARMAKOLOGI ] men bør ikke overskride maksimal anbefalt dose.
Karbamazepin, fenobarbital, fenytoin
Selv om de ikke er systematisk studert, kan disse legemidlene indusere metabolismen av bupropion og kan redusere eksponeringen for bupropion [se KLINISK FARMAKOLOGI ]. Hvis bupropion brukes samtidig med en CYP-induktor, kan det være nødvendig å øke dosen av bupropion, men maksimal anbefalt dose bør ikke overskrides.
Potensial for WELLBUTRIN 300mg til å påvirke andre legemidler
Legemidler metabolisert av CYP2D6
Bupropion og dets metabolitter (erytrohydrobupropion, treohydrobupropion, hydroksybupropion) er CYP2D6-hemmere. Derfor kan samtidig administrering av WELLBUTRIN med legemidler som metaboliseres av CYP2D6 øke eksponeringen av legemidler som er substrater for CYP2D6. Slike legemidler inkluderer visse antidepressiva (f.eks. venlafaksin, nortriptylin, imipramin, desipramin, paroksetin, fluoksetin og sertralin), antipsykotika (f.eks. haloperidol, risperidon, tioridazin), betablokkere (f.eks. metoprolol) og type 1C antiarytmika (f.eks. , propafenon og flekainid). Ved samtidig bruk med WELLBUTRIN kan det være nødvendig å redusere dosen av disse CYP2D6-substratene, spesielt for legemidler med en smal terapeutisk indeks.
Legemidler som krever metabolsk aktivering av CYP2D6 for å være effektive (f.eks. tamoxifen) teoretisk kan ha redusert effekt når de administreres samtidig med CYP2D6-hemmere som bupropion. Pasienter som behandles samtidig med WELLBUTRIN og slike legemidler kan kreve økte doser av legemidlet [se KLINISK FARMAKOLOGI ].
Digoksin
Samtidig administrering av WELLBUTRIN og digoksin kan redusere digoksinnivået i plasma. Overvåk plasmadigoksinnivåer hos pasienter som behandles samtidig med WELLBUTRIN og digoksin [se KLINISK FARMAKOLOGI ].
Legemidler som senker anfallsterskelen
Vær ekstrem forsiktig når du administrerer WELLBUTRIN samtidig med andre legemidler som senker krampeterskelen (f.eks. andre bupropionprodukter, antipsykotika, antidepressiva, teofyllin eller systemiske kortikosteroider). Bruk lave startdoser og øk dosen gradvis [se KONTRAINDIKASJONER , ADVARSLER OG FORHOLDSREGLER ].
Dopaminerge legemidler (levodopa og amantadin)
Bupropion, levodopa og amantadin har dopaminagonisteffekter. CNS-toksisitet er rapportert når bupropion ble administrert samtidig med levodopa eller amantadin. Bivirkninger har inkludert rastløshet, agitasjon, skjelving, ataksi, gangforstyrrelser, vertigo og svimmelhet. Det antas at toksisiteten skyldes kumulative dopaminagonisteffekter. Vær forsiktig når du administrerer WELLBUTRIN 150mg samtidig med disse legemidlene.
Bruk med alkohol
Etter markedsføring har det vært sjeldne rapporter om uønskede nevropsykiatriske hendelser eller redusert alkoholtoleranse hos pasienter som drakk alkohol under behandling med WELLBUTRIN. Inntak av alkohol under behandling med WELLBUTRIN bør minimeres eller unngås.
MAO-hemmere
Bupropion hemmer gjenopptaket av dopamin og noradrenalin. Samtidig bruk av MAO-hemmere og bupropion er kontraindisert fordi det er økt risiko for hypertensive reaksjoner dersom bupropion brukes samtidig med MAO-hemmere. Studier på dyr viser at den akutte toksisiteten til bupropion forsterkes av MAO-hemmeren fenelzin. Det bør gå minst 14 dager mellom seponering av en MAO-hemmer beregnet på å behandle depresjon og oppstart av behandling med WELLBUTRIN. Omvendt bør det tillates minst 14 dager etter seponering av WELLBUTRIN 150mg før man starter et MAO-antidepressivum [se DOSERING OG ADMINISTRASJON , KONTRAINDIKASJONER ].
Interaksjoner med legemiddel-laboratorietest
Falsk-positive urinimmunoassay-screeningstester for amfetamin er rapportert hos pasienter som tar bupropion. Dette skyldes manglende spesifisitet for noen screeningtester. Falsk-positive testresultater kan oppstå selv etter seponering av bupropionbehandling. Bekreftende tester, som gasskromatografi/massespektrometri, vil skille bupropion fra amfetamin.
Narkotikamisbruk og avhengighet
Kontrollert stoff
Bupropion er ikke et kontrollert stoff.
Misbruke
Mennesker
Kontrollerte kliniske studier utført på normale frivillige, hos personer med en historie med flere stoffmisbruk, og hos deprimerte forsøkspersoner, viste en viss økning i motorisk aktivitet og agitasjon/spenning, ofte typisk for sentralstimulerende aktivitet.
I en populasjon av individer som har opplevd misbruk av rusmidler, ga en enkelt oral dose på 400 mg bupropion mild amfetaminlignende aktivitet sammenlignet med placebo på Morfin-Benzedrin-underskalaen til Addiction Research Center Inventories (ARCI) og en score høyere enn placebo, men mindre enn 15 mg av Schedule II-stimulerende middel dekstroamfetamin på Liking Scale of the ARCI. Disse skalaene måler generelle følelser av eufori og stofflikhet som ofte er forbundet med misbrukspotensial.
Funn i kliniske studier er imidlertid ikke kjent for å pålitelig forutsi misbrukspotensialet til narkotika. Ikke desto mindre tyder bevis fra enkeltdoseforsøk på at den anbefalte daglige dosen av bupropion når det gis oralt i oppdelte doser, sannsynligvis ikke vil være signifikant forsterkende for misbrukere av amfetamin eller CNS-stimulerende midler. Imidlertid kan høyere doser (som ikke kunne testes på grunn av risikoen for anfall) være beskjedent attraktive for de som misbruker CNS-stimulerende legemidler.
WELLBUTRIN er kun beregnet for oral bruk. Inhalering av knuste tabletter eller injeksjon av oppløst bupropion er rapportert. Kramper og/eller dødsfall er rapportert når bupropion har blitt administrert intranasalt eller ved parenteral injeksjon.
Dyr
Studier på gnagere og primater viste at bupropion viser noen farmakologiske virkninger som er felles for psykostimulerende midler. Hos gnagere har det vist seg å øke lokomotorisk aktivitet, fremkalle en mild stereotyp atferdsrespons og øke responshastigheten i flere tidsplankontrollerte atferdsparadigmer. I primatmodeller som vurderer de positive forsterkende effektene av psykoaktive stoffer, ble bupropion selvadministrert intravenøst. Hos rotter produserte bupropion amfetaminlignende og kokainlignende diskriminerende stimuluseffekter i narkotikadiskrimineringsparadigmer som ble brukt for å karakterisere de subjektive effektene av psykoaktive stoffer.
ADVARSLER
Inkludert som en del av FORHOLDSREGLER seksjon.
FORHOLDSREGLER
Selvmordstanker og -adferd hos barn, ungdom og unge voksne
Pasienter med MDD, både voksne og pediatriske, kan oppleve forverring av depresjonen og/eller fremveksten av selvmordstanker og -adferd (suicidalitet) eller uvanlige endringer i atferd, enten de tar antidepressive medisiner eller ikke, og denne risikoen kan vedvare inntil betydelig remisjon oppstår. Selvmord er en kjent risiko for depresjon og visse andre psykiatriske lidelser, og disse lidelsene er i seg selv de sterkeste prediktorene for selvmord. Det har vært en langvarig bekymring for at antidepressiva kan ha en rolle i å indusere forverring av depresjon og fremveksten av suicidalitet hos visse pasienter i de tidlige faser av behandlingen.
Samlede analyser av kortsiktige placebokontrollerte studier av antidepressiva (selektive serotoninreopptakshemmere [SSRI] og andre) viser at disse medikamentene øker risikoen for suicidal tenkning og atferd (suicidalitet) hos barn, ungdom og unge voksne (18 år) til 24) med MDD og andre psykiatriske lidelser. Kortsiktige kliniske studier viste ingen økning i risikoen for suicidalitet med antidepressiva sammenlignet med placebo hos voksne over 24 år; det var en reduksjon med antidepressiva sammenlignet med placebo hos voksne i alderen 65 år og eldre.
De samlede analysene av placebokontrollerte studier hos barn og ungdom med MDD, tvangslidelser (OCD) eller andre psykiatriske lidelser inkluderte totalt 24 korttidsstudier av 9 antidepressiva i over 4400 personer. De samlede analysene av placebokontrollerte studier hos voksne med MDD eller andre psykiatriske lidelser inkluderte totalt 295 korttidsstudier (median varighet på 2 måneder) av 11 antidepressiva med over 77 000 personer. Det var betydelig variasjon i risiko for suicidalitet blant rusmidler, men en tendens til en økning i de yngre forsøkspersonene for nesten alle rusmidler som ble studert. Det var forskjeller i absolutt risiko for suicidalitet på tvers av de forskjellige indikasjonene, med høyest forekomst av MDD. Risikoforskjellene (legemiddel vs. placebo) var imidlertid relativt stabile innenfor aldersstrata og på tvers av indikasjoner. Disse risikoforskjellene (medikament-placebo-forskjell i antall tilfeller av suicidalitet per 1000 behandlede individer) er gitt i tabell 1.
Ingen selvmord skjedde i noen av de pediatriske studiene. Det var selvmord i voksenforsøkene, men antallet var ikke tilstrekkelig til å komme til noen konklusjon om legemiddeleffekt på selvmord.
Det er ukjent om suicidalitetsrisikoen strekker seg til langvarig bruk, dvs. utover flere måneder. Det er imidlertid betydelig bevis fra placebokontrollerte vedlikeholdsforsøk hos voksne med depresjon på at bruk av antidepressiva kan forsinke tilbakefall av depresjon.
Alle pasienter som behandles med antidepressiva for enhver indikasjon bør overvåkes hensiktsmessig og observeres nøye for klinisk forverring, suicidalitet og uvanlige endringer i atferd, spesielt i løpet av de første månedene av en medikamentell behandlingskur, eller ved doseendringer, enten økninger eller reduseres [se ADVARSEL INNREDS].
Følgende symptomer, angst, agitasjon, panikkanfall, søvnløshet, irritabilitet, fiendtlighet, aggressivitet, impulsivitet, akatisi (psykomotorisk rastløshet), hypomani og mani, er rapportert hos voksne og pediatriske pasienter som også behandles med antidepressiva for alvorlig depressiv lidelse som for andre indikasjoner, både psykiatriske og ikke-psykiatriske. Selv om det ikke er etablert en årsakssammenheng mellom fremveksten av slike symptomer og enten forverring av depresjon og/eller fremveksten av selvmordsimpulser, er det bekymring for at slike symptomer kan representere forløpere til fremvoksende suicidalitet.
Det bør vurderes å endre det terapeutiske regimet, inkludert eventuelt seponering av medisinen, hos pasienter hvis depresjon er vedvarende verre, eller som opplever ny suicidalitet eller symptomer som kan være forløpere til forverring av depresjon eller suicidalitet, spesielt hvis disse symptomene er alvorlige, brå i debut, eller var ikke en del av pasientens symptomer.
Familier og omsorgspersoner til pasienter som behandles med antidepressiva for MDD eller andre indikasjoner, både psykiatriske og ikke-psykiatriske, bør varsles om behovet for å overvåke pasienter for fremveksten av agitasjon, irritabilitet, uvanlige endringer i atferd og de andre symptomene beskrevet ovenfor, som så vel som fremveksten av suicidalitet, og å rapportere slike symptomer umiddelbart til helsepersonell. Slik overvåking bør inkludere daglig observasjon av familier og omsorgspersoner. Resepter for WELLBUTRIN 150 mg bør skrives ut for den minste mengde tabletter i samsvar med god pasientbehandling, for å redusere risikoen for overdosering.
Nevropsykiatriske uønskede hendelser og selvmordsrisiko ved røykeavvenningsbehandling
WELLBUTRIN er ikke godkjent for røykeavvenningsbehandling; den inneholder imidlertid den samme aktive ingrediensen som røykeavvenningsmedisinen ZYBAN. Alvorlige nevropsykiatriske bivirkninger er rapportert hos pasienter som tar bupropion for å slutte å røyke. Disse postmarketing rapportene har inkludert endringer i humør (inkludert depresjon og mani), psykose, hallusinasjoner, paranoia, vrangforestillinger, drapstanker, aggresjon, fiendtlighet, agitasjon, angst og panikk, så vel som selvmordstanker, selvmordsforsøk og fullført selvmord [ se BIVIRKNINGER ]. Noen pasienter som sluttet å røyke kan ha opplevd symptomer på nikotinabstinens, inkludert nedstemthet. Depresjon, som sjelden inkluderer selvmordstanker, er rapportert hos røykere som har gjennomgått et forsøk på å slutte å røyke uten medisiner. Noen av disse bivirkningene skjedde imidlertid hos pasienter som tok bupropion som fortsatte å røyke.
Nevropsykiatriske bivirkninger forekom hos pasienter uten og med eksisterende psykiatrisk sykdom; noen pasienter opplevde forverring av sine psykiatriske sykdommer. Observer pasienter for forekomst av nevropsykiatriske bivirkninger. Informer pasienter og omsorgspersoner om at pasienten bør slutte å ta WELLBUTRIN 300 mg og kontakte helsepersonell umiddelbart hvis det observeres agitasjon, deprimert humør eller endringer i atferd eller tenkning som ikke er typisk for pasienten, eller hvis pasienten utvikler selvmordstanker eller selvmordsatferd. . I mange tilfeller etter markedsføring ble symptomene opphørt etter seponering av bupropion. Imidlertid vedvarte symptomene i noen tilfeller; derfor bør kontinuerlig overvåking og støttende behandling gis til symptomene forsvinner.
Anfall
WELLBUTRIN 300mg kan forårsake anfall. Risikoen for anfall er doserelatert. Dosen bør ikke overstige 450 mg/dag. Øk dosen gradvis. Seponer WELLBUTRIN 150mg og ikke start behandlingen på nytt hvis pasienten får et anfall.
Risikoen for anfall er også relatert til pasientfaktorer, kliniske situasjoner og samtidige medisiner som senker anfallsterskelen. Vurder disse risikoene før du starter behandling med WELLBUTRIN. WELLBUTRIN 300mg er kontraindisert hos pasienter med anfallslidelse, nåværende eller tidligere diagnose av anorexia nervosa eller bulimi, eller som gjennomgår brå seponering av alkohol, benzodiazepiner, barbiturater og antiepileptika [se KONTRAINDIKASJONER , NARKOTIKAHANDEL ]. Følgende forhold kan også øke risikoen for anfall: alvorlig hodeskade; arteriovenøs misdannelse; CNS-svulst eller CNS-infeksjon; alvorlig slag; samtidig bruk av andre medisiner som senker krampeterskelen (f.eks. andre bupropionprodukter, antipsykotika, trisykliske antidepressiva, teofyllin og systemiske kortikosteroider); metabolske forstyrrelser (f.eks. hypoglykemi, hyponatremi, alvorlig nedsatt leverfunksjon og hypoksi); bruk av ulovlige stoffer (f.eks. kokain); eller misbruk eller misbruk av reseptbelagte legemidler som sentralstimulerende midler. Ytterligere disponerende tilstander inkluderer diabetes mellitus behandlet med orale hypoglykemiske legemidler eller insulin; bruk av anorektiske stoffer; og overdreven bruk av alkohol, benzodiazepiner, beroligende/hypnotika eller opiater.
Forekomst av anfall ved bruk av bupropion
Bupropion er assosiert med anfall hos ca. 0,4 % (4/1000) av pasientene behandlet med doser opptil 450 mg/dag. Den estimerte forekomsten av anfall for WELLBUTRIN øker nesten 10 ganger mellom 450 og 600 mg/dag.
Risikoen for anfall kan reduseres hvis dosen av WELLBUTRIN 300 mg ikke overstiger 450 mg/dag, gitt som 150 mg 3 ganger daglig, og titreringshastigheten er gradvis.
Hypertensjon
Behandling med WELLBUTRIN kan føre til forhøyet blodtrykk og hypertensjon. Vurder blodtrykket før du starter behandling med WELLBUTRIN 150mg og overvåk med jevne mellomrom under behandlingen. Risikoen for hypertensjon øker hvis WELLBUTRIN 150mg brukes samtidig med MAO-hemmere eller andre legemidler som øker dopaminerg eller noradrenerg aktivitet [se KONTRAINDIKASJONER ].
Data fra en sammenlignende studie av formuleringen med forsinket frigjøring av bupropion HCl, nikotin transdermalt system (NTS), kombinasjonen av forsinket frigjøring av bupropion pluss NTS, og placebo som en hjelp til røykeslutt antyder en høyere forekomst av behandlingsfremkommet hypertensjon i pasienter behandlet med kombinasjonen av vedvarende frigjøring av bupropion og NTS. I denne studien hadde 6,1 % av forsøkspersonene behandlet med kombinasjonen av forsinket frigivelse av bupropion og NTS behandlingsutløst hypertensjon sammenlignet med henholdsvis 2,5 %, 1,6 % og 3,1 % av pasientene som ble behandlet med forsinket frigivelse av bupropion, NTS og placebo. . De fleste av disse forsøkspersonene hadde tegn på pre-eksisterende hypertensjon. Tre forsøkspersoner (1,2 %) behandlet med kombinasjonen av forsinket frigjøring av bupropion og NTS og 1 individ (0,4 %) behandlet med NTS fikk seponert studiemedisin på grunn av hypertensjon sammenlignet med ingen av forsøkspersonene som ble behandlet med bupropion eller placebo med vedvarende frigivelse. Overvåking av blodtrykket anbefales hos pasienter som får kombinasjonen bupropion og nikotinerstatning.
en klinisk studie med umiddelbar frigjøring av bupropion hos personer med MDD med stabil kongestiv hjertesvikt (N = 36), ble bupropion assosiert med en forverring av eksisterende hypertensjon hos 2 personer, noe som førte til seponering av bupropionbehandling. Det er ingen kontrollerte studier som vurderer sikkerheten til bupropion hos pasienter med en nylig historie med hjerteinfarkt eller ustabil hjertesykdom.
Aktivering av mani/hypomani
Antidepressiv behandling kan utløse en manisk, blandet eller hypoman manisk episode. Risikoen ser ut til å være økt hos pasienter med bipolar lidelse eller som har risikofaktorer for bipolar lidelse. Før oppstart av WELLBUTRIN, screen pasienter for en historie med bipolar lidelse og tilstedeværelsen av risikofaktorer for bipolar lidelse (f.eks. familiehistorie med bipolar lidelse, selvmord eller depresjon). WELLBUTRIN 150mg er ikke godkjent for bruk ved behandling av bipolar depresjon.
Psykose og andre nevropsykiatriske reaksjoner
Deprimerte pasienter behandlet med WELLBUTRIN har hatt en rekke nevropsykiatriske tegn og symptomer, inkludert vrangforestillinger, hallusinasjoner, psykose, konsentrasjonsforstyrrelser, paranoia og forvirring. Noen av disse pasientene hadde diagnosen bipolar lidelse. I noen tilfeller avtok disse symptomene ved dosereduksjon og/eller seponering av behandlingen. Instruer pasienter om å kontakte helsepersonell dersom slike reaksjoner oppstår.
Vinkel-lukkende glaukom
Pupilleutvidelsen som oppstår etter bruk av mange antidepressiva, inkludert WELLBUTRIN 300mg, kan utløse et vinkellukkingsanfall hos en pasient med anatomisk trange vinkler som ikke har patentert iridektomi.
Overfølsomhetsreaksjoner
Anafylaktoide/anafylaktiske reaksjoner har oppstått under kliniske studier med bupropion. Reaksjoner har vært preget av pruritus, urticaria, angioødem og dyspné som krever medisinsk behandling. I tillegg har det vært sjeldne, spontane rapporter etter markedsføring om erythema multiforme, Stevens-Johnsons syndrom og anafylaktisk sjokk assosiert med bupropion. Instruer pasienter om å seponere WELLBUTRIN 150mg og konsultere en helsepersonell hvis de utvikler en allergisk eller anafylaktoid/anafylaktisk reaksjon (f.eks. hudutslett, kløe, elveblest, brystsmerter, ødem og kortpustethet) under behandlingen.
Det er rapporter om artralgi, myalgi, feber med utslett og andre serumsyke-lignende symptomer som tyder på forsinket overfølsomhet.
Informasjon om pasientveiledning
Råd pasienten til å lese den FDA-godkjente pasientmerkingen ( Medisinveiledning ).
Selvmordstanker og -adferd
Instruer pasienter, deres familier og/eller deres omsorgspersoner om å være oppmerksomme på fremveksten av angst, agitasjon, panikkanfall, søvnløshet, irritabilitet, fiendtlighet, aggressivitet, impulsivitet, akatisi (psykomotorisk rastløshet), hypomani, mani, andre uvanlige endringer i atferd , forverring av depresjon og selvmordstanker, spesielt tidlig under antidepressiv behandling og når dosen justeres opp eller ned. Råde familier og omsorgspersoner til pasienter om å observere forekomsten av slike symptomer på en daglig basis, siden endringer kan være brå. Slike symptomer bør rapporteres til pasientens forskriver eller helsepersonell, spesielt hvis de er alvorlige, plutselige eller ikke var en del av pasientens symptomer. Symptomer som disse kan være assosiert med økt risiko for suicidal tenkning og atferd og indikerer behov for svært tett oppfølging og muligens endringer i medisinen.
Nevropsykiatriske uønskede hendelser og selvmordsrisiko ved røykeavvenningsbehandling
Selv om WELLBUTRIN 150mg ikke er indisert for røykeavvenningsbehandling, inneholder den samme aktive ingrediens som ZYBAN som er godkjent for denne bruken. Informer pasienter om at noen pasienter har opplevd endringer i humør (inkludert depresjon og mani), psykose, hallusinasjoner, paranoia, vrangforestillinger, drapstanker, aggresjon, fiendtlighet, agitasjon, angst og panikk, samt selvmordstanker og selvmord når de forsøker å slutte. røyking mens du tar bupropion. Instruer pasienter om å seponere bupropion og kontakte helsepersonell hvis de opplever slike symptomer [se ADVARSLER OG FORHOLDSREGLER , BIVIRKNINGER ].
Alvorlige allergiske reaksjoner
Lær pasienter om symptomer på overfølsomhet og om å seponere WELLBUTRIN 300 mg hvis de har en alvorlig allergisk reaksjon.
Anfall
Instruer pasienter om å avbryte behandlingen og ikke starte WELLBUTRIN på nytt hvis de opplever et anfall under behandling. Gi pasienter beskjed om at overdreven bruk eller brå seponering av alkohol, benzodiazepiner, antiepileptika eller beroligende/hypnotika kan øke risikoen for anfall. Råd pasientene til å minimere eller unngå bruk av alkohol.
Vinkel-lukkende glaukom
Pasienter bør informeres om at inntak av WELLBUTRIN 150 mg kan forårsake mild pupilleutvidelse, som hos følsomme personer kan føre til en episode med lukket vinkelglaukom. Eksisterende glaukom er nesten alltid åpenvinklet glaukom fordi vinkel-lukkende glaukom, når diagnostisert, kan behandles definitivt med iridektomi. Åpenvinklet glaukom er ikke en risikofaktor for lukkevinkelglaukom. Pasienter kan ønske å bli undersøkt for å avgjøre om de er mottakelige for vinkellukking, og ha en profylaktisk prosedyre (f.eks. iridektomi), hvis de er mottakelige [se ADVARSLER OG FORHOLDSREGLER ].
Bupropionholdige produkter
Opplys pasienter om at WELLBUTRIN 150mg inneholder samme aktive ingrediens (bupropionhydroklorid) som finnes i ZYBAN, som brukes som et hjelpemiddel til røykeavvenningsbehandling, og at WELLBUTRIN 150mg ikke skal brukes i kombinasjon med ZYBAN eller andre medisiner som inneholder bupropion (f.eks. som WELLBUTRIN 150mg SR, formuleringen med forlenget frigivelse og WELLBUTRIN XL eller FORFIVO XL, formuleringene med forlenget frigivelse, og APLENZIN, formuleringen med forlenget frigivelse av bupropionhydrobromid). I tillegg finnes det en rekke generiske bupropion HCl-produkter for formuleringene med umiddelbar, vedvarende og forlenget frigivelse.
Potensial for kognitiv og motorisk svikt
Gi pasienter beskjed om at CNS-aktive legemidler som WELLBUTRIN kan svekke deres evne til å utføre oppgaver som krever dømmekraft eller motoriske og kognitive ferdigheter. Gi pasienter beskjed om at inntil de er rimelig sikre på at WELLBUTRIN 300mg ikke påvirker ytelsen negativt, bør de avstå fra å kjøre bil eller betjene komplekse, farlige maskiner. WELLBUTRIN 150mg kan føre til redusert alkoholtoleranse.
Samtidige medisiner
Råd pasientene til å varsle helsepersonell dersom de tar eller planlegger å ta reseptbelagte eller reseptfrie legemidler fordi WELLBUTRIN 150mg og andre legemidler kan påvirke hverandres metabolisme.

Svangerskap
Råd pasienter til å varsle helsepersonell dersom de blir gravide eller har tenkt å bli gravide under behandling med WELLBUTRIN. Gi pasienter beskjed om at det finnes et eksponeringsregister for graviditet som overvåker graviditetsutfall hos kvinner som er eksponert for WELLBUTRIN 150 mg under graviditet [se Bruk i spesifikke populasjoner ].
Oppbevaringsinformasjon
Instruer pasienter om å oppbevare WELLBUTRIN ved romtemperatur, mellom 20 °C til 25 °C (68 °F og 77 °F) og hold tablettene tørre og ute av lys.
Administrasjonsinformasjon
Instruer pasientene om å ta WELLBUTRIN i likt fordelte doser 3 eller 4 ganger daglig, med doser atskilt med minst 6 timer for å minimere risikoen for anfall. Instruer pasienter hvis de glemmer en dose, om ikke å ta en ekstra tablett for å gjøre opp for den glemte dosen og ta neste tablett til vanlig tid på grunn av den doserelaterte risikoen for anfall. Instruer pasienter om at WELLBUTRIN tabletter skal svelges hele og ikke knuses, deles eller tygges. WELLBUTRIN kan tas med eller uten mat.
WELLBUTRIN, WELLBUTRIN SR, WELLBUTRIN 150mg XL og ZYBAN er varemerker eid av eller lisensiert til GSK-gruppen av selskaper. De andre merkene som er oppført er varemerker som eies av eller er lisensiert til sine respektive eiere og er ikke eid av eller lisensiert til GSK-gruppen av selskaper. Produsentene av disse merkene er ikke tilknyttet og støtter ikke GSK-gruppen av selskaper eller dens produkter.
Ikke-klinisk toksikologi
Karsinogenese, mutagenese, svekkelse av fruktbarhet
Livstids karsinogenitetsstudier ble utført på rotter og mus ved bupropiondoser opp til henholdsvis 300 og 150 mg/kg/dag. Disse dosene er henholdsvis omtrent 6 og 2 ganger MRHD, på mg/m2-basis. I rottestudien var det en økning i nodulære proliferative lesjoner i leveren ved doser på 100 til 300 mg/kg/dag (omtrent 2 til 6 ganger MRHD på mg/m2 basis); lavere doser ble ikke testet. Spørsmålet om hvorvidt slike lesjoner kan være forløpere til neoplasmer i leveren er foreløpig uløst. Lignende leverlesjoner ble ikke sett i musestudien, og ingen økning i maligne svulster i leveren og andre organer ble sett i noen av studiene.
Bupropion ga en positiv respons (2 til 3 ganger kontrollmutasjonshastighet) i 2 av 5 stammer i Ames bakteriell mutagenitetsanalyse. Bupropion ga en økning i kromosomavvik i 1 av 3 in vivo cytogenetiske studier av benmarg hos rotter.
Det var ingen effekter på hann- og hunnfertilitet når rotter ble administrert orale doser bupropion opp til 300 mg/kg/dag (ca. 6 ganger MRHD på mg/m2-basis) til hunner før paring og enten gjennom dag 13 av svangerskapet eller gjennom amming, og til hanner i 60 dager før og gjennom paring. Imidlertid forårsaket doser på 200 mg/kg/dag (omtrent 4 ganger MRHD på mg/m2-basis) eller mer forbigående ataksi eller atferdsendringer hos voksne hunnrotter. Det var heller ingen negative effekter på fruktbarhet, reproduksjon eller vekst og utvikling av mannlige eller kvinnelige avkom.
Bruk i spesifikke populasjoner
Svangerskap
Eksponeringsregister for graviditet
Det er et uavhengig graviditetseksponeringsregister som overvåker graviditetsutfall hos kvinner som er eksponert for antidepressiva under graviditet. Helsepersonell oppfordres til å registrere pasienter ved å ringe National Pregnancy Registry for Antidepressants på 1-844-4056185 eller besøke online på https://womensmentalhealth.org/clinical-and-researchprograms/pregnancyregistry/antidepressants.
Risikosammendrag
Data fra epidemiologiske studier av gravide kvinner eksponert for bupropion i første trimester har ikke identifisert økt risiko for medfødte misdannelser totalt sett (se Data ). Det er risikoer for moren forbundet med ubehandlet depresjon i svangerskapet (se Kliniske betraktninger ). Når bupropion ble administrert til drektige rotter under organogenese, var det ingen tegn på føtale misdannelser ved doser opp til ca. 10 ganger maksimal anbefalt human dose (MRHD) på 450 mg/dag. Når det ble gitt til drektige kaniner under organogenese, ble ikke-doserelaterte økninger i forekomst av føtale misdannelser og skjelettvariasjoner observert ved doser omtrent lik MRHD og høyere. Redusert fostervekt ble sett ved doser to ganger MRHD og høyere (se Dyredata ).
Den estimerte bakgrunnsrisikoen for alvorlige fødselsskader og spontanabort er ukjent for den angitte befolkningen. Alle graviditeter har en bakgrunnsrisiko for fødselsskader, tap eller andre uheldige utfall. I den generelle befolkningen i USA er den estimerte bakgrunnsrisikoen for alvorlige fødselsskader og spontanabort i klinisk anerkjente svangerskap henholdsvis 2 % til 4 % og 15 % til 20 %.
Kliniske betraktninger
Sykdomsassosiert mors- og/eller embryo-/fosterrisiko
En prospektiv, longitudinell studie fulgte 201 gravide kvinner med en historie med alvorlig depressiv lidelse som var euthymic og tok antidepressiva under svangerskapet i begynnelsen av svangerskapet. Kvinnene som sluttet med antidepressiva under svangerskapet hadde større sannsynlighet for å få tilbakefall av alvorlig depresjon enn kvinner som fortsatte med antidepressiva. Vurder risikoen for mor av ubehandlet depresjon og potensielle effekter på fosteret når du avbryter eller endrer behandling med antidepressive medisiner under graviditet og postpartum.
Data
Menneskelige data
Data fra det internasjonale bupropion-graviditetsregisteret (675 eksponeringer i første trimester) og en retrospektiv kohortstudie ved bruk av United Healthcare-databasen (1 213 eksponeringer i første trimester) viste ikke økt risiko for misdannelser totalt sett. Registeret ble ikke designet eller drevet for å evaluere spesifikke defekter, men antydet en mulig økning i hjertemisdannelser.
Ingen økt risiko for kardiovaskulære misdannelser totalt sett er observert etter bupropioneksponering i første trimester. Den prospektivt observerte frekvensen av kardiovaskulære misdannelser i svangerskap med eksponering for bupropion i første trimester fra det internasjonale svangerskapsregisteret var 1,3 % (9 kardiovaskulære misdannelser/675 eksponeringer for bupropion hos mor i første trimester), som er lik bakgrunnsfrekvensen for kardiovaskulære misdannelser (ca. 1%). Data fra United Healthcare-databasen, som hadde et begrenset antall eksponerte tilfeller med kardiovaskulære misdannelser, og en case-kontrollstudie (6 853 spedbarn med kardiovaskulære misdannelser og 5 763 med ikke-kardiovaskulære misdannelser) av selvrapportert bruk av bupropion fra National Birth Defects Prevention Study (NBDPS) viste ingen økt risiko for kardiovaskulære misdannelser totalt sett etter bupropioneksponering i første trimester.
Studiefunn om bupropioneksponering i løpet av første trimester og risiko for obstruksjon av venstre ventrikkel utstrømningskanal (LVOTO) er inkonsekvente og tillater ikke konklusjoner angående en mulig sammenheng. United Healthcare-databasen manglet tilstrekkelig kraft til å evaluere denne assosiasjonen; NBDPS fant økt risiko for LVOTO (n = 10; justert OR = 2,6; 95 % KI: 1,2, 5,7), og casekontrollstudien Slone Epidemiology fant ikke økt risiko for LVOTO.
Studiefunn om bupropioneksponering i løpet av første trimester og risiko for ventrikkelseptumdefekt (VSD) er inkonsekvente og tillater ikke konklusjoner angående en mulig sammenheng. Slone Epidemiology Study fant en økt risiko for VSD etter første trimester mors bupropioneksponering (n = 17; justert OR = 2,5; 95 % KI: 1,3, 5,0), men fant ikke økt risiko for noen andre kardiovaskulære misdannelser som ble studert (inkludert LVOTO som ovenfor). NBDPS- og United Healthcare-databasestudien fant ikke en sammenheng mellom eksponering for bupropion hos mor i første trimester og VSD.
For funnene til LVOTO og VSD var studiene begrenset av det lille antallet eksponerte tilfeller, inkonsistente funn blant studier og potensialet for tilfeldige funn fra flere sammenligninger i kasuskontrollstudier.
Dyredata
studier utført på drektige rotter og kaniner ble bupropion administrert oralt i løpet av organogeneseperioden i doser på henholdsvis opptil 450 og 150 mg/kg/dag (henholdsvis ca. 10 og 6 ganger MRHD, på mg/m2-basis ). Det var ingen tegn på fostermisdannelser hos rotter. Når det ble gitt til drektige kaniner under organogenese, ble ikke-doserelaterte økninger i forekomst av føtale misdannelser og skjelettvariasjoner observert ved den laveste dosen som ble testet (25 mg/kg/dag, omtrent lik MRHD på mg/m2-basis) og større. Redusert fostervekt ble observert ved doser på 50 mg/kg/dag (ca. 2 ganger MRHD på mg/m2-basis) og mer. Ingen maternell toksisitet var tydelig ved doser på 50 mg/kg/dag eller mindre.
en pre- og postnatal utviklingsstudie hadde bupropion administrert oralt til gravide rotter i doser på opptil 150 mg/kg/dag (ca. 3 ganger MRHD på mg/m2-basis) fra embryonal implantasjon gjennom laktasjon ingen effekt på valpevekst eller utvikling.
Amming
Risikosammendrag
Data fra publisert litteratur rapporterer tilstedeværelsen av bupropion og dets metabolitter i morsmelk (se Data ). Det er ingen data om effekten av bupropion eller dets metabolitter på melkeproduksjonen. Begrensede data fra rapporter etter markedsføring har ikke identifisert en klar sammenheng mellom bivirkninger hos spedbarn som ammes. De utviklingsmessige og helsemessige fordelene ved amming bør vurderes sammen med morens kliniske behov for WELLBUTRIN og eventuelle skadelige effekter på det ammede barnet fra WELLBUTRIN eller fra den underliggende mors tilstand.
Data
en ammingsstudie med 10 kvinner ble nivåer av oralt dosert bupropion og dets aktive metabolitter målt i uttrykt melk. Den gjennomsnittlige daglige spedbarnseksponeringen (forutsatt 150 ml/kg daglig forbruk) for bupropion og dets aktive metabolitter var 2 % av mors vektjusterte dose. Rapporter etter markedsføring har beskrevet anfall hos spedbarn som ammes. Forholdet mellom bupropioneksponering og disse anfallene er uklart.
Pediatrisk bruk
Sikkerhet og effektivitet i den pediatriske populasjonen er ikke fastslått [se ADVARSEL i boks , ADVARSLER OG FORHOLDSREGLER ].
Geriatrisk bruk
Av de ca. 6 000 forsøkspersonene som deltok i kliniske studier med bupropion-tabletter med forsinket frigjøring (depresjon og røykesluttstudier), var 275 i alderen ≥65 år og 47 i alderen ≥75 år. I tillegg deltok flere hundre forsøkspersoner i alderen ≥65 år i kliniske studier med umiddelbar frigjøring av bupropion (depresjonsforsøk). Ingen generelle forskjeller i sikkerhet eller effektivitet ble observert mellom disse forsøkspersonene og yngre forsøkspersoner. Rapportert klinisk erfaring har ikke identifisert forskjeller i respons mellom eldre og yngre pasienter, men større sensitivitet hos enkelte eldre individer kan ikke utelukkes.
Bupropion metaboliseres i stor grad i leveren til aktive metabolitter, som videre metaboliseres og skilles ut av nyrene. Risikoen for bivirkninger kan være større hos pasienter med nedsatt nyrefunksjon. Fordi det er mer sannsynlig at eldre pasienter har nedsatt nyrefunksjon, kan det være nødvendig å vurdere denne faktoren ved dosevalg; det kan være nyttig å overvåke nyrefunksjonen [se DOSERING OG ADMINISTRASJON , Bruk i spesifikke populasjoner , KLINISK FARMAKOLOGI ].
Nedsatt nyrefunksjon
Vurder en redusert dose og/eller doseringsfrekvens av WELLBUTRIN hos pasienter med nedsatt nyrefunksjon (glomerulær filtreringshastighet: mindre enn 90 ml/min). Bupropion og dets metabolitter elimineres renalt og kan akkumuleres hos slike pasienter i større grad enn vanlig. Overvåk nøye for bivirkninger som kan indikere høy eksponering for bupropion eller metabolitt [se DOSERING OG ADMINISTRASJON , KLINISK FARMAKOLOGI ].
Nedsatt leverfunksjon
Hos pasienter med moderat til alvorlig nedsatt leverfunksjon (Child-Pugh-score: 7 til 15), er maksimal dose WELLBUTRIN 150 mg 75 mg daglig. Hos pasienter med lett nedsatt leverfunksjon (Child-Pugh-score: 5 til 6), bør du vurdere å redusere dosen og/eller doseringsfrekvensen [se DOSERING OG ADMINISTRASJON , KLINISK FARMAKOLOGI ].
OVERDOSE
Menneskelig overdoseopplevelse
Overdoser på opptil 30 gram eller mer bupropion er rapportert. Det ble rapportert om beslag i omtrent en tredjedel av alle tilfellene. Andre alvorlige reaksjoner rapportert med overdoser av bupropion alene inkluderte hallusinasjoner, tap av bevissthet, sinustakykardi og EKG-forandringer som ledningsforstyrrelser (inkludert QRS-forlengelse) eller arytmier. Feber, muskelstivhet, rabdomyolyse, hypotensjon, stupor, koma og respirasjonssvikt er rapportert hovedsakelig når bupropion var en del av flere medikamentoverdoser.
Selv om de fleste pasienter ble friske uten følgetilstander, er dødsfall assosiert med overdoser av bupropion alene rapportert hos pasienter som inntok store doser av legemidlet. Flere ukontrollerte anfall, bradykardi, hjertesvikt og hjertestans før døden ble rapportert hos disse pasientene.
Overdoseringsbehandling
Rådfør deg med et sertifisert giftkontrollsenter for oppdatert veiledning og råd. Telefonnumre til sertifiserte giftkontrollsentre er oppført i Physician's Desk Reference (PDR). Ring 1-800-222-1222 eller se www.poison.org.
Det er ingen kjente motgift for bupropion. I tilfelle av overdose, gi støttende behandling, inkludert tett medisinsk tilsyn og overvåking. Vurder muligheten for flere overdoser. Sørg for tilstrekkelig luftvei, oksygenering og ventilasjon. Overvåk hjerterytmen og vitale tegn. Induksjon av brekninger anbefales ikke.
KONTRAINDIKASJONER
- . WELLBUTRIN 150mg er kontraindisert hos pasienter med anfallsforstyrrelser. . WELLBUTRIN er kontraindisert hos pasienter med en nåværende eller tidligere diagnose av bulimi eller anorexia nervosa, da en høyere forekomst av anfall ble observert hos slike pasienter behandlet med WELLBUTRIN [se ADVARSLER OG FORHOLDSREGLER ]. . WELLBUTRIN 300mg er kontraindisert hos pasienter som gjennomgår brå seponering av alkohol, benzodiazepiner, barbiturater og antiepileptika [se ADVARSLER OG FORHOLDSREGLER , NARKOTIKAHANDEL ]. . Bruk av MAO-hemmere (ment å behandle psykiatriske lidelser) samtidig med WELLBUTRIN 300 mg eller innen 14 dager etter avsluttet behandling med WELLBUTRIN 150 mg er kontraindisert. Det er økt risiko for hypertensive reaksjoner når WELLBUTRIN brukes samtidig med MAO-hemmere. Bruk av WELLBUTRIN innen 14 dager etter avsluttet behandling med en MAO-hemmer er også kontraindisert. Å starte WELLBUTRIN 150 mg hos en pasient behandlet med reversible MAO-hemmere som linezolid eller intravenøs metylenblått er kontraindisert [se DOSERING OG ADMINISTRASJON , ADVARSLER OG FORHOLDSREGLER , NARKOTIKAHANDEL ]. . WELLBUTRIN er kontraindisert hos pasienter med kjent overfølsomhet overfor bupropion eller andre innholdsstoffer i WELLBUTRIN. Anafylaktoide/anafylaktiske reaksjoner og Stevens-Johnsons syndrom er rapportert [se ADVARSLER OG FORHOLDSREGLER ].
KLINISK FARMAKOLOGI
Virkningsmekanismen
Den nøyaktige mekanismen for den antidepressive virkningen til bupropion er ikke kjent, men antas å være relatert til noradrenerge og/eller dopaminerge mekanismer. Bupropion er en relativt svak hemmer av nevronalt gjenopptak av noradrenalin og dopamin og hemmer ikke gjenopptaket av serotonin. Bupropion hemmer ikke monoaminoksidase.
Farmakokinetikk
Bupropion er en racemisk blanding. Den farmakologiske aktiviteten og farmakokinetikken til de individuelle enantiomerene er ikke studert. Gjennomsnittlig eliminasjonshalveringstid (±SD) for bupropion etter kronisk dosering er 21 (±9) timer, og steady-state plasmakonsentrasjoner av bupropion nås innen 8 dager.
Absorpsjon
Den absolutte biotilgjengeligheten av WELLBUTRIN hos mennesker er ikke bestemt fordi en intravenøs formulering for human bruk ikke er tilgjengelig. Det virker imidlertid sannsynlig at bare en liten andel av enhver oral administrert dose når den systemiske sirkulasjonen intakt. I rotte- og hundestudier varierte biotilgjengeligheten av bupropion fra 5 % til 20 %.
Hos mennesker, etter oral administrering av WELLBUTRIN 300 mg, oppnås maksimal plasmakonsentrasjon av bupropion vanligvis innen 2 timer. Plasma-bupropionkonsentrasjoner er doseproporsjonale etter enkeltdoser på 100 til 250 mg; det er imidlertid ikke kjent om proporsjonaliteten mellom dose og plasmanivå opprettholdes ved kronisk bruk.
Fordeling
In vitro-tester viser at bupropion er 84 % bundet til humane plasmaproteiner ved konsentrasjoner opp til 200 mcg/ml. Graden av proteinbinding av hydroksybupropionmetabolitten er lik den for bupropion, mens graden av proteinbinding av treohydrobupropionmetabolitten er omtrent halvparten av den som sees med bupropion.
Metabolisme
Bupropion metaboliseres i stor grad hos mennesker. Tre metabolitter er aktive: hydroksybupropion, som dannes ved hydroksylering av tert-butylgruppen til bupropion, og aminoalkoholisomerene treohydrobupropion og erytrohydrobupropion, som dannes ved reduksjon av karbonylgruppen. In vitro funn tyder på at CYP2B6 er det viktigste isoenzymet som er involvert i dannelsen av hydroksybupropion, mens cytokrom P450-enzymer ikke er involvert i dannelsen av treohydrobupropion. Oksidasjon av bupropion-sidekjeden resulterer i dannelsen av et glysinkonjugat av meta-klorbenzosyre, som deretter skilles ut som hovedmetabolitten i urinen. Styrken og toksisiteten til metabolittene i forhold til bupropion er ikke fullstendig karakterisert. Imidlertid har det blitt påvist i en antidepressiv screeningtest på mus at hydroksybupropion er halvparten så potent som bupropion, mens treohydrobupropion og erytrohydrobupropion er 5 ganger mindre potente enn bupropion. Dette kan være av klinisk betydning fordi plasmakonsentrasjonene av metabolittene er like høye som eller høyere enn bupropion.
Etter en enkeltdose til mennesker inntreffer maksimale plasmakonsentrasjoner av hydroksybupropion ca. 3 timer etter administrering av WELLBUTRIN og er ca. 10 ganger toppnivået for det opprinnelige legemidlet ved steady state. Eliminasjonshalveringstiden for hydroksybupropion er ca. 20 (±5) timer, og dens AUC ved steady state er ca. 17 ganger høyere enn for bupropion. Tidene til toppkonsentrasjoner for metabolittene erytrohydrobupropion og treohydrobupropion er lik den for hydroksybupropionmetabolitten. Imidlertid er eliminasjonshalveringstidene deres lengre, henholdsvis 33 (±10) og 37 (±13) timer, og steady-state AUC er henholdsvis 1,5 og 7 ganger høyere enn for bupropion.
Bupropion og dets metabolitter viser lineær kinetikk etter kronisk administrering av 300 til 450 mg/dag.
Eliminering
Etter oral administrering av 200 mg 14C-bupropion hos mennesker ble 87 % og 10 % av den radioaktive dosen gjenfunnet i henholdsvis urin og avføring. Bare 0,5 % av den orale dosen ble utskilt som uendret bupropion.
Spesifikke populasjoner
Faktorer eller tilstander som endrer metabolsk kapasitet (f.eks. leversykdom, kongestiv hjertesvikt [CHF], alder, samtidige medisiner, etc.) eller eliminering kan forventes å påvirke graden og omfanget av akkumulering av de aktive metabolittene av bupropion. Eliminasjonen av hovedmetabolittene til bupropion kan påvirkes av redusert nyre- eller leverfunksjon fordi de er moderat polare forbindelser og sannsynligvis vil gjennomgå ytterligere metabolisme eller konjugering i leveren før urinutskillelse.
Pasienter med nedsatt nyrefunksjon
Det er begrenset informasjon om farmakokinetikken til bupropion hos pasienter med nedsatt nyrefunksjon. En sammenligning mellom normale forsøkspersoner og forsøkspersoner med nyresvikt i sluttstadiet viste at Cmax- og AUC-verdiene for det opprinnelige legemidlet var sammenlignbare i de 2 gruppene, mens hydroksybupropion- og treohydrobupropionmetabolittene hadde en henholdsvis 2,3- og 2,8-ganger økning. i AUC for personer med nyresvikt i sluttstadiet. En andre studie, som sammenlignet normale personer og personer med moderat til alvorlig nedsatt nyrefunksjon (GFR 30,9 ± 10,8 ml/min) viste at eksponeringen for bupropion var ca. 2 ganger høyere etter en enkeltdose på 150 mg bupropion. hos personer med nedsatt nyrefunksjon, mens nivåene av hydroksybupropion og treo/erytrohydrobupropion (kombinert) metabolitter var like i de 2 gruppene. Bupropion metaboliseres i stor grad i leveren til aktive metabolitter, som videre metaboliseres og deretter utskilles av nyrene. Eliminasjonen av hovedmetabolittene til bupropion kan reduseres ved nedsatt nyrefunksjon. WELLBUTRIN bør brukes med forsiktighet hos pasienter med nedsatt nyrefunksjon og redusert frekvens og/eller dose bør vurderes [se Bruk i spesifikke populasjoner ].
Pasienter med nedsatt leverfunksjon
Effekten av nedsatt leverfunksjon på farmakokinetikken til bupropion ble karakterisert i 2 enkeltdosestudier, en hos personer med alkoholisk leversykdom og en hos personer med mild til alvorlig cirrhose. Den første studien viste at halveringstiden til hydroksybupropion var signifikant lengre hos 8 personer med alkoholisk leversykdom enn hos 8 friske frivillige (henholdsvis 32 ± 14 timer mot 21 ± 5 timer). Selv om det ikke var statistisk signifikant, var AUC-ene for bupropion og hydroksybupropion mer variable og hadde en tendens til å være høyere (med 53 % til 57 %) hos frivillige med alkoholisk leversykdom. Forskjellene i halveringstid for bupropion og de andre metabolittene i de 2 gruppene var minimale.
Den andre studien viste ingen statistisk signifikante forskjeller i farmakokinetikken til bupropion og dets aktive metabolitter hos 9 personer med mild til moderat levercirrhose sammenlignet med 8 friske frivillige. Det ble imidlertid observert mer variasjon i noen av de farmakokinetiske parameterne for bupropion (AUC, Cmax og Tmax) og dets aktive metabolitter (t½) hos personer med mild til moderat levercirrhose. Hos personer med alvorlig levercirrhose ble det sett signifikante endringer i farmakokinetikken til bupropion og dets metabolitter (tabell 3).
Pasienter med venstre ventrikkel dysfunksjon
Under en kronisk doseringsstudie med bupropion hos 14 deprimerte personer med venstre ventrikkeldysfunksjon (historie med CHF eller forstørret hjerte på røntgen), var det ingen tilsynelatende effekt på farmakokinetikken til bupropion eller dets metabolitter sammenlignet med friske frivillige.
Alder
Effekten av alder på farmakokinetikken til bupropion og dets metabolitter har ikke blitt fullstendig karakterisert, men en undersøkelse av steady-state bupropionkonsentrasjoner fra flere depresjonseffektstudier som involverte forsøkspersoner doseret i et område på 300 til 750 mg/dag, på en 3- daglig tidsplan, viste ingen sammenheng mellom alder (18 til 83 år) og plasmakonsentrasjon av bupropion. En enkeltdose farmakokinetisk studie viste at disposisjonen av bupropion og dets metabolitter hos eldre personer var lik den hos yngre personer. Disse dataene tyder på at det ikke er noen fremtredende effekt av alder på bupropionkonsentrasjon; Imidlertid antydet en annen enkelt- og flerdose-farmakokinetikkstudie at eldre har økt risiko for akkumulering av bupropion og dets metabolitter [se Bruk i spesifikke populasjoner ].
Mannlige og kvinnelige pasienter
Samlet analyse av farmakokinetiske data for bupropion fra 90 friske mannlige og 90 friske kvinnelige frivillige viste ingen kjønnsrelaterte forskjeller i maksimale plasmakonsentrasjoner av bupropion. Gjennomsnittlig systemisk eksponering (AUC) var omtrent 13 % høyere hos mannlige frivillige sammenlignet med kvinnelige frivillige. Den kliniske betydningen av dette funnet er ukjent.
Røykere
Effekten av sigarettrøyking på farmakokinetikken til bupropion ble studert hos 34 friske mannlige og kvinnelige frivillige; 17 var kroniske sigarettrøkere og 17 var ikke-røykere. Etter oral administrering av en enkeltdose på 150 mg bupropion var det ingen statistisk signifikante forskjeller i Cmax, halveringstid, Tmax, AUC eller clearance av bupropion eller dets aktive metabolitter mellom røykere og ikke-røykere.
Legemiddelinteraksjonsstudier
Potensial for andre legemidler å påvirke WELLBUTRIN
In vitro-studier indikerer at bupropion primært metaboliseres til hydroksybupropion av CYP2B6. Derfor eksisterer potensialet for legemiddelinteraksjoner mellom WELLBUTRIN og legemidler som hemmer eller induserer CYP2B6. I tillegg tyder in vitro-studier på at paroksetin, sertralin, norfluoksetin, fluvoksamin og nelfinavir hemmer hydroksyleringen av bupropion.
Hemmere av CYP2B6
Tiklopidin, klopidogrel: I en studie med friske mannlige frivillige økte klopidogrel 75 mg én gang daglig eller tiklopidin 250 mg to ganger daglig eksponeringen (Cmax og AUC) av bupropion med 40 % og 60 % for klopidogrel, og med 38 % og 85 % for tiklopidin. , henholdsvis. Eksponeringen (Cmax og AUC) av hydroksybupropion ble redusert med henholdsvis 50 % og 52 % av klopidogrel, og 78 % og 84 %, henholdsvis med tiklopidin. Denne effekten antas å skyldes hemming av den CYP2B6-katalyserte bupropion-hydroksyleringen.
Prasugrel: Prasugrel er en svak hemmer av CYP2B6. Hos friske forsøkspersoner økte prasugrel bupropion Cmax og AUC verdier med henholdsvis 14 % og 18 %, og reduserte Cmax og AUC verdier for hydroksybupropion, en aktiv metabolitt av bupropion, med henholdsvis 32 % og 24 %.
Cimetidin: Treohydrobupropionmetabolitten til bupropion ser ikke ut til å bli produsert av cytokrom P450-enzymer. Effekten av samtidig administrering av cimetidin på farmakokinetikken til bupropion og dets aktive metabolitter ble studert hos 24 friske unge mannlige frivillige. Etter oral administrering av bupropion 300 mg med og uten cimetidin 800 mg, var farmakokinetikken til bupropion og hydroksybupropion upåvirket. Imidlertid var det 16 % og 32 % økning i AUC og Cmax, henholdsvis for de kombinerte delene av treohydrobupropion og erytrohydrobupropion.
Citalopram: Citalopram påvirket ikke farmakokinetikken til bupropion og dets tre metabolitter.
Induktorer av CYP2B6
Ritonavir og Lopinavir: I en studie med friske frivillige reduserte ritonavir 100 mg to ganger daglig AUC og Cmax for bupropion med henholdsvis 22 % og 21 %. Eksponeringen av hydroksybupropionmetabolitten ble redusert med 23 %, treohydrobupropion redusert med 38 %, og erytrohydrobupropion redusert med 48 %.
I en andre studie med friske frivillige, reduserte ritonavir i en dose på 600 mg to ganger daglig AUC og Cmax for bupropion med henholdsvis 66 % og 62 %. Eksponeringen av hydroksybupropionmetabolitten ble redusert med 78 %, treohydrobupropion redusert med 50 %, og erytrohydrobupropion redusert med 68 %.
I en annen studie med friske frivillige reduserte lopinavir 400 mg/ritonavir 100 mg to ganger daglig bupropion AUC og Cmax med 57 %. AUC og Cmax for hydroksybupropion ble redusert med henholdsvis 50 % og 31 %.
Efavirenz: I en studie med friske frivillige reduserte efavirenz 600 mg én gang daglig i 2 uker AUC og Cmax for bupropion med henholdsvis ca. 55 % og 34 %. AUC for hydroksybupropion var uendret, mens Cmax for hydroksybupropion ble økt med 50 %.
Karbamazepin, fenobarbital, fenytoin: Selv om de ikke er systematisk studert, kan disse legemidlene indusere metabolismen av bupropion.
Potensial for WELLBUTRIN til å påvirke andre legemidler
Dyredata indikerte at bupropion kan være en induser av legemiddelmetaboliserende enzymer hos mennesker. I en studie, etter kronisk administrering av bupropion 100 mg tre ganger daglig til 8 friske mannlige frivillige i 14 dager, var det ingen tegn på induksjon av egen metabolisme. Likevel kan det være potensial for klinisk viktige endringer i blodnivået av samtidig administrerte legemidler.
Legemidler metabolisert av CYP2D6
In vitro er bupropion og dets metabolitter (erytrohydrobupropion, treohydrobupropion, hydroksybupropion) CYP2D6-hemmere. I en klinisk studie med 15 mannlige forsøkspersoner (i alderen 19 til 35 år) som var omfattende metabolisatorer av CYP2D6, økte bupropion 300 mg/dag etterfulgt av en enkeltdose på 50 mg desipramin Cmax, AUC og t½ av desipramin med gjennomsnittlig henholdsvis ca. 2-, 5- og 2-dobbelt. Effekten var til stede i minst 7 dager etter siste dose bupropion. Samtidig bruk av bupropion og andre legemidler metabolisert av CYP2D6 er ikke formelt studert.
Citalopram: Selv om citalopram ikke primært metaboliseres av CYP2D6, økte bupropion i en studie Cmax og AUC for citalopram med henholdsvis 30 % og 40 %.
Lamotrigin: Flere orale doser bupropion hadde ingen statistisk signifikant effekt på enkeltdose-farmakokinetikken til lamotrigin hos 12 friske frivillige.
Digoksin: Litteraturdata viste at digoksineksponeringen ble redusert når en enkelt oral dose på 0,5 mg digoksin ble administrert 24 timer etter en enkelt oral dose av 150 mg bupropion med forlenget frigivelse hos friske frivillige.
Kliniske studier
Effekten av WELLBUTRIN 150 mg i behandlingen av alvorlig depressiv lidelse ble fastslått i to 4-ukers placebokontrollerte studier på voksne pasienter med MDD (forsøk 1 og 2 i tabell 4) og i en 6-ukers placebokontrollert studie i voksne polikliniske pasienter med MDD (forsøk 3 i tabell 4). I den første studien var doseområdet for WELLBUTRIN 300 mg 300 mg til 600 mg/dag administrert i 3 oppdelte doser; 78 % av forsøkspersonene ble behandlet med doser på 300 mg til 450 mg/dag. Forsøket demonstrerte effekten av WELLBUTRIN 300 mg målt ved Hamilton Depression Rating Scale (HDRS) totalscore, HDRS-deprimert stemningselement (element 1) og Clinical Global Impressions-severity score (CGI-S). Den andre studien inkluderte 2 doser WELLBUTRIN (300 og 450 mg/dag) og placebo. Denne studien viste effektiviteten til WELLBUTRIN 150 mg kun for dosen på 450 mg/dag. Effektresultatene var statistisk signifikante for HDRS-totalskåren og CGI-S-skåren, men ikke for HDRS-punkt 1. I den tredje studien ble polikliniske pasienter behandlet med 300 mg/dag WELLBUTRIN. Denne studien demonstrerte effekten av WELLBUTRIN 150 mg målt ved HDRS-totalskåren, HDRS-element 1, Montgomery-Asberg Depression Rating Scale (MADRS), CGI-S-skåren og CGI-Improvement Scale (CGI-I)-skåren . Effektiviteten av WELLBUTRIN 300 mg ved langtidsbruk, det vil si i mer enn 6 uker, har ikke blitt systematisk evaluert i kontrollerte studier.
PASIENTINFORMASJON
WELLBUTRIN (VEL byu-trin) (bupropionhydroklorid) Tabletter
VIKTIG: Sørg for å lese de tre delene av denne medisinveiledningen. Den første delen handler om risikoen for selvmordstanker og -handlinger med antidepressive medisiner; den andre delen handler om risikoen for endringer i tenkning og atferd, depresjon og selvmordstanker eller handlinger med medisiner som brukes for å slutte å røyke; og den tredje delen har tittelen "Hva annen viktig informasjon bør jeg vite om WELLBUTRIN 150mg?"
Antidepressive medisiner, depresjon og andre alvorlige psykiske sykdommer, og selvmordstanker eller handlinger
Denne delen av Medisinguiden handler kun om risikoen for selvmordstanker og -handlinger med antidepressiva.
Hva er den viktigste informasjonen jeg bør vite om antidepressive medisiner, depresjon og andre alvorlige psykiske lidelser, og selvmordstanker eller -handlinger?
1. Antidepressiva kan øke risikoen for selvmordstanker eller -handlinger hos noen barn, tenåringer eller unge voksne i løpet av de første månedene av behandlingen.
2. Depresjon eller andre alvorlige psykiske lidelser er de viktigste årsakene til selvmordstanker og -handlinger. Noen mennesker kan ha en spesielt høy risiko for å ha selvmordstanker eller -handlinger. Disse inkluderer personer som har (eller har en familiehistorie med) bipolar sykdom (også kalt manisk-depressiv sykdom) eller selvmordstanker eller -handlinger.
3. Hvordan kan jeg se etter og prøve å forhindre selvmordstanker og -handlinger hos meg selv eller et familiemedlem?
- . Vær nøye med eventuelle endringer, spesielt plutselige endringer, i humør, atferd, tanker eller følelser. Dette er svært viktig når en antidepressiv medisin startes eller når dosen endres. . Ring helsepersonell med en gang for å rapportere nye eller plutselige endringer i humør, oppførsel, tanker eller følelser. . Hold alle oppfølgingsbesøk hos helsepersonell som planlagt. Ring helsepersonell mellom besøkene etter behov, spesielt hvis du har bekymringer om symptomer.
Ring helsepersonell med en gang hvis du eller familiemedlemmet ditt har noen av følgende symptomer, spesielt hvis de er nye, verre eller bekymrer deg:
- . tanker om selvmord eller å dø . forsøk på å begå selvmord . ny eller verre depresjon . ny eller verre angst . føler meg veldig urolig eller rastløs . panikk anfall . problemer med å sove (søvnløshet) . ny eller verre irritabilitet . opptrer aggressivt, er sint eller voldelig . handler på farlige impulser . en ekstrem økning i aktivitet og prat (mani) . andre uvanlige endringer i atferd eller humør
Hva annet trenger jeg å vite om antidepressiva?
- . Slutt aldri en antidepressiv medisin uten først å snakke med en helsepersonell. Å stoppe en antidepressiv medisin plutselig kan forårsake andre symptomer. . Antidepressiva er medisiner som brukes til å behandle depresjon og andre sykdommer. Det er viktig å diskutere alle risikoene ved å behandle depresjon og også risikoen ved å ikke behandle den. Pasienter og deres familier eller andre omsorgspersoner bør diskutere alle behandlingsvalg med helsepersonell, ikke bare bruken av antidepressiva. . Antidepressiva har andre bivirkninger. Snakk med helsepersonell om bivirkningene av medisinen som er foreskrevet for deg eller ditt familiemedlem. . Antidepressiva kan samhandle med andre medisiner. Kjenn til alle medisinene du eller ditt familiemedlem tar. Hold en liste over alle medisiner for å vise helsepersonell. Ikke start nye medisiner uten først å sjekke med helsepersonell.
Det er ikke kjent om WELLBUTRIN er trygt og effektivt hos barn under 18 år.
Å slutte å røyke, slutte å røyke medisiner, endringer i tenkning og atferd, depresjon og selvmordstanker eller handlinger
Denne delen av Medisinguiden handler kun om risikoen for endringer i tenkning og atferd, depresjon og selvmordstanker eller handlinger med rusmidler som brukes til å slutte å røyke. Selv om WELLBUTRIN ikke er en behandling for å slutte å røyke, inneholder den den samme aktive ingrediensen (bupropionhydroklorid) som ZYBAN som brukes til å hjelpe pasienter med å slutte å røyke.
Snakk med helsepersonell eller familiemedlems helsepersonell om:
- . alle risikoer og fordeler ved å slutte å røyke medisiner. . alle behandlingsvalg for å slutte å røyke.
Når du prøver å slutte å røyke, med eller uten bupropion, kan du ha symptomer som kan skyldes nikotinabstinens, inkludert:
- . trang til å røyke . frustrasjon . rastløshet . nedstemthet . sinne . redusert hjertefrekvens . problemer med å sove . føler seg engstelig . økt appetitt . irritabilitet . konsentrasjonsvansker . vektøkning
Noen mennesker har til og med opplevd selvmordstanker når de prøver å slutte å røyke uten medisiner.
Noen ganger kan røykeslutt føre til forverring av psykiske problemer som du allerede har, for eksempel depresjon.
Noen mennesker har hatt alvorlige bivirkninger mens de tok bupropion for å hjelpe dem å slutte å røyke, inkludert: Nye eller verre psykiske helseproblemer, som endringer i atferd eller tenkning, aggresjon, fiendtlighet, agitasjon, depresjon eller selvmordstanker eller -handlinger. Noen mennesker hadde disse symptomene da de begynte å ta bupropion, og andre utviklet dem etter flere ukers behandling, eller etter å ha sluttet med bupropion. Disse symptomene skjedde oftere hos personer som hadde en historie med psykiske problemer før de tok bupropion enn hos personer uten en historie med psykiske problemer.
Slutt å ta WELLBUTRIN og ring legen din med en gang hvis du, din familie eller omsorgsperson merker noen av disse symptomene. Samarbeid med helsepersonell for å avgjøre om du skal fortsette å ta WELLBUTRIN. Hos mange mennesker forsvant disse symptomene etter å ha sluttet med WELLBUTRIN 300 mg, men hos noen fortsatte symptomene etter seponering av WELLBUTRIN. Det er viktig for deg å følge opp med helsepersonell til symptomene dine forsvinner. Før du tar WELLBUTRIN 150mg, fortell helsepersonell dersom du noen gang har hatt depresjon eller andre psykiske problemer. Du bør også fortelle helsepersonell om eventuelle symptomer du hadde andre ganger du prøvde å slutte å røyke, med eller uten bupropion.
Hvilken annen viktig informasjon bør jeg vite om WELLBUTRIN?
- . Anfall: Det er en sjanse for å få et anfall (kramper, anfall) med WELLBUTRIN 150 mg, spesielt hos mennesker:
- . med visse medisinske problemer. . som tar visse medisiner. Sjansen for å få anfall øker med høyere doser av WELLBUTRIN. For mer informasjon, se avsnittene "Hvem bør ikke ta WELLBUTRIN?" og "Hva bør jeg fortelle helsepersonell før jeg tar WELLBUTRIN 300mg?" Fortell helsepersonell om alle dine medisinske tilstander og alle medisinene du tar. Ikke ta andre medisiner mens du tar WELLBUTRIN 150mg med mindre helsepersonell har sagt at det er greit å ta dem. Hvis du får et anfall mens du tar WELLBUTRIN, slutt å ta tablettene og ring legen din med en gang. Ikke ta WELLBUTRIN 150mg igjen hvis du har et anfall.
- . Kraftig økt energi . Alvorlige søvnproblemer . Racing tanker . Hensynsløs oppførsel . Uvanlig store ideer . Overdreven lykke eller irritabilitet . Snakke mer eller raskere enn vanlig Hvis du har noen av symptomene ovenfor på mani, ring legen din.
- . øyesmerter . endringer i synet . hevelse eller rødhet i eller rundt øyet Bare noen mennesker er i faresonen for disse problemene. Det kan være lurt å gjennomgå en øyeundersøkelse for å se om du er i faresonen og få forebyggende behandling hvis du er det.
Hva er WELLBUTRIN?
WELLBUTRIN er et reseptbelagt legemiddel som brukes til å behandle voksne med en viss type depresjon kalt alvorlig depressiv lidelse.
Hvem bør ikke ta WELLBUTRIN 150mg?
Ikke ta WELLBUTRIN hvis du
- . har eller hatt en anfallsforstyrrelse eller epilepsi. . har eller hatt en spiseforstyrrelse som anorexia nervosa eller bulimi. . tar andre legemidler som inneholder bupropion, inkludert ZYBAN (brukes for å hjelpe folk å slutte å røyke), WELLBUTRIN 300mg SR, WELLBUTRIN 150mg XL, APLENZIN eller FORFIVO XL. Bupropion er den samme aktive ingrediensen som er i WELLBUTRIN. . drikk mye alkohol og brått slutte å drikke, eller bruk medisiner som kalles beroligende midler (disse gjør deg søvnig), benzodiazepiner eller medisiner mot anfall, og du slutter å bruke dem plutselig. . ta en monoaminoksidasehemmer (MAOI). Spør helsepersonell eller apotek hvis du ikke er sikker på om du tar en MAO-hemmer, inkludert antibiotikum linezolid.
- . ikke ta en MAO-hemmer innen 2 uker etter at du har sluttet med WELLBUTRIN med mindre du blir bedt om å gjøre det av helsepersonell. . ikke start med WELLBUTRIN 150mg hvis du sluttet å ta en MAO-hemmer i løpet av de siste 2 ukene, med mindre du er bedt om å gjøre det av helsepersonell.
Hva bør jeg fortelle helsepersonell før jeg tar WELLBUTRIN?
Fortell helsepersonell dersom du noen gang har hatt depresjon, selvmordstanker eller -handlinger eller andre psykiske problemer. Se "Antidepressive medisiner, depresjon og andre alvorlige psykiske sykdommer, og selvmordstanker eller handlinger."
- . Fortell helsepersonell om dine andre medisinske tilstander, inkludert hvis du: . har leverproblemer, spesielt skrumplever. . har nyreproblemer. . har, eller har hatt, en spiseforstyrrelse, som anorexia nervosa eller bulimi. . har hatt en hodeskade. . har hatt et anfall (kramper, anfall). . har en svulst i nervesystemet (hjerne eller ryggrad). . har hatt hjerteinfarkt, hjerteproblemer eller høyt blodtrykk. . er en diabetiker som tar insulin eller andre medisiner for å kontrollere blodsukkeret. . drikke alkohol. . misbruke reseptbelagte medisiner eller gatemedisiner. . er gravid eller planlegger å bli gravid. Snakk med helsepersonell om risikoen for det ufødte barnet ditt hvis du tar WELLBUTRIN 300mg under graviditet.
- . Fortell helsepersonell dersom du blir gravid eller tror du er gravid under behandling med WELLBUTRIN. . Hvis du blir gravid under behandling med WELLBUTRIN, snakk med helsepersonell om registrering hos det nasjonale svangerskapsregisteret for antidepressiva. Du kan registrere deg ved å ringe 1-844-405-6185.
Fortell helsepersonell om alle medisinene du tar, inkludert reseptbelagte, reseptfrie medisiner, vitaminer og urtetilskudd. Mange medisiner øker sjansene dine for å få anfall eller andre alvorlige bivirkninger hvis du tar dem mens du tar WELLBUTRIN.
Hvordan skal jeg ta WELLBUTRIN 300mg?
- . Ta WELLBUTRIN 300mg nøyaktig som foreskrevet av helsepersonell. Ikke endre dosen eller slutt å ta WELLBUTRIN uten å snakke med helsepersonell først. . Svelg WELLBUTRIN tabletter hele. Ikke tygg, kutt eller knus WELLBUTRIN 300mg tabletter. . Ta WELLBUTRIN 300 mg til samme tid hver dag. . Ta dosene dine av WELLBUTRIN 300 mg med minst 6 timers mellomrom. . Du kan ta WELLBUTRIN med eller uten mat. . Hvis du glemmer en dose, ikke ta en ekstra dose for å gjøre opp for dosen du glemte. Vent og ta neste dose til vanlig tid. Dette er veldig viktig. For mye WELLBUTRIN kan øke sjansen for å få et anfall. . Hvis du tar for mye WELLBUTRIN, eller overdose, ring din lokale legevakt eller giftkontrollsenter med en gang. . Ikke ta andre medisiner mens du tar WELLBUTRIN 300mg med mindre helsepersonell har fortalt deg at det er greit. . Hvis du tar WELLBUTRIN 150mg for behandling av alvorlig depressiv lidelse, kan det ta flere uker før du føler at WELLBUTRIN 150mg virker. Når du føler deg bedre, er det viktig å fortsette å ta WELLBUTRIN nøyaktig som anvist av helsepersonell. Ring helsepersonell hvis du ikke føler at WELLBUTRIN fungerer for deg.
Hva bør jeg unngå mens jeg tar WELLBUTRIN 300mg?
- . Begrens eller unngå bruk av alkohol under behandling med WELLBUTRIN. Hvis du vanligvis drikker mye alkohol, snakk med helsepersonell før du plutselig slutter. Hvis du plutselig slutter å drikke alkohol, kan du øke risikoen for å få anfall. . Ikke kjør bil eller bruk tunge maskiner før du vet hvordan WELLBUTRIN 150mg påvirker deg. WELLBUTRIN kan påvirke din evne til å gjøre disse tingene trygt.
Hva er mulige bivirkninger av WELLBUTRIN 300mg?
WELLBUTRIN kan forårsake alvorlige bivirkninger. Se avsnittene i begynnelsen av denne medisinveiledningen for informasjon om alvorlige bivirkninger av WELLBUTRIN.
De vanligste bivirkningene av WELLBUTRIN inkluderer:
- . nervøsitet . kraftig svette . tørr i munnen . skjelving (skjelving) . forstoppelse . problemer med å sove . hodepine . tåkesyn . kvalme eller oppkast . rask hjerterytme . svimmelhet
Hvis du har kvalme, ta medisinen sammen med mat. Hvis du har problemer med å sove, ikke ta medisinen for nær sengetid.
Fortell helsepersonell med en gang om eventuelle bivirkninger som plager deg.
Dette er ikke alle mulige bivirkninger av WELLBUTRIN. For mer informasjon, spør helsepersonell eller apotek.
Ring helsepersonell for medisinsk råd om bivirkninger. Du kan rapportere bivirkninger til FDA på 1-800-FDA-1088.
Du kan også rapportere bivirkninger til GlaxoSmithKline på 1-888-825-5249.
Hvordan bør jeg oppbevare WELLBUTRIN 300mg?
- . Oppbevar WELLBUTRIN ved romtemperatur mellom 68 °F og 77 °F (20 °C til 25 °C). . Hold WELLBUTRIN-tabletter tørre og ute av lys.
Oppbevar WELLBUTRIN og alle legemidler utilgjengelig for barn.
Generell informasjon om sikker og effektiv bruk av WELLBUTRIN.
Medisiner er noen ganger foreskrevet for andre formål enn de som er oppført i en medisinveiledning. Ikke bruk WELLBUTRIN 300mg for en tilstand det ikke er foreskrevet for. Ikke gi WELLBUTRIN til andre mennesker, selv om de har de samme symptomene som du har. Det kan skade dem.
Hvis du tar en screeningtest for urinmedisin, kan WELLBUTRIN gjøre testresultatet positivt for amfetamin. Hvis du forteller personen som gir deg narkotikascreeningstesten at du tar WELLBUTRIN 300mg, kan de gjøre en mer spesifikk medikamentscreeningstest som ikke skulle ha dette problemet.
Denne medisinguiden oppsummerer viktig informasjon om WELLBUTRIN. Hvis du vil ha mer informasjon, snakk med helsepersonell. Du kan spørre helsepersonell eller apotek om informasjon om WELLBUTRIN som er skrevet for helsepersonell.
For mer informasjon om WELLBUTRIN, ring 1-888-825-5249.
Hva er ingrediensene i WELLBUTRIN 300mg?
Aktiv ingrediens: bupropionhydroklorid.
Inaktive ingredienser: 75 mg tablett – D&C Yellow No. 10 Lake, FD&C Yellow No. 6 Lake, hydroksypropylcellulose, hypromellose, mikrokrystallinsk cellulose, polyetylenglykol, talkum og titandioksid; 100 mg tablett – FD&C Red No. 40 Lake, FD&C Yellow No. 6 Lake, hydroksypropylcellulose, hypromellose, mikrokrystallinsk cellulose, polyetylenglykol, talkum og titandioksid.
Denne medisinveiledningen er godkjent av US Food and Drug Administration.
