Tofranil 25mg, 50mg, 75mg Imipramine Bruk, bivirkninger og dosering. Pris i nettapotek. Generisk medisin uten resept.
Hva er Tofranil og hvordan brukes det?
Tofranil 50mg er et reseptbelagt legemiddel som brukes til å behandle symptomene på depresjon. Tofranil 25mg kan brukes alene eller sammen med andre medisiner.
Tofranil tilhører en klasse legemidler som kalles antidepressiva, TCA.
Det er ikke kjent om Tofranil er trygt og effektivt hos barn under 6 år.
Hva er de mulige bivirkningene av Tofranil 50mg?
Tofranil kan forårsake alvorlige bivirkninger, inkludert:
- . humør eller atferdsendringer, . angst, . panikk anfall, . problemer med å sove, . impulsiv oppførsel, . irritabilitet, . opphisselse, . fiendtlighet, . aggresjon, . rastløshet, . hyperaktivitet (mentalt eller fysisk), . mer depresjon, . selvmordstanker, . tåkesyn, . tunnelsyn, . øyesmerter eller hevelse, . ser glorier rundt lys, . svimmelhet, . nye eller forverrede brystsmerter, . bankende hjerteslag, . flagrende i brystet, . plutselig nummenhet eller svakhet, . problemer med syn, tale eller balanse, . feber, . sår hals, . forvirring, . hallusinasjoner, . uvanlige tanker eller oppførsel, . smertefull eller vanskelig vannlating, . anfall, og . gulfarging av hud eller øyne (gulsott)
Få medisinsk hjelp med en gang hvis du har noen av symptomene nevnt ovenfor.
De vanligste bivirkningene av Tofranil inkluderer:
- . prikkende følelse, . svakhet, . mangel på koordinering, . tørr i munnen, . kvalme, . oppkast, . forstoppelse, . diaré, . synsforandringer, . ringer i ørene dine, . brystkreft (både menn og kvinner), . redusert sexlyst, . impotens, og . problemer med å få orgasme
Fortell legen dersom du har noen bivirkninger som plager deg eller som ikke går over.
Dette er ikke alle mulige bivirkninger av Tofranil. Spør legen din eller apoteket for mer informasjon.
Suicidalitet og antidepressiva
Antidepressiva økte risikoen sammenlignet med placebo for selvmordstenkning og -adferd (suicidalitet) hos barn, ungdom og unge voksne i korttidsstudier av alvorlig depressiv lidelse (MDD) og andre psykiatriske lidelser. Alle som vurderer bruk av imipraminhydroklorid eller andre antidepressiva hos et barn, ungdom eller ung voksen må balansere denne risikoen med det kliniske behovet. Korttidsstudier viste ikke en økning i risikoen for suicidalitet med antidepressiva sammenlignet med placebo hos voksne over 24 år; det var en reduksjon i risiko med antidepressiva sammenlignet med placebo hos voksne i alderen 65 år og eldre. Depresjon og visse andre psykiatriske lidelser er i seg selv assosiert med økt risiko for selvmord. Pasienter i alle aldre som starter på antidepressiv behandling bør overvåkes på passende måte og observeres nøye for klinisk forverring, suicidalitet eller uvanlige endringer i atferd. Familier og omsorgspersoner bør informeres om behovet for tett observasjon og kommunikasjon med forskriveren. Imipraminhydroklorid er ikke godkjent for bruk hos pediatriske pasienter (se ADVARSLER Klinisk forverring og selvmordsrisiko; FORHOLDSREGLER Informasjon for pasienter; og FORHOLDSREGLER , Pediatrisk bruk).
BESKRIVELSE
Tofranil™ leveres i tablettform for oral administrering.
Tofranil 75mg, imipraminhydroklorid USP, det originale trisykliske antidepressive midlet, er medlem av dibenzazepingruppen av forbindelser. Det er betegnet 5-3-(dimetylamino)propyl-10,11-dihydro-5Hdibenz [b,f]-azepinmonohydroklorid. Dens strukturformel er:
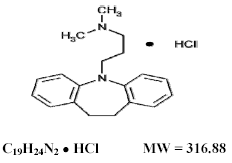
Imipraminhydroklorid USP er et hvitt til off-white, luktfritt eller praktisk talt luktfritt krystallinsk pulver. Det er fritt løselig i vann og alkohol, løselig i aceton og uløselig i eter og i benzen.
Inaktive ingredienser
Kalsiumfosfat, celluloseforbindelser, docusatnatrium, jernoksider, magnesiumstearat, polyetylenglykol, povidon, natriumstivelsesglykolat, sukrose, talkum og titandioksid.
INDIKASJONER
Depresjon
For lindring av symptomer på depresjon. Endogen depresjon er mer sannsynlig å bli lindret enn andre depressive tilstander. En til tre ukers behandling kan være nødvendig før optimal terapeutisk effekt er tydelig.
Enuresis i barndommen
Kan være nyttig som midlertidig tilleggsterapi for å redusere enurese hos barn i alderen 6 år og eldre, etter at mulige organiske årsaker er utelukket av passende tester. Hos pasienter som har symptomer på dagtid med hyppighet og haster, bør undersøkelsen inkludere tømmecystouretrografi og cystoskopi, etter behov. Effektiviteten av behandlingen kan reduseres ved fortsatt legemiddeladministrering.
DOSERING OG ADMINISTRASJON
Depresjon
Lavere doser anbefales for eldre pasienter og ungdom. Lavere doser anbefales også for polikliniske pasienter sammenlignet med sykehusinnlagte pasienter som vil være under nøye tilsyn. Dosering bør startes på et lavt nivå og økes gradvis, og noter nøye den kliniske responsen og eventuelle tegn på intoleranse. Etter remisjon kan vedlikeholdsmedisin være nødvendig over lengre tid, med den laveste dosen som vil opprettholde remisjon.
Vanlig voksendose
Innlagte pasienter
Til å begynne med økte 100 mg/dag i delte doser gradvis til 200 mg/dag etter behov. Hvis ingen respons etter to uker, øk til 250 til 300 mg/dag.
Polikliniske pasienter
Til å begynne med økte 75 mg/dag til 150 mg/dag. Doser over 200 mg/dag anbefales ikke. Vedlikehold, 50 til 150 mg/dag.
Ungdoms- og geriatriske pasienter
Til å begynne med 30 til 40 mg/dag; det er vanligvis ikke nødvendig å overstige 100 mg/dag.
Enuresis i barndommen
utgangspunktet bør en oral dose på 25 mg/dag prøves hos barn fra 6 år og eldre. Medisiner bør gis en time før leggetid. Hvis en tilfredsstillende respons ikke oppstår innen en uke, øk dosen til 50 mg per natt hos barn under 12 år; barn over 12 år kan få opptil 75 mg per natt. En daglig dose større enn 75 mg øker ikke effekten og har en tendens til å øke bivirkninger. Bevis tyder på at hos sengevætere tidlig på natten er stoffet mer effektivt gitt tidligere og i delte mengder, dvs. 25 mg midt på ettermiddagen, gjentatt ved sengetid. Det bør vurderes å innlede en legemiddelfri periode etter en adekvat terapeutisk utprøving med gunstig respons. Doseringen bør trappes ned gradvis i stedet for å avbrytes brått; dette kan redusere tendensen til tilbakefall. Barn som får tilbakefall når stoffet seponeres, reagerer ikke alltid på et påfølgende behandlingsforløp.
En dose på 2,5 mg/kg/dag bør ikke overskrides. EKG-endringer av ukjent betydning er rapportert hos pediatriske pasienter med doser som er dobbelt så stor.
Sikkerheten og effektiviteten av Tofranil som midlertidig tilleggsbehandling for nattlig enurese hos barn under 6 år er ikke fastslått.
HVORDAN LEVERES
De tre styrkene til Tofranil™ (imipraminhydroklorid USP) er tilgjengelige som følger:
– trekantet, bikonveks, korallrødbrun, sukkerdrasjert tablett, merket med på den ene siden og "10" på den andre siden i svart.
30 flasker NDC 0406-9920-03 Flasker à 100 stk NDC 0406-9920-01
– rund, bikonveks, korallrødbrun, sukkerdrasjert tablett, merket med på den ene siden og "25" på den andre siden i svart.
30 flasker NDC 0406-9921-03 Flasker à 100 stk NDC 0406-9921-01
– rund, bikonveks, korallrødbrun, sukkerdrasjert tablett, merket med på den ene siden og "50" på den andre siden i svart.
30 flasker NDC 0406-9922-03 Flasker à 100 stk NDC 0406-9922-01
Oppbevares ved 20° til 25°C (68° til 77°F) [se USP kontrollert romtemperatur].
Dispenser i tett beholder (USP) med barnesikret lukking.
Produsert av: Patheon Inc. Whitby, Ontario, Canada, L1N 5Z5. Revidert: april 2017
BIVIRKNINGER
Merk – Selv om listen som følger inkluderer noen få bivirkninger som ikke er rapportert med dette spesifikke legemidlet, krever de farmakologiske likhetene mellom de trisykliske antidepressiva at hver av reaksjonene vurderes når Tofranil 25 mg administreres.
Kardiovaskulær: Ortostatisk hypotensjon, hypertensjon, takykardi, hjertebank, hjerteinfarkt, arytmier, hjerteblokk, EKG-forandringer, utfelling av kongestiv hjertesvikt, hjerneslag.
Psykiatrisk: Forvirringstilstander (spesielt hos eldre) med hallusinasjoner, desorientering, vrangforestillinger; angst, rastløshet, agitasjon; søvnløshet og mareritt; hypomani; forverring av psykose.
Nevrologisk: Nummenhet, prikking, parestesier av ekstremiteter; ukoordinasjon, ataksi, skjelvinger; perifer nevropati; ekstrapyramidale symptomer; anfall, endringer i EEG-mønstre; tinnitus.
Antikolinergisk: Munntørrhet og, sjelden, assosiert sublingual adenitt; tåkesyn, akkommodasjonsforstyrrelser, mydriasis; forstoppelse, paralytisk ileus; urinretensjon, forsinket vannlating, utvidelse av urinveiene.
Allergisk: Hudutslett, petekkier, urticaria, kløe, fotosensibilisering; ødem (generelt eller i ansikt og tunge); narkotika feber; kryssfølsomhet med desipramin.
Hematologisk: Benmargsdepresjon inkludert agranulocytose; eosinofili; purpura; trombocytopeni.
Gastrointestinale: Kvalme og oppkast, anoreksi, epigastrisk lidelse, diaré; særegen smak, stomatitt, magekramper, svart tunge.
Endokrine: Gynekomasti hos hannen; brystforstørrelse og galaktoré hos hunnen; økt eller redusert libido, impotens; testikkel hevelse; forhøyelse eller depresjon av blodsukkernivået; upassende antidiuretisk hormon (ADH) sekresjonssyndrom.
Annen: Gulsott (simulerer obstruktiv); endret leverfunksjon; vektøkning eller tap; svette; rødming; urin frekvens; døsighet, svimmelhet, svakhet og tretthet; hodepine; parotis hevelse; alopecia; tilbøyelighet til å falle.
Abstinenssymptomer: Selv om det ikke tyder på avhengighet, kan brå seponering av behandlingen etter langvarig behandling gi kvalme, hodepine og ubehag.
Merk – Hos enuretiske barn behandlet med Tofranil 75 mg har de vanligste bivirkningene vært nervøsitet, søvnforstyrrelser, tretthet og milde gastrointestinale forstyrrelser. Disse forsvinner vanligvis under fortsatt legemiddeladministrering eller når dosen reduseres. Andre reaksjoner som er rapportert inkluderer forstoppelse, kramper, angst, emosjonell ustabilitet, synkope og kollaps. Alle bivirkninger rapportert ved bruk av voksne bør vurderes.
NARKOTIKAHANDEL
Legemidler metabolisert av P450 2D6
Den biokjemiske aktiviteten til legemiddelmetaboliserende isozym cytokrom P450 2D6 (debrisoquinhydroksylase) er redusert i en undergruppe av den kaukasiske befolkningen (omtrent 7 % til 10 % av kaukasiere er såkalte "dårlige metabolisatorer"); pålitelige estimater av prevalensen av redusert P450 2D6 isozymaktivitet blant asiatiske, afrikanske og andre populasjoner er ennå ikke tilgjengelig. Dårlige metabolisatorer har høyere enn forventet plasmakonsentrasjoner av trisykliske antidepressiva (TCA) når de gis vanlige doser. Avhengig av andelen legemiddel som metaboliseres av P450 2D6, kan økningen i plasmakonsentrasjon være liten eller ganske stor (8 ganger økning i plasma AUC for TCA).
tillegg hemmer visse legemidler aktiviteten til dette isozymet og får normale metabolisatorer til å ligne dårlige metabolisatorer. Et individ som er stabilt på en gitt dose TCA kan bli brått giftig når det gis en av disse hemmende medikamentene som samtidig behandling. Legemidlene som hemmer cytokrom P450 2D6 inkluderer noen som ikke metaboliseres av enzymet (kinidin; cimetidin) og mange som er substrater for P450 2D6 (mange andre antidepressiva, fenotiaziner og Type 1C antiarytmika propafenon og flekainid). Mens alle selektive serotoninreopptakshemmere (SSRI), f.eks. fluoksetin, sertralin og paroksetin, hemmer P450 2D6, kan de variere i omfanget av hemming. I hvilken grad SSRI-TCA-interaksjon kan gi kliniske problemer, vil avhenge av graden av hemming og farmakokinetikken til den involverte SSRI. Likevel er forsiktighet indikert ved samtidig administrering av TCA med noen av SSRIene og også ved bytte fra en klasse til en annen. Det er spesielt viktig at det må gå tilstrekkelig tid før TCA-behandling igangsettes hos en pasient som seponeres fra fluoksetin, gitt den lange halveringstiden til forelderen og den aktive metabolitten (minst 5 uker kan være nødvendig).
Samtidig bruk av trisykliske antidepressiva med legemidler som kan hemme cytokrom P450 2D6 kan kreve lavere doser enn det som vanligvis er foreskrevet for enten det trisykliske antidepressivet eller det andre legemidlet. Videre, hver gang et av disse andre legemidlene trekkes ut av samtidig behandling, kan det være nødvendig med en økt dose trisyklisk antidepressivum. Det er ønskelig å overvåke TCA-plasmanivåer når en TCA skal gis samtidig med et annet medikament kjent for å være en hemmer av P450 2D6.
Plasmakonsentrasjonen av imipramin kan øke når legemidlet gis samtidig med leverenzyminhibitorer (f.eks. cimetidin, fluoksetin) og reduseres ved samtidig administrasjon med leverenzyminduktorer (f.eks. barbiturater, fenytoin), og justering av dosen av imipramin kan derfor være nødvendig.
Hos enkelte følsomme pasienter eller hos de som i tillegg får antikolinerge legemidler (inkludert antiparkinsonismemidler), kan de atropinlignende effektene bli mer uttalte (f.eks. paralytisk ileus). Nøye overvåking og nøye justering av dosen er nødvendig når imipraminhydroklorid administreres samtidig med antikolinerge legemidler.
Unngå bruk av preparater, som dekongestanter og lokalbedøvelsesmidler, som inneholder sympatomimetiske aminer (f.eks. epinefrin, noradrenalin), siden det er rapportert at trisykliske antidepressiva kan potensere effekten av katekolaminer.
Forsiktighet bør utvises når imipraminhydroklorid brukes sammen med midler som senker blodtrykket. Imipraminhydroklorid kan potensere effekten av CNS-dempende legemidler.
Pasienter bør advares om at imipraminhydroklorid kan forsterke de CNS-dempende effektene av alkohol (se ADVARSLER ).
ADVARSLER
Klinisk forverring og selvmordsrisiko
Pasienter med alvorlig depressiv lidelse (MDD), både voksne og barn, kan oppleve forverring av depresjonen og/eller fremveksten av selvmordstanker og -adferd (suicidalitet) eller uvanlige endringer i atferd, enten de tar antidepressive medisiner eller ikke, og dette risikoen kan vedvare inntil betydelig remisjon oppstår. Selvmord er en kjent risiko for depresjon og visse andre psykiatriske lidelser, og disse lidelsene er i seg selv de sterkeste prediktorene for selvmord. Det har imidlertid vært en langvarig bekymring for at antidepressiva kan ha en rolle i å indusere forverring av depresjon og fremveksten av suicidalitet hos visse pasienter i de tidlige faser av behandlingen. Samlede analyser av kortsiktige placebokontrollerte studier av antidepressiva (SSRI og andre) viste at disse medikamentene øker risikoen for suicidal tenkning og atferd (suicidalitet) hos barn, ungdom og unge voksne (alder 18 til 24) med alvorlig depressiv sykdom. lidelse (MDD) og andre psykiatriske lidelser. Korttidsstudier viste ikke en økning i risikoen for suicidalitet med antidepressiva sammenlignet med placebo hos voksne over 24 år; det var en reduksjon med antidepressiva sammenlignet med placebo hos voksne i alderen 65 år og eldre.
De samlede analysene av placebokontrollerte studier hos barn og ungdom med MDD, tvangslidelse (OCD) eller andre psykiatriske lidelser inkluderte totalt 24 korttidsstudier av 9 antidepressiva med over 4400 pasienter. De samlede analysene av placebokontrollerte studier hos voksne med MDD eller andre psykiatriske lidelser inkluderte totalt 295 korttidsstudier (median varighet på 2 måneder) med 11 antidepressiva med over 77 000 pasienter. Det var betydelig variasjon i risiko for suicidalitet blant legemidler, men en tendens til en økning i yngre pasienter for nesten alle legemidler som ble studert. Det var forskjeller i absolutt risiko for suicidalitet på tvers av de forskjellige indikasjonene, med høyest forekomst av MDD. Risikoforskjellene (legemiddel vs. placebo) var imidlertid relativt stabile innenfor aldersstrata og på tvers av indikasjoner. Disse risikoforskjellene (medikament-placebo-forskjell i antall tilfeller av suicidalitet per 1000 behandlede pasienter) er gitt i tabell 1.
Ingen selvmord skjedde i noen av de pediatriske studiene. Det var selvmord i voksenforsøkene, men antallet var ikke tilstrekkelig til å komme til noen konklusjon om legemiddeleffekt på selvmord.
Det er ukjent om suicidalitetsrisikoen strekker seg til langvarig bruk, dvs. utover flere måneder. Det er imidlertid betydelig bevis fra placebokontrollerte vedlikeholdsforsøk hos voksne med depresjon på at bruk av antidepressiva kan forsinke tilbakefall av depresjon.
Alle pasienter som behandles med antidepressiva for enhver indikasjon bør overvåkes hensiktsmessig og observeres nøye for klinisk forverring, suicidalitet og uvanlige endringer i atferd, spesielt i løpet av de første månedene av en medikamentell behandlingskur, eller ved doseendringer, enten økninger eller synker.

Følgende symptomer, angst, agitasjon, panikkanfall, søvnløshet, irritabilitet, fiendtlighet, aggressivitet, impulsivitet, akatisi (psykomotorisk rastløshet), hypomani og mani, er rapportert hos voksne og pediatriske pasienter som også behandles med antidepressiva for alvorlig depressiv lidelse som for andre indikasjoner, både psykiatriske og ikke-psykiatriske. Selv om det ikke er etablert en årsakssammenheng mellom fremveksten av slike symptomer og enten forverring av depresjon og/eller fremveksten av selvmordsimpulser, er det bekymring for at slike symptomer kan representere forløpere til fremvoksende suicidalitet.
Det bør vurderes å endre det terapeutiske regimet, inkludert eventuelt seponering av medisinen, hos pasienter hvis depresjon er vedvarende verre, eller som opplever ny suicidalitet eller symptomer som kan være forløpere til forverring av depresjon eller suicidalitet, spesielt hvis disse symptomene er alvorlige, brå i debut, eller var ikke en del av pasientens tilstedeværende symptomer.
Familier og omsorgspersoner til pasienter som behandles med antidepressiva for alvorlig depressiv lidelse eller andre indikasjoner, både psykiatriske og ikke-psykiatriske, bør varsles om behovet for å overvåke pasienter for fremveksten av agitasjon, irritabilitet, uvanlige endringer i atferd og de andre symptomene beskrevet ovenfor , samt fremveksten av suicidalitet, og å rapportere slike symptomer umiddelbart til helsepersonell. Slik overvåking bør inkludere daglig observasjon av familier og omsorgspersoner. Resepter for imipraminhydroklorid bør skrives ut for den minste mengde tabletter i samsvar med god pasientbehandling, for å redusere risikoen for overdosering.
Screening av pasienter for bipolar lidelse
En alvorlig depressiv episode kan være den første presentasjonen av bipolar lidelse. Det er generelt antatt (men ikke etablert i kontrollerte studier) at behandling av en slik episode med et antidepressivum alene kan øke sannsynligheten for utfelling av en blandet/manisk episode hos pasienter med risiko for bipolar lidelse. Hvorvidt noen av symptomene beskrevet ovenfor representerer en slik konvertering er ukjent. Før behandling med et antidepressivum startes, bør imidlertid pasienter med depressive symptomer undersøkes tilstrekkelig for å avgjøre om de har risiko for bipolar lidelse; slik screening bør inkludere en detaljert psykiatrisk historie, inkludert en familiehistorie med selvmord, bipolar lidelse og depresjon. Det skal bemerkes at imipraminhydroklorid ikke er godkjent for bruk ved behandling av bipolar depresjon.
Vinkel-lukkende glaukom
Pupilleutvidelsen som oppstår etter bruk av mange antidepressiva, inkludert Tofranil, kan utløse et vinkellukkende angrep hos en pasient med anatomisk smale vinkler som ikke har patentert iridektomi.
Barn
En dose på 2,5 mg/kg/dag av Tofranil 25 mg bør ikke overskrides i barndommen. EKG-endringer av ukjent betydning er rapportert hos pediatriske pasienter med doser som er dobbelt så stor.
Ekstrem forsiktighet bør utvises når dette legemidlet gis til: pasienter med kardiovaskulær sykdom på grunn av muligheten for ledningsfeil, arytmier, kongestiv hjertesvikt, hjerteinfarkt, hjerneslag og takykardi. Disse pasientene krever hjerteovervåking ved alle doseringsnivåer av legemidlet;
pasienter med tidligere urinretensjon, eller historie med trangvinklet glaukom på grunn av legemidlets antikolinerge egenskaper; hypertyreoideapasienter eller de som bruker skjoldbruskmedisin på grunn av muligheten for kardiovaskulær toksisitet;
pasienter med anfallsforstyrrelse i anamnesen fordi dette legemidlet har vist seg å senke anfallsterskelen;
pasienter som får guanethidin, klonidin eller lignende midler, siden Tofranil kan blokkere den farmakologiske effekten av disse legemidlene;
pasienter som får metylfenidathydroklorid. Siden metylfenidathydroklorid kan hemme metabolismen av Tofranil 75 mg, kan det være nødvendig med nedjustering av dosen av imipraminhydroklorid når det gis samtidig med metylfenidathydroklorid.
Tofranil kan forsterke de CNS-dempende effektene av alkohol. Derfor bør man huske på at farene forbundet med et selvmordsforsøk eller utilsiktet overdosering med stoffet kan øke for pasienten som bruker for store mengder alkohol (se FORHOLDSREGLER ).
Siden Tofranil kan svekke de mentale og/eller fysiske evnene som kreves for å utføre potensielt farlige oppgaver, for eksempel å betjene en bil eller maskiner, bør pasienten advares tilsvarende.
FORHOLDSREGLER
Generell
En EKG-registrering bør tas før initiering av større doser av Tofranil enn vanlig og med passende intervaller deretter til steady state oppnås. (Pasienter med tegn på kardiovaskulær sykdom krever hjerteovervåking ved alle doseringsnivåer av legemidlet. Se ADVARSLER .) Eldre pasienter og pasienter med hjertesykdom eller tidligere hjertesykdom i anamnesen har en spesiell risiko for å utvikle hjerteabnormaliteter forbundet med bruk av Tofranil.
Det bør huskes at muligheten for selvmord hos alvorlig deprimerte pasienter er iboende i sykdommen og kan vedvare inntil betydelig remisjon inntreffer. Slike pasienter bør overvåkes nøye i den tidlige fasen av behandlingen med Tofranil 75 mg, og kan kreve sykehusinnleggelse. Resepter bør skrives ut for den minste mengden som er mulig. Hypomane eller maniske episoder kan forekomme, spesielt hos pasienter med sykliske lidelser. Slike reaksjoner kan nødvendiggjøre seponering av legemidlet. Om nødvendig kan Tofranil 75 mg gjenopptas i lavere dose når disse episodene er lindret.
Administrering av et beroligende middel kan være nyttig for å kontrollere slike episoder.
En aktivering av psykosen kan av og til observeres hos schizofrene pasienter og kan kreve dosereduksjon og tillegg av fentiazin.
Samtidig administrering av Tofranil 50 mg og elektrosjokkbehandling kan øke farene; slik behandling bør begrenses til de pasientene som det er viktig for, siden det er begrenset klinisk erfaring.
Pasienter som tar imipraminhydroklorid bør unngå overdreven eksponering for sollys siden det har vært rapporter om fotosensibilisering.
Både økning og reduksjon av blodsukkernivået er rapportert ved bruk av imipraminhydroklorid.
Imipraminhydroklorid bør brukes med forsiktighet hos pasienter med betydelig nedsatt nyre- eller leverfunksjon.
Pasienter som utvikler feber og sår hals under behandling med imipraminhydroklorid bør få utført leukocytt- og differensialblodtelling. Imipraminhydroklorid bør seponeres hvis det er tegn på patologisk nøytrofil depresjon.
Før elektiv kirurgi bør imipraminhydroklorid seponeres så lenge den kliniske situasjonen tillater det.
Informasjon til pasienter
Forskrivere eller annet helsepersonell bør informere pasienter, deres familier og deres omsorgspersoner om fordelene og risikoene forbundet med behandling med imipraminhydroklorid og bør gi dem råd om riktig bruk. En pasient Medisinveiledning om "Antidepressive medisiner, depresjon og andre alvorlige psykiske lidelser, og selvmordstanker eller handlinger" er tilgjengelig for imipraminhydroklorid. Forskriveren eller helsepersonell bør instruere pasienter, deres familier og deres omsorgspersoner om å lese medisinveiledningen og bør hjelpe dem med å forstå innholdet. Pasienter bør gis mulighet til å diskutere innholdet i legemiddelveiledningen og få svar på spørsmål de måtte ha. Den fullstendige teksten til medisinveiledningen er skrevet ut på nytt på slutten av dette dokumentet.
Pasienter bør informeres om følgende problemer og bes om å varsle sin forskriver dersom disse oppstår mens de tar imipraminhydroklorid.
Pasienter bør informeres om at inntak av Tofranil kan forårsake mild pupilleutvidelse, som hos følsomme personer kan føre til en episode med lukket vinkelglaukom. Eksisterende glaukom er nesten alltid åpenvinklet glaukom fordi vinkel-lukkende glaukom, når diagnostisert, kan behandles definitivt med iridektomi. Åpenvinklet glaukom er ikke en risikofaktor for lukkevinkelglaukom. Pasienter kan ønske å bli undersøkt for å finne ut om de er mottakelige for vinkellukking, og ha en profylaktisk prosedyre (f.eks. iridektomi), hvis de er mottakelige.
Klinisk forverring og selvmordsrisiko
Pasienter, deres familier og deres omsorgspersoner bør oppmuntres til å være oppmerksomme på fremveksten av angst, agitasjon, panikkanfall, søvnløshet, irritabilitet, fiendtlighet, aggressivitet, impulsivitet, akatisi (psykomotorisk rastløshet), hypomani, mani, andre uvanlige endringer i atferd. , forverring av depresjon og selvmordstanker, spesielt tidlig under antidepressiv behandling og når dosen justeres opp eller ned. Familier og omsorgspersoner til pasienter bør rådes til å se etter forekomsten av slike symptomer på daglig basis, siden endringer kan være brå. Slike symptomer bør rapporteres til pasientens forskriver eller helsepersonell, spesielt hvis de er alvorlige, plutselige eller ikke var en del av pasientens symptomer. Symptomer som disse kan være assosiert med økt risiko for suicidal tenkning og atferd og indikerer behov for svært tett oppfølging og muligens endringer i medisinen.
Svangerskap
Reproduksjonsstudier på dyr har gitt usikre resultater (se også Dyrefarmakologi ).
Det er ikke utført noen godt kontrollerte studier med gravide kvinner for å bestemme effekten av Tofranil på fosteret. Det har imidlertid vært kliniske rapporter om medfødte misdannelser forbundet med bruk av legemidlet. Selv om en årsakssammenheng mellom disse effektene og stoffet ikke kunne fastslås, kan muligheten for fosterrisiko fra mors inntak av Tofranil ikke utelukkes. Derfor bør Tofranil kun brukes til kvinner som er eller kan bli gravide dersom den kliniske tilstanden klart rettferdiggjør potensiell risiko for fosteret.
Ammende mødre
Begrensede data tyder på at Tofranil 75 mg sannsynligvis vil bli utskilt i morsmelk hos mennesker. Som en generell regel bør en kvinne som tar et legemiddel ikke amme siden det er en mulighet for at legemidlet kan skilles ut i morsmelk og være skadelig for barnet.
Pediatrisk bruk
Sikkerhet og effektivitet i den pediatriske populasjonen andre enn pediatriske pasienter med nattlig enurese er ikke fastslått (se BOKS ADVARSEL og ADVARSLER , Klinisk forverring og selvmordsrisiko ). Alle som vurderer bruk av imipraminhydroklorid hos et barn eller ungdom, må balansere den potensielle risikoen med det kliniske behovet.
Sikkerheten og effektiviteten til legemidlet som midlertidig tilleggsbehandling for nattlig enurese hos pediatriske pasienter under 6 år er ikke fastslått.
Sikkerheten til legemidlet for langvarig, kronisk bruk som tilleggsbehandling for nattlig enurese hos pediatriske pasienter 6 år eller eldre er ikke fastslått; Det bør vurderes å innlede en medikamentfri periode etter en adekvat terapeutisk utprøving med gunstig respons.
En dose på 2,5 mg/kg/dag bør ikke overskrides i barndommen. EKG-endringer av ukjent betydning er rapportert hos pediatriske pasienter med doser som er dobbelt så stor.
Geriatrisk bruk
litteraturen var det fire godt kontrollerte, randomiserte, dobbeltblinde, parallelle gruppesammenligningsstudier utført med Tofranil 50 mg i den eldre befolkningen. Det var totalt 651 personer inkludert i disse studiene. Disse studiene ga ingen sammenligning med yngre forsøkspersoner. Det ble ikke identifisert ytterligere bivirkninger hos eldre.
Kliniske studier av Tofranil 75 mg i den opprinnelige søknaden inkluderte ikke tilstrekkelig antall forsøkspersoner i alderen 65 år og over til å avgjøre om de reagerer annerledes enn yngre forsøkspersoner. Klinisk erfaring etter markedsføring har ikke identifisert forskjeller i respons mellom eldre og yngre personer. Generelt bør dosevalg for eldre være forsiktig, vanligvis med start i den lave enden av doseringsområdet, noe som gjenspeiler større frekvens av nedsatt lever-, nyre- eller hjertefunksjon, og samtidig sykdom eller annen medikamentell behandling.
(Se også DOSERING OG ADMINISTRASJON , Tenåring og Geriatriske pasienter .)
(Se også FORHOLDSREGLER , Generell. )
OVERDOSE
Dødsfall kan oppstå på grunn av overdosering med denne klassen medikamenter. Multiple stoffinntak (inkludert alkohol) er vanlig ved bevisst trisyklisk overdose. Siden håndteringen er kompleks og i endring, anbefales det at legen kontakter en giftsentral for å få oppdatert informasjon om behandling. Tegn og symptomer på toksisitet utvikler seg raskt etter trisyklisk overdose. Derfor er sykehusovervåking nødvendig så snart som mulig.
Barn har blitt rapportert å være mer følsomme enn voksne for en akutt overdosering av imipraminhydroklorid. En akutt overdose av en hvilken som helst mengde hos spedbarn eller små barn, spesielt, må betraktes som alvorlig og potensielt dødelig.
Manifestasjoner
Disse kan variere i alvorlighetsgrad avhengig av faktorer som mengden medikament som absorberes, pasientens alder og intervallet mellom legemiddelinntak og behandlingsstart. Kritiske manifestasjoner av overdose inkluderer hjertedysrytmier, alvorlig hypotensjon, kramper og CNS-depresjon inkludert koma. Endringer i elektrokardiogrammet, spesielt i QRS-aksen eller -bredden, er klinisk signifikante indikatorer på trisyklisk toksisitet.
Andre CNS-manifestasjoner kan inkludere døsighet, stupor, ataksi, rastløshet, agitasjon, hyperaktive reflekser, muskelstivhet, atetoide og choreiforme bevegelser.
Hjerteavvik kan omfatte takykardi og tegn på kongestiv svikt. Respirasjonsdepresjon, cyanose, sjokk, oppkast, hyperpyreksi, mydriasis og diaforese kan også være tilstede.
Ledelse
Ta EKG og start hjerteovervåking umiddelbart. Beskytt pasientens luftveier, opprett en intravenøs linje og start gastrisk dekontaminering. Minimum 6 timers observasjon med hjerteovervåking og observasjon for tegn på CNS eller respirasjonsdepresjon, hypotensjon, hjerterytmeforstyrrelser og/eller ledningsblokker og anfall er nødvendig. Hvis tegn på toksisitet oppstår når som helst i denne perioden, er utvidet overvåking nødvendig. Det er kasusrapporter om pasienter som bukker under for fatale dysrytmier sent etter overdose; disse pasientene hadde kliniske bevis på betydelig forgiftning før døden, og de fleste fikk utilstrekkelig gastrointestinal dekontaminering. Overvåking av plasmanivåer av medikamenter bør ikke veilede behandlingen av pasienten.
Gastrointestinal dekontaminering
Alle pasienter som mistenkes for trisyklisk overdose bør få gastrointestinal dekontaminering. Dette bør inkludere store volum mageskylling etterfulgt av aktivt kull. Hvis bevisstheten er svekket, bør luftveiene sikres før skylling. Emesis er kontraindisert.
Kardiovaskulær
En maksimal QRS-lengde på ≥0,10 sekunder kan være den beste indikasjonen på alvorlighetsgraden av overdosen. Intravenøst natriumbikarbonat bør brukes for å opprettholde serum-pH i området 7,45 til 7,55. Hvis pH-responsen er utilstrekkelig, kan hyperventilering også brukes. Samtidig bruk av hyperventilering og natriumbikarbonat bør gjøres med ekstrem forsiktighet, med hyppig pH-overvåking. En pH >7,60 eller en pCO2
sjeldne tilfeller kan hemoperfusjon være gunstig ved akutt refraktær kardiovaskulær ustabilitet hos pasienter med akutt toksisitet. Imidlertid har hemodialyse, peritonealdialyse, utvekslingstransfusjoner og tvungen diurese generelt blitt rapportert som ineffektive ved trisykliske forgiftninger.
CNS
Hos pasienter med CNS-depresjon anbefales tidlig intubering på grunn av potensialet for brå forverring. Anfall bør kontrolleres med benzodiazepiner, eller hvis disse er ineffektive, andre antikonvulsiva (f.eks. fenobarbital, fenytoin). Fysiostigmin anbefales ikke unntatt for å behandle livstruende symptomer som ikke har respondert på andre terapier, og da kun i samråd med et giftkontrollsenter.
Psykiatrisk oppfølging
Siden overdosering ofte er bevisst, kan pasienter forsøke selvmord på andre måter i restitusjonsfasen. Psykiatrisk henvisning kan være aktuelt.
Pediatrisk ledelse
Prinsippene for behandling av overdosering av barn og voksne er like. Det anbefales sterkt at legen kontakter det lokale giftkontrollsenteret for spesifikk pediatrisk behandling.
KONTRAINDIKASJONER
Samtidig bruk av monoaminoksidasehemmende forbindelser er kontraindisert. Hyperpyretiske kriser eller alvorlige krampeanfall kan forekomme hos pasienter som får slike kombinasjoner. Potenseringen av bivirkninger kan være alvorlig, eller til og med dødelig. Når det er ønskelig å erstatte Tofranil hos pasienter som får en monoaminoksidasehemmer, bør det gå så lenge et intervall som den kliniske situasjonen tillater, med minimum 14 dager. Startdosen bør være lav og økningen bør foreskrives gradvis og med forsiktighet.
Legemidlet er kontraindisert i den akutte restitusjonsperioden etter et hjerteinfarkt. Pasienter med kjent overfølsomhet overfor denne forbindelsen bør ikke gis legemidlet. Man bør huske på muligheten for kryssfølsomhet overfor andre dibenzazepinforbindelser.
KLINISK FARMAKOLOGI
Virkningsmekanismen til Tofranil 25 mg er ikke definitivt kjent. Den virker imidlertid ikke primært ved stimulering av sentralnervesystemet. Den kliniske effekten antas å skyldes potensering av adrenerge synapser ved å blokkere opptak av noradrenalin i nerveender. Virkningsmåten til stoffet for å kontrollere enuresis i barndommen antas å være bortsett fra dets antidepressive effekt.
Dyrefarmakologi og toksikologi
A. Akutt
Orale LD50-områder er som følger:
Rotte 355 til 682 mg/kg Hund 100 til 215 mg/kg
Avhengig av doseringen hos begge artene, fortsatte toksiske tegn gradvis fra depresjon, uregelmessig respirasjon og ataksi til kramper og død.
B. Reproduksjon/teratogent
Den samlede vurderingen kan oppsummeres på følgende måte:
Oral: Uavhengige studier på tre arter (rotte, mus og kanin) viste at når Tofranil administreres oralt i doser opptil ca. 2-1/2 ganger maksimal human dose i de to første artene og opptil 25 ganger maksimal human dose. dose i den tredje arten, er stoffet i det vesentlige fritt for teratogent potensial. I de tre undersøkte artene forekom bare ett tilfelle av fosteravvik (hos kaninen), og i den studien var det også en abnormitet i kontrollgruppen. Imidlertid eksisterer det bevis fra rottestudiene for at noe systemisk og embryotoksisk potensial er påviselig. Dette kommer til uttrykk ved redusert kullstørrelse, en liten økning i dødfødte og en reduksjon i gjennomsnittlig fødselsvekt.
